Beruflich Dokumente
Kultur Dokumente
4 Aula Teste Da Chama
Hochgeladen von
Luciana GuilhermeOriginalbeschreibung:
Originaltitel
Copyright
Verfügbare Formate
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
Verfügbare Formate
4 Aula Teste Da Chama
Hochgeladen von
Luciana GuilhermeCopyright:
Verfügbare Formate
Universidade Estadual de Gois Disciplina de Qumica I Curso de Engenharia Agrcola Professora: Luciana Rebelo Guilherme Aula 4: Teste de Chama
a 1 - INTRODUO O teste de chama uma tcnica usada em qumica para detectar a presena de alguns ons metlicos, tendo por base o espectro de emisso caracterstico para cada elemento (1-4). O teste de chama baseado no fato de que quando certa quantidade de energia fornecida a um determinado elemento qumico (no caso da chama, energia em forma de calor), alguns eltrons da ltima camada de valncia absorvem esta energia passando para um nvel de energia mais elevado, produzindo o que chamamos de estado excitado (14). Quando um desses eltrons excitados retorna ao estado fundamental, ele libera a energia recebida anteriormente em forma de radiao. Cada elemento libera a radiao em um comprimento de onda caracterstico, pois a quantidade de energia necessria para excitar um eltron nica para cada elemento. A radiao liberada por alguns elementos possui comprimento de onda na faixa do espectro visvel, ou seja, o olho humano capaz de enxerg-las atravs de cores. Assim, possvel identificar a presena de certos elementos devido cor caracterstica que eles emitem quando aquecidos numa chama(1-4). A temperatura da chama do bico de Bnsen suficiente para excitar uma quantidade de eltrons de certos elementos que emitem luz ao retornarem ao estado fundamental de cor e intensidade, que podem ser detectados com considervel certeza e sensibilidade atravs da observao visual da chama (1-4). O teste de chama rpido e fcil de ser feito, e no requer nenhum equipamento que no seja encontrado normalmente num
laboratrio de qumica. Porm, a quantidade de elementos detectveis pequena e existe uma dificuldade em detectar concentraes baixas de alguns elementos, enquanto que outros elementos produzem cores muito fortes que tendem a mascarar sinais mais fracos (1-4).
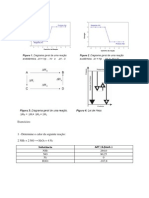
n=3 n=2 n=1 Absoro de Energia E=h Estado fundamental n=3 n=2 n=1
Ef Emiss de energi E=h Depois de absorver energia
Estado excitado Antes de absorver
E=
hc
2 - OBJETIVOS Detectar os elementos de um determinado composto, atravs do ensaio por via seca (ensaio de colorao de chama), observando a cor das radiaes emitidas pelos elementos qumicos, e que possam ser vistas a olho nu.
3 - PARTE EXPERIMENTAL 3.1 - Materiais e reagentes 3.1.1 Materiais Bico de Bunsen com regulador de oxignio; Garra de madeira; Arame; cido clordrico (0,1mol/L); Bqueres; 3.1.2 Reagentes Cloreto de cobre (CuCl2); Nitrato de brio (Ba(NO3)2); Cloreto de sdio (NaCl); Cloreto de clcio (CaCl2); Cloreto de potssio (KCl); Magnsio (Mg). Sal de ltio (a definir)
f) Fazer a limpeza do fio, cujo procedimento foi citado anteriormente (a), e repetir o procedimento com os demais reagentes notando-se que todos produziro coloraes caractersticas g) Repetir o procedimento 3 toda vez que se ia utilizar um reagente diferente. Tabela 1- Coloraes observadas. REAGENTES Cloreto de cobre Nitrato de brio Cloreto de sdio Cloreto de clcio Cloreto de potssio Magnsio Ltio 4 - REFERNCIAS BIBLIOGRFICAS Bibliografia: 1.PINTO, Helena Castro; Carvalho, M de Jesus; Fialho, M Margarida (1997); Tcnicas Laboratoriais de Qumica II-1 edio; Texto Editora; Captulo I; pgs. 70-74 e 181 2.Enciclopdia Universal Multimdia (1996); Texto Editora 3. ALCNTARA, L. <http://pontociencia.org.br/experimentosinterna.php?experimento=160&TESTE+DA+CHAMA> Disponvel em: 19 de maro de 2011. 4. PORTUGAL, P. <http://profs.ccems.pt/PauloPortugal/CFQ/Fichas/Teste_da_Chama.htm> Disponvel em 19 de maro de 2011. COLORAO
3.2 - Procedimento Experimental a) Prender o arame ao pregador de madeira. b) Colocar 5mL de uma soluo de cido clordrico em um bquer. c) Molhar o arame na soluo de cido clordrico. Em seguida, colocar o arame na chama do bico de Bunsen. Repetir o procedimento at que o fio esteja completamente limpo, aproximadamente cinco vezes. d) Com o fio j limpo, mergulhar o mesmo em 5mL de uma soluo de cido clordrico contida em um bquer e, depois, em 0,5g de cloreto de cobre contido em outro bquer, de modo que o sal fique aderido ao fio. e) Levar o fio (contendo a amostra) zona oxidante inferior da chama, podendo-se observar que ao queimar-se, o cloreto de cobre apresenta uma colorao, anotar na Tabela 1 a colorao observada.
Das könnte Ihnen auch gefallen
- Ácidos e Bases de Brönsted e Lowry: Uma visão aplicada ao meio ambienteVon EverandÁcidos e Bases de Brönsted e Lowry: Uma visão aplicada ao meio ambienteNoch keine Bewertungen
- Apostila de Introdução A QuímicaDokument87 SeitenApostila de Introdução A QuímicaVinícius FabroNoch keine Bewertungen
- Potenciometria: aspectos teóricos e práticosVon EverandPotenciometria: aspectos teóricos e práticosNoch keine Bewertungen
- Exercícios de Química Analítica QuantitativaDokument21 SeitenExercícios de Química Analítica QuantitativaLídia LeiteNoch keine Bewertungen
- Solubilidade de Compostos OrgânicosDokument7 SeitenSolubilidade de Compostos OrgânicosAmanda AguiarNoch keine Bewertungen
- Aula 04-EQUILIBRIO QUIMICOSDokument33 SeitenAula 04-EQUILIBRIO QUIMICOSLeonardo Maciel100% (2)
- Detetive Por Um Dia: Aprendendo A Investigar Por Meio Da Química ForenseVon EverandDetetive Por Um Dia: Aprendendo A Investigar Por Meio Da Química ForenseNoch keine Bewertungen
- Relatório de Aula Prática 2Dokument5 SeitenRelatório de Aula Prática 2Livia FraticelliNoch keine Bewertungen
- Sobre o (Não) Domínio da Linguagem Química e sua Influência na AprendizagemVon EverandSobre o (Não) Domínio da Linguagem Química e sua Influência na AprendizagemNoch keine Bewertungen
- Cinética QuímicaDokument29 SeitenCinética QuímicaProfessoraGianiNoch keine Bewertungen
- Aplicações Da Volumetria de Oxirredução em Indústria - Passei DiretoDokument10 SeitenAplicações Da Volumetria de Oxirredução em Indústria - Passei DiretoProfa Vanessa Monteiro100% (1)
- 1 Lista de Química Analítica 2021Dokument6 Seiten1 Lista de Química Analítica 2021Acisseid SaidNoch keine Bewertungen
- Apostila Espectrometria de Massas Débora AzevedoDokument106 SeitenApostila Espectrometria de Massas Débora AzevedoGaby Salazar Mogollón100% (1)
- Vídeo/Software em Powerpoint®: Métodos Para Ensino-Aprendizagem de EletroquímicaVon EverandVídeo/Software em Powerpoint®: Métodos Para Ensino-Aprendizagem de EletroquímicaBewertung: 5 von 5 Sternen5/5 (1)
- Plano de AulaDokument2 SeitenPlano de AulaWilson XavierNoch keine Bewertungen
- Relatório de Química - Identificação de SubstânciasDokument9 SeitenRelatório de Química - Identificação de SubstânciasCharlescrossNoch keine Bewertungen
- Eletroanálises: aspectos teóricos e práticosVon EverandEletroanálises: aspectos teóricos e práticosNoch keine Bewertungen
- Calculo Estequiometrico - Rendimento - 65 QuestõesDokument24 SeitenCalculo Estequiometrico - Rendimento - 65 QuestõesJoão Victor PereiraNoch keine Bewertungen
- Exercicios PDFFQDokument25 SeitenExercicios PDFFQDiego67% (3)
- Avaliação da erva-mate como biossorventeVon EverandAvaliação da erva-mate como biossorventeNoch keine Bewertungen
- Apostila QualitativaDokument45 SeitenApostila Qualitativabruno100% (1)
- Guia para aulas práticas de biotecnologia de enzimas e fermentaçãoVon EverandGuia para aulas práticas de biotecnologia de enzimas e fermentaçãoNoch keine Bewertungen
- Relatório de Aminoácidos (Bioquimica)Dokument10 SeitenRelatório de Aminoácidos (Bioquimica)Beatriz MarimNoch keine Bewertungen
- Fisico Quimica ADokument51 SeitenFisico Quimica AGisa Jacques100% (2)
- A Teoria de ArrheniusDokument20 SeitenA Teoria de ArrheniusBárbara Sprocati100% (1)
- Vestibulares de Química - UPEDokument111 SeitenVestibulares de Química - UPEcb_penatrujillo100% (2)
- LIVRO PROPRIETARIO - Quimica Geral PDFDokument217 SeitenLIVRO PROPRIETARIO - Quimica Geral PDFJalmir Lima100% (1)
- O Ensino de Química Nas Escolas Da Rede Pública de Ensino Fundamental e Médio Do Município de Itapetinga-BA - O Olhar Dos AlunosDokument7 SeitenO Ensino de Química Nas Escolas Da Rede Pública de Ensino Fundamental e Médio Do Município de Itapetinga-BA - O Olhar Dos Alunoslaycds100% (1)
- Química de CoordenaçãoDokument5 SeitenQuímica de CoordenaçãoAnderson Ribeiro100% (2)
- 02QOI NomenclaturaDokument25 Seiten02QOI NomenclaturaDiana DiasNoch keine Bewertungen
- Lista de Exercícios de Ligações, Termodinâmica e Oxidação-Redução (Recuperado)Dokument5 SeitenLista de Exercícios de Ligações, Termodinâmica e Oxidação-Redução (Recuperado)S.V.W.M ELÉTRICANoch keine Bewertungen
- Relatório Natureza Dos Compostos Orgânicos e Inorgânicos Propriedades FísicasDokument6 SeitenRelatório Natureza Dos Compostos Orgânicos e Inorgânicos Propriedades FísicasGui LhermeNoch keine Bewertungen
- Lista de Exercícios - Geometria e Forças IntermolecularesDokument7 SeitenLista de Exercícios - Geometria e Forças Intermolecularesalexchacal67% (3)
- Tabela Periódica e EletronegatividadeDokument2 SeitenTabela Periódica e EletronegatividadeLUIS HENRIQUE DA SILVA NASCIMENTO100% (1)
- Slides Uv-Vis - EQ PDFDokument49 SeitenSlides Uv-Vis - EQ PDFSilvio Marinho100% (1)
- 233-Manuscrito de Livro-568-1-10-20190704 PDFDokument82 Seiten233-Manuscrito de Livro-568-1-10-20190704 PDFLucas OliveiraNoch keine Bewertungen
- Apostila de Química de Coordenação (Eunice-Midori) - 2013Dokument34 SeitenApostila de Química de Coordenação (Eunice-Midori) - 2013shakarotto100% (1)
- Aula6 Acidez e BasicidadeDokument2 SeitenAula6 Acidez e BasicidadeRukario1Noch keine Bewertungen
- Determinação de Pontos de Fusão e EbuliçãoDokument11 SeitenDeterminação de Pontos de Fusão e EbuliçãoTonny BarbosaNoch keine Bewertungen
- Volumetria IIDokument45 SeitenVolumetria IIAgar Abel MatsinheNoch keine Bewertungen
- Aula 2 - Cálculos Básicos de QuímicaDokument40 SeitenAula 2 - Cálculos Básicos de QuímicaSr Soulo542Noch keine Bewertungen
- Equilibrio de Precipitacao PDFDokument21 SeitenEquilibrio de Precipitacao PDFJoel SamuelNoch keine Bewertungen
- Escolha Do Método AnalíticoDokument16 SeitenEscolha Do Método AnalíticoNelson SouzaNoch keine Bewertungen
- c6 Curso A Prof QuimicaDokument20 Seitenc6 Curso A Prof QuimicaTiago RodriguesNoch keine Bewertungen
- Relatório - 01 Hidrólise de Sais (Íons Ácidos e Básicos)Dokument3 SeitenRelatório - 01 Hidrólise de Sais (Íons Ácidos e Básicos)Halana NascimentoNoch keine Bewertungen
- Quimica Organica Exercicios Classificacao Nomenclatura GabaritoDokument26 SeitenQuimica Organica Exercicios Classificacao Nomenclatura GabaritoRones DiasNoch keine Bewertungen
- Relatório de Teste de ChamasDokument13 SeitenRelatório de Teste de ChamasJunior SouzaNoch keine Bewertungen
- Quimica Organica Experimental-2001Dokument98 SeitenQuimica Organica Experimental-2001lucaslucas10Noch keine Bewertungen
- Tabela Periódica - 1 SérieDokument22 SeitenTabela Periódica - 1 SérieTatianePintoNoch keine Bewertungen
- Roteiro Determinação FerroDokument2 SeitenRoteiro Determinação FerroLarissa BritoNoch keine Bewertungen
- Apostila Química Geral - 2018 NovoDokument57 SeitenApostila Química Geral - 2018 NovoGabriel LeiteNoch keine Bewertungen
- Apontamento 12 AnoDokument19 SeitenApontamento 12 AnoJoaquim BandeiraNoch keine Bewertungen
- Aula 8 Distorc3a7c3a3o de Jahn TellerDokument18 SeitenAula 8 Distorc3a7c3a3o de Jahn TellerMarcio PereiraNoch keine Bewertungen
- Aula 8Dokument65 SeitenAula 8Luciana GuilhermeNoch keine Bewertungen
- 2011 CQ134 ListaExercicios2Dokument2 Seiten2011 CQ134 ListaExercicios2Luciana GuilhermeNoch keine Bewertungen
- CondutividadeDokument3 SeitenCondutividadeLuciana GuilhermeNoch keine Bewertungen
- Exercícios CalorDokument2 SeitenExercícios CalorLuciana GuilhermeNoch keine Bewertungen
- 1 Lista de ExercíciosDokument3 Seiten1 Lista de ExercíciosLuciana GuilhermeNoch keine Bewertungen
- 1 Lista de Exercícios - Farmácia - 2011Dokument2 Seiten1 Lista de Exercícios - Farmácia - 2011Luciana GuilhermeNoch keine Bewertungen
- Quimica Atividade 12Dokument14 SeitenQuimica Atividade 12Luciana GuilhermeNoch keine Bewertungen
- Aula 4-Metalicas OriginalDokument14 SeitenAula 4-Metalicas OriginalLuciana GuilhermeNoch keine Bewertungen
- BIKEFIT v6.0Dokument1 SeiteBIKEFIT v6.0airtonpaulo2Noch keine Bewertungen
- Homônios Veetais GAS ETILENODokument36 SeitenHomônios Veetais GAS ETILENOCleber AssisNoch keine Bewertungen
- Exercicios - 2 - AlgoritmosDokument3 SeitenExercicios - 2 - AlgoritmosPedro CândidoNoch keine Bewertungen
- DestilacaoDokument6 SeitenDestilacaoMartinõ MarcellNoch keine Bewertungen
- Produção de Conteúdo para Audiência CriativaDokument17 SeitenProdução de Conteúdo para Audiência CriativaJoão Paulo HergeselNoch keine Bewertungen
- #6 Construção de MASMORRAS 1 PGDokument1 Seite#6 Construção de MASMORRAS 1 PGLIE glcNoch keine Bewertungen
- Ebook Estratégias Que Eu Usei para Faturar Mais de 10k Por MêsDokument61 SeitenEbook Estratégias Que Eu Usei para Faturar Mais de 10k Por Mêsju.balanNoch keine Bewertungen
- Modelos de LaudosDokument6 SeitenModelos de Laudoswillams AlvesNoch keine Bewertungen
- Boletim Técnico Textura DesignerDokument3 SeitenBoletim Técnico Textura DesignerGabriel AvelinoNoch keine Bewertungen
- Texto Empuxo e Principio de ArquimedesDokument5 SeitenTexto Empuxo e Principio de ArquimedesAlberto MaiaNoch keine Bewertungen
- Peça de Arquitetura - IniciaçãoDokument1 SeitePeça de Arquitetura - Iniciaçãoleonardo barcelosNoch keine Bewertungen
- Marvel RPGDokument6 SeitenMarvel RPGChaulin Diogo da CostaNoch keine Bewertungen
- 12.07 - PortuguesDokument9 Seiten12.07 - PortuguesMarcos HenriqueNoch keine Bewertungen
- 5 Documentários Brasileiros para Se Refletir Sobre EducaçãoDokument5 Seiten5 Documentários Brasileiros para Se Refletir Sobre EducaçãoAparecida De Fatima Gomes MacaubasNoch keine Bewertungen
- NBR 5858 - 1983Dokument15 SeitenNBR 5858 - 1983telnet837Noch keine Bewertungen
- 2.7 Aula de Laboratório de Anatomia Do Olho e Do Ouvido 2020 Dra. Leny Van SwaaijDokument6 Seiten2.7 Aula de Laboratório de Anatomia Do Olho e Do Ouvido 2020 Dra. Leny Van SwaaijNorvaldo PedroNoch keine Bewertungen
- Formação Serviço AlentejoDokument125 SeitenFormação Serviço AlentejoCrisNoch keine Bewertungen
- Relatório de EstagioDokument14 SeitenRelatório de EstagioCastro Naldo0% (1)
- Analise Corporal 3Dokument34 SeitenAnalise Corporal 3Christiane Barbi100% (1)
- giroscópio2012editadoPDF (Roteiro) III PDFDokument8 Seitengiroscópio2012editadoPDF (Roteiro) III PDFxotunredmailtopNoch keine Bewertungen
- Resolucaotjoe 1 2017 AnexosconsolidadosDokument283 SeitenResolucaotjoe 1 2017 AnexosconsolidadosPaholaNoch keine Bewertungen
- Fundamentos Da Enfermagem - Trabalho FeridasDokument13 SeitenFundamentos Da Enfermagem - Trabalho FeridasVanessa DuarteNoch keine Bewertungen
- Apostila Irrigação 2012Dokument77 SeitenApostila Irrigação 2012anon_140267718Noch keine Bewertungen
- Alcoolismo No TrabalhoDokument18 SeitenAlcoolismo No TrabalhoJuliana SouzaNoch keine Bewertungen
- Apostila Fazendo Seu Dicionario de AcordesDokument8 SeitenApostila Fazendo Seu Dicionario de AcordesNelson PedonNoch keine Bewertungen
- A Importância Da SeletividadeDokument5 SeitenA Importância Da SeletividadeSergio Ricardo NobreNoch keine Bewertungen
- Avaliação - Educação Do Deficiente Físico e Do Múltiplo DeficienteDokument3 SeitenAvaliação - Educação Do Deficiente Físico e Do Múltiplo DeficienteAngelo ParriniNoch keine Bewertungen
- Aula 0 - Equipamentos PDFDokument6 SeitenAula 0 - Equipamentos PDFPaulo VitorNoch keine Bewertungen
- Dilatação Linear de Um Sólido MetálicoDokument9 SeitenDilatação Linear de Um Sólido MetálicoCarlos HenriqueNoch keine Bewertungen
- Bambozzi Talha Eletrica Manual de Instrucao 439850Dokument34 SeitenBambozzi Talha Eletrica Manual de Instrucao 439850MárcioHenriqueNoch keine Bewertungen
- Focar: Supere a procrastinação e aumente a força de vontade e a atençãoVon EverandFocar: Supere a procrastinação e aumente a força de vontade e a atençãoBewertung: 4.5 von 5 Sternen4.5/5 (53)
- Treinamento cerebral: Compreendendo inteligência emocional, atenção e muito maisVon EverandTreinamento cerebral: Compreendendo inteligência emocional, atenção e muito maisBewertung: 4.5 von 5 Sternen4.5/5 (169)
- Os Códigos do Mindset da Prosperidade: destrave os bloqueios em sua mente e cresça em todos os aspectos de sua vidaVon EverandOs Códigos do Mindset da Prosperidade: destrave os bloqueios em sua mente e cresça em todos os aspectos de sua vidaNoch keine Bewertungen
- Técnicas Proibidas de Manipulação Mental e PersuasãoVon EverandTécnicas Proibidas de Manipulação Mental e PersuasãoBewertung: 5 von 5 Sternen5/5 (3)
- Bololô: contém ferramentas de treinamento para pais e filhosVon EverandBololô: contém ferramentas de treinamento para pais e filhosNoch keine Bewertungen
- Psicologia sombria: Poderosas técnicas de controle mental e persuasãoVon EverandPsicologia sombria: Poderosas técnicas de controle mental e persuasãoBewertung: 4 von 5 Sternen4/5 (92)
- Técnicas De Terapia Cognitivo-comportamental (tcc)Von EverandTécnicas De Terapia Cognitivo-comportamental (tcc)Noch keine Bewertungen
- Diálogo entre Terapia do Esquema e Terapia Focada na Compaixão: Contribuição à integração em Psicoterapias Cognitivo-ComportamentaisVon EverandDiálogo entre Terapia do Esquema e Terapia Focada na Compaixão: Contribuição à integração em Psicoterapias Cognitivo-ComportamentaisBewertung: 5 von 5 Sternen5/5 (1)
- Treinamento cerebral: Como funcionam a inteligência e o pensamento cognitivo (2 em 1)Von EverandTreinamento cerebral: Como funcionam a inteligência e o pensamento cognitivo (2 em 1)Bewertung: 4.5 von 5 Sternen4.5/5 (29)
- 35 Técnicas e Curiosidades Mentais: Porque a mente também deve evoluirVon Everand35 Técnicas e Curiosidades Mentais: Porque a mente também deve evoluirBewertung: 5 von 5 Sternen5/5 (3)
- Treino de Habilidades Sociais: processo, avaliação e resultadosVon EverandTreino de Habilidades Sociais: processo, avaliação e resultadosBewertung: 5 von 5 Sternen5/5 (2)
- Biomecânica Básica dos Exercícios: Membros InferioresVon EverandBiomecânica Básica dos Exercícios: Membros InferioresBewertung: 3.5 von 5 Sternen3.5/5 (8)
- Elaboração de programas de ensino: material autoinstrutivoVon EverandElaboração de programas de ensino: material autoinstrutivoNoch keine Bewertungen
- Psicanálise de boteco: O inconsciente na vida cotidianaVon EverandPsicanálise de boteco: O inconsciente na vida cotidianaBewertung: 5 von 5 Sternen5/5 (1)
- Cartas de um terapeuta para seus momentos de criseVon EverandCartas de um terapeuta para seus momentos de criseBewertung: 4 von 5 Sternen4/5 (11)
- Simplificando o Autismo: Para pais, familiares e profissionaisVon EverandSimplificando o Autismo: Para pais, familiares e profissionaisNoch keine Bewertungen