Beruflich Dokumente
Kultur Dokumente
Tabalho Bioquímica Inicio P2 Integração e Regulação Metabólica
Hochgeladen von
Harlyson David BotelhoOriginaltitel
Copyright
Verfügbare Formate
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
Verfügbare Formate
Tabalho Bioquímica Inicio P2 Integração e Regulação Metabólica
Hochgeladen von
Harlyson David BotelhoCopyright:
Verfügbare Formate
FUNDAO UNIRG FACULDADE UNIRG CURSO DE MEDICINA
INTEGRAO DE METABOLISMOS
GURUPI-TO NOVEMBRO DE 2009 DANIELLE FRANCYWAGNER JSSICA WILSON
INTEGRAO DE METABOLISMOS
Trabalho apresentado na disciplina de bioqumica do primeiro perodo do curso de Medicina do Centro Universitrio UNIRG, como requisito parcial de avaliao. Prof. Dr.: Joaquim Penonni
GURUPI-TO NOVEMBRO DE 2009 SUMRIO 1 japiasu, 2 hlio 3 delval 4 jaime 5 alisson 1.Introduo.....................................................................................................4 2.Desenvolvimento..................5 2.1. O metabolismo e suas vias altamente interligada.....................................5 2.1.1 Junes importantes:Glicose-6 Fosfatos, Piruvato, e Acetil..................6 2.1.2. Principais vias metablicas e locais de controle....................................8 2.1.2.1Gliclise................................................................................................8 2.1.2 .2 Ciclo do Acido Ctrico e Fosforilao Oxidativa...............................9 2.1.2.3Via da pentose Fosfato.......................................................................10 2.1.2.4 Gliconeognese..................................................................................10 2.1.2.5.Sntese da Degradao do Glicognio...............................................11 2.1.2.6 Sntese e degradao do acido graxo.................................................11 2.1.3.Regulao metablica...........................................................................12 2.2 Perfil metablico dos rgos...................................................................13 2.2.1Tecido Adiposo..................................................................................... 13 2.2.2.Fgado...................................................................................................14 2.2.3.Crebro.................................................................................................16 2.2.4.Rim.......................................................................................................17 2.2.5.Msculo................................................................................................17 2.3 A ingesto de alimentos e o jejum...........................................................18 2.3.1. estado inicial de jejum.........................................................................18 2.3.2 Os transtornos metablicos do Diabetes resultam da insuficincia relativa da insulina e do excesso de glucagon...............................................20 3
2.3.3 O estado realimentado..........................................................................21 2.3.4.O estado bem alimento (saciado) ou ps - absortivo............................21 2.4. A escolha da fonte de energia.................................................................23 2.5 O etanol e o metabolismo energtico no fgado......................................25 3. Concluso...................................................................................................27 4.Bibliografia.................................................................................................29
1. Introduo.
Para um melhor rendimento energtico, o organismo tem suas principais vias metablicas e seus respectivos locais de controle, o qual s permitido pela capacidade orgnica de sntese e degradao de uma mesma molcula em eventos diferentes. A integrao das diferentes vias metablicas descrita em termos do fluxo de molculas em trs cruzamentos principais: glicose 6-fosfato, piruvato e acetil CoA Em funo dessa variedade de processos o metabolismo se adapta as diferenas estruturais das molculas usadas na produo energtica. E estes processos so regulados a partir do controle do catabolismo e anabolismo. Um grande auxlio para este mecanismo a especializao metablica dos rgos. A principal adaptao dos rgos ocorre a nvel histolgico, existem dois exemplos considerveis: o tecido adiposo que tem como principal especializao a capacidade de armazenar uma grande capacidade de energia em um menor espao; j o fgado responsvel pela parte de metabolizao de substancias como por exemplo a esterificao. Faz-se aqui uma abordagem sobre a diferena nos padres metablicos do crebro, msculo, tecido adiposo e fgado. O rendimento energtico referido depende de uma srie de fatores que aqui sero tratados.
2. Desenvolvimento.
2.1. O metabolismo e suas vias altamente interligadas.
O intuito bsico do catabolismo formar ATP, poder redutor e elementos de construo para as biossnteses. Revisemos resumidamente esses temas centrais: O ATP gerado pela oxidao de molculas energticas, tais como glicose, cidos graxos e aminocidos. O intermedirio comum na maioria destas oxidaes o acetil CoA. Os carbonos de unidade acetila so completamente oxidados a CO2 pelo ciclo do cido ctrico, com formao concomitante de NADH e FADH2. Estes carreadores de eltrons transferem ento seus eltrons de alto potencial cadeia respiratria. O fluxo subseqente de eltrons ao O2 leva ao bombeamento de prtons atravs da membrana interna da mitocndria. Este gradiente ento usado para sintetizar ATP. A gliclise gera tambm ATP, mas a quantidade formada muito menor que na fosforilao oxidativa.A oxidao da glicose a piruvato fornece somente dois ATP, ao passo que 30 ATP so formados quando a glicose completamente oxidada a CO2. O ATP a moeda corrente universal de energia. O alto potencial de transferncia de fosforilas do ATP permite que ele sirva como uma fonte de energia em contrao muscular, transporte ativo, amplificao de sinais e biossnteses. A hidrlise de uma molcula de ATP altera a proporo de equilbrio entre produtos e reagentes em uma reao acoplada. Assim, uma seqncia de reaes termodinamicamente desfavorvel pode tornar-se altamente favorvel pelo acoplamento hidrlise de um nmero suficiente de molculas de ATP. As vias de biossntese e de degradao so quase sempre diferentes. Por exemplo, a via para biossntese de cidos graxos diferente daquela de sua degradao. Esta separao permite s vias de biossntese e degradao serem termodinamicamente favorveis a todo instante. Uma via de 6
biossntese, torna-se exergnica pelo acoplamento hidrlise de uma quantidade suficiente de ATP. A separao das vias de biossntese e de degradao contribui grandemente para a eficcia do controle metablico. As biomolculas so construdas a partir de um conjunto relativamente pequeno de unidades fundamentais. Molculas altamente diferenciadas da vida so sintetizadas a partir de um nmero bem menor de precursores. As vias metablicas que geram ATP e NADPH tambm fornecem as unidades fundamentais para biossnteses de molculas mais complexas. Por exemplo, a acetil CoA, o intermedirio comum na degradao da maioria dos alimentos, supre uma unidade de dois carbonos para uma ampla gama de biossnteses, como as de cidos graxos, prostaglandinas e colesterol. Assim, as vias centrais do metabolismo tm papis anablicos e catablicos. O NADPH o principal doador de eltrons nas biossnteses redutoras. Na maioria das biossnteses, os produtos so mais reduzidos que os precursores, e, deste modo, necessrio poder redutor, alm de ATP. Os eltrons de alto potencial necessrios para acionar essas reaes so, em geral, proporcionados pelo NADPH. A via pentose fosfato supre grande parte do NADPH necessrio do controle metablico.
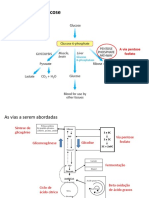
2.1.1. Junes Importantes: Glicose 6-fosfato, Piruvato e Acetil CoA
Os fatores que comandam o fluxo de molculas no metabolismo podem ser mais bem conhecidos pelo exame de trs molculas importantes: glicose 6-fosfato, piruvato e acetil CoA. Cada uma destas molculas tem diversos destinos contrastantes: Glicose 6-fosfato. A glicose que entra em uma clula rapidamente fosforilada a glicose 6-fosfato, que em seguida armazenada como glicognio, degradada a piruvato, ou transformada em ribose 5-fosfato. O glicognio formado quando h fartura de glicose 6-fosfato e ATP. Ao contrrio, a glicose 6-fosfato flui para via glicoltica quando ATP quando esqueletos carbonados so necessrios para biossnteses. Assim, a 7
transformao da glicose 6-fosfato em piruvato pode ser anablica e catablica. O terceiro destino principal da glicose 6-fosfato, fluir atravs da via pentose fosfato, proporciona NADPH para as biossnteses redutoras e ribose 5-fosfato para sntese de nucleotdeos. A glicose 6-fosfato pode ser formada pela mobilizao de glicognio ou pode ser sintetizada a partir de piruvato e aminocidos glicognicos pela gliconeognese. Piruvato. Este a-cetocido com trs carbonos uma outra importante juno metablica. O piruvato derivado primariamente de glicose 6-fosfato, alanina e lactato. Ele pode ser reduzido a lactato pela lactato desidrogenase, regenerando NAD. Esta reao permite gliclise ocorrer temporariamente em condies anaerbias em tecidos ativos, como o msculo em contrao. O lactato formado em tecidos ativos em seguida oxidado de volta para piruvato em outros tecidos. A essncia desta interconverso que ganha tempo e transfere parte da carga metablica do msculo ativo para outros tecidos. Uma outra reao prontamente reversvel no citossol a transaminao do piruvato, um acetocido, para alanina, o aminocido correspondente. Ao contrrio, vrios aminocidos podem ser transformados em piruvato. Assim, a transaminao a principal ligao entre o metabolismo de aminocidos e o de glicdios. Um terceiro destino do piruvato sua carboxilao a oxaloacetato dentro da mitocndria, a primeira etapa da gliconeognese. Esta reao e a transformao subseqente do oxaloacetato em fosfoenolpiruvato contornam uma etapa irreversvel da glicose e, por isto, permitem que a glicose seja sintetizada a partir de piruvato. A carboxilao do piruvato tambm importante para reposio de intermedirios do ciclo do cido ctrico. A acetil CoA ativa a piruvato carboxilase, estimulando a sntese de oxaloacetato quando o ciclo do cido ctrico est lento por uma escassez deste intermedirio. Uma quarto destino do piruvato sua descarboxilao oxidativa a acetil CoA. Esta reao irreversvel no interior da mitocndria uma reao decisiva do metabolismo: entrega os tomos de carbono de glicdeos e aminocidos para oxidao pelo ciclo do cido ctrico ou para sntese de lipdeos. O complexo de piruvato desidrogenase, que catalisa este encaminhamento irreversvel, rigidamente regulado por mltiplas interaes alostricas e modificaes covalentes. O piruvato s prontamente transformado em acetil CoA se o
ATP for necessrio ou se forem necessrios fragmentos de dois carbonos para sntese de lipdeos. Acetil CoA. As principais fontes desta unidade ativada de dois carbonos so a descarboxilao oxidativa do piruvato e a b-oxidao de cidos graxos. A acetil CoA, tambm derivada de aminocidos cetognicos. O destino da acetil CoA, em contraste com o de muitas molculas de metabolismo, bastante restrito. A unidade aceita pode ser completamente oxidada a CO2 pelo ciclo do cido ctrico. Como alternativa, pode-se formar 3-hidroxi 3-metil glutaril CoA a partir de trs molculas de acetil CoA. Esta unidade com seis carbonos um precursor de colesterol de colesterol e de corpos cetnicos; estes ltimos so formas de transporte de unidades acetila liberadas pelo fgado para uso em alguns tecidos perifricos. Um terceiro destino importante da acetil CoA sua exportao para o citossol, na forma de citrato, para a sntese de cidos graxos.
2.1.2. Principais Vias Metablicas e Locais de Controle
2.1.2.1. Gliclise.
Esta seqncia de reaes, no citossol, transforma uma molcula de glicose em duas de piruvato, com gerao concomitante de duas de ATP e duas de NADPH. O NAD consumido na reao catalisada pela gliceraldedo 3-fosfato desidrogenase tem de ser regenerado para prosseguimento da gliclise. Em condies anaerbias, como no msculo esqueltico em grande atividade, isto efetuado pela reduo do piruvato a lactato. Por outro lado, em condies aerbias, o NAD regenerado pela transferncia de eltrons do NADPH ao O2 atravs da cadeia transportadora de eltrons. A gliclise serve para dois propsitos principais: degrada a glicose para gerar ATP e fornece esqueletos carbonados para biossnteses. A fosfofrutocinase, que catalisa a etapa limitante na gliclise, o mais importante local de controle. O ATP no um substrato na reao de transferncia de fosforila, mas tambm uma molcula reguladora. Um nvel alto de ATP inibe a fosfofrutocinase os centros reguladores so distintos dos stios para ligao do substrato e tm uma afinidade 9
menor para o nucleotdeo. Este efeito inibidor acentuado por citrato e revertido por AMP. Assim, a velocidade da gliclise depende da necessidade de ATP, como sinalizado pela relao ATP/AMP, e da necessidade de unidades fundamentais, como sinalizado pelo nvel de citrato. No fgado, o regulador mais importante da atividade da fosfofrutocinase a frutose 2,6-bisfosfato (F-2,6- BP). Lembre-se de que o nvel de F-2,6-BP determinado pela atividade da cinase, que a forma a partir da frutose 6-fosfato, e da fosfatase, que hidrolisa a fosforila no C-2. Quando o nvel da glicose no sangue est baixo, uma cascata disparada pela glucagon leva a ativao desta fosfatase e inibio desta cinase do fgado. O nvel de F-2,6-BP cai e, em conseqncia, a atividade liberada pelo sangue para ser utilizada por outros tecidos. 2.1.2.2. Ciclo do cido ctrico e fosforilao oxidativa.
As reaes desta via comum para oxidao de molculas alimentares glicdeos, aminocidos e cidos graxos ocorrem no interior da mitocndria. A maioria destas molculas entra no ciclo como acetil CoA. A oxidao completa de uma unidade acetila gera uma molcula de GTP e quatro pares de eltrons, na forma de trs molculas de NADH e uma FADH2. Estes eltrons so transferidos ento ao O2 atravs da cadeia e uma de FADH2. Estes eltrons so transferidos ento ao O2 atravs da cadeia transportadora de eltrons, o que resulta na formao de um gradiente de prtons que impulsiona sntese de nove molculas de ATP. Os doadores de eltrons s so oxidados e reciclados de volta ao ciclo do cido ctrico se o ADP for simultaneamente fosforilado a ATP. Este firme acoplamento, chamado controle respiratrio, garante que a velocidade do ciclo do cido ctrico corresponda necessidade de ATP. A fartura de ATP diminui tambm as atividades de duas enzimas do ciclo: isocitrato desidrogenase e cetoglutarato desidrogenase. O ciclo do cido ctrico tambm tem um papel anablico. Em unio com a piruvato carboxilase, o ciclo do cido ctrico fornece intermedirios para biossnteses, tal como succinil CoA para a formao de porfirinas e citrato para formao de cidos graxos.
10
2.1.2.3. Via pentose fosfato.
Esta srie de reaes, que ocorre no citossol, constituda de dois estgios. O primeiro a descarboxilao oxidativa da glicose 6-fosfato. Seu propsito a gerao de NADPH para biossnteses redutoras e formao de ribose 5-fosfato para sntese de nucleotdeos. Dois NADPH so gerados na converso de glicose 6-fosfato ribose 5-fosfato. A desidrogenao da glicose 6-fosfato a etapa reguladora desta via. Esta reao controlada pelo nvel de NADP, o aceptor de eltrons. O segundo estgio da via pentose fosfato o metabolismo reversvel, no oxidativo, de pentoses-fosfato para intermedirios da gliclise com trs e seis carbonos. Assim, o ramo no oxidativo pode introduzir ribose na gliclise para catabolismo, ou gerar ribose para biossnteses a partir de intermedirios da gliclise.
2.1.2.4. Gliconeognese.
A glicose ser sintetizada pelo fgado e pelos rins a partir de precursores no glicdicos, tais como lactato, glicerol e aminocidos. O principal ponto de entrada desta via o piruvato, carboxilado a oxaloacetato na mitocndria.O oxaloacetato ento descarboxilado e fosforilado no citossol, formando fosfoenolpiruvato. As outras reaes caractersticas da gliconeognese so duas etapas de hidrlise que contornam as reaes irreversveis da gliclise. A gliconeognese e a gliclise so, em geral, reguladas reciprocamente, de modo que uma via esteja no mnimo de atividade enquanto a outra estiver muito ativa. Por exemplo, o AMP inibe e o citrato ativa a frutose 1,6-bisfosfatase, uma enzima importante da gliconeognese, ao passo que estas molculas tm efeitos opostos sobre a fosfofrutocinase, o marca-passo da gliclise. A frutose 2,6-bisfosfato tambm coordena esses processos por inibio da frutose 1,6-bisfosfatase. Por isto, quando a glicose farta, o alto nvel de F-2,6-BP inibe a gliconeognese e ativa a gliclise.
11
2.1.2.5. Sntese e degradao do glicognio.
O glicognio, uma reserva energtica prontamente mobilizvel, um polmero ramificado de glicose . Na degradao deste, uma fosforilase catalisa a clivagem do glicognio pelo ortofosfato, dando glicose 1-fosfato, que rapidamente transformada em glicose 6-fosfato, para posterior metabolizao. Na sntese de glicognio, o intermedirio ativado a UDP-glicose, que formada a partir de glicose 1-fosfato e UTP. A glicognio sintase catalisa a transferncia de glicose da UDP-glicose hidroxila terminal de uma cadeia em crescimento. A sntese e a degradao do glicognio so controladas coordenadamente por uma cascata de amplificao disparada por hormnios, de modo que a sintase esteja inativa quando a fosforilase estiver ativa, e vice-versa. A fosforilao e as interaes alostricas regulam estas enzimas.
2.1.2.6. Sntese e degradao de cidos graxos.
Os cidos graxos so sintetizados no citossol pela adio de unidades de dois carbonos a uma cadeia em crescimento ligada a uma protena carreadora de acilas. A malonil CoA . As acetilas so carreadas da mitocndria para o citossol pela lanadeira citrato-malato. No citossol, o citrato clivado originando acetil CoA. Alm do transporte de acetil CoA, o citrato de citossol estimula a acetil CoA carboxilase, a enzima que catalisa a etapa reguladora. Quando ATP acetil CoA so fartos, o nvel de citrato aumenta, o que acelera a velocidade de sntese de cidos graxos. Os cidos graxos so degradados por uma via diferente em um compartimento diferente. A carnitina transporta os cidos graxos para a matriz mitocondrial, onde a so degradados a acetil CoA na matriz mitocondrial, pela b-oxidao. A acetil CoA entra ento no ciclo do cido ctrico, se o suprimento de oxaloacetato for suficiente. Por outro lado, a acetil CoA pode dar origem a corpos cetnicos. O FADH e o NADH, formados na via de b-oxidao, transferem seus eltrons ao O2 atravs da cadeia transportadora de eltrons. Como o ciclo do cido ctrico, a b-oxidao somente pode ocorrer se NAD e FAD forem regenerados. Assim, a velocidade de degradao dos cidos graxos tambm est acoplada 12
necessidade de ATP. A malonil CoA, o percursor para sntese de cidos graxos, inibe a degradao por inibir a formao de acilcarnitina pela carnitina aciltransferase 1,impedindo portanto a translocao de cidos graxos para dentro da mitocndria. 2.1.3. Regulao metablica.
O anabolismo e o catabolismo tm de ser coordenados com preciso. A rede metablica sente a informao do estado de suas vias componentes e responde a ela. A informao recebida e o metabolismo controlado por vrios modos: Interaes alostricas. O fluxo de molculas na maioria das vias metablicas determinado primariamente pelas atividades de determinadas enzimas, mais do que pela quantidade de substrato disponvel. As enzimas que catalisam reaes essencialmente irreversveis so locais provveis de controle. A primeira reao irreversvel em uma via metablica (etapa reguladora, ou limitante, ou comprometida) quase sempre firmemente controlada. As enzimas que catalisam as etapas limitantes so reguladas alostericamente, como exemplificado pela fosfofrutocinase na gliclise e pela acetil CoA carboxilase na sntese de cidos graxos. Interaes alostricas permitem a tais enzimas detectar rapidamente diversos sinais e ajustar sua atividade de acordo. Modificao covalente. Algumas enzimas reguladoras so controladas por modificao covalente, alm das interaes alostricas. Por exemplo, a atividade cataltica da glicognio fosforilase aumentada por fosforilao, ao passo que aquela da glicognio sintase diminuda. Enzimas especficas catalisam a adio e a remoo destes grupamentos modificadores. Por que a modificao covalente usada, alm do controle alostrico no covalente? A modificao covalente de uma enzima essencial em uma via com freqncia o estgio final de uma cascata de amplificao, e permite s reaes serem rapidamente ligadas ou desligadas por sinais de disparo em muito baixa concentrao. Tambm, as modificaes covalentes so, em geral, mais duradouras (segundos a minutos ) do que as interaes alostricas reversveis (milissegundos a segundos).
13
Nveis enzimticos. As quantidades de enzimas, bem como suas atividades, so controladas. As velocidades de sntese e degradao de muitas enzimas reguladoras so alteradas por hormnios.
Compartimentao.
Os
padres
metablicos
de
clulas
eucariticas
so
marcadamente afetados pela presena de compartimentos. Os destinos de certas molculas dependem de elas estarem no citossol ou na mitocndria, e por isso seus fluxos atravs da membrana mitocondrial interna so freqentemente controlados. Por exemplo, os cidos graxos s so transportados para mitocndria para degradao quando necessria energia, ao passo que os cidos graxos no citossol so esterificados ou exportados. Especializao metablica dos rgos. A regulao e eucariontes superiores acentuada pela existncia de rgos com diferentes papis metablicos. A especializao metablica o resultado da expresso gnica diferenciada.
2.2. Perfil metablico dos rgos
Os padres metablicos do crebro, msculo, tecido adiposo e fgado so notavelmente diferentes. Consideraremos como estes tecidos diferem no uso dos alimentos para satisfazer as suas necessidades energticas. 2.2.1. Tecido adiposo.
Os triacilgliceris no tecido adiposo constituem imenso reservatrio de energia metablica. Num homem adulto de 70kg, os 15kg de triacilgliceris tm um contedo energtico de 135.000 kcal, (565.000 kj ). O tecido adiposo especializado para esterificao de cidos graxos e para sua liberao a partir de triacilgliceris. Em seres humanos, o fgado o principal de snteses de cidos graxos. Relembre que estes cidos graxos so esterificados no fgado, com o glicerol fosfato formando triacilglicerol, e so transportados ao tecido adiposo por partculas de lipoprotenas, tais como lipoprotena de muita baixa densidade . Os triacilgliceris no so captados pelos adipcitos e sim so antes hidrolisados por uma lipoprotena lpase extracelular para captao. Esta lpase 14
iniciada por processos iniciados pela insulina. Aps os cidos graxos entrarem na clula, a principal tarefa do tecido adiposo ativ-los e transferir os derivados resultantes de CoA ao glicerol, na forma de glicerol 3-fosfato. Este intermedirio essencial na biossntese de lipdios provm da reduo da di-hidroxiacetona fosfato, um intermedirio da gliclise. Portanto, as clulas adiposas necessitam de glicose para sintetizar triacilglicerol. Os triacilgliceris so hidrolisados para os cidos graxos e glicerol por lpases intracelulares. A liberao do primeiro cido graxo de um triacilglicerol, etapa limitante de velocidade, catalisada por uma lpase hormnio-sensvel, de fosforilao reversvel. O hormnio epinefrina estimula a formao de AMP cclico, o mensageiro intracelular amplificador da cascata que ativa uma protena cinase um tema repetitivo na ao hormonal. Os triacilgliceris no tecido adiposo esto sendo continuamente hidrolisados e ressintetizados.O glicerol derivado dessa hidrlise transportado para o fgado. A maior parte dos cidos graxos formados na hidrlise esterificada se o glicerol 3-fosfato for farto. Ao contrrio, eles so liberados no plasma se o glicerol 3-fosfato for escasso por causa da falta de glicose. Assim, o nvel de glicose dentro das clulas adiposas um dos fatores principais na determinao de se os cidos graxos so liberados no sangue. 2.2.2. Fgado.
As atividades metablicas do fgado so essenciais para o provimento de material energtico para o crebro, msculo e outros rgos perifricos. De fato, o fgado, que pode ter de 2 % a 4% do peso corporal, a usina metablica do organismo. A maior parte dos compostos absorvidos no intestinos passa atravs do fgado, o que permite que ele regule o nvel de muitos metablitos no sangue. Consideremos inicialmente como o fgado metaboliza glicdeos. Ele remove dois teros da glicose do sangue e todas as outras oses restantes. Alguma glicose deixada no sangue por outros tecidos. A glicose absorvida transformada em glicose 6-fosfato pela hexocinase e pela glicocinase especfica do fgado. A glicose 6-fosfato, como j dito, tem uma gama de destinos, embora o fgado utilize-a pouco para prover suas prprias necessidades energticas. A maior parte da glicose 6-fosfato convertida a glicognio. At 400 kcal (1.700 kj) podem ser armazenadas dessa maneira. O excesso de glicose 6-fosfato metabolizado a acetil CoA, que usada para formar cidos graxos,colesterol e sais biliares. 15
A via pentose fosfato, um outro meio de processar a glicose 6-fosfato, supre o NADPH para estas biossnteses redutoras. O fgado poder produzir glicose para liberao no sangue, pela degradao de suas reservas de glicognio e por executar a gliconeognese. Os principais precursores da gliconeognese so lactato e alanina a partir do msculo, glicerol a partir do tecido adiposo e aminocidos glicognicos a partir da dieta. O fgado tambm desempenha um papel central na regulao do metabolismo lipdico. Quando h alimento abundante, os cidos graxos derivados da dieta ou sintetizados pelo fgado so esterificados e secretados no sangue na forma de lipoprotenas de muito baixa densidade. Contudo, no jejum, o fgado transforma os cidos graxos em corpos cetnicos. Como determinado o destino dos cidos graxos no fgado? A seleo feita de acordo com a entrada de cidos graxos na matriz mitocondrial. Lembre-se de que os cidos de cadeia longa s atravessam a membrana mitocondrial interna se estiverem esterificados carnitina. A carnitina aciltransferase I (tambm conhecida como carnitina palmitil transferase I ) que catalisa a formao da acilcarnitina, inibida pela malonil CoA, o intermedirio comprometido na sntese de cidos graxos. Assim, quando a malonil CoA farta, os cidos graxos de cadeia longa so impedidos de entrar na matriz mitocondrial, o compartimento da b-oxidao e da formao de corpos cetnicos. Em vez disto, os cidos graxos so exportados para o tecido adiposo, para incorporao em triacilgliceris. Ao contrrio, o nvel de malonil CoA est baixo quando os alimentos esto escassos. Nestas condies, os cidos graxos liberados do tecido adiposo entram na matriz mitocondrial para converso a corpos cetnicos. O fgado tambm desempenha um papel essencial no metabolismo dos aminocidos alimentares. Ele absorve a maior parte dos aminocidos, deixando um pouco no sangue para os tecidos perifricos. O uso prioritrio dos aminocidos para a sntese de protena e no para o catabolismo. Por qual mecanismo so os aminocidos direcionados para sntese de protenas em preferncia a seu uso como fonte de energia? O valor de Km para os aminoacil-tRNA sintetases mais baixo do que o das enzimas que tomam parte do catabolismo dos aminocidos. Assim, os aminocidos so utilizados para sintetizar aminoacil-tRNAs antes de serem catabolizados. Quando ocorre o catabolismo, a primeira etapa a remoo do nitrognio, que a seguir processado a uria. O fgado secreta de 20 a 30g de uria por dia. Os a-cetocidos so a seguir usados para a gliconeognese ou para a 16
sntese de cidos graxos. De maneira interessante, o fgado no pode remover o nitrognio dos aminocidos ramificados (leucina, isoleucina e valina). A transaminao destes ocorre no msculo. Como o fgado satisfaz s suas prprias necessidades energticas? Os a-cetocidos derivados da degradao dos aminocidos so a fonte de energia do prprio fgado. De fato, a finalidade principal da gliclise no fgado formar blocos de construo para biossnteses. Outrossim, o fgado no pode usar acetoacetato como alimento, porque tem pouco da transferase necessria para sua ativao a acetil CoA. Assim, ele se abstm dos alimentos que exporta para o msculo e o crebro.
2.2.3. Crebro.
A glicose virtualmente o nico alimento para o crebro humano, exceto durante o jejum prolongado.O crebro no tem reservas energticas e, por isto, necessita de um suprimento contnuo de glicose. Ele consome cerca de 120 g diariamente, o que corresponde a uma captao de energia de aproximadamente 420 kcal (1.760 kj), o que d conta de cerca de 60% da utilizao de glicose por todo organismo no estado de repouso.Estimativas sugerem que a maior parte desta energia, de 60% a 70%, utilizada para impulsionar mecanismos de transporte que mantm o potencial Na+ -k+ de membrana, necessrio transmisso de impulsos nervosos. O crebro tambm tem de sintetizar neurotransmissores e seus receptores para propagar os impulsos nervosos. Globalmente, o metabolismo da glicose permanece inalterado durante a atividade mental, embora aumentos locais sejam detectados quando uma pessoa executa certas tarefas. A glicose transportada pelas clulas cerebrais pelo transportador de glicose GLUT3. Este transportador tem uma baixa km para a glicose (1,6 mM), o que significa que est saturado na maioria das condies. Portanto, geralmente fornecido um suprimento constante de glicose ao crebro. Medidas invasoras de ressonncia nuclear magntica com 13C mostraram que a concentrao de glicose no crebro cerca de 1 mM quando o nvel plasmtico de 4,7 mM (84,7mg/ dl) , um valor normal. A gliclise fica mais lenta quando o nvel de glicose aproxima-se do Km da hexocinase, a enzima que captura glicose na 17
clula. Este ponto perigoso alcanado quando o nvel plasmtico de glicose cai abaixo de cerca de 2 mm (39,6 mg /dl) e portanto se aproxima do valor de Km do GLUT3. Os cidos graxos no servem como fontes de energia de crebro, porque esto ligados albumina no plasma e, deste modo, no atravessam a barreira hemato-enceflica. Em jejum, os corpos cetnicos gerados do fgado substituem parcialmente a glicose como alimento para o crebro. 2.2.4. Rim.
O propsito principal do rim produzir urina, que serve como veculo para excreo de produtos indesejados do metabolismo e mantenedor osmolaridade dos lquidos corporais. O plasma sanguneo filtrado quase 60 vezes ao dia nos tbulos renais. A maior parte do material filtrado do sangue reabsorvida, somente 1 a 2 litros de urina produzida. Materiais hidrossolveis no plasma, como glicose e a prpria gua, so reabsorvidos para impedir perda devastadora. Os rins necessitam grande quantidade de energia para cumprirem a reabsoro. Embora constituindo somente 0.5% da massa corporal, os rins consomem 10% do oxignio utilizado na respirao celular. Grande parte da glicose que reabsorvida transportada para dentro das clulas renais pelo cotransportador de sdio e glicose. Lembre-se que este transportador impulsionado pelo gradiente de Na+ e k+ , que ele prprio mantido pela Na+ e K+ ATPase . Durante o jejum prolongado, o rim torna-se um local importante de gliconeognese, e pode contribuir com a metade da glicose sangnea.
2.2.5. Msculo.
Os principais alimentos para o msculo so glicoses, cidos graxos e corpos cetnicos. O msculo difere do crebro por ter grande depsito de glicognio (1.200 kcal ou 5.000 kj). De fato, cerca de trs quartos do glicognio do organismo esto armazenados no msculo. Este glicognio prontamente transformado em glicose 6-fosfato para uso dentro de clulas musculares. O msculo, como crebro, no possui glicose 6-fosfatase e 18
assim no exporta glicose. Melhor, o msculo retm glicose, sua principal fonte de energia, para exploses de atividade. No msculo esqueltico em contrao ativa, a velocidade da glicose excede aquela do ciclo do cido ctrico, e muito do piruvato formada nessas condies reduzido a lactato, do qual uma parte flui para o fgado, onde transformado em glicose. Estas permutas, conhecidas como ciclo de Cori, transferem parte da carga metablica do msculo para o fgado. Alm disso, grande quantidade de alanina, formada no msculo ativo, por transaminao do piruvato. A alanina, como lactato, pode ser transformada em glicose pelo fgado. Por que o msculo libera alanina? O msculo pode absorver e transaminar aminocidos de cadeia ramificada, contudo no pode formar uria. Em conseqncia, o nitrognio liberado no sangue como alanina. O fgado absorve alanina, remove o nitrognio para excret-lo como uria e processa a piruvato a glicose ou cidos graxos. O padro metablico do msculo em repouso bem diferente. No msculo em repouso, os cidos graxos so as principais fontes de energia, proporcionando 85% das necessidades energticas. Diferente do msculo esqueltico, o msculo cardaco funciona quase exclusivamente em aerobiose, como evidenciado pela sua densidade de mitocndrias. Alm disso, o corao no tem reservas de glicognio. Os cidos graxos so as principais fontes de energia do corao, embora os corpos cetnicos, assim como o lactato, possam servir como fonte de energia para o msculo cardaco. De fato, o msculo cardaco consome acetoacetato de preferncia a glicose.
2.3. A ingesto de alimentos e o jejum.
Abordemos agora as respostas bioqumicas a uma srie de condies fisiolgicas. Nosso primeiro exemplo o ciclo fome-saciedade de que todos ns temos experincia nas horas aps uma ceia e durante o jejum noturno. Este ciclo tem trs estgios. O estado psabsortivo aps uma refeio, o incio do jejum durante noite e o estado de volta a saciedade aps o desjejum (refeio matinal). Um princpio objetivo de muitas alteraes bioqumicas neste perodo manter a homeostase da glicose, isto , um nvel constante de glicose sangunea (glicemia). 19
2.3.1. Estado inicial de jejum.
O nvel sangneo de glicose comea a cair algumas horas aps uma refeio, levando a uma diminuio na secreo de insulina e uma elevao na secxreo de glucagon, este secretado pelas clulas a do pncreas em resposta a um baixo nvel glicmico no perodo de jejum. Exatamente como a insulina sinaliza o estado de saciedade, o glucagon sinaliza o estado de jejum. Ele serve para mobilizaras reservas de glicognio quando no h ingesto alimentar de glicose. O principal rgo-alvo do glucagon o fgado. Este hormnio estimula a quebra e inibe a sntese de glicognio por disparar a cascata de AMP cclico, que leva fosforilao e ativao da fosforilase e inibio da glicognio sintase. O glucagon inibe tambm a sntese de cidos graxos por diminuir a produo de piruvato e a atividade da acetil CoA carboxilase, por mant-la em um estado no fosforilado. Alm disto, o glucagon estimula a gliconeognese e bloqueia a gliclise por reduzir o nvel de F-2,6-BP. Todas as aes conhecidas do glucagon so mediadas por protena cinases ativadas pelo AMP cclico. A ativao da cascata de cAMP resulta em alto nvel de atividade de fosforilase a e um nvel mais baixo de atividade de glicognio sintase a. O efeito do glucagon nesta cascata reforado pela diminuio de ligao de glicose fosforilase a, o que o torna menos suscetvel ao hidroltica da fosfatase. Em vez disto, a fosfatase permanece ligada a fosforilase a e, deste modo, a sintase fica na forma fosforilada inativa. Em conseqncia, h uma rpida mobilizao de glicognio. A grande quantidade de glicose formada pela hidrlise da glicose 6-fosfato derivada do glicognio liberada ento do fgado para o sangue. A entrada de glicose no msculo e no tecido adiposo diminui, em resposta a um nvel baixo de insulina. A utilizao diminuda de glicose pelo msculo e pelo tecido adiposo tambm contribui para a manuteno do nvel plasmtico de glicose. O resultado global dessas aes do glucagon aumentar de modo marcante a liberao de glicose pelo fgado. Tanto o fgado como os msculos utilizam cidos graxos como fonte de energia quando cai o nvel sanguneo de glicose. Portanto, o nvel sanguneo de glicose mantido em torno de 80 mg/ dl, ou acima, por trs fatores principais: (1) a mobilizao de glicognio e a liberao de glicose pelo fgado, (2) a liberao de cidos graxos pelo tecido 20
adiposo, e (3) o desvio do alimento utilizado, de glicose para cidos graxos, pelo msculo e pelo fgado. Qual o resultado do esgotamento das reservas hepticas de glicognio? A gliconeognese a partir de lactato e alanina continua, mas este processo simplesmente retorna a glicose que j foi transformada em lactato e alanina pelos tecidos perifricos. Alm disto, o crebro oxida glicose completamente a CO2 e H2O. Portanto, para ocorrer a sntese global de glicose, uma outra fonte necessria. O glicerol liberado pelo tecido adiposo durante a liplise fornece alguns dos carbonos, sendo os carbonos restantes provenientes da hidrlise das protenas musculares. 2.3.2. Os transtornos metablicos no Diabetes resultam da insuficincia relativa de insulina e do excesso de glucagon.
Diabetes mellitus, uma doena complexa caracterizada pelo uso bem anormal de alimentos: a glicose superproduzida pelo fgado e subutilizada pelos outros rgos. A incidncia de diabetes mellitus de aproximadamente 5% da populao. De fato, o diabetes a doena metablica sria mais comum no mundo. O diabetes do tipo I, ou diabetes mellitus dependente de insulina (DMDI), causada pela destruio auto-imune das clulas beta do pncreas, que secretam insulina, e geralmente comea antes dos 20 anos. Ao contrrio, a maioria dos diabticos tem um nvel normal ou mesmo mais elevado de insulina no seu sangue, mas no respondem bem ao hormnio. Esta forma de diabetes, conhecida como diabetes mellitus do tipo II, ou independente de insulina (DMII), surge mais tarde na vida do que a forma dependente de insulina. No diabetes do tipo I, a insulina est ausente, e em conseqncia o glucagon est presente em nveis acima do normal. Em essncia, a pessoa diabtica est num modo de jejum bioqumico apesar da alta concentrao sangunea de glicose. Devido insulina ser deficiente, a entrada de glicose nas clulas est prejudicada. O fgado fica preso em um estado de gliconeognese e cetognese. O nvel excessivo de glucagon em relao ao de insulina leva a um decrscimo da quantidade de F-2,6-BP no fgado. Por isso a gliclise inibida e a gliconeognese estimulada por causa dos efeitos opostos da F-2,6-BP sobre a fosfofrutocinas e a frutose 1,6 bifosfatase. A alta relao glucagon/insulina no diabetes tambm promove a quebra de glicognio. Por isso uma quantidade excessiva de glicose 21
produzida pelo fgado e liberada no sangue, a glicose excretada na urina (da o nome mellitus) quando sua concentrao no sangue excede a capacidade de reabsoro dos tbulos renais, a gua acompanha a glicose excretada, e assim um diabtico no tratado, na fase aguda da doena, tem fome e sede. Devido utilizao de glicdeos estar diminuda, a falta de insulina leva quebra descontrolada de lipdeos e protenas. Grandes quantidades de Acetil CoA so ento produzidas pela beta-oxidao. Contudo, muito da acetil CoA no pode entrar no ciclo do cido ctrico, por que h insuficiente oxalacetato para a etapa de condensao. Lembre-se de que os mamferos podem sintetizar oxalacetato a partir de piruvato, um produto da gliclise, mas no apartir de acetil CoA; em vez disso, geram corpos cetnicos. Um aspecto notvel do diabetes a mudana no uso de alimento, de glicdios para lipdeos, a glicose, mais abundante que nunca, desprezada. Em altas concentraes, os corpos cetnicos suplantam a capacidade dos rins de manter o equilbrio cido-base. O diabtico no tratado pode entrar em coma, por causa da diminuio do pH sanguneo e da desidratao. O diabetes do tipo II, ou independente da insulina, responsvel por mais de 90% dos casos, e geralmente desenvolve-se em pessoas de meia-idade e obesas. A causa exata de diabetes do tipo II permanece por ser elucidada, embora parea ser provvel uma base gentica.
2.3.3. O estado realimentado.
Quais so as respostas bioqumicas a uma refeio matinal abundante? Os lipdeos so processados exatamente como quando do estado de saciedade normal. Contudo no este o caso da glicose. O fgado inicialmente no absorve glicose diretamente no sangue, e sim a deixa para os tecidos perifricos. Alm disto, ele permanece em um modo de gliconeognese. Contudo agora, a glicose recm-sintetizada utilizada para repor as reservas hepticas de glicognio. A medida que os nveis sanguneos de glicose continuam a se elevar, o fgado completa a reposio de suas reservas de glicognio e comea a processar o excesso restante de glicose para a sntese de cidos graxos.
22
2.3.4. O estado bem alimentado (saciado) ou ps-absortivo.
Aps consumirmos e digerirmos uma alimentao leve noturna, a glicose e os aminocidos so transportados no intestino para o sangue. Os lipdios alimentares so embalados dentro de quilomcrons e transportados para o sangue atravs do sistema linftico. Esta condio de saciedade leva a secreo de insulina, que um dos dois mais importantes reguladores do metabolismo energtico, sendo o glucagon o outro. A secreo de insulina pela clula b do pncreas estimulada pela glicose e pelo sistema nervoso parassimptico. Em essncia, a insulina sinaliza o estado alimentado: estimula o armazenamento de alimentos e a sntese de protena, de vrios modos. Por exemplo, a insulina d incio a cascatas de protena cinases: estimula a sntese de glicognio em msculo fgado, e suprime a gliconeognese pelo fgado. Ela tambm acelera a gliclise no fgado, o que, por sua vez, aumenta a sntese de cidos graxos. O fgado ajuda a limitar a quantidade de glicose no sangue durante os perodos de fartura, armazenando-a como glicognio, e assim ser capaz de liberar glicose em tempo de escassez. Como removido o excesso de glicose presente no sangue aps uma refeio? A insulina acelera a captao da glicose sangunea no fgado pelo GLUT2. O nvel de glicose 6-fosfato no fgado eleva-se porque s ento os centros catalticos da glicocinase estaro repletos de glicose. Relembre que a glicocinase s ativa quando os nveis sanguneos de glicose esto altos. Em conseqncia, o fgado forma glicose 6-fosfato mais rapidamente, medida em que se elevam os nveis sanguneos de glicose. O aumento de glicose 6-fosfato acoplado ao de insulina leva a uma elevao de reservas de glicognio. Os efeitos hormonais sobre a sntese e o armazenamento de glicognio so reforados por uma ao direta da prpria glicose. A fosforilase um sensor de glicose, alm do seu papel de clivar o glicognio. Quando o nvel de glicose est alto, a ligao da glicose fosforilase a torna a enzima susceptvel ao da fosfatase que transforma em fosforilase b, que no degrada prontamente o glicognio. Assim, a glicose, por efeito alostrico, desvia o sistema de glicognio de um modo de degradao para uma sntese. O alto nvel de insulina no estado de saciedade promove a entrada de glicose no msculo e no tecido adiposo. A insulina estimula a sntese de glicognio tanto no fgado 23
como no msculo. A entrada de glicose no tecido adiposo fornece glicerol 3-fosfato para sntese de triacilgliceris. A ao de insulina tambm se estende ao metabolismo de aminocidos e de protenas. Ela promove a captao de aminocidos ramificados (valina, leucina e isoleucina) pelo msculo. Realmente, a insulina tem um efeito estimulador geral sobre a sntese de protenas, que favorece a construo das protenas musculares. Alm disto, inibe a degradao intracelular de protenas. 2.4. A escolha da fonte de energia. As fontes de energia utilizadas em exerccios anaerbios por exemplo, uma corrida de 100 m diferem daquelas usadas em exerccios aerbios como a corrida em distncia. A seleo dos alimentos para essas formas diferentes de exerccio ilustra muitas facetas importantes da transformao de energia e da integrao do metabolismo. O ATP impulsiona diretamente a miosina, a protena responsvel de modo imediato pela transformao de energia qumica em movimento. Contudo, a quantidade de ATP no msculo pequena. Por isto, a produo de potncia e, por sua vez, a velocidade de corrida dependem da taxa de produo de ATP a partir de outras fontes. A creatina fosfato (fosfocreatina) pode transferir rapidamente sua fosforila de alto potencial para o ADP, a fim de gerar ATP. Contudo, a quantidade de creatina fosfato, como a do prprio ATP, limitada. A creatina fosfato e o ATP podem impulsionar uma intensa contrao muscular por 5 a 6 s. A velocidade mxima em um sprint (arrancada) pode portanto ser mantida somente por 5 ou 6 s. Portanto, o vencedor de uma corrida de 100 m o que por ltimo retarda a marcha. Uma arrancada de 100 m impulsionada pelas reservas de ATP e creatina fosfato, e pela gliclise anaerbia do glicognio muscular. A converso de glicognio muscular a lactato pode gerar bem mais ATP, mas a velocidade menor do que a transferncia da fosforila da creatina fosfato. Durante uma segunda arrancada de ~10 segundos, o nvel de ATP no msculo cai de 5,2 para 3,7 mM, e aquele da cretina fosfato de 9,1 para 2,6. O papel essencial da gliclise anaerbia aqui refletido na elevao do nvel sanguneo de lactato de 1,6 para 8,3 mM. A liberao de H+ do msculo em atividade intensa cai concomitantemente: o pH do sangue vai de 7,42 para 7,24. Este passo no pode ser mantido 24
em uma corrida de 1.000 metros (~132 s), por duas razes. Primeira, a creatina fosfato seria consumida dentro de poucos segundos. Segunda, o lactato produzido causaria acidose. Portanto, so necessrias fontes alternativas de energia. A oxidao completa do glicognio muscular a CO2 aumenta substancialmente a energia produzida, mas este processo aerbio substancialmente mais lento do que a gliclise anaerbia. Contudo, quando aumenta a distncia de uma corrida, a respirao aerbia, ou fosforilao oxidativa, torna-se muito importante. Por exemplo, parte do ATP consumido em uma corrida de 1.000 metros tem de vir da fosforilao oxidativa. Porque o ATP produzido mais lentamente pela fosforilao oxidativa do que pela gliclise, o passo necessariamente mais lento do que em uma arrancada de 100 metros. A velocidade do campeo para 1.000 metros de 7,6 m/s, em comparao com 10,2 m/s para o evento de 100 metros. A corrida de uma maratona (42.200 metros ou 26 milhas e 385 jardas) necessita de uma seleo diferente de alimentos e caracteriza-se pela cooperao de msculo, fgado e tecido adiposo. O glicognio heptico complementa o muscular como reserva de energia que pode ser mobilizada. Contudo, as reservas totais de glicognio (103 moles de ATP, quando muito) so suficientes para fornecer 150 moles de ATP necessrios para esta extenuante competio de ~2 horas. Quantidades muito maiores de ATP podem ser obtidas de oxidao de cidos graxos derivados da quebra de lipdeos no tecido adiposo, mas a velocidade mxima de gerao de ATP mais lenta do que a oxidao do glicognio, e mais de dez vezes mais lenta do que a com creatina fosfato. Portanto, o ATP gerado muito mais lentamente das reservas de alta capacidade do que daquelas que so limitadas, explicando as diferentes velocidades dos eventos anaerbios e aerbios. A gerao de ATP a partir dos cidos graxos essencial para a corrida de distncia. Contudo, uma maratona deveria levar cerca de 6 horas se todo o ATP viesse da oxidao do glicognio. Os melhores corredores consomem quantidades aproximadamente iguais de glicognio e cidos graxos durante uma maratona, para obter uma velocidade mdia de 5.5 m/s, aproximadamente metade daquela de uma arrancada de 100 metros. Como obtida uma mistura tima destes alimentos? Um nvel glicdico baixo no sangue leva a uma alta relao glucagon/insulina, o que, por sua vez, mobiliza os cidos graxos do tecido adiposo. Os cidos graxos entram prontamente no msculo, onde so degradados, por b-oxidao, a 25
acetil CoA e ento a CO2. O nvel elevado de acetil CoA diminui a atividade do complexo de piruvato desidrogenase, bloqueando a converso do piruvato a acetil CoA. Por isto, a oxidao de cidos graxos diminui o encaminhamento de oses para o ciclo do cido ctrico e para a fosforilao oxidativa. A glicose poupada, de modo que permanea disponvel o suficiente para o final da maratona. O uso simultneo de ambas as fontes de energia permite uma velocidade mdia maior do que a que seria alcanada se o glicognio fosse totalmente consumido antes de comear a oxidao dos cidos graxos. 2.5. O etanol e o metabolismo energtico no fgado. O etanol faz parte da alimentao humana h sculos. Contudo, seu consumo em excesso pode resultar em uma gama de problemas de sade, de modo mais notvel, leso heptica. Qual a base bioqumica desses problemas de sade? O etanol no pode ser excretado e tem de ser metabolizado, principalmente pelo fgado. O metabolismo ocorre por duas vias. A primeira compreende duas etapas. A primeira etapa catalisa pela lcool desidrogenase, ocorre no citoplasma. Observe que o consumo de etanol leva a um acmulo de NADH. Esta alta concentrao de NADH inibe a gliconeognese por impedir a oxidao do lactato a piruvato. De fato, as altas concentraes de NADH faro predominar a reao inversa, e o lactato acumular-se-. As conseqncias podem ser hipoglicemia e acidose ltica. A fartura de NADH tambm inibe a oxidao de cidos graxos. O propsito metablico da oxidao de cidos graxos gerar NADH para produo de ATP pela fosforilao oxidativa, mas as necessidades de NADH de um consumidor de lcool so proporcionadas pelo metabolismo do etanol. De fato, o excesso de NADH sinaliza que as condies direcionam-se para a sntese de cidos graxos. Da, acumulam-se triacilgliceris no fgado, conduzindo a uma condio desconhecida como fgado gorduroso (esteatose heptica). A segunda via para o metabolismo do etanol dita sistema microssmico oxidante de etanol, induzvel pelo etanol (MEOS, do ingls, Microsomal Ethanol-Oxidizing System). Esta via depende do citocromo,gera DPH, se oxida a NADP+. Como ela utiliza oxignio, esta via gera radicais livres que lesam os tecidos. Alm do mais, porque o sistema 26
consome NADPH, o antioxidante glutatio no pode ser regenerado, exacerbando a agresso oxidativa. Quais so os efeitos dos outros metablitos do etanol? As mitocndrias hepticas podem transformar acetato em acetil CoA, em uma reao que necessita de ATP. A enzima a tiocinase que normalmente ativa os cidos graxos de cadeia curta. Contudo, o posterior processamento da acetil CoA pelo ciclo de krebs bloqueado, devido ao NADH inibir duas enzimas reguladoras importantes isocitrato desidrogenase e a-cetoglutarato desidrogenase. O acmulo de acetil CoA tem vrias conseqncias. Primeira: Formar-se-o corpos cetnicos e sero liberados no sangue, exacerbando a acidose j resultante da alta concentrao de lactato. O processamento de acetato no fgado torna-se ineficiente, levando a uma formao de aldedo actico. Este composto muito reativo forma ligaes covalentes com muitos grupamentos funcionais na protenas, bloqueando a funo proteica. Se o etanol for consumido continuadamente em altos nveis,o aldedo actico pode lesar o fgado de modo significante, levando eventualmente morte celular. A leso heptica pelo consumo excessivo de lcool ocorre em trs estgios. O primeiro estgio j mencionado o desenvolvimento do fgado gorduroso. No segundo estgio hepatite alcolica grupos de clulas morrem e resulta inflamao. Este estgio por si s pode ser fatal. No terceiro estgio cirrose estruturas fibrosas e tecido cicatricial so produzidos ao redor das clulas mortas. A cirrose bloqueia muitas funes bioqumicas do fgado. O fgado cirrtico incapaz de transformar amnia em uria, e elevam-se os nveis sanguneos de amnia. A amnia txica ao sistema nervoso e pode causar coma e morte. A cirrose heptica surge em cerca de 25% dos alcolatras, e cerca de 75% dos casos de cirrose heptica so resultado do alcoolismo. A hepatite por vrus uma causa no alcolica do fgado cirrtico.
27
3. Concluso. Podemos concluir que o catabolismo gira em torno da formao de ATP e elementos precursores para as biossinteses, como acetil CoA que um intermedirio comum na maioria das oscilaes de molculas energticas. A formao de ATP priorizada no metabolismo que ocorre no nosso organismo, pois este utilizado como fonte energtica para o organismo realizar suas funes, mecanismo permitido pelo alto potencial de transferencia de fosforela. A eficcia do controle metablico d-se pela separao da via da biossintese da degradao molecular, a qual vantajosa a nosso organismo pela independencia entre si. A biossintese ocorre devido ao confronto de molculas que de acordo com a organizao e as enzimas atuantes formam molculas mais complexas, utilizadas para as mais diversas finalidades do organismo do indivduo. Estas molculas so como combustveis, a maior delas a glicose, que utilizada por rgos de grande atividade metablica como o crebro. O fgado e os msculos,por exemplo, possuem a capacidade de armazenamento de glicose na forma de glicogenio. J o cerebro no consegue armazenar a glicose em seu tecido, mesmo tendo a necessidade de consumi-lo em sua manuteno metabolica e na sintese de neurotransmissores. Porm im portante ressaltar a manuteno dos hormonios insulina e glucagon no ciclo fome-saciedade e na manuteno da glicemia, que quando no ;e mantido, tem se o quadro de diabetes, podendo ser de dois tipos: tipo 1, ou diabetes Mellitus, dependente de insulina e a do tipo 2, ou independente de insulina. Em ambos os tipos o diabtico encontra-se em jejum bioquimico, pois h alta concentrao de glicose no sangue, mas a deficiencia de insulina prejudica a entrada de glicose nas clulas. Nessa situao, o organismo usa como fonte de energia a quebra de lideos e protenas. Sendo assim a insulina um dos dois mais importantes reguladores do metabolismo energtico.
28
Para fazer o equilbrio entre consumo e produo energtica, nosso organismo analisa : quantidade de energia produzida , matria prima que ser utilizada ( aspectos quantitativos e qualitativos) e a velocidade com que o ATP ser produzido e consumido. Como analisado neste material, os processo que nosso organismo capaz de fazer, muitas vezes so realizados isoladamente. Porm, se a situao for de esforo extremo e prolongado, ocorre mistura de processos. No podemos deixar de citar o o papel singular do tecido muscular, adiposo e fgado nesta alternancia de metabolismo. Salientando a histrica agresso do fgado pelo etanol, o que leva aquele ametabolizvel composto que quebra etapas energticas levando a consequencias como acidose sanguinea e estenose heptica.
29
4. Bibliografia.
BERG, Jeremy M. TYMOCZKO, John L. STYER, Lubert. Bioqumica. 5 edio. Rio de Janeiro: Guanabara Koogan. 2002. CONN, Eric. E. STUMPF, P.K. Introduo Bioqumica. Traduo da 4 edio americana. 8 reimpresso. So Paulo: Editora Edgard Blcher Ltda. 2001. NELSON, D. L. and COX, M. M. Lehninger principles of biochemistry. 3ed. New York: Worth Publishers. 2000.
30
Das könnte Ihnen auch gefallen
- Prova Objetiva Final de BioquímicaDokument5 SeitenProva Objetiva Final de BioquímicaCarolina Vilela50% (2)
- Gliconeogenese ResumoDokument2 SeitenGliconeogenese ResumoHarlyson David BotelhoNoch keine Bewertungen
- PDF Integração Do Metabolismo - Sugestões de RespostasDokument10 SeitenPDF Integração Do Metabolismo - Sugestões de RespostasHarlyson David BotelhoNoch keine Bewertungen
- 04 EnfermagemDokument6 Seiten04 EnfermagemHarlyson David BotelhoNoch keine Bewertungen
- FisiologiaDokument7 SeitenFisiologiaHarlyson David BotelhoNoch keine Bewertungen
- Original Edital03 2012PPGBRPH PublicarDokument9 SeitenOriginal Edital03 2012PPGBRPH PublicarHarlyson David BotelhoNoch keine Bewertungen
- Colesterol ELDokument4 SeitenColesterol ELHarlyson David BotelhoNoch keine Bewertungen
- Apostila Licao1 PDFDokument4 SeitenApostila Licao1 PDFDebora MouraNoch keine Bewertungen
- Caderno de Apoio Às Aulas Teóricas 1 Apontamentos PDFDokument113 SeitenCaderno de Apoio Às Aulas Teóricas 1 Apontamentos PDFFCiênciasNoch keine Bewertungen
- Pentose Phosphate Pathway (PPPDokument20 SeitenPentose Phosphate Pathway (PPPwalas joãoNoch keine Bewertungen
- Carnes Pse e DFDDokument3 SeitenCarnes Pse e DFDisenefretNoch keine Bewertungen
- Metabolismo de Lipídios emDokument33 SeitenMetabolismo de Lipídios emNayara Andrade Duque OliveiraNoch keine Bewertungen
- Fisiologia Do Esforço e Do ExercícioDokument28 SeitenFisiologia Do Esforço e Do ExercícioStefânia MoraisNoch keine Bewertungen
- Bioenergética aplicada à Atividade Física e EsporteDokument46 SeitenBioenergética aplicada à Atividade Física e EsporteMarilia TarragoNoch keine Bewertungen
- Metabolismo, exercício e obtenção de energiaDokument35 SeitenMetabolismo, exercício e obtenção de energiaEliabe Do Carmo AlmeidaNoch keine Bewertungen
- Observação e Análise Da Respiração Celular em Tecidos Animais e VegetaisDokument4 SeitenObservação e Análise Da Respiração Celular em Tecidos Animais e VegetaisPedro NascimentoNoch keine Bewertungen
- Bioenergética e MetabolismoDokument47 SeitenBioenergética e MetabolismoValeskaSenaNoch keine Bewertungen
- Resumo BioenergéticaDokument5 SeitenResumo BioenergéticaPaulo CuevasNoch keine Bewertungen
- Sistemas Energéticos - Anaeróbio e Aeróbio PDFDokument36 SeitenSistemas Energéticos - Anaeróbio e Aeróbio PDFEvelyn MendesNoch keine Bewertungen
- 2° EJA Pet 1 Biologia FINALDokument23 Seiten2° EJA Pet 1 Biologia FINALNayara DutraaNoch keine Bewertungen
- Vias Metabólicas - Bioquimica PDFDokument11 SeitenVias Metabólicas - Bioquimica PDFLuanNoch keine Bewertungen
- Bioenergética e respiração celularDokument4 SeitenBioenergética e respiração celularAfonso ParanhosNoch keine Bewertungen
- GlicóliseDokument4 SeitenGlicóliseLivia RossetiNoch keine Bewertungen
- Glúcidos PDFDokument122 SeitenGlúcidos PDFJoana CardosoNoch keine Bewertungen
- Análise de Um Processo Fermentativo para Desenvolvimento de Um Produto AlimentarDokument119 SeitenAnálise de Um Processo Fermentativo para Desenvolvimento de Um Produto AlimentarRenata CalixtoNoch keine Bewertungen
- Produção de lactato e vias metabólicasDokument2 SeitenProdução de lactato e vias metabólicasDavidNoch keine Bewertungen
- Fisiologia Do ExercícioDokument59 SeitenFisiologia Do ExercícioDavi FelicioNoch keine Bewertungen
- Glicogenolise Glicogenese e GliconeogeneseDokument35 SeitenGlicogenolise Glicogenese e GliconeogeneseJéssica Vasconcelos100% (6)
- Bioquímica da nutrição e atividade físicaDokument60 SeitenBioquímica da nutrição e atividade físicaMileny AugustoNoch keine Bewertungen
- Aula Metabolismo Microbiano Parte BDokument46 SeitenAula Metabolismo Microbiano Parte BMilton Luiz da Paz LimaNoch keine Bewertungen
- Questionários de BioquímicaDokument8 SeitenQuestionários de Bioquímicaramonfarma1140Noch keine Bewertungen
- Resistência à insulina em paciente com diabetes tipo 2Dokument2 SeitenResistência à insulina em paciente com diabetes tipo 2Ricardo Francisco dos SantosNoch keine Bewertungen
- FotossinteseDokument8 SeitenFotossinteseanon-309063100% (3)
- Questionário - Questões Marks - 2 ProvaDokument8 SeitenQuestionário - Questões Marks - 2 ProvaJohanaNoch keine Bewertungen
- Prova - Parte 2Dokument36 SeitenProva - Parte 2Beatriz MateusNoch keine Bewertungen
- Respiração aeróbica: processo energético mitocondrialDokument27 SeitenRespiração aeróbica: processo energético mitocondrialAna Carolina Alcântara AgnesiniNoch keine Bewertungen
- Lactato DesidrogenaseDokument16 SeitenLactato DesidrogenaseGustavo BalliniNoch keine Bewertungen