Beruflich Dokumente
Kultur Dokumente
98 209
Hochgeladen von
hizballah27Originaltitel
Copyright
Verfügbare Formate
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
Verfügbare Formate
98 209
Hochgeladen von
hizballah27Copyright:
Verfügbare Formate
Pneumologie
B 94
Cancers bronchiques
à petites cellules
Épidémiologie, anatomie pathologique, étiologie, diagnostic, évolution, traitement
Dr Claire LEGRAND 1, Pr Christian BRAMBILLA 1, Dr Sylvie LANTUEJOUL 2
1. Service de pneumologie
2. Service de pathologie cellulaire, CHRU, 38043 Grenoble cedex 09
Points Forts à comprendre primer. Le tabagisme passif augmente le risque de 1 à 3
selon les études.
Nous n’insisterons pas sur les autres facteurs de risque
Les cancers bronchiques à petites cellules notamment professionnels qui sont communs à tous les types
représentent environ 20 % de l’ensemble histologiques de cancers broncho-pulmonaires, mais sim-
des tumeurs bronchiques. Ils se caractérisent par plement sur 2 facteurs qui semblent plus spécifiquement
leur agressivité, leur lien au tabac, leur associés avec le CBPC : le bis-chlorométhyl-éther (utilisé
chimiosensibilité et radiosensibilité spectaculaires notamment lors de la fabrication des résines échangeuses
mais éphémères dans la majorité des cas, d’ions) induit des cancers bronchiques qui sont plus de 2 fois
et par leurs caractéristiques biologiques dues sur 3 de type à petites cellules ; le radon et ses dérivés, pol-
à leur différenciation neuro-endocrine. Leur luants gazeux et particulaires émis dans les mines d’uranium
évolution spontanément explosive, la constance augmentent la survenue des carcinomes bronchiques : le
et la précocité des métastases ainsi que leur risque relatif est beaucoup plus élevé pour le CBPC (33,5
extrême sensibilité aux thérapeutiques font contre 8,3 et 4,3 pour le cancer épidermoïde et l’adénocar-
de ces cancers une urgence médicale. cinome respectivement) ; la proportion de CBPC est encore
plus forte parmi les patients de moins de 55 ans.
Épidémiologie Anatomo-pathologie
Épidémiologie descriptive Les cancers à petites cellules sont des tumeurs neuro-endo-
crines malignes, caractérisées par : la présence de granules
Le cancer bronchique à petites cellules (CBPC) représente
neurosécrétoires en microscopie électronique, une argyro-
15 à 25 % de l’ensemble des carcinomes bronchiques
philie cytoplasmique dans 20 % des cas (Grimélius +), la
observés en France, et serait responsable de 9 à
coexpression immunohistochimique d’une différenciation
15 décès/100 000 habitants par an. En Europe, il représente
neuro-endocrine et épithéliale, l’association à des syn-
20 à 25 % des tumeurs pulmonaires, mais seulement 15 %
dromes paranéoplasiques.
d’entre elles au Japon. Il représente à lui seul la quatrième
cause de mortalité par cancer. Les femmes sont moins sou- Macroscopie
vent atteintes par ce cancer, compte tenu de leur moindre Sur le plan macroscopique, il s’agit de tumeurs proximales
tabagisme ; en France, la répartition inégale des sexes extensives, classiquement de type médiastino-pulmonaire,
(6 hommes pour 1 femme) persiste mais le sex ratio tend ou très rarement d’un nodule périphérique. Le CBPC hilaire
à se rapprocher de 1 dans certains états des États-Unis où naît au niveau de la muqueuse des troncs bronchiques et,
le tabagisme féminin continue d’augmenter alors que celui le plus souvent, des gros troncs bronchiques (2 fois sur 3).
des hommes diminue. Le CBPC est plus fréquent que les Il s’étend rapidement le long des axes bronchiques de façon
autres types histologiques dans la tranche d’âge inférieure hilifuge, infiltrant les parois avec rétrécissement irrégulier
à 50 ans. Cependant, il survient surtout après l’âge de 50 des lumières et surtout de façon lymphophile vers les gan-
ans (en nombre absolu), avec un pic de fréquence pendant glions lobaires, hilaires et médiastinaux. Cette extension
la 6e décennie. ganglionnaire importante explique l’élargissement habi-
tuel des éperons et les aspects de compression extrinsèque
Épidémiologie analytique observés lors de l’endoscopie, tandis que la diffusion à la
Le tabagisme est le principal facteur exogène associé à la surface de l’épithélium produit un aspect endoscopique de
survenue du CBPC ; moins de 5 % des patients sont des rétrécissement en cheminée de pipe.
non fumeurs. La durée du tabagisme et le nombre de ciga- La progression tumorale du CBPC périphérique est de type
rettes quotidien sont des facteurs affectant le risque. L’ar- nodulaire ; la tumeur tend à combler les espaces alvéolaires
rêt du tabagisme diminue le risque de survenue sans le sup- en entraînant peu de lésion au niveau des septa. Ce mode
LA REVUE DU PRATICIEN (Paris) 1998, 48 209
CANCERS BRONCHIQUES À PETITES CELLULES
d’extension, ainsi que l’exiguïté du stroma pauvre en infil-
trat inflammatoire expliquent l’absence de tissu cicatriciel
après radiothérapie et chimiothérapie, si bien que dans cer-
tains cas le site primitif ne peut plus être identifié. À la
coupe, les masses tumorales sont friables, encéphaloïdes,
témoins de la discrétion de la stroma-réaction conjonctive.
Étude microscopique
La classification anatomo-pathologique des cancers bron-
chiques actuellement en vigueur dans le monde est celle
de l’Organisation mondiale de la santé (OMS) de 1981.
L’OMS décrit les CBPC comme des tumeurs faites de cel-
lules de petite taille, très peu différenciées et en indivi-
dualise 3 sous-types :
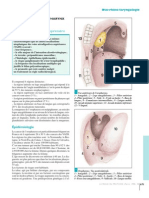
– le CBPC en grains d’avoine est composé de petites cel- 1
lules monomorphes, à peine plus grandes qu’un lympho- Aspect histologique typique d’un carcinome à petites cel-
lules oat cell (à cellules en grain d’avoine) : petites cellules à
cyte, à cytoplasme très peu abondant ; la chromatine noyau fusiforme, chromatine dense, nucléole et sertissure
nucléaire est dense ou poussiéreuse, à nucléole petit ou cytoplasmique inapparents, et haute activité mitotique. Stroma
indistinct ; resteint aux vaisseaux (HES ; T 400).
– le CBPC de type intermédiaire comporte les mêmes cri-
tères nucléaires que la forme en grains d’avoine, mais le
cytoplasme est plus abondant, les cellules ont des contours
polygonaux ou fusiformes ;
– le CBPC composite à grains d’avoine est constitué d’une
prolifération à nette prédominance de cellules en grains
d’avoine, accompagnée d’un contingent de cellules épi-
dermoïdes ou glandulaires.
En fait, cette classification correspond plutôt à des diffé-
rences morphologiques induites par des techniques de pré-
lèvement différentes. Lors des prélèvements chirurgicaux,
les cellules sont mieux conservées et sont classées dans le
type intermédiaire, alors qu’il existe plus de cellules en
grains d’avoine sur un prélèvement par biopsie du fait d’ar-
téfacts induits par l’écrasement et la nécrose cellulaire. La
corrélation entre l’aspect cytologique des frottis et le type 2
histologique est élevée pour les CBPC ; ainsi les prélève- Marquage intense membranaire d’un CBPC fait par un
ments cytologiques obtenus par brossage bronchique sont anticorps dirigé contre une molécule NCAM (neural cell adhe-
sion molecule) et Leu 19 (immunoperoxydase indirecte ; T 400).
aussi fiables que ceux obtenus lors de biopsies bronchiques
au cours de la fibroscopie.
Lorsque la tumeur est constituée de petites cellules tumo- l’altération de proto-oncogènes, séquences génétiques
rales d’aspect non caractéristique du CBPC typique, le dia- constitutionnelles du génome cellulaire normal. Ils ont un
gnostic différentiel nécessite une étude immunohistochi- effet phénotypique dominant vis-à-vis de l’autre allèle.
mique. Le CBPC est surtout caractérisé en Leur transcription correspond à un gain de fonction par sur-
immunohistochimie par une différenciation neuro-endo- production d’une protéine normale ou par production d’une
crine. Le marqueur le plus sensible et le plus spécifique est protéine anormale à fonction pervertie.
l’expression de molécules NCAM (Neural Cell Adhesion Les proto-oncogènes de la famille myc produisent des pro-
Molecules). La chromogramine et la synaptophysine, téines nucléaires phosphorylées impliquées dans la régu-
constituants de la paroi du granule, sont très spécifiques. lation du cycle cellulaire. C-myc code pour un facteur de
La neurone spécifique enolase (NSE) est plus sensible mais transcription et peut induire l’apoptose (mort cellulaire)
beaucoup moins spécifique (positivité de 30 % pour les dans certaines conditions. Dans les cancers bronchiques,
tumeurs non neuro-endocrines, notamment malpighiennes on observe dans 18 % des cas une amplification du gène
et glandulaires) (voir : pour approfondir / 1). myc (plusieurs centaines de copies), entraînant une sur-
production de la protéine correspondante. Plus souvent
(46 % des cas), il s’agit d’un mécanisme de surexpression
Étiopathogénie du gène myc (augmentation de l’ARN messager et non de
l’ADN). Le gène ras n’est pas muté dans les TNEP.
Oncogenèse et CBPC (voir : pour approfondir / 2)
1. Oncongènes 2. Anti-oncogènes
Il s’agit de gènes dominants exerçant un rôle positif sur la Ce sont des gènes récessifs exerçant un contrôle négatif sur
prolifération cellulaire (type myc et ras). Ils dérivent de la prolifération et situés sur des bras chromosomiques fré-
210 LA REVUE DU PRATICIEN (Paris) 1998, 48
Pneumologie
quemment délétés dans les cancers (type p53 et Rb). dans un contexte de tabagisme. Les signes généraux (amai-
• Inactivation de p53 : p53 est un anti-oncogène impliqué grissement, asthénie) sont présents dans environ 50 % des
dans la régulation du cycle cellulaire ; il bloque le passage cas lors du diagnostic initial de même que les métastases
de la phase G1 à la phase S, induisant ainsi l’apoptose symptomatiques.
lorsque la cellule présente une accumulation anormale d’al-
térations de son ADN. Radiographie
L’altération du gène ou de la protéine p53 (17p13) est La radiographie pulmonaire montre des opacités hilaires
actuellement l’événement le plus fréquent retrouvé dans tumorales (irrégulières, spiculées) ou ganglionnaires
les cancers bronchiques, toutes histologies confondues. Elle (régulières) et des opacités parenchymateuses par trouble
concerne 50 % des CBPC testés. Par ailleurs, la mutation de la ventilation, ou pneumopathie, ou plus rarement
du gène p53 serait un événement précoce au cours de l’on- d’origine tumorale. Ces anomalies sont le plus souvent
cogenèse des cancers bronchiques. unilatérales et toujours asymétriques. La radiographie
• L’inactivation de Rb, autre anti-oncogène situé sur le peut être normale.
chromosome 13, région 13q14, empêche le
contrôle négatif au point de restriction G1 et
accélère le passage G1/S. L’inactivation de Rb
est un phénomène très fréquemment retrouvé
au cours des CBPC (90 % des cas), et beau-
coup plus rarement au cours du cancer bron-
chique non à petites cellules (CBNPC, 10 à 15
% des cas).
• Il existe des anti-oncogènes potentiels non
encore identifiés sur le bras court du chromo-
some 3, presque constamment délétés dans le
CBPC.
3. Facteurs de croissance
Il existe d’une façon générale une surproduc-
tion ou une production inappropriée de fac- 3a 3b
teurs de croissance dans les tissus néopla- Élargissement du médiastin sur la radiographie pulmonaire de face (3a) par
siques. De nombreux oncogènes codent soit une volumineuse masse tumorale prenant le contraste et située dans le médias-
pour des facteurs de croissance, soit pour leurs tin postérieur sur les données scanographiques (3b), au contact du rachis et
récepteurs, soit pour des enzymes associés à de l’aorte descendante, comprimant les deux bronches souches.
la transmission du signal mitotique.
Les lignées cellulaires de CBPC sécrètent de nombreux Syndromes paranéoplasiques
peptides in vitro. In vivo, l’excrétion de ces peptides s’ex- Présents dans environ 15 à 20 % des cas de CBPC, ils sont
prime sous la forme de syndromes paranéoplasiques. majoritairement endocriniens et métaboliques, mais aussi
neurologiques.
Diagnostic 1. Syndromes endocriniens et métaboliques
Clinique • Le syndrome de sécrétion inappropriée d’ADH (anti-
L’expression clinique du CBPC est conditionnée par la rapi- diuretic hormone) est presque exclusivement associé aux
dité de l’extension médiastinale et métastatique, jointe à la carcinomes à petites cellules, avec des taux sériques d’ADH
fréquence des syndromes paranéoplasiques. Le délai anormaux dans 50 % des cas ; toutefois seulement 1 à 5 %
moyen entre les premiers signes fonctionnels et le dia- des patients présentent des signes cliniques ou biologiques
gnostic est assez bref, inférieur à 2 mois. La découverte de évocateurs : confusion, coma, crises comitiales associés à
la maladie sur une radiographie systématique est rare (5 % une hyponatrémie et à une augmentation de l’osmolalité
des cas). Les signes thoraciques lors du diagnostic sont urinaire.
communs avec les autres types histologiques de cancers • Le syndrome de Cushing paranéoplasique (1 à 5 % des
pulmonaires. Par ordre de fréquence, on retrouve la toux, cas de CBPC) est lié à la production dérégulée par les cel-
l’infection révélatrice d’une obstruction bronchique, la lules tumorales d’ACTH (adreno-corticotrophic hormone)
douleur thoracique, l’hémoptysie, la dyspnée, l’épanche- et de précurseurs de l’ACTH tels que la propiomélanocor-
ment pleural ; puis les signes témoignant plus spécifique- tine. Ces peptides peuvent être dosés dans le sang des
ment de l’atteinte médiastinale ganglionnaire avec com- patients où ils sont en général à des taux plus élevés que
pression des différents éléments médiastinaux : sifflements dans la maladie de Cushing et surtout avec une grande pré-
intrathoraciques, paralysie récurrentielle gauche, syndrome dominance de précurseurs de l’ACTH. Le tableau clinique
cave supérieur, dysphagie, adénopathies sus-claviculaires est beaucoup plus fruste, d’apparition rapide : les patients
(le CBPC est la cause la plus fréquente du syndrome cave se présentent avec une asthénie, une amyotrophie récente
supérieur). Ces signes d’installation rapide sont évocateurs avec perte de poids, ces signes étant non spécifiques dans
LA REVUE DU PRATICIEN (Paris) 1998, 48 211
CANCERS BRONCHIQUES À PETITES CELLULES
un contexte tumoral ; l’obésité tronculaire, les vergetures (surtout destinée à l’estimation de l’extirpabilité des can-
et la « bosse de bison » sont généralement absents. Les cers non à petites cellules). Le stade limité au thorax repré-
signes plus spécifiques sont la mélanodermie, l’alcalose sente environ 30 % des cas au moment du diagnostic. Il se
métabolique difficile à corriger, ou encore l’hypertension définit par : une tumeur primitive limitée à un hémithorax,
artérielle, l’hyperglycémie et les œdèmes. La sécrétion des adénopathies hilaires homolatérales, des adénopathies
d’ACTH paranéoplasique est un critère de gravité dans le médiastinales homo- ou controlatérales ; des adénopathies
CBPC de par la fréquence et la sévérité des complications sus-claviculaires homo- ou controlatérales. Cela corres-
infectieuses opportunistes et aussi par une moindre réponse pond à la notion de tissu tumoral pouvant être inclus dans
à la chimiothérapie. un champ d’irradiation et il s’agit donc de tumeurs sans
• L’hypercalcémie paranéoplasique est plus rare et plus métastase extrathoracique, envahissant l’hémithorax (T1 à
souvent associée aux carcinomes épidermoïdes. T4), le médiastin (N0 à N3), mais n’envahissant ni le pou-
mon controlatéral ni la plèvre. Cela correspondant aux
2. Syndromes neurologiques sous-groupes I, II et IIIA de la stadification TNM.
Les syndromes paranéoplasiques neurologiques sont rares La forme diffuse (au-delà de l’hémithorax) représente envi-
(2 % des cancers bronchiques) mais le plus souvent le fait ron 70 % des cas et se définit par : des lésions hilaires ou
de carcinomes à petites cellules, et sont en rapport avec une pulmonaires controlatérales, des lésions métastatiques à
réaction auto-immune, fondée sur la réactivité croisée entre distance du thorax, l’existence d’un épanchement pleural
des épitopes de la tumeur et du tissu nerveux. Le rôle patho- métastatique, une seule de ces conditions étant suffisante.
gène d’anticorps dirigés contre différents antigènes du tissu Cela correspond aux sous-groupes IIIB et IV de la stadifi-
nerveux et du CBPC est bien identifié dans le syndrome de cation TNM. Le pronostic et la stratégie thérapeutique dif-
Lambert-Eaton (pseudo-myasthénie) mais reste imprécis fèrent pour ces 2 groupes.
dans la majorité des autres affections neurologiques para-
néoplasiques : syndrome anti-Hu (ou polyencéphalomyé- Bilan d’extension ou préthérapeutique
lites subaiguës), neuropathies gastro-intestinales paranéo- Le bilan préthérapeutique comporte un examen clinique
plasiques, rétinopathie associée au cancer. Les signes complet, avec pesée et estimation de la perte de poids, et
neurologiques peuvent précéder l’apparition de la tumeur évaluation de l’indice de Karnofsky (ou du performance
ou sa rechute de plusieurs mois. Ces signes sont indépen- status). Sur le plan biologique : numération formule san-
dants du volume tumoral et la maladie neurologique évo- guine, ionogramme, clairance de la créatinine-vitesse de
lue et se complique pour son propre compte. sédimentation, lactico-déshydrogénase, bilan hépatique, et
L’hippocratisme digital est le plus souvent rencontré au NSE (neuron specific enolase) sont communément réali-
cours des cancers non à petites cellules, le CBPC n’en est sés.
responsable que dans 5 % des cas. La tomodensitométrie thoracique, élément essentiel du
bilan locorégional, permet de préciser le siège de la tumeur,
Stratégie diagnostique son extension à la paroi, au médiastin, de visualiser des
Le CBPC ayant une présentation le plus souvent médias- adénomégalies homolatérales ou controlatérales et de juger
tino-hilaire, le diagnostic est le plus souvent réalisé par de l’envahissement des vaisseaux, en particulier de la veine
fibroscopie, plus rarement par médiastinoscopie et biopsie cave supérieure.
ganglionnaire périphérique. Le diagnostic positif repose La recherche de métastases est systématique, même en l’ab-
habituellement sur l’endoscopie bronchique avec biopsies sence de signe clinique d’appel, par le scanner cérébral,
multiples, associées aux prélèvements cytologiques (aspi- l’échographie ou le scanner abdominal, la scintigraphie
ration bronchique ou brossage). Cette technique permet osseuse et la biopsie ostéomédullaire ou le myélogramme.
d’accéder au diagnostic de CBPC chez plus de 90 % des En pratique, en dehors d’essais thérapeutiques où le bilan
patients. L’aspect macroscopique n’est pas spécifique : élar- d’extension doit être complet, les examens peuvent être inter-
gissement des éperons, muqueuse irrégulière et infiltrée. rompus à la première métastase découverte, le traitement
Un bourgeon unique est rarement observé en cas de CBPC. étant alors de toute façon celui des formes disséminées.
Ailleurs, le diagnostic reposera sur la répétition de l’en- Lors du bilan d’extension au moment du diagnostic, on
doscopie bronchique, sur un prélèvement obtenu par retrouve 35 à 40 % de métastases osseuses, 20 à 30 % de
médiastinoscopie si la tomodensitométrie a montré une localisations hépatiques, 20 à 25 % pour la moelle osseuse
extension ganglionnaire accessible par cette technique, ou mais en fait beaucoup plus avec des techniques très sen-
encore sur la ponction et la biopsie-exérèse d’une locali- sibles (55 % avec immunomarquage sur biopsie médullaire
sation métastatique accessible, notamment ganglionnaire. couplée à l’IRM), 10 à 15 % pour la glande surrénale de
L’ensemble du bilan d’extension initial permet de distin- même que pour le système nerveux central, puis viennent
guer 2 stades cliniques de la maladie : les formes limitées l’atteinte de la peau, des ganglions périphériques et de la
au thorax (où la masse tumorale ne déborde pas les limites plèvre de fréquence moindre. Ces localisations métasta-
d’un hémithorax) et les formes disséminées (métastatiques tiques sont globalement sous-estimées par manque de sen-
d’emblée). Cette classification en 2 groupes semble mieux sibilité des moyens de détection utilisés, et le pourcentage
adaptée au CBPC où la tumeur est le plus souvent volu- de formes disséminées augmente progressivement avec le
mineuse et inopérable et l’atteinte médiastinale ganglion- développement des techniques de détection (65 à 70 %
naire pratiquement constante, que la classification TNM actuellement selon les équipes).
212 LA REVUE DU PRATICIEN (Paris) 1998, 48
Pneumologie
Évolution
Patients longs survivants
La médiane de survie des patients non traités est de 4 à 6 Les patients longs survivants (à partir de 24 ou 30 mois de survie après
semaines. L’introduction de la chimiothérapie au début des la découverte de la maladie selon la définition anglo-saxonne ou fran-
çaise) évoluent le plus souvent vers la rechute tardive, ou vers l’ap-
années 1970 a amélioré le pronostic de la maladie, du moins parition d’un 2e cancer aérodigestif ou pulmonaire au-delà de 10 ans.
à court terme, avec des médianes de survie s’établissant Le risque de 2e cancer est prépondérant par rapport à la rechute après
entre 7 et 17 mois selon l’extension de la maladie, les sur- 5 ans.
vies à long terme restant rares. Le taux de survie global à
2 ans est de 5 à 10 %, et de 3 % à 5 ans.
Traitement
Pronostic
Principes
Le performance status ou index d’activité est le facteur pro- Le CBPC est une maladie systémique avec peu de survi-
nostique le plus important de la survie ; il est en effet cor- vants après un traitement local ou locorégional seul [chi-
rélé à la masse tumorale et au taux de LDH ; c’est un fac- rurgie et (ou) radiothérapie]. La chimiothérapie est donc
teur de pronostic indépendant dans les formes disséminées. l’élément thérapeutique dominant et augmente de façon
Le stade d’extension initial : pour les formes localisées le significative la survie. L’attitude thérapeutique diffère en
taux de survie est respectivement à 2 et 5 ans de 13 et 4 %. fonction de la forme localisée ou diffuse.
Pour les formes diffuses, il est de 4 et 2 %. La médiane de En cas de CBPC localisé, deux objectifs s’imposent : le
survie est de 7 à 11 mois pour les formes diffuses et de 10 contrôle local de la tumeur et le traitement des micromé-
à 17,5 mois pour les formes localisées. Plus récemment, il tastases. L’association radio-chimiothérapie permet une
a été mis en évidence un pronostic plus sombre des formes amélioration modeste mais significative de la survie à 2 ans
limitées au thorax avec atteinte ganglionnaire médiastinale d’environ 5 à 6 % (de 16 à 20 %) et de 5,4 % à 3 ans par
ou sus-claviculaire par rapport aux autres formes limitées, rapport à la chimiothérapie seule. Cette association apporte
et l’on s’achemine à nouveau vers une classification plus un meilleur contrôle local (seul garant d’une réponse com-
précise, proche du TNM. La réponse complète au traite- plète prolongée), et une action sur l’émergence de clones
ment constitue également un facteur pronostique majeur. chimiorésistants apparaissant précocement après le début
Les autres facteurs sont d’importance moindre ; la NSE est de la chimiothérapie. Un autre intérêt du traitement com-
plus élevée en cas de maladie disséminée qu’en cas de biné est l’existence d’une toxicité indépendante, et une
maladie localisée mais ne permet pas de prédire l’exten- meilleure protection du tissu dain.
sion de la maladie. Son augmentation transitoire constitue Les formes disséminées de CBPC, les plus graves des
un facteur prédictif de la réponse à la chimiothérapie. tumeurs solides, ont un pronostic sombre. La notion de dis-
TABLEAU
Facteurs pronostiques pour la survie des patients
atteints de CBPC
Facteurs pronostiques Bon Mauvais
1. Index d’activité élevé faible
2. Stade d’extension initiale localisée diffuse
3. Âge < 70 ans > 70 ans
4. Réponse complète au traitement oui non
5. Réponse au traitement oui non
6. Atteinte ganglionnaire médiastinale ou sus-claviculaire non oui
7. Sexe féminin masculin
8. Pour les formes diffuses métastase unique (voire double) métastases multiples
9. Nature des localisations secondaires controversé controversé
10. Marqueurs tumoraux augmentation transitoire
de la NSE lors de la chimiothérapie
11. LDH taux normal taux > 450 UI
12. Phosphatases alcalines taux normal taux > la normale
13. Syndrome de Cushing non oui
14. Hyponatrémie non oui
LA REVUE DU PRATICIEN (Paris) 1998, 48 213
CANCERS BRONCHIQUES À PETITES CELLULES
sémination, bien qu’elle soit un élément pronostique fon- 2. Radiothérapie
damental, est à relativiser ; de nombreuses formes dites
localisées sont en fait disséminées avec de multiples micro- Le CBPC est caractérisé par une importante radiosensibi-
métastases non détectées lors du bilan d’extension clas- lité. Le volume à traiter en radiothérapie thoracique externe
sique ; certaines formes métastatiques limitées à l’atteinte correspond classiquement à l’ensemble du volume tumo-
d’un site, osseux ou médullaire notamment, ont un pro- ral présent avant le début de la chimiothérapie avec une
nostic proche des formes en apparence localisées. La notion marge de 1,5 à 2 cm. La dose totale optimale de radiothé-
de dissémination, même très étendue, ne doit pas être une rapie à administrer est de l’ordre de 45 à 55 Gy, ce qui per-
contre-indication à la chimiothérapie, mais les traitements met un bon contrôle local immédiat au prix d’une toxicité
locorégionaux (chirurgie et radiothérapie) n’ont plus acceptable. L’irradiation des creux sus-claviculaires et du
aucune indication autre qu’exceptionnelle ou palliative. hile controlatéral reste un sujet controversé actuellement.
Le scanner dosimétrique permet de mieux déterminer le
volume à irradier avec une réduction de la toxicité pulmo-
Modalités thérapeutiques naire.
Le fractionnement habituellement proposé délivre 2 Gy par
1. Chimiothérapie fraction 5 fois/semaine, mais plusieurs études récentes sug-
gèrent comme fractionnement optimal un bifractionnement
Le bénéfice obtenu par la chimiothérapie dans les CBPC quotidien qui permettrait une amélioration du contrôle local
repose sur l’emploi d’une polychimiothérapie associant 2 (au prix d’une plus importante toxicité immédiate). L’ad-
à 4 médicaments actifs en monothérapie, avec un taux de ministration de la dose quotidienne est alors faite en deux
réponse objective d’au moins 20 % pour chacun des médi- fois avec un délai de 6 à 8 heures, ce qui permet la répara-
caments utilisé seul. Douze substances ont été ainsi mises tion des radiolésions des tissus sains mais pas du tissu tumo-
en évidence comme étant efficaces. Parmi elles, on retrouve ral ; la seconde fraction permet de tuer un nouveau contin-
l’ifosfamide, le cisplatine (CDDP), le carboplatine pour gent tumoral.
lequel le taux de réponses chez des patients non prétraités
peut atteindre 60 %, l’étoposide (VP16) qui peut être admi- Les métastases cérébrales sont fréquentes et surviennent à
nistrée per os avec 33 % de réponses complètes (dans les n’importe quel stade de la maladie : l’incidence est de
formes limitées), la vinorelbine, dérivé semi-synthétique de 10 % lors du diagnostic et de 20 % durant le traitement.
la 5’ norvinca-alcaloïde, et agissant par inhibition de la poly- L’irradiation cérébrale prophylactique consiste à irradier
mérisation de la tubuline pendant la mitose. Actuellement, l’ensemble du cerveau avec une dose totale d’environ 30
les associations comportant l’étoposide (75 à 100 mg/m2 Gy en 10 fractions. Elle permet une diminution du taux de
trois jours consécutifs) et le cisplatine (100 mg/m2 un jour) rechute cérébrale mais n’a pas d’impact significatif sur la
sont les schémas de référence les plus couramment utilisés survie pour l’instant. Les patients susceptibles d’en tirer
en association avec la radiothérapie compte tenu d’une bénéfice sont ceux mis en rémission complète par le trai-
synergie prouvée entre l’étoposide et les radiations, et entre tement systémique.
l’étoposide et le cisplatine. D’autres protocoles de chimio-
thérapie de première ligne incluant de nouveaux médica- 3. Chirurgie
ments ont montré des résultats encourageants comme les La majorité des CBPC considérés comme limités se pré-
associations CDDP/paclitaxel, ou CDDP/VP16/paclitaxel. sente avec une maladie localement évoluée, par envahis-
En seconde ligne, de nouveaux médicaments peuvent être sement ganglionnaire médiastinal homolatéral et (ou)
étudiés dans le cadre de protocoles. controlatéral. Néanmoins, quelques patients ont une petite
Il n’y a pas de différence entre les protocoles utilisant 3 ou tumeur et un envahissement ganglionnaire modéré (stades
4 médicaments en terme d’efficacité. I et II TNM). Chez ces patients, une exérèse chirurgicale
En ce qui concerne le concept de dose-intensité, la sensi- peut être discutée. La chirurgie seule ne peut en aucun cas
bilité des CBPC à la chimiothérapie a conduit à se poser la apporter une guérison mais, dans les stades extrêmement
question de l’intérêt d’une augmentation de l’intensité de limités, elle pourrait donner un meilleur contrôle local de
la dose. L’augmentation des doses initiales a augmenté la la maladie sans limiter l’intensité des doses de chimiothé-
survie, ce qui montre l’importance du contrôle initial de la rapie. On ne sait pas si la meilleure survie de ces stades
maladie et de l’obtention précoce d’une réponse complète. localisés avec résection complète suivie ou précédée de
Par contre, la chimiothérapie intensive tardive avec auto- chimiothérapie est attribuable à la résection elle-même ou
greffe de moelle augmente la médiane de survie sans réci- liée à un meilleur pronostic initial.
dive, mais n’a pas d’impact sur la survie en raison de l’exis-
tence de rechutes locales et d’une forte toxicité. 4. Autres thérapeutiques
Le nombre de cures de polychimiothérapie se situe entre 4 Les autres traitements hors chimiothérapie sont les facteurs
et 6 selon les équipes, à intervalle de 3 à 4 semaines. de croissance hématopoïétiques et les anticoagulants, à
Parmi les perspectives thérapeutiques, de nouveaux médi- l’étude pour l’optimisation de l’action de la chimiothéra-
caments actifs ont été identifiés : paclitaxel (Taxol), docé- pie. L’interféron α joue un rôle de régulation de la réponse
taxel (Taxotère), difluorodéoxycytidine (Gemcitabine) et immune du poumon en augmentant l’activité cytotoxique
CPT-11 (Irinotecan). des macrophages et des lymphocytes (également à l’étude).
214 LA REVUE DU PRATICIEN (Paris) 1998, 48
Pneumologie
Indications POUR APPROFONDIR
Pour le traitement du CBPC localisé, la radiothérapie tho-
racique externe associée à la chimiothérapie apporte un 1 / Place du CBPC à l’intérieur
gain de survie par rapport à la chimiothérapie seule, mais de la famille des tumeurs
80 % des patients présentent une rechute, le plus souvent neuro-endocrines pulmonaires (TNEP)
dans les 2 premières années suivant la première manifes-
tation de leur maladie. En cas de rechute locale, une confir- Les travaux anatomo-pathologiques modernes ont apporté un gain notoire
mation histologique est indispensable car il peut s’agir d’un en ce qui concerne la classification des TNEP initiée par Gould et pour-
suivie par Travis. L’histogenèse des TNEP a été longtemps débattue. Clas-
cancer non à petites cellules dont la thérapeutique serait siquement elles dérivent des cellules endocrines bronchiques ou cellules de
alors différente. Une irradiation est possible si le patient Kultchitzky, et s’intègrent dans le cadre des tumeurs du système APUD
n’en a pas bénéficié auparavant. Si la rechute se fait à plus (Amine Precursor Uptake Decarboxylase). On a montré que les cellules
d’un an de la fin du traitement d’induction, la reprise de la tumorales neuro-endocrines naissent en réalité d’une cellule épithéliale
bronchique totipotente. En effet, les données récentes de l’embryologie ont
même polychimiothérapie peut entraîner une réponse. En fait abandonner l’hypothèse de l’origine neuro-ectodermique commune aux
cas de récidive précoce, il faut introduire d’autres familles cellules APUD, car les cellules endocrines bronchiques ou digestives sont
cytostatiques que celles utilisées dans le protocole initial d’origine endodermique. Par ailleurs, des modèles expérimentaux ont mon-
tré qu’il existe des formes de passage entre hyperplasie neuro-endocrine et
pour éviter les résistances croisées. Le taux de réponses tumeurs à différenciation épidermoïde ou glandulaire.
espéré est de 20 à 25 % avec une médiane de survie de 3 à La classification proposée par Travis en 1992 comporte 4 groupes dont le
4 mois. L’association étoposide et cisplatyl donne une assez 2e nous intéresse particulièrement.
bonne réponse en deuxième ligne si elle n’a pas été utili- I. Petites lésions neuro-endocrines : corps neuro-endocrine et tumorlet ; ce
sont des proliférations cellulaires bénignes souvent associées à des bron-
sée en première ligne. chectasies et de découverte histologique fortuite.
Pour le traitement du CBPC diffus la polychimiothérapie II. Néoplasmes avec aspect histologique neuro-endocrine de type commun.
est toujours retenue, avec comme risque majeur celui d’une III. Carcinomes non à petites cellules avec des aspects neuro-endocrines :
carcinome glandulaire, malpighien ou indifférencié à grandes cellules avec
toxicité hématologique compte tenu d’une atteinte médul- des caractéristiques neuro-endocrines détectables par immunohistochimie
laire osseuse quasi constante. En cas de non-réponse après ou ultrastructure (microscopie électronique).
2 cures, une modification de traitement peut être proposée IV. Néoplasmes primitifs neuro-endocrines de type rare.
Le groupe II est lui-même divisé en 4 sous-groupes de malignité croissante.
si l’état général le permet. La chimiothérapie est sinon A. Carcinoïde typique : il représente 5 % des tumeurs pulmonaires et son
abandonnée. En cas de réponse partielle, le même proto- index mitotique est faible, son architecture régulière et endocrinoïde. Son
cole est maintenu jusqu’à évidence de progression. La pronostic est excellent, le traitement est chirurgical et les métastases à dis-
radiothérapie est utile à titre symptomatique pour : des dou- tance sont exceptionnelles.
B. Carcinoïde atypique : c’est un véritable néoplasme avec potentiel méta-
leurs osseuses sur une métastase osseuse localisée, une statique à distance (métastases présentes dans 20 % des cas lors du dia-
localisation cérébrale, un syndrome cave supérieur ou gnostic), son index mitotique est plus élevé et il existe des anomalies
encore un foie hyperalgique. Enfin les soins palliatifs sont nucléaires.
C. Carcinome neuro-endocrine à grandes cellules : l’index mitotique est
d’une extrême importance, puisqu’ils intéresseront 95 % encore plus élevé, la nécrose est fréquente, le pléiomorphisme cellulaire
des patients atteints de CBPC au terme de l’évolution de élevé, le pronostic est réservé et le traitement est celui des carcinomes
la maladie. ■ non à petites cellules. Le tabagisme est un facteur de risque.
D. Carcinome à petites cellules (CPC) : pur (à grains d’avoine ou inter-
médiaires) ; à petites et grandes cellules ; CPC combiné à un adénocarci-
Points Forts à retenir nome ou à un carcinome malpighien (CPC composite à grains d’avoine).
Le CBPC se présente plus de 6 fois sur 10 sous 2 / Oncogenèse et CBPC
une forme métastatique de pronostic extrêmement
sombre. Sa caractérisation anatomo-pathologique Les cancers bronchiques sont caractérisés sur le plan moléculaire par une
a évolué et il est considéré maintenant comme altération conjointe de l’expression de proto-oncogènes et d’anti-onco-
étant la forme histologique la plus grave gènes. Sur le plan thérapeutique, l’observation de la réversion du phéno-
type tumoral par la réintroduction d’anti-oncogènes fonctionnels (p53
des tumeurs neuro-endocrines pulmonaires ; sauvage) dans les cellules tumorales a autorisé la promotion d’études cli-
la chimiothérapie permet d’obtenir environ 30 à niques de thérapie génique. Les facteurs de croissance et leurs récepteurs
50 % de réponses complètes, mais elle est en règle dont l’expression est dérégulée dans les cancers bronchiques, apparais-
général insuffisante pour assurer la destruction sent comme des indicateurs pronostiques potentiels et comme de nou-
velles cibles thérapeutiques.
de l’ensemble du tissu tumoral. La récidive locale
survient dans 80 à 100 % des cas avec apparition
de cellules devenues chimiorésistantes. POUR EN SAVOIR PLUS
La radiothérapie augmente la survie Crémoux H, Ruffié P, Bignon J. Cancers bronchiques à petites
dans les formes limitées au thorax. L’agressivité cellules. Encycl Med Chir (Paris-France), Poumon, 6002 G61, 9-
thérapeutique comporte une gradation en fonction 1988 : 12 pp.
Milleron B. Cancer bronchique. Paris : Laboratoires Sandoz, 1995.
des facteurs pronostiques, le CBPC reste une Quoix E. Cancers broncho-pulmonaires primitifs. Rev Prat (Paris)
maladie peu curable, la prévention par l’arrêt 1994 ; 44 : 2237-43.
du tabagisme est manifestement la mesure de santé Sasco AJ. Tendances épidémiologiques des cancers bronchiques
primitifs. Rev Prat (Paris) 1993 ; 43 (7) : 799-805.
publique la plus efficace à développer Trillet-Lenoir V, Cordier JF. Originalité des cancers bronchiques
afin de diminuer la mortalité liée au CBPC. à petites cellules. Rev Prat (Paris) 1993 ; 43 (7) : 841-4.
LA REVUE DU PRATICIEN (Paris) 1998, 48 215
Das könnte Ihnen auch gefallen
- 98 991Dokument7 Seiten98 991hizballah27Noch keine Bewertungen
- 98 1003Dokument7 Seiten98 1003hizballah27Noch keine Bewertungen
- 98 1011Dokument7 Seiten98 1011hizballah27100% (1)
- 98 999Dokument4 Seiten98 999hizballah27Noch keine Bewertungen
- 98 919Dokument5 Seiten98 919hizballah27Noch keine Bewertungen
- 98 913Dokument6 Seiten98 913hizballah27Noch keine Bewertungen
- 98 987Dokument3 Seiten98 987hizballah27Noch keine Bewertungen
- 98 875Dokument5 Seiten98 875hizballah27Noch keine Bewertungen
- 98 765Dokument5 Seiten98 765hizballah27Noch keine Bewertungen
- 98 905Dokument4 Seiten98 905hizballah27Noch keine Bewertungen
- Antagonistes Des Récepteurs H Et Inhibiteurs de La Pompe À ProtonsDokument6 SeitenAntagonistes Des Récepteurs H Et Inhibiteurs de La Pompe À Protonshizballah27Noch keine Bewertungen
- 98 899Dokument6 Seiten98 899hizballah27Noch keine Bewertungen
- 98 909Dokument3 Seiten98 909hizballah27Noch keine Bewertungen
- 98 881Dokument5 Seiten98 881hizballah27Noch keine Bewertungen
- 98 887Dokument5 Seiten98 887hizballah27100% (1)
- 98 802Dokument3 Seiten98 802hizballah27Noch keine Bewertungen
- 98 805Dokument5 Seiten98 805hizballah27Noch keine Bewertungen
- 98 781Dokument5 Seiten98 781hizballah27Noch keine Bewertungen
- 98 797Dokument5 Seiten98 797hizballah27Noch keine Bewertungen
- 98 685Dokument3 Seiten98 685hizballah27Noch keine Bewertungen
- 98 771Dokument6 Seiten98 771hizballah27100% (1)
- 98 787Dokument10 Seiten98 787hizballah27Noch keine Bewertungen
- 98 689Dokument5 Seiten98 689hizballah27Noch keine Bewertungen
- 98 661Dokument6 Seiten98 661hizballah27Noch keine Bewertungen
- 98 657Dokument3 Seiten98 657hizballah27Noch keine Bewertungen
- Lipothymie, Syncope Et Perte de Connaissance Brève: Orientation DiagnostiqueDokument4 SeitenLipothymie, Syncope Et Perte de Connaissance Brève: Orientation Diagnostiquehizballah27100% (1)
- 98 679Dokument6 Seiten98 679hizballah27Noch keine Bewertungen
- 98 671Dokument4 Seiten98 671hizballah27Noch keine Bewertungen
- 98 667Dokument4 Seiten98 667hizballah27Noch keine Bewertungen
- 98 653Dokument4 Seiten98 653hizballah27Noch keine Bewertungen
- Livre Et Si On S Arretait Un Peu de Manger - Bernard - Clavière PDFDokument249 SeitenLivre Et Si On S Arretait Un Peu de Manger - Bernard - Clavière PDFNatalia Rosa100% (1)
- Michèle Levy - Comment Stimuler Les 7 Points D'énergie Qui GuerissentDokument13 SeitenMichèle Levy - Comment Stimuler Les 7 Points D'énergie Qui GuerissentChantal D'HulsterNoch keine Bewertungen
- Catalogue Thematique Des Theses 2021Dokument461 SeitenCatalogue Thematique Des Theses 2021Ikbel GhachemNoch keine Bewertungen
- DS44 Cancer Broncho PulmonaireDokument10 SeitenDS44 Cancer Broncho PulmonaireWafa HamdiNoch keine Bewertungen
- Ddoc T 2013 0232 Colin CassinDokument359 SeitenDdoc T 2013 0232 Colin CassinHitsho medNoch keine Bewertungen
- spf00004682Dokument9 Seitenspf00004682France 3 Franche-ComtéNoch keine Bewertungen
- Une Araignee Dans Le VentreDokument272 SeitenUne Araignee Dans Le Ventredagoiso100% (2)
- ABEILLE Repertoire Alphabetique Avec Table Des Matieres1Dokument46 SeitenABEILLE Repertoire Alphabetique Avec Table Des Matieres1MonsieurOmbreNoch keine Bewertungen
- Institut National Sup de Formation Paramédicale de MEDEA: Enseignant MR Cha/ADokument78 SeitenInstitut National Sup de Formation Paramédicale de MEDEA: Enseignant MR Cha/Ananou touatNoch keine Bewertungen
- 20-22 Huile de Foie Morue BS132 PP 2Dokument3 Seiten20-22 Huile de Foie Morue BS132 PP 2Franck YvesNoch keine Bewertungen
- DS A PURST Curcuma PDFDokument7 SeitenDS A PURST Curcuma PDFAmelNesrine100% (2)
- QCM HgeDokument25 SeitenQCM HgeFernando Kolla100% (1)
- Analyse D - Articles Scientifiques - Remini - HocineDokument142 SeitenAnalyse D - Articles Scientifiques - Remini - HocineDjahid Jo100% (6)
- Hennequin 2013Dokument5 SeitenHennequin 2013Saadia BenhaloucheNoch keine Bewertungen
- FicheTox 87Dokument7 SeitenFicheTox 87Afoufou FatehNoch keine Bewertungen
- Physiopathologie Des MI MASTER Biologie Santé 2019-2020Dokument2 SeitenPhysiopathologie Des MI MASTER Biologie Santé 2019-2020Massouh AssouiNoch keine Bewertungen
- Decrevoisier2016 PDFDokument9 SeitenDecrevoisier2016 PDFface bookNoch keine Bewertungen
- svt03580412 ch19 325 LDPDokument6 Seitensvt03580412 ch19 325 LDPZeltyNoch keine Bewertungen
- Alimentation Selon Groupes SanguinsDokument21 SeitenAlimentation Selon Groupes SanguinsChéirif Richard BoussariNoch keine Bewertungen
- Cours3 BIM503 A2023Dokument15 SeitenCours3 BIM503 A2023braultNoch keine Bewertungen
- Lymphome Testicule TunisieDokument3 SeitenLymphome Testicule TunisierabahkhemiletNoch keine Bewertungen
- GUERRACHE A., SAMER A. Et MERAKEB M. S., Treg Et Cancer Colorectal, 2016 PDFDokument93 SeitenGUERRACHE A., SAMER A. Et MERAKEB M. S., Treg Et Cancer Colorectal, 2016 PDFGUERRACHE AbderrahmaneNoch keine Bewertungen
- Cancer de L - EndomètreDokument38 SeitenCancer de L - Endomètreanis anisNoch keine Bewertungen
- Dossier 33 - 50 Dossiers Dermato PDFDokument3 SeitenDossier 33 - 50 Dossiers Dermato PDFOussama AbounasrNoch keine Bewertungen
- Reco 2023Dokument24 SeitenReco 2023Amina NibouchaNoch keine Bewertungen
- 2011GRE15093 Rabeyrin Maud 1 DDokument108 Seiten2011GRE15093 Rabeyrin Maud 1 Danisse89Noch keine Bewertungen
- 2013 Goetz OrianneDokument88 Seiten2013 Goetz OrianneFrançois DossaNoch keine Bewertungen
- NéoplasieDokument32 SeitenNéoplasieAthmani Nabil100% (1)
- Un Manuel de Soins Palliatifs en AfriqueDokument97 SeitenUn Manuel de Soins Palliatifs en Afriquelegma InnocentNoch keine Bewertungen
- CCR Cas Clinique Samedi PedagogiqueDokument3 SeitenCCR Cas Clinique Samedi Pedagogiquemohamedlakehal192Noch keine Bewertungen