Beruflich Dokumente
Kultur Dokumente
Dialnet MicotoxinasYAflatoxinaB1UnProblemaEnSaludAnimal 3702403
Hochgeladen von
Tania Quispe CuelaOriginaltitel
Copyright
Verfügbare Formate
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
Verfügbare Formate
Dialnet MicotoxinasYAflatoxinaB1UnProblemaEnSaludAnimal 3702403
Hochgeladen von
Tania Quispe CuelaCopyright:
Verfügbare Formate
Revista TEORA Y PRAXIS INVESTIGATIVA, Volumen 5 - No.
2, Julio - Diciembre 2010
Centro de Investigacin y Desarrollo CID / Fundacin Universitaria de rea Andina
71
Micotoxinas y Aflatoxina B1, un problema en
salud animal
Micotoxins and Aflatoxin B1, a animal health problem
Hansen Wilber Murcia Rodrguez
1
1 hmurcia@areandina.edu.co
Resumen
Las micotoxinas son metabolitos secundarios producidos por algunas cepas de hongos micotoxignicos
que crecen sobre diferentes tipos de granos utilizados en alimentacin de animales de produccin.
Al momento de ser ingeridas estas toxinas son metabolizadas por un tipo de enzimas llamadas
citocromo P450 (CYP450), una familia de enzimas relacionadas con la biotransformacin de productos
endgenos y xenobiticos. Una de las ms importantes micotoxinas se conoce como aflatoxina
B1 (AFB1). El producto de biotransformacin de la AFB1 es una molcula altamente reactiva
conocida como AFB1-8,9-epxido (AFBO). Este producto es capaz de reaccionar con protenas y ADN
produciendo efectos citotxicos y mutagnicos. Esto se ve representado en problemas en la salud
animal y humana.
Palabras clave: Aflatoxina B1, micotoxinas, salud animal, hongos micotoxignicos, Aflatoxina B1
epxido.
Abstract
Mycotoxins are secondary metabolites produced by some fungi mycotoxigenic strains that are able to
grow on different kinds of production animal feedstuff. When ingested, these toxins are metabolized
by cytochrome P450 enzymes (CYP450), a family of enzymes related with biotransformation of
endogenous and xenobiotic molecules. One of the most important mycotoxins is known as aflatoxin
B1 (AFB1) and its biotransformation product is known as AFB1-8,9-epoxide (AFBO). This enzymatic
product is able to react with cellular proteins and DNA causing cytotoxic and mutagenic effects,
producing great animal and human health consequences.
Key words: Aflatoxin B1, micotoxins, animal health, micotoxigenic fungi, epoxic Aflatoxin B1.
Revista TEORA Y PRAXIS INVESTIGATIVA, Volumen 5 - No. 2, Julio - Diciembre 2010
Centro de Investigacin y Desarrollo CID / Fundacin Universitaria de rea Andina
Hansen Wilber Murcia Rodrguez
72
nucin de la respuesta inmune, e hiperestrogenismo,
entre otras (Bnger et al., 2004).
Despus de haberse descubierto el efecto carcinog-
nico de las aflatoxinas, la bsqueda de micotoxinas
ha llevado a la identificacin de ms de 10 tipos de
hongos toxignicos, cuya gentica y metabolismo
han sido descritos recientemente. Debido a esto se
han generado diferentes estrategias para inactivar o
disminuir el impacto de la presencia de micotoxinas,
en especial de las aflatoxinas, en los lugares de alma-
cenamiento (Tabla 1) (Groopman, Kensler & Wild,
2008).
Diferentes factores afectan el crecimiento de los hon-
gos toxignicos, clasificndose estas condiciones en
intrnsecas y extrnsecas. Las condiciones intrnsecas
hacen referencia a las condiciones del sustrato sobre
el cual crece el hongo e incluyen la composicin de
carbohidratos, grasas, protena, macro y microele-
mentos, entre otros. Adems de la composicin del
grano existen otros factores como la actividad del
agua (Aw), pH y potencial de xido-reduccin (Daz,
1996a).
Los factores extrnsecos estn relacionados con la at-
msfera en la cual se encuentra almacenado el grano
y puede crecer un hongo toxignico como humedad
de la atmsfera de almacenamiento (ptima >70%),
temperatura atmosfrica la cual varia de acuerdo al
hongo y adecuado suministro de oxgeno, el cual no
es un factor limitante en condiciones normales de
almacenamiento (Daz, 1996a). Por lo general se
afectan sustratos como el maz, el trigo, el sorgo, la
torta de algodn, la cebada y el man (Daz, 1996b).
Los hongos toxignicos se clasifican de acuerdo con
el momento de infeccin en hongos de campo (fito-
patognicos) que infectan las plantas antes de la co-
secha y hongos de almacenamiento (saprofticos) que
invaden los granos almacenados. Dentro del primer
grupo se encuentran los gneros Fusarium (el ms
comn), Alternaria, Cladosporium, Helminthospo-
rium, Pullaria y Aspergillus. Entre los hongos sapro-
fticos los gneros ms importantes son Aspergillus y
Penicillium (Daz, 1996a).
Es importante anotar que la presencia del hongo
toxignico en un sustrato no implica por necesidad
la existencia de micotoxinas. Esto se debe a que ge-
neralmente solo un pequeo porcentaje de las cepas
de hongos posee la capacidad gentica de sintetizar
micotoxinas y a que la produccin de estos metaboli-
tos ocurre solo bajo estrictas condiciones ambientales
que no siempre se cumplen (Daz, 1996a).
INTRODUCCIN
Las Micotoxinas
Las micotoxinas surgen como compuestos de inters
toxicolgico luego de descubrirse su rol como agen-
tes etiolgicos de la enfermedad X de los pavos
reportada en los aos 60. Esta enfermedad asociada
al consumo de una harina de man procedente de
Brasil caus la muerte de ms de 100.000 pavitos
en Inglaterra. Con el tiempo se descubri que cier-
tas sustancias txicas aisladas del alimento causaron
dicha enfermedad. Estas sustancias se denominaron
aflatoxinas ya que el principal hongo productor de
estas result ser Aspergillus flavus (Sargeant, Sheri-
dan, O`Kelly & Carnaghan, 1961). Despus de las
aflatoxinas se descubrieron otras micotoxinas entre
las cuales se incluyen los tricoticenos, la ocratoxina
A, la zearalenona y hacia finales de la dcada de los
noventa un grupo de micotoxinas producidas por
hongos del gnero Fusarium a las cuales se les dio el
nombre de fumonisinas (Bezuidenhout et al, 1988).
La habilidad de las micotoxinas para inducir varios
tipos de cncer en animales domsticos y de experi-
mentacin constituye una gran preocupacin para la
salud pblica. En 1993 la Agencia Internacional de
Investigacin sobre el Cncer clasific las micotoxinas
de acuerdo a su carcinogenicidad, encontrando mico-
toxinas clasificables en el grupo 1 correspondientes
a compuestos carcingenos para humanos (como la
aflatoxina B1), en el grupo 2 correspondiente a com-
puestos posiblemente carcingenos para humanos
(aflatoxina M1, ocratoxina, fumonisina B1) y en el
grupo 3, correspondiente a compuestos no carcin-
genos para humanos (como zearalenona y tricotice-
nos) (Lesson et al., 1995).
Teniendo en cuenta que los metabolitos primarios
son aquellas molculas sintetizadas durante el creci-
miento del hongo, las micotoxinas son metabolitos
secundarios producidos cuando la fase de crecimien-
to termina o cuando hay deficiencias en nutrientes
esenciales. Bajo estas condiciones los procesos de
sntesis se encaminan hacia la produccin de pig-
mentos, antibiticos y micotoxinas, los cuales son
excretados de manera abundante durante la fase
estacionaria de crecimiento del hongo. Cuando las
micotoxinas son producidas en granos o alimentos
destinados a la alimentacin de animales o humanos
se convierten en un peligro potencial tanto para la sa-
lud humana como para la salud y produccin animal
(Daz, 1995). Hasta el 2004 se haban detectado y
clasificado como micotoxinas ms de 300 metabo-
litos secundarios provenientes de hongos filamento-
sos. Estas sustancias son producidas principalmente
por los gneros Aspergillus, Penicillium y Fusarium.
Se conoce que estos compuestos causan enfermeda-
des severas incluyendo ciertos tipos de cncer, dismi-
Revista TEORA Y PRAXIS INVESTIGATIVA, Volumen 5 - No. 2, Julio - Diciembre 2010
Centro de Investigacin y Desarrollo CID / Fundacin Universitaria de rea Andina
Micotoxinas y Aflatoxina B1, un problema en salud animal
73
Aflatoxinas
Las aflatoxinas (AF) son un grupo de metabolitos
heterocclicos sintetizados por algunas cepas de As-
pergillus flavus y Aspergillus parasiticus. La palabra
aflatoxina se deriva del principal hongo productor de
esta (Aspergillus flavus) y del sufijo toxina. Los Asper-
gillus son generalmente hongos de almacenamiento
y por lo comn no contaminan los granos antes de
la cosecha, sin embargo, condiciones de estrs en las
plantas y dao producido por insectos pueden dar
lugar a la infeccin a nivel de campo y a la produc-
cin de AF en los granos an no cosechados (Daz,
1996b).
Estudios realizados por el Laboratorio de Toxicologa
de la Facultad de Medicina Veterinaria y Zootecnia de
la Universidad Nacional de Colombia demostraron la
presencia de varias especies del gnero Aspergillus
spp. en muestras de maz y mazorca tomadas en la
regin del atlntico colombiano, donde se encontra-
ron niveles muy altos de aflatoxinas, en especial la B1
y la B2. Al parecer la gran produccin de estas mico-
toxinas y gran incidencia de hongos aflatoxignicos
se encontraron relacionadas con aspectos medioam-
bientales como elevadas precipitaciones, plagas y di-
versidad de hongos aflatoxignicos y cepas presentes
con gran capacidad de sntesis de aflatoxinas (Acua,
Daz & Espitia 2005), demostrando la importancia de
las condiciones tanto macro como microambientales
para el crecimiento de hongos micotoxignicos y la
produccin de micotoxinas. En otro estudio se co-
rrobor la prevalencia del gnero Aspergillus spp. en
granos de maz y algodn, en especial las especies A.
flavus y A. parasiticus, este ltimo capaz de producir
las cuatro aflatoxinas de ocurrencia natural (B1, B2,
G1 y G2) (Daz, Lozano & Acua, 2009). Hasta el
momento se han identificado cerca de 18 tipos de
aflatoxinas, siendo las nicas que se presentan de
manera natural la B1, B2, G1 y G2, mientras las de-
ms aflatoxinas como M1, M2, P1, Q1, aflatoxicol,
etc. se presentan como productos del metabolismo
(productos de biotransformacin) de sistemas micro-
bianos o animales. La existencia de cepas aflatoxig-
nicas de Aspergillus spp. y presencia de aflatoxinas
ha sido reportada en los cinco continentes (Daz,
1996b) donde se han hecho grandes esfuerzos por
controlar tanto el crecimiento del hongo toxignico
como de la produccin de la micotoxina (Daz et al.,
2009; Felix D` Mello, Macdonald, Postel, Dijksma,
Dujardin, & Placinta., 1998).
Tabla 1. Estrntoglns pnrn roJuclr ln oxposlcln , ol rlosgo Jo prosoncln Jo
nllntoxlnns AJnptnJo Jo Groopmnn ., 2008.
Tipo de intervencin Enfoque Resultado
Prlmnrlo ConJlclonos Jo
nlmnconnmlonto pos-
cosochn
RoJuccln on ln oxposlcln
n nllntoxlnns moJlJo por ln
roJuccln Jo los nlvolos Jo
nJuctos nllntoxlnn-nlbmlnn.
Prlmnrlo Agontos nJsorbontos
nlumlnoslllcntos
RoJuccln on ln oxposlcln
n nllntoxlnn on nnlmnlos
moJolo , onsn,os cllnlcos.
Prlmnrlo Clorollllnn Ellcncln JomostrnJn on
moJolos oxporlmontnlos ,
un 55/ Jo roJuccln on
nJuctos nllntoxlnn-ADN
urlnnrlos on onsn,os cllnlcos
humnnos.
SocunJnrlo Polllonolos Jo to vorJo Provoncln Jo cnncor
JomostrnJo on rntns ,
roJuccln Jo blomnrcnJoros
Jnno oxlJntlvo nl ADN on
onsn,os cllnlcos.
SocunJnrlo Dltlolotlonos oltlprnz
SocunJnrlo Brotos Jo brcoll
sullornlnno
Provoncln Jo cnncor on
moJolos murlnos. RoJuc-
cln Josls JoponJlonto Jo
nJuctos nllntoxlnn-ADN on
onsn,os cllnlcos humnnos.
Ellcncln JomostrnJn on ln
provoncln Jo tumoros
hopntlcos on rntns , moJu-
lncln Jo blomnrcnJoros
pnrn nllntoxlnn, proJlclonJo
ol olocto protoctor, sogn
onsn,os cllnlcos.
Revista TEORA Y PRAXIS INVESTIGATIVA, Volumen 5 - No. 2, Julio - Diciembre 2010
Centro de Investigacin y Desarrollo CID / Fundacin Universitaria de rea Andina
Hansen Wilber Murcia Rodrguez
74
Efectos De La Afb1 En La Salud Animal
Adems de los efectos carcingenos se conocen
efectos adversos de las micotoxinas en la salud en
general tanto de animales de produccin como mas-
cotas. Dentro de los sntomas se encuentran la re-
duccin en la ganancia de peso, efectos adversos en
la reproduccin, dao al sistema inmunolgico, sn-
tomas severos de intoxicacin e incluso muerte cuan-
do la dosis de micotoxina es demasiado alta (Hussein
& Brasel, 2001; Leeson , Diaz & Summers, 1995).
Diferentes estudios han demostrado los efectos ad-
versos sobre el sistema inmune de pollos en estadios
tempranos del desarrollo (Qureshi, Brake, Hamilton,
Hagler, & Nesheim, 1998) y efectos hematolgicos
y hepticos significativos a altas concentraciones en
adultos (Del Bianchi, Oliveira, Albuquerque, Guerra
& Correa, 2005) y durante el desarrollo, evaluan-
do su efecto en enzimas sricas, renales y hepti-
cas (Quezada, Cuellar, Jaramillo-Jurez, Valdivia &
Reyes, 2000). Tambin se han presentado efectos
hepatotxicos a altas concentraciones en codornices
(Oliveira et al. 2002), adems de afectar la produc-
cin de huevos (Ogido et al., 2004).
Dentro de las aflatoxinas, la AFB1 se encuentra como
un compuesto altamente txico para la mayora de
las especies y en especial aquellas muy susceptibles
como la trucha arco iris, los gatos o los patos. En
ensayos in vitro la toxicidad de la aflatoxinas G1, B2
y G2 es aproximadamente 50, 20 y 10% de la que
presenta la AFB1, respectivamente. Existen diferen-
cias de susceptibilidad entre animales de diferentes
especies frente a la AFB1. Los animales ms suscep-
tibles son el pato, el conejo y el gato, mientras que
los ms resistentes son el pollo, ratn, hmster y rata
(Tabla 2). En las aves la susceptibilidad vara teniendo
como ms susceptibles a los patos, seguido de los
pavos, gansos, faisanes y los pollos como la especie
aviar menos afectada. A su vez los animales jvenes
son ms susceptibles que los adultos y las hembras
ms resistentes que los machos (Daz, 1996b).
Tabla 2. DL
50
ornl nguJn Jo AFB1 on Jllorontos ospoclos AJnptnJo Jo Dlnz, 1996b.
Especie DL
50
(mg/kg)
Conoo 0.3-0.5
Pntlto 0.34-0.56
Gnto 0.55
CorJo 0.62
Truchn nrco lrls
lntrnporltononl
0.81
Porro 1.0
Cobn,o 1.4-2.0
von 2.0
Mlco 2.2
Polllto 6.5-16.5
Rntn 9.0
Hnmstor 10.2
Rntn 5.5-17.9
Alteracin del Adn y Carcinogenicidad
La AFB1 se bioactiva a travs de las citocromos
P450 a un metabolito electroflico altamente reacti-
vo e inestable que una vez formado reacciona con
macromolculas, especialmente con el ADN (produ-
ce alquilacin del ADN). Este metabolito, conocido
como aflatoxina-8,9-epxido (AFBO) es capaz de
unirse a los residuos de guanina de los cidos nuclei-
cos causando alteraciones irreversibles que pueden
llevar a carcinogenicidad, mutagenicidad y teratoge-
nicidad (Do & Choi, 2007; Eaton & Gallager, 1994;
Ferguson & Philpott, 2008; Verma, 2004). La bio-
transformacin de la AFB1 se inicia en las enzimas
citocromo P450 (CYP450) donde sufre oxidacin a
AFBO. La forma epxido puede conjugarse con glu-
tatin para continuar con la va de detoxificacin o
ser hidrolizada por una epxido hidrolasa para gene-
rar un hidrodiol (AFB1-8,9-dihidrodiol o dhd-AFB1),
el cual puede reaccionar fuertemente con protenas
Revista TEORA Y PRAXIS INVESTIGATIVA, Volumen 5 - No. 2, Julio - Diciembre 2010
Centro de Investigacin y Desarrollo CID / Fundacin Universitaria de rea Andina
Micotoxinas y Aflatoxina B1, un problema en salud animal
75
Se han reconocido que tanto la CYP1A2 como la
3A4 son capaces de oxidar la AFB1 tanto a formas
reactivas que incluyen la AFB1 endo-8,9-epxido y
AFB1 exo-8,9-epxido (forma mas toxica del epxi-
do), como a productos no activos que no son sus-
tratos ptimos para epoxidacin, como la AFM1,
AFQ1 (Figura 2) (Gallagher, Kunze, Stapleton &
Eaton, 1996; Guengerich et al., 1998; Guengerich,
Johnson, Ueng, Yamazaki & Shimada, 1996).
Figura 1. Rutns Jo blotrnnslormncln Jo ln AFB1 MoJlllcnJo Jo Enton ,
Gnllnghor, 1994. CYP450s: cltocromo P450s; PHS: prostnglnnJlnn H-slntnsn;
GSTs: glutntln S-trnnslornsns; UDP-GTs: UDP-glucuronoslltrnnslornsns; ST:
sullotrnnslornsns.
Allntoxlnn B1 Motnbolltos hlJroxllnJos
UDP-GT, ST
GlucurnlJos , conugnJos
con sullnto
AJuctos
Jo ADN
Allntoxlnn B1-8,9-opxlJo
oxo-,onJo-,ostorolsmoros
EpxlJo
hlJrolnsn?
ConugnJos GSH
DlhlJroJlol
Unln n protolnns
Muorto colulnr
ToxlclJnJ
Mutnclonos
GSTs
Ropnrncln
Jol ADN
CYP450s
Llpoxlgonnsns
PHS
CANCER
Figura 2.ProJuctos Jo oxlJncln Jo ln AFB1 TomnJo Jo Guongorlch cI a!., 1998.
8
9 H
H
H
H
H
H
H
H
H
9n
6n
H
H
CH
3
CH
3
CH
3
CH
3
CH
3
AFB
1
-cxo-8,9-oxlJo
AFB
1
-cndo-8,9-oxlJo
2
3
AFB
1
AFM
1
AFQ
1
y tener efectos citotxicos. En los casos en que el
epxido llega a conjugarse con glutatin, o la AFB1
no sufre epoxidacin sino adicin grupos OH- y pos-
terior conjugacin con acido glucurnico o sulfato,
los efectos txicos de la molcula se ven neutraliza-
dos (Figura 1) (Eaton & Gallagher, 1994).
Revista TEORA Y PRAXIS INVESTIGATIVA, Volumen 5 - No. 2, Julio - Diciembre 2010
Centro de Investigacin y Desarrollo CID / Fundacin Universitaria de rea Andina
Hansen Wilber Murcia Rodrguez
76
Bioactivacin de la Afb1 En Aves y Mamferos
El hecho de que se presenten diferentes tipos de ci-
tocromos P450 capaces de transformar la AFB1 a
formas reactivas (fase I de detoxificacin), adems de
una pobre conjugacin de estas formas reactivas con
glutatin o sulfatos (fase II de detoxificacin) hace que
diferentes especies de aves y de mamferos presenten
diferentes niveles de susceptibilidad.
En la mayora de las especies de mamferos la bio-
transformacin de la AFB1 ocurre a travs de cito-
cromos P450, encontrndose a las citocromo 1A1,
2A3, 2B7, 2C8, 2K1 y 3A3/4 implicadas en la acti-
vacin heptica y produccin de AFBO (Klein et al.,
2003). En humanos se han reportado estas mismas
citocromos como agentes bioactivadores de la AFB1
(Doi, Patterson, Gallagher, 2002; Omiecinski, Rem-
mel &Hosagrahara,1999) al igual que a la CYP2A6
(Pelkonen, Rautio, A., Raunio, H. & Pasanen, 2000).
Las enzimas citocromo P450 aviares parecen ser del
mismo tipo de aquellas encontradas en mamferos,
incluyendo la especie humana. Por ejemplo, estudios
realizados por Nebbia, Dacasto, Rossetto, Giuliano
y Carletti en el 2003 demostraron la presencia de
CYP2B1, 3E1, 1A1 y 3A4 en pollos. Asi mismo,
Gorman, Walton, Sinclair y Sinclair en el ao de
1998, realizando immunoblots de microsomas
extrados de embriones de pato y pollo identificaron
otlogos aviares CYP1A1, 1A2, 1A4 y 1A5.
En pavos, especie altamente sensible a los efectos
adversos de las aflatoxinas se ha atribuido el efec-
to txico a la actividad de las enzimas CYP1A1 y
3A4, capaces de biotransformar la AFB1 a su forma
epxido (Klein, Buckner, Kelly & Coulombe, 2000).
En esta especie se ha demostrado que el efecto es
ms pronunciado en aves jvenes que en adultas y se
ha demostrando que cantidades relativamente bajas
de AFB1 presentes en el alimento pueden llegar a
causar efectos deletreos (Klein, Van Vleet, Hall &
Coulombe, 2002). Tambin se ha encontrado un or-
tlogo aviar de la citocromo 1A5 humana que ha
presentado actividad metoxiresorufin O-dealquilasa
y oxidacin del AFB1 (Yip & Coulombe Jr., 2006),
lo cual ayuda a explicar la alta susceptibilidad de los
pavos, ya que el efecto de la aflatoxina depende de su
oxidacin a la forma exo-epxido.
En embriones de pollos como de patos y pavos se
ha demostrado actividad EROD (etoxiresorufin orto-
deetilasa), los cual indica la presencia de citocromos
1A que no necesariamente corresponden a ortlogos
a los de mamferos, pero que presentan una actividad
enzimtica similar (Brunstrm & Halldin, 1998). Yip
y Coulombe en el 2006 demostraron la presencia
de un ortlogo de pollos en pavos, la CYP1A5, con
capacidad tanto de oxidar la AFB1 a su forma epxi-
do como de producir AFM1. En patos, pollos, pavos
y codornices se demostr la capacidad de biotrans-
formacin de la AFB1 a su forma AFBO (Lozano
& Daz, 2005), pero no se determin cual o cuales
de los ortlogos aviares eran los responsables de la
transformacin de la aflatoxina a su forma epxido.
Aunque las aflatoxinas y sus efectos txicos se co-
nocen desde los aos sesenta (Newberne & Butler;
1969; Patterson, 1973), las enzimas responsables de
su metabolismo en algunas especies de mamferos
y en muchas especies aviares (especialmente pollos,
patos, pavos y codornices) no han sido caracterizadas
de manera completa. Por esto es necesario investigar
cuales enzimas de la superfamilia de las citocromos
P450 son las responsables del metabolismo y bioac-
tivacin de la AFB1 en especies aviares de inters
comercial.
REFERENCIAS
Acua, C.A., Daz, G.J., Espitia, M.E. (2005). Afla-
toxinas en maz: reporte de caso en la costa
atlntica colombiana. Revista de la Facultad de
Medicina Veterinaria 52: 156-162.
Bezuidenhout, S.C., Gelderblom, W.C.A., Gorst -
Allman, C.P., Horak, R.M., Marasas, W.F.O.,
Spiteller, G., Vleggaar, R. (1988). Structure
elucidation of the fumonisins, mycotoxins from
Fusarium moniliforme. Journal of the Chemical
Society. Chemical Communications 743-745.
Brunstrm, B., Halldin, K. (1998). EROD induction
by environmental contaminants in avian embr-
yo livers. Comparative Biochemistry and Phy-
siology Part C 121: 213219.
Bnger, J., Westphal, G., Mnnich, A., Hinnendahl,
B., Hallier, E., Mller, M. (2004). Cytotoxicity
of occupationally and environmentally relevant
mycotoxins. Toxicology 202: 199211.
Del Bianchi, M., Oliveira, C.A.F., Albuquerque, R.,
Guerra, J.L., Correa B. (2005). Effects of pro-
longed oral administration of aflatoxin B1 and
fumonisin B1 in broiler chickens. Poultry Scien-
ce 84: 1835-1840.
Revista TEORA Y PRAXIS INVESTIGATIVA, Volumen 5 - No. 2, Julio - Diciembre 2010
Centro de Investigacin y Desarrollo CID / Fundacin Universitaria de rea Andina
Micotoxinas y Aflatoxina B1, un problema en salud animal
77
Daz, G. J. (1995). Regulacin de los niveles mxi-
mos tolerables de micotoxinas en materias pri-
mas y alimentos terminados. Veterinaria al Da
1(3):22-27.
Daz, G., J. (1996a). Micotoxinas y micotoxicosis en
salud humana y animal. Primera Parte. Veteri-
naria al Da 2(1):28-34.
Daz, G., J. (1996b). Micotoxinas y micotoxicosis en
salud humana y animal. Segunda Parte. Veteri-
naria al Da 2(3):3-8.
Daz, G.J., Lozano, M.C., Acua, A. (2009). Pre-
valence of Aspergillus species on selected Co-
lombian animal feedstuffs and ability of Asper-
gillus section Flavi to produce aflatoxins. World
Mycotoxin Journal 2 (1): 31-34.
Do, J.H., Choi, D. (2007). Aflatoxins: detection,
toxicity, and biosynthesis. Biotechnology and
Bioprocesses Eng. 12: 585-593.
Doi, A.M., Patterson, P.E., Gallagher, E.P. (2002).
Variability in aflatoxin B1macromolecular bin-
ding and relationship to biotransformation en-
zyme expression in human prenatal and adult
liver. Toxicology and Applied Pharmacology
181: 4859.
Eaton, D.L., Gallagher, E.P. (1994). Mechanisms
of aflatoxin carcinogenesis. Annual Review of
Pharmacology and Toxicology 34: 135-172.
Felix D` Mello, J.P., Macdonald, A.M.C., Postel, D.,
Dijksma, W.T.P., Dujardin, A., Placinta, C.M.
(1998). Pesticide use and mycotoxin production
in Fusarium and Aspergillus phytopathogens.
European Journal of Plant Pathology 104:
741-751.
Ferguson, L.R., Philpott, M. (2008). Nutrition and
mutagenesis. Annual Review of Nutrition 28:
31329.
Gallagher, E., Kunze, K.L., Stapleton, P.L., Eaton,
D.L. (1996). The Kinetics of aflatoxin B1 oxi-
dation by human cDNA-expressed and human
liver microsomal cytochromes P450 1A2 and
3A4. Toxicology and Applied Pharmacology
141: 595-606.
Gorman, N., Walton, H.S., Sinclair, J.F., Sinclair,
P.R. (1998). CYP1A-catalyzed uroporphyri-
nogen oxidation in hepatic microsomas from
non-mammalian vertebrates (chick and duck
embryos, scup and alligator). Comparative Bio-
chemistry and Physiology Part C 121: 405
412.
Groopman, J.D., Kensler, T.W., Wild, C.P. (2008).
Protective interventions to prevent aflatoxin-
induced carcinogenesis in developing countries.
Annual Review of Pubblic Health 29: 187203.
Guengerich, F.P., Johnson, W.W., Shimada, T.,
Ueng, Y., Yamazaki, H., Langout, S. (1998).
Activation and detoxication of aflatoxin B1.
Mutation Research 402:121-128.
Guengerich, F.P., Johnson, W.W., Ueng, Y., Yama-
zaki, H., Shimada, T (1996). Involvement of
cytochrome P450, glutathione S-transferase
and epoxide hydrolase in the metabolism of
aflatoxin B1 and relevance to risk of human li-
ver cancer. Environmental Health Perspectives
104(3): 557 562.
Hussein, H.S., Brasel, J.M. (2001). Toxicity, meta-
bolism, and impact of mycotoxins on humans
and animals. Toxicology 167: 101134.
Klein, P.J., Van Vleet, T.R., Hall, J.O., Coulombe
Jr., R.A. (2003). Effects of dietary butylated
hydroxytoluene on aflatoxin B1-relevant meta-
bolic enzymes in turkeys. Food Chemistry and
Toxicology 41: 671678.
Klein, P.J., Van Vleet, T.R., Hall, J.O., Coulombe,
R.A. (2002). Biochemical factors underlying the
age-related sensitivity of turkeys to aflatoxin B1.
Comparative Biochemistry and Physiology Part
C132: 193201.
Klein P., Buckner R., Kelly J. and Coulombe R.
(2000). Biochemical basis for the extreme sen-
sivity of turkeys to aflatoxin B1. Toxicology and
Applied Pharmacology 151:152-158.
Leeson S., Diaz G.J., and Summers J.D. (1995).
Poultry metabolic disorders and mycotoxins.
University Books, Guelph, Ontario, pp 249-
280.
Revista TEORA Y PRAXIS INVESTIGATIVA, Volumen 5 - No. 2, Julio - Diciembre 2010
Centro de Investigacin y Desarrollo CID / Fundacin Universitaria de rea Andina
Hansen Wilber Murcia Rodrguez
78
Lozano, M.C. and Diaz, G.J. (2005). Microsomal
and cytosolic phase I biotransformation of afla-
toxin B1 in four poultry species. British Poultry
Science 47:734-741.
Nebbia, C., Dacasto, M., Rossetto, A., Giuliano, A.,
Carletti, M. (2003). Comparative expression of
liver cytochrome P450-dependent monooxyge-
nases in the horse and in other agricultural and
laboratory species. Veterinary Journal 165: 53-
64.
Newberne, P.M., Butler, W.H. (1969). Acute and
chronic effects of aflatoxin on the liver of do-
mestic and laboratory animals: A review. Can-
cer Research 29: 236-250.
Ogido, R., Oliveira, C.A.F., Ledoux, D.R., Rot-
tinghaus, G.E., Corra, B., Butkeraitis, P., Reis,
T.A., Gonales, E., Albuquerque, R. (2004).
Effects of prolonged administration of aflatoxin
B1 and fumonisin B1 in laying japanese quail.
Poultry Science 83: 1953-1958.
Oliveira, C.A.F., Rosmaninho, J.F., Butkeraitis, P.,
Corra B., Reis, T.A., Guerra, J.L., Albuquer-
que, R., Moro, M.E.G. (2002). Effect of low le-
vels of dietary aflatoxin B1 on laying japanese
quail. Poultry Science 81: 976-980.
Omiecinski, C.J., Remmel, R.P., Hosagrahara, V.P.
(1999). Concise review of the cytochrome
P450s and their roles in toxicology. Toxicologi-
cal Sciences 48: 151-156.
Patterrson, D.S.P. (1973). Metabolism as a factor in
determining the toxic action of the aflatoxins in
different animal species. Food and Cosmetics
Toxicology 11: 287-294.
Pelkonen, O., Rautio, A., Raunio, H., Pasanen, M.
(2000). CYP2A6: a human coumarin 7-hydro-
xylase. Toxicology 144: 139147.
Quezada, T., Cuellar H., Jaramillo-Jurez, F., Valdi-
via, A.G., Reyes, J.L. (2000). Effects of aflatoxin
B1 on the liver and kidney of broiler chickens
during development. Comparative biochemos-
try and Physiology Part C 125: 265272.
Qureshi, M.A., Brake, J., Hamilton, P.B. Hagler,
W.M., Nesheim S. (1998). Dietary exposure of
broiler breeders to aflatoxin results in immune
dysfunction in progeny chicks. Poultry Science
77: 812-819.
Sargeant, K., Sheridan, A., O`kelly, J., Carnaghan,
R.B.A. (1961). Toxicity associated with certain
samples of groundnuts. Nature 192: 1096-
1097.
SAS Institute Inc. (2008). SAS/STAT 9.2 Users
Guide. Cary, NC: SAS Institute Inc.
Verma, R.J. (2004). Aflatoxin causes DNA damage.
International Journal of Human Genetics 4(4):
231-236.
Yip, S.S.M., Coulombe Jr., R.A. (2006). Molecular
cloning and expression of a novel cytochrome
P450 from turkey liver with aflatoxin B1 oxidi-
zing activity. Chemical Research in Toxicology.
19: 30-37.
Das könnte Ihnen auch gefallen
- GUÍA PARA EL DESARROLLO DE LA INTELIGENCIA EMOCIONAL GRADO 1° y 2°Dokument11 SeitenGUÍA PARA EL DESARROLLO DE LA INTELIGENCIA EMOCIONAL GRADO 1° y 2°Angela CastelblancoNoch keine Bewertungen
- Ordenanza MunicipalDokument6 SeitenOrdenanza MunicipalElianaEstelaBejaranoNoch keine Bewertungen
- Anexo 2-Fase 2 - Identificación de Biomoléculas en Los AlimentosDokument4 SeitenAnexo 2-Fase 2 - Identificación de Biomoléculas en Los AlimentosJaime CucaitaNoch keine Bewertungen
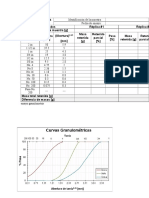
- Ensayos de Granulometria Contenidode Humedad y Conprecion SimpleDokument4 SeitenEnsayos de Granulometria Contenidode Humedad y Conprecion SimpleOber ZelaNoch keine Bewertungen
- La Informática y La Educación InicialDokument5 SeitenLa Informática y La Educación InicialKirsy Johanna Pérez MejíaNoch keine Bewertungen
- Generos Discurcivos 1Dokument2 SeitenGeneros Discurcivos 1Tachi HaMNoch keine Bewertungen
- Lista de Ejercicios - BloqueADokument3 SeitenLista de Ejercicios - BloqueAFrancisco palacios abarcaNoch keine Bewertungen
- TotoraDokument27 SeitenTotoraKatia Huaraya MamaniNoch keine Bewertungen
- Material 13 EstrategiaDokument5 SeitenMaterial 13 EstrategiaJaime Mauricio Caceres LealNoch keine Bewertungen
- Biografía de Ovide DecrolyDokument5 SeitenBiografía de Ovide DecrolyCamilo AndradeNoch keine Bewertungen
- Ejemplo Informe Examen MentalDokument2 SeitenEjemplo Informe Examen MentalMarcela Elizabeth LaraNoch keine Bewertungen
- Psicologia EspecialDokument8 SeitenPsicologia EspecialLuis Marcelo ValergaNoch keine Bewertungen
- Pronunciacion ELEDokument18 SeitenPronunciacion ELEOscar ArevaloNoch keine Bewertungen
- Autorización A Persona Juridica para Vender Vehículo en ConsignaciónDokument2 SeitenAutorización A Persona Juridica para Vender Vehículo en ConsignaciónGerardo AmosNoch keine Bewertungen
- Guía 1 PEIDokument10 SeitenGuía 1 PEIJessica HernándezNoch keine Bewertungen
- Crítica Literaria y GéneroDokument164 SeitenCrítica Literaria y GéneroAnaLauraNoch keine Bewertungen
- Principios Regulatorios Del PresupuestoDokument3 SeitenPrincipios Regulatorios Del PresupuestoJose Luis Rodriguez100% (2)
- I. Diagrama de ParetoDokument3 SeitenI. Diagrama de ParetoJamirNoch keine Bewertungen
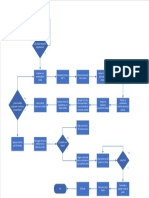
- Diagrama de Flujo Panque de ZanahoriaDokument1 SeiteDiagrama de Flujo Panque de ZanahoriaSugey de Omar100% (1)
- PNF MIC Orientaciones Estudiantes y Profesores Semana 7 Del 8 Al 13 de JunioDokument62 SeitenPNF MIC Orientaciones Estudiantes y Profesores Semana 7 Del 8 Al 13 de JunioLA India Romero100% (1)
- El Artículo 2011 Hasta El 2022 Del Código Civil DominicanoDokument8 SeitenEl Artículo 2011 Hasta El 2022 Del Código Civil Dominicanofrancisco vilorioNoch keine Bewertungen
- Heredia - Adrian - Riesgos de Seguridad - 5tosoftware - AplicacionesAutonoDokument5 SeitenHeredia - Adrian - Riesgos de Seguridad - 5tosoftware - AplicacionesAutonoJonathan QuezadaNoch keine Bewertungen
- Comunicado 003-2020 ActualizadoDokument1 SeiteComunicado 003-2020 Actualizadocibernauta14Noch keine Bewertungen
- Tesis Web PDFDokument21 SeitenTesis Web PDFRead ReadNoch keine Bewertungen
- La Leccion de Los GansosDokument3 SeitenLa Leccion de Los GansosLeslie Escobar100% (2)
- Algunos de Los Prefijos Más UsadosDokument3 SeitenAlgunos de Los Prefijos Más UsadosYessenia Velasquez Aros ʚϊɞNoch keine Bewertungen
- Curso: EE354 Análisis de Sistemas de Potencia II: Escuela Profesional de Ingeniería EléctricaDokument21 SeitenCurso: EE354 Análisis de Sistemas de Potencia II: Escuela Profesional de Ingeniería EléctricaULISES MARIANO MAYANGA MENDOZANoch keine Bewertungen
- Recurso de InconformidadDokument4 SeitenRecurso de InconformidadMario Alberto Islas TorresNoch keine Bewertungen
- Diario de Campo 2Dokument3 SeitenDiario de Campo 2Jose Millan100% (4)
- Unificación de Italia y Alemania - PDF ResumidoDokument2 SeitenUnificación de Italia y Alemania - PDF ResumidoSabrina SP100% (2)