Beruflich Dokumente
Kultur Dokumente
Curso de HPLC Ecuacion de Van Deemter
Hochgeladen von
alextm89Originaltitel
Copyright
Verfügbare Formate
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
Verfügbare Formate
Curso de HPLC Ecuacion de Van Deemter
Hochgeladen von
alextm89Copyright:
Verfügbare Formate
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
Curso de cromatografa de lquidos de alta resolucin (HPLC): Prcticas de laboratorio y cuestiones terico-prcticas. Parte I. Introduccin y prctica de laboratorio: clculo de la eficiencia y representacin grfica de la ecuacin de van Deemter
Mara Estrella Legaz Gonzlez. Mara Sacristn San Cristbal. Eva Mara Daz Pea. Borja Alarcn Aguareles. Carlos Vicente Crdoba.
Departamento de Biologa Vegetal I (Fisiologa Vegetal). Facultad de Biologa. Universidad Complutense de Madrid. Avenida Jos Antonio Novais, 2. 28040 Madrid. Espaa. melegaz@bio.ucm.es marasacristan@bio.ucm.es evam.diaz@bio.ucm.es borjaestremera@hotmail.com cvicente@bio.ucm.es
Resumen: En el presente curso de HPLC se plantean tres prcticas de laboratorio, de la ms fcil a la ms compleja, publicadas en tres partes en las que el alumno trata de resolver los problemas iniciales que cualquier investigador debe plantearse a la hora de realizar un anlisis cromatogrfico. En la primera prctica: clculo de la eficiencia y representacin grfica de la ecuacin de van Deemter (Parte I), se calcula el flujo de fase mvil ptimo, coincidente con la menor altura equivalente de plato terico. En la segunda prctica: anlisis cuantitativo bsico (Parte II), se estudia la respuesta del detector en funcin de la masa de analito inyectada. La obtencin de ecuaciones, por regresin lineal, permite el clculo de masas desconocidas de analitos inyectados cuando se interpola en las mismas. La tercera prctica: optimizacin en la separacin de compuestos semejantes mediante modificacin de la fase mvil (Parte III), trata de resolver la separacin de una muestra patrn de seis substancias, de naturaleza semejante, en sus componentes individuales. Para ello se realizan separaciones con fases mviles isocrticas o en gradiente. El curso se completa con una serie de cuestiones terico-prcticas (Parte IV), elaboradas a partir de separaciones reales en las que el alumno debe discutir las posibles respuestas a las preguntas que se formulan. Palabras clave: Fase estacionaria. Fase mvil. Columna analtica. Analito. HPLC. Eficiencia. Platos tericos. Tiempo de retencin. Masa inyectada. Anlisis en gradiente. Anlisis isocrtico.
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
PRESENTACIN El origen y la base de este curso fue la asignatura que la Prof. Legaz imparti como curso de Doctorado en la Facultad de Biologa de la UCM bajo el ttulo de Fitoqumica Experimental, despus denominada Anlisis Fitoqumico: Cromatografa y Tcnicas Afines, con una duracin de 75h, desde 1983 a 2006, veintitrs aos consecutivos. Con las ampliaciones y adaptaciones necesarias para la finalidad que persegua, la Prof. Legaz imparti el curso de Especializacin de Instrumentacin en Tecnologa Ambiental: Cromatografa de Gases y Lquidos y Espectrometra de masas , durante 5 aos acadmicos, con una duracin de 90h, en el Instituto Universitario de Ciencias Ambientales (IUCA) de la Universidad Complutense de Madrid, desde 1986 a 1991. Cuando este Centro estableci su Master Universitario bianual en Ciencias Ambientales, pionero de los Masters Complutenses, este mismo curso fue impartido entre 1992 y 1994. A requerimiento de diferentes Universidades Iberoamericanas, se hicieron modificaciones del curso, de acuerdo con las necesidades de cada Centro y fue impartido: En la Universidad de La Habana (Cuba) en Junio de 1988, con el ttulo de I Curso de Postgrado "Cromatografa de Gases y Lquidos. En la Universidad de La Habana (Cuba) en Octubre de 1989, con el ttulo de IV Curso Internacional de Postgrado: Curso Terico-Prctico sobre Cromatografa Lquida de Alta Resolucin", en colaboracin con el Instituto de Investigaciones Nucleares. En la Universidade Federal da Paraiba (Pb, Brasil) en Mayo de 1988, con el ttulo de II Curso de Postgrado "Curso Internacional do Cromatografa Lquida de Alta Pressao (HPLC)", aprobado por el Conselho Superior de Ensino (Resoluao No 023/88). En el Laboratorio de Tecnologa Farmacutica de la Universidade Federal da Paraiba (Pb, Brasil) en Septiembre de 1991, con el ttulo de V Curso Internacional Terico-Prctico de Cromatografa de Alta Resoluao. En el Departamento de Fisiologa Vegetal de la Facultad de Ciencias Agrarias de la Universidad Nacional de Rosario (Argentina), en Marzo de 1989, con el ttulo de "III Curso Terico-Prctico sobre Cromatografa Lquida de Alta Resolucin". En el Departamento de Botnica, Centro de Ciencias Biolgicas, de la Universidad Federal de Pernambuco (PE, Brasil) en Noviembre de 1993, con el ttulo de VI Curso Internacional de HPLC e bases tericas de Electroforese Capilar. En el Departamento de Biologa, Facultad de Ciencias de la Universidad Nacional
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
Autnoma de Mxico en Diciembre de 1993, con el ttulo de VII Curso TericoPrctico: Cromatografa Lquida de Alta Presin de Biomolculas con bases tericas de Electroforesis Capilar. Y, finalmente, en la Universidade de Tiradentes (Aracaju, SE, Brasil), en Marzo de 2010, con el ttulo de VIII Curso terico-Prctico sobre Cromatografa Lquida de Alta Resolucin". Desgloses de este curso han sido mdulos de enseanza en el Colegio Oficial de Bilogos (Delegacin de Madrid), impartindose el Curso Electroforesis Capilar, Nivel I, en Diciembre de 1996, el Curso HPLC, Nivel I, en Abril de 1998 y el curso Electroforesis Capilar, Nivel I, en Mayo de 1998. En resumen, las diferentes versiones, modificaciones y actualizaciones de este curso han constituido Curso de Doctorado (23 aos), asignatura de Master (7 aos), curso Internacional de Postgrado (8 aos) y cursos de iniciacin (3 aos). Parte de la experiencia adquirida durante este largo periodo de docencia terico-prctica constituye el ncleo fundamental de estas pginas.
INTRODUCCIN GENERAL
El trmino cromatografa deriva de las palabras griegas chroma (color) y graphein (escribir), aludiendo a que los pigmentos vegetales separados originalmente por Mikhail Semenovich Tswett se ponen de manifiesto como bandas coloreadas. No obstante, el mismo Tswett indic (Tswett, 1906) que tambin podan separarse substancias incoloras por el mismo procedimiento. Sin duda, la cromatografa es uno de los mtodos de separacin ms poderosos que se hayan descubierto. La I.U.P.A.C. la define como: "Un mtodo utilizado inicialmente para la separacin de los componentes de una muestra en la cual los componentes se distribuyen en dos fases, una de las cuales es estacionaria, mientras que la otra se mueve. La fase estacionaria puede ser un slido, un lquido sobre un soporte slido, o un gel. La fase estacionaria puede estar contenida en una columna, extendida en forma de capa o dispuesta en forma de pelcula. La fase mvil puede ser gaseosa o lquida". La cromatografa es una tcnica cuyo campo de aplicacin se extiende a todas las reas de investigacin, Qumica, Bioqumica o Biologa, entre otras, aplicndose a escala macro o micro. Los mtodos cromatogrficos se clasifican atendiendo a la naturaleza de la fase mvil (gas o lquido), de la fase estacionaria (lquido o slido), del soporte utilizado (columna, papel o placa), del mecanismo de separacin (adsorcin, reparto, intercambio inico o permeacin en gel) e incluso del tipo de soluto (iones, protenas,
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
polmeros, etc.). En cromatografa lquida, utilizando como mecanismo de separacin el reparto, cuando la fase estacionaria es menos polar que la fase mvil el sistema se denomina fase reversa y, por tanto, los analitos polares tienen menos afinidad por la fase estacionaria que los apolares, eluyendo en primer lugar. Este sistema es el utilizado en la mayora de las separaciones lquido-lquido de alta resolucin (HPLC) y el que se emplear en las tres prcticas propuestas. El mecanismo de separacin ser, principalmente, el reparto, por lo que los solutos se repartirn entre una fase estacionaria lquida y apolar y una fase mvil tambin lquida, ms polar que la anterior, si bien no se descarta una cierta adsorcin. En cualquier caso, la separacin se produce porque las molculas de soluto se distribuyen entre las dos fases en funcin de su solubilidad relativa en cada una de ellas. En su desplazamiento a lo largo del sistema cromatogrfico, los solutos se mueven a diferentes velocidades, dependiendo de su afinidad por la fase estacionaria respecto a la fase mvil. Cada analito, por tanto, se distribuir entre ambas fases segn un equilibrio caracterizado por una constante denominada constante de distribucin, coeficiente de distribucin o coeficiente de reparto (K). Para un soluto, s, Ks = ss / sm donde, ss es la concentracin de soluto, s, en fase estacionaria y sm es la concentracin de soluto, s, en fase mvil. Cuanto mayor sea el valor de K, mayor ser la afinidad del soluto por la fase estacionaria y, por tanto, menor la velocidad de desplazamiento a travs de la columna. La concentracin de cada analito, medida a la salida de la columna mediante un sistema de deteccin, se representa en funcin del volumen de la fase mvil o del tiempo transcurrido desde la introduccin de la muestra, obtenindose una grfica denominada cromatograma que contiene diferentes picos, cada uno de los cuales se corresponde con un analito diferente. Cuanto mayor sea el tiempo de permanencia de un soluto en la columna, mayor ser su coeficiente de reparto y ms ancho ser el pico representado en el cromatograma. El porqu del ensanchamiento de los picos y la optimizacin del sistema cromatogrfico para evitar este fenmeno en la medida de lo posible, ser tratado en la Prctica 1: Clculo de la eficiencia y representacin grfica de la ecuacin de van Deemter (ver Parte I). Aunque la cromatografa es uno de los mtodos de separacin por excelencia, tambin es posible su empleo en anlisis cualitativo (aplicando sistemas de deteccin especficos como espectrmetros de masas, infrarrojos o resonancia magntica nuclear, entre otros) y, sobre todo, cuantitativo. Las aplicaciones cuantitativas de la cromatografa en columna, como la que se propone, se basan en la comparacin de la altura o el rea del pico del analito, obtenido en el cromatograma, con respecto a los patrones de concentracin conocida. Normalmente se utiliza la medida del rea del pico, ya que la mayora de los sistemas cromatogrficos modernos estn acoplados a sistemas de integracin elctricos mediante softwares especficos que permiten este clculo. En sistemas cromatogrficos que utilizan detectores ultravioleta, la respuesta de sos depende de la absortividad de los correspondientes analitos, por lo que
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
normalmente se utilizan los denominados factores de respuesta. El clculo de estos factores, as como la cuantificacin basada en la construccin de rectas de calibrado ser objeto de la Prctica 2: Anlisis cuantitativo bsico (ver Parte II). El fin ltimo que persigue la cromatografa, como se ha comentado ampliamente, es la separacin. En un sistema cromatogrfico, empleando como mecanismo de separacin el reparto y con una fase estacionaria determinada apolar, la nica posibilidad que se nos ofrece para optimizar el sistema, sin modificar la temperatura, es variar la fase mvil, bien modificando su velocidad o su composicin. Si la composicin de la fase mvil no vara durante el anlisis, se habla de sistema de fase mvil isocrtico, mientras que si sta vara durante la elucin, se denomina sistema de fase mvil en gradiente. La variacin de la composicin pue de ser lineal, cncava o convexa en sus mltiples formas (respecto al porcentaje de disolvente principal en el otro u otros) en el tiempo. Los sistemas de fase mvil isocrticos se utilizan cuando el nmero de analitos de la muestra problema no es demasiado grande, mientras que si ste es elevado, para conseguir condiciones ptimas de separacin se debe recurrir a sistemas de fase mvil en gradiente. En estos casos puede ocurrir que se consigan buenas condiciones para la separacin de algunos analitos pero que esto vaya en detrimento de otros. El objetivo de la Prctica 3: Optimizacin en la separacin de compuestos semejantes mediante modificacin de la fase mvil (ver Parte III) es justamente ste, tratar de buscar el gradiente de fase mvil adecuado que permita la separacin de todos los compuestos en el menor tiempo de anlisis y con la mxima eficiencia. Como colofn a esta segunda parte del curso de HPLC, se proponen Cuestiones Terico-Prcticas (ver Parte IV), en las cuales se piden posibles respuestas a unos supuestos prcticos obtenidos de separaciones reales, que el alumno deber discutir. La experiencia a lo largo de todos estos aos en los que el curso se ha venido impartiendo a diferentes niveles, nos dice que stas constituyen un complemento indispensable de las prcticas de laboratorio.
PRCTICA DE LABORATORIO CLCULO DE LA EFICIENCIA Y REPRESENTACIN GRFICA DE LA ECUACIN DE van DEEMTER
Resumen: En la prctica que se plantea, el alumno calcula diferentes parmetros cromatogrficos sobre el pico de cido p-hidroxibenzoico, segn el flujo de fase mvil empleado, entre 0,2 y 1 mLmin-1. Se realiza la representacin grfica de la ecuacin de van Deemter (altura equivalente de plato terico (H) frente a flujo de fase mvil), con objeto de precisar el mnimo de la curva. La mxima eficiencia del pico se corresponde con el flujo de fase mvil que proporciona el mnimo valor de H.
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
Palabras clave: analito. Columna analtica. Eficiencia fase estacionaria. Fase mvil. HPLC. Platos tericos. Tiempo de retencin.
INTRODUCCIN
La mayor o menor retencin de los analitos de una muestra en la fase estacionaria depende de las correspondientes afinidades de stos. Estas afinidades, a su vez, dependen de diversos factores entre los que cabe mencionar: interacciones inicas entre especies de carga opuesta, interacciones de van der Waals, del tipo dipolo-dipolo o dipolo-dipolo inducido, interacciones por fuerzas de dispersin o formacin de enlaces de hidrgeno. La banda cromatogrfica, expresada en forma de picos en el cromatograma, cuando es ideal muestra una gran semejanza con las curvas de error normal o Gaussianas que se pueden atribuir a la combinacin aditiva de los movimientos aleatorios de las numerosas molculas de soluto durante el proceso. Mientras sucede el desplazamiento por el interior de la columna cromatogrfica, un analito experimenta miles de transferencias entre las fases mvil y estacionaria. El tiempo que pasa en cada una es muy irregular y depende de que gane accidentalmente suficiente energa trmica del medio para que se produzca la transferencia. Dado que la molcula slo eluye cuando reside en la fase mvil, su migracin a travs de la columna es muy irregular. Unas molculas se desplazan con rapidez y otras se retrasan debido a que se retienen mayor tiempo que el promedio en la fase estacionaria. La consecuencia de estos procesos individuales aleatorios es una dispersin simtrica de las velocidades alrededor del valor medio, originndose un pico Gaussiano en el que casi el 96% del rea se encuentra dentro del intervalo comprendido entre ms y menos dos veces la desviacin estndar alrededor del mximo (Fig. 1 A).
a=b
a<b
a>b
Figura 1. Forma de los picos cromatogrficos. A, pico Gaussiano ideal con b=4. B, pico con tailing. C, pico con fronting.
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
Sin embargo, no siempre sucede as y los picos pueden presentar distintas formas. Por ejemplo, cuando se produce retencin excesiva del soluto en la fase estacionaria, debido a multitud de causas, se habla del fenmeno tailing (Fig. 1 B), mientras que si existen problemas fsicos en el interior de la columna que distorsionan la trayectoria de paso, se habla del fenmeno fronting (Fig. 1 C), hechos que se comentarn ms adelante cuando se trate la triangulacin de los picos. La anchura de una banda cromatogrfica aumenta a medida que se mueve a travs de la columna, debido a que cuanto ms tiempo transcurre dentro de ella, mayor es la dispersin que puede tener lugar. Por ello, la anchura de la zona est relacionada directamente con el tiempo de residencia en la columna e inversamente con la velocidad a la que eluye la fase mvil. Desde el descubrimiento de la cromatografa se han propuesto diferentes teoras para explicar el modelo cromatogrfico. Una de las ms conocidas es la Teora de platos, propuesta por Martin y Synge en 1941 que, aunque antigua, permite describir de forma sencilla la separacin. Teora de platos La teora de platos consiste en considerar la columna cromatogrfica compuesta de un nmero de zonas adyacentes en cada una de las cuales hay suficiente espacio para que un analito est en equilibrio entre las dos fases. Cada una de estas zonas se denomina plato terico (de los que hay N en cada columna de longitud, L). Es importante recordar que, aunque los platos no existen realmente sino que son producto de la imaginacin, nos ayudan a comprender el proceso. Su significado proviene de la teora de platos descrita para explicar el fenmeno de la destilacin fraccionada o de la extraccin en contracorriente. La longitud de una columna contiene una HETP (altura equivalente de plato terico), H, expresada en unidades de longitud, normalmente m. El valor numrico de N y H, para cada columna en particular, es propio de cada analito. H est relacionada con la anchura del pico del analito y la distancia que recorre dentro de la columna, X, de tal manera que: *H =
2
/X
*, del ingls, High Equivalent to a Theoretical Plate
donde, , es la desviacin estndar del pico Gaussiano. Para los picos Gaussianos simtricos, la anchura en la base ( b) es igual a 4 y la anchura del pico en el punto de inflexin, 1/2, es igual a 2 . Por tanto, el valor de H puede ser calculado desde el cromatograma midiendo la anchura del pico. El nmero de platos tericos en la columna entera viene dado por: N = L/H = L X/
2
donde, L, es la longitud de la columna.
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
Si consideramos la posicin del pico a X=L con el hecho de que la anchura del pico en su base es b, obtenida de las tangentes dibujadas desde los dos puntos con ms pendiente del pico,
b=
la ecuacin anterior se convierte por tanto en:
2 b
N = 16 L2/
Si en lugar de medir L y tiempo, la ecuacin queda N = 16 (tR/
2 b)
en unidades de longitud, se hace en unidades de
Si dividimos la longitud de la columna, L, por el valor de HETP, H, se obtiene el nmero de platos en la columna N = L/H La eficiencia de una columna para separar solutos depende del nmero de platos tericos (N). A mayor valor de N, mejor es la separacin. Para una columna de longitud dada, la eficiencia de la separacin (es decir, el nmero de transferencias del analito entre la fase mvil y la fase estacionaria) ser tanto mejor cuanto menor sea la altura equivalente de plato terico (HETP o H). La teora de platos explica satisfactoriamente la forma de los picos cromatogrficos pero falla al intentar justificar el ensanchamiento de los mismos. En las expresiones consideradas hasta el momento, slo se ha tenido en cuenta la naturaleza del soluto y de las fases mvil y estacionaria para alcanzar los sucesivos equilibrios. Sin embargo, la fase mvil se desplaza a travs de la fase estacionaria con una cierta velocidad. Por tanto, el movimiento del soluto no puede ser completamente descrito en trminos de equilibrio pues se estara suponiendo que el equilibrio se alcanza de forma infinitamente rpida. Por tanto, es de suponer que la velocidad de la fase mvil debe tener incidencia en el avance de los solutos, su dispersin y, por tanto, en la eficiencia de la separacin. Teora cintica La teora cintica considera que el ensanchamiento de las bandas cromatogrficas (picos) es una consecuencia de que el desplazamiento del soluto a lo largo de la columna ocurre a velocidad finita. La forma de las bandas, por tanto, es afectada por la velocidad de elucin y depende de los siguientes factores: Trmino A. Difusin turbulenta o en remolino o Difusin de Eddy. Es debida a las mltiples trayectorias seguidas por la fase mvil. Al ser columnas empaquetadas con diferentes tamaos y formas de partculas, stas se asientan de manera irregular por lo
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
que la trayectoria seguida por la fase mvil puede ser mltiple. El trmino A es independiente de la velocidad de la fase mvil, A = dp donde, , es una constante que depende de las dimensiones, geometra y uniformidad del empaquetamiento de la columna y dp es el dimetro medio de las partculas de fase estacionaria. Trmino B/u. Difusin longitudinal del soluto a lo largo de la columna. Es debido a la tortuosidad de los canales en las columnas empaquetadas y el coeficiente de difusin molecular del soluto en la fase mvil. Se produce como consecuencia de que la concentracin de soluto es menor en los bordes de la banda que en el centro y, entonces, el soluto tiende a difundir hacia los bordes de la zona. Cuanto menor es la velocidad lineal media de la fase mvil, mayor es el ensanchamiento. Este trmino suele ser despreciable en cromatografa lquida, siendo B = 2 Dm donde, , es un factor de impedimento que depende de las caractersticas del relleno de la columna (0,7 para columnas de relleno) y Dm el coeficiente de difusin molecular del soluto en la fase mvil. Trmino Cu. Resistencia a la transferencia de masa. Es debido al lento equilibrio del soluto entre las fases mvil y estacionaria. Las columnas cromatogrficas siempre trabajan alejadas del equilibrio entre las dos fases. El trmino C se descompone en dos, Cs y Cm, segn se considere la transferencia de masa en la fase estacionaria y mvil, respectivamente. Cs = df2/Ds donde, df, es el espesor de la pelcula y Ds el coeficiente de difusin molecular del soluto en la fase estacionaria. Cm = dp2/Dm donde, dp, es el dimetro de la partcula y Dm el coeficiente de difusin molecular del soluto en la fase mvil. Esta influencia de la fase mvil en el ensanchamiento de banda y, por tanto, en la eficiencia queda reflejado en la primera ecuacin cintica, formulada por van Deemter quin la desarroll para columnas empaquetadas en cromatografa de gases (van Deemter et al., 1956). H = A + B/u + C u Ecuacin de van Deemter
donde u = L/tM, en (cms-1), siendo L, la longitud de la columna.
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
Posteriormente, Giddings (1965) elabor su propia ecuacin, basada en la anterior pero con discrepancia en cuanto a la descripcin de las propiedades de dispersin de la fase mvil, considerando que la difusin de Eddy y la resistencia a la transferencia de masa deban ser tratadas de forma dependiente. H = A/1 + (E/u) + B/u + C u Ecuacin de Giddings
Horvath y Lin (1976) y Knox (1977) tambin elaboraron sus propias teoras. Recientemente, Miyabe (2007) formula las nuevas ecuaciones del momento utilizando fases estacionarias de diferentes caractersticas estructurales. La Fig. 2 muestra la representacin grfica, determinada experimentalmente, de HETP (H) en funcin de la velocidad lineal media de fase mvil (u), para cromatografa de gases y de lquidos. En el inserto de la Fig. 2 se muestra la contribucin de los tres trminos explicados anteriormente, A, B y C que contribuyen al ensanchamiento de banda.
H
H HPLC GLC
Figura 2. Representacin grfica de la ecuacin de van Deemter. En el inserto, las diferencias existentes entre Cromatografa Gas-Lquido (GLC) y Cromatografa Lquida de Alta Resolucin (HPLC).
En las dos curvas, para cromatografa de gases (GLC) y de lquidos (HPLC), existe un valor mnimo de H para una velocidad de fase mvil determinada (condicin ptima de trabajo). En cromatografa de gases, las separaciones se hacen normalmente cerca del punto ptimo. Sin embargo, en cromatografa de lquidos, normalmente se trabaja a velocidades medias superiores al mnimo valor de H, con objeto de reducir el tiempo de anlisis. En la prctica, la representacin de van Deemter se determina experimentalmente utilizando valores de tiempos de retencin y anchuras de pico, con objeto de obtener valores de N y H a distintas velocidades de fase mvil.
10
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
Existen adems otros factores extra-columna que tambin contribuyen al ensanchamiento de la banda cromatogrfica, como son el sistema de inyeccin de muestra y los volmenes muertos de los diferentes tubos de conexin, que no son objeto de estudio en este momento. En resumen, a la hora de obtener alto valor de eficiencia en una separacin cromatogrfica determinada, habra que trabajar con pequeos dimetros de partcula (dp), con empaquetamientos uniformes ( ), con capas finas de fase estacionaria (df), de baja viscosidad, a temperaturas elevadas, minimizando los volmenes muertos de las conexiones y aplicando la muestra en una zona lo ms estrecha posible en la cabeza de la columna.
OBJETIVO DE LA PRCTICA Se calcular el flujo ptimo de la fase mvil, (en mLmin-1), con objeto de obtener la mxima eficiencia (mayor nmero de platos tericos o mnimo valor de HETP) en el anlisis del cido p-hidroxibenzoico utilizando una concentracin del mismo de 0,5 mgmL-1. Se realizarn las siguientes representaciones grficas: 1. Curva de van Deemter. HETP (H) frente a flujo de fase mvil (u), en (mLmin -1). 2. Presin en cabeza de columna (P), en (bar), frente a flujo de fase mvil (u), en (mLmin -1). 3. Tiempo de retencin (tR) del cido p-hidroxibenzoico, en (min) y (mm), frente a flujo de fase mvil (u), en (mLmin -1). 4. Tiempo de retencin (tR) del cido p-hidroxibenzoico, en (min) y (mm) frente a presin (P), en (bar). 5. Respuesta del detector (cuentas de rea) frente a anchura de pico en la base (b), en mm y frente a flujo de fase mvil (u), en (mLmin -1). 6. Tiempo de retencin (tR) del cido p-hidroxibenzoico, en (min) frente a anchura de pico en la base (b), en (mm). 7. Eficiencia del pico, medida como nmero de platos tericos (N), frente a respuesta del detector en (cuentas de rea) y frente a anchura de pico en la base (b), en (mm). Para realizar la representacin de van Deemter, es necesario calcular primero el valor del nmero de platos tericos (N) y el de HETP (H) en cada condicin de flujo de fase mvil y, para ello, triangular el pico. La triangulacin del pico se hace prolongando la lnea base y despus trazando las tangentes al punto de inflexin, segn el esquema
11
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
que se presenta en la Fig. 3. El tringulo formado tiene una base que es la porcin de la lnea base intersectada por las tangentes dibujadas en el pico y una altura desde esta base hasta el punto de corte con las tangentes. De esta manera se obtiene el valor de la anchura en la base ( b=4 ) y a media altura ( 1/2=2,35 ). Mediante esta representacin, tambin se calcula la altura del pico (h), desde el punto de corte de las tangentes hasta la anchura en la base. La altura a media anchura (h1/2) es justo la mitad del valor de h.
Tangentes al punto de inflexin
Puntos de inflexin
Figura 3. Esquema de triangulacin de un pico Gaussiano, indicando los valores de la anchura () a diferentes alturas.
La anchura en la base, ( b), est dividida en dos partes por la perpendicular trazada desde el punto de corte de las tangentes, la parte izquierda (a) y la derecha (b), de forma que ( b = 4 = a + b). En el caso de un pico Gaussiano simtrico (Fig. 1 A), a=b. Si el pico es asimtrico (Figs. 1 A y 1 B), a b. En el caso de pico con tailing (Fig. 1 B), a b y en el caso de pico con fronting (Fig. 1 C), a b. Segn la definicin de Dal Nogare y Chiu (1962), el factor de asimetra (As) se expresa como: (As) = (a+b)/2a Para un pico Gaussiano, As = 1, para un pico con tailing, As con fronting, As 1. 1 y para un pico
Una vez realizada la triangulacin del pico en cada condicin de flujo de fase mvil, se calcularn los siguientes parmetros cromatogrficos:
12
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
1. 2. 3. 4. 5. 6. 7. 8.
Tiempo de retencin (tR), en (mm) y en (min). Altura de pico (h'), en (mm). Altura de pico a media altura (h'1/2), en (mm). Ancho del pico en la base (b), en (mm). Ancho del pico a media altura (1/2),en (mm). Nmero de platos tericos (N). Altura equivalente de plato terico (H). Altura reducida de plato terico (h).
A continuacin se detallan las frmulas matemticas que nos permiten el clculo de dichos parmetros, as como diferentes unidades de expresin de la presin y la conversin entre ellas.
FRMULAS MATEMTICAS PARA EL CLCULO DE PARMETROS CROMATOGRFICOS
1. Tiempo de retencin, tR (min) o (mm). Es el tiempo transcurrido desde la inyeccin hasta la deteccin del mximo nmero de molculas de cada soluto. 2. Tiempo muerto, tM (min) o (mm). Es el tiempo requerido para que eluya un compuesto no retenido por la columna. Tambin se conoce como tiempo cero o tiempo de retencin del disolvente. 3. Tiempo de retencin corregido, tR (min) o (mm). Representa el tiempo que el soluto pasa absorbido dentro del empaquetamiento de la colu mna. tR = tR - tM 4. Factor de capacidad, k (adimensional). Representa el nmero de molculas que, en el equilibrio, pasan a la fase estacionaria respecto a las que permanecen en la fase mvil. Tambin se denomina relacin de capacidad o factor de retencin. k = (tR - tM / tM) = tR / tM 5. Selectividad, (adimensional). Determina la separacin entre picos y representa una relacin de la retencin relativa de dos compuestos que eluyen uno a continuacin del otro. Un valor de igual a 1 representa tiempos de retencin iguales y por lo tanto no existe separacin. Un nmero ms grande representa una columna ms selectiva. Cuanto ms alejado de 1, mayor separacin. 2:1= (tR - tM)2 /.(tR - tM)1 = tR2 / tR1 6. Resolucin, Rs (adimensional). Es una medida cuantitativa del grado de separacin de dos picos. Un valor de 1,5 representa una separacin hasta la lnea base de ambos picos y un valor de 1,0 representa una resolucin del 90%. En algunos casos esto es
13
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
suficiente para los clculos del rea de los picos (anlisis cuantitativo). Valores de Rs < 1 indican solapamiento; valores de Rs 1 indican separacin. Existen diferentes expresiones para calcular la resolucin; las ms utilizadas son las siguientes: Rs = (N / 4) ( / -1)(k2 /1+ k2) Rs = (2tR) / (b1 + b2) Rs = (N / 2) [ (k2-k1) / (k2+k1+2) ] Rs = (N / 2) [ (VR,2-VR,1) (VR,2+ VR,1) ] 7. Nmero de platos tericos, eficiencia, N (adimensional). Es la longitud de columna requerida para que se establezca un equilibrio del soluto entre la fase mvil y la estacionaria. Es una medida estimada de la agudeza del pico y es caracterstico de cada soluto en cada sistema cromatogrfico. N = 16 (tR / b)2 5,54 (tR / 1/2)2
8. Nmero de platos efectivos, eficiencia, Neff (adimensional). Considerando tR en lugar de tR. Neff = 16 (tR / b)2 5,54 (tR / 1/2)2 9. Altura equivalente de plato terico, H (mm). Es la distancia que separa dos platos consecutivos o, dicho de otra manera, el largo de columna requerido por un plato terico. H= L / N L = longitud de la columna (mm) 10. Altura efectiva de plato terico, Heff (mm). Considerando N eff en lugar de N. Heff = L / N eff 11. Altura reducida de plato terico, h (adimensional). Es la distancia que separa dos platos consecutivos en funcin del dimetro de partcula. h = H / dp dp = dimetro de partcula (mm) 12. Altura reducida efectiva de plato terico, heff (adimensional). Considerando H eff en lugar de H. h eff = H eff / dp
14
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
13. Seccin de la columna, s (mm2). s = r2 donde, r, es el radio de la columna. La presin en cabeza de columna no debe exceder el lmite impuesto por el fabricante. Dependiendo del tipo de fase estacionaria y del flujo de fase mvil empleado, la presin puede alcanzar diferentes valores. Es conveniente fijar en el equipo, antes de empezar a trabajar, los lmites de presin inferior y superior que no deben ser excedidos. Se detalla a continuacin la conversin entre unidades de presin ya que, dependiendo del equipo cromatogrfico pueden ser unas u otras.
UNIDADES DE PRESIN 1 MPa = 1106 Pa = 10 bar. 1 Pa = 1 Nm-2 = 110-5 bar. 1 bar = 1105 Pa = 0,9869 atm = 14,5038 lbpul-2 = 1,0197 kgcm-2 = 0,1 MPa. 1 psi = 1 lbpul-2 = 0,06895 bar = 0,06805 atm.
MATERIAL Y MTODOS Equipo cromatogrfico. Cromatgrafo de Lquidos de Alta Resolucin. Cromatgrafo lquido. Spectra Physics 8810 (Thermo Electron Corporation, Asheville, NC, USA) con un loop de inyeccin de 20 L. Bomba. SP 8810 LC (Thermo Electron Corporation, Asheville, NC, USA), elctrica alternante de pistn recproco. Fase estacionaria. Columna: Mediterranea sea C18 (Teknokroma, S.C.L. Spain). Tipo: Fase Reversa. Longitud (L): 120 mm. Dimetro de partcula (dp): 5m. Dimetro interno (di): 4,6 mm. Temperatura. 25oC Fase mvil. Reservorio A: Acetonitrilo (ACN). Reservorio B: 4% de cido actico en agua Milli-Q. Fase mvil: 30% de A y 70% de B, en condiciones isocrticas.
15
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
Flujo de fase mvil: de 0,2 mLmin -1 a 1,0 mLmin 1. Detector SP 8490 UV-Visible (Thermo Electron Corporation, Asheville, NC, USA). Longitud de onda de anlisis: 256 nm (segn el mximo de absorbancia obtenido en el espectro de absorbancia). Rango (UAFE): 0,005 unidades. Sistema de integracin. DataApex Clarity LiteTM software para Windows (DataApex Ltd., Praha, Czech Republic). Muestra empleada. cido p-hidroxibenzoico (M.M.=138,1).
COOH
OH
Figura 4. Frmula estructural del cido p-hidroxibenzoico.
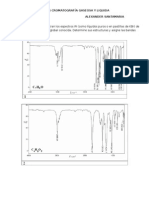
RESULTADOS Y DISCUSIN En primer lugar, se procede a realizar el espectro de absorbancia de la muestra que vamos a emplear, el cido p-hidroxibenzoico, disuelto en 4% cido actico en agua Milli-Q:ACN (80:20, v/v), con objeto de adecuar la longitud de onda de anlisis. En la Fig. 5 se muestra dicho espectro, donde se observa un pico de densidad ptica mxima a 256 nm.
Figura 5. Espectro de absorbancia del cido p-hidroxibenzoico a una concentracin de 5 gmL disuelto en 4% cido actico en agua Milli-Q:ACN (80:20, v/v). Sobre la curva, el nmero 1 representa el mximo principal de absorcin a 256 nm.
-1
16
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
Una vez seleccionado el mximo de absorbancia o, por lo menos, el entorno de longitudes de onda que muestran una cierta absorbancia, se procede a inyectar la muestra, cido p-hidroxibenzoico, a una concentracin fija de 0,05 mgmL-1,empleando diferentes flujos de fase mvil, entre 0,2 y 1,0 mLmin-1. En las siguientes Figs. (6, 8, 10, 12 y 14) se muestran los cromatogramas obtenidos en cada una de las condiciones. Despus de cada una de estas Figs., aparece la Tabla que muestra el porcentaje y las cuentas de rea de cada pico (Tablas 1, 2, 3, 4 y 5). Con objeto de poder realizar la triangulacin del pico mayoritario, cido p-hidroxibenzoico, se obtiene un cromatograma ampliado, copia del original pero con mayor aumento. Las Figuras 7, 9, 11, 13 y 15 muestran estas ampliaciones en las cuales, 1 min equivale a 33,5 mm., de tal manera que el alumno pueda triangular directamente los picos sobre las Figuras.
Unidades de Absorbancia
Tiempo (minutos)
Figura 6. Cromatograma de cido p-hidroxibenzoico a una concentracin 0,05 mgmL con un flujo de -1 fase mvil 0,2 mLmin .
-1
Pico Resultado (nmero) (%) 1 10,46 2 1,2 3 0,93 4 87,4
tR (min) 9,39 13,53 14,46 15,21
Cuentas de rea ( 106) 56,56 6,51 5,01 472,42
Tabla 1. Resultados del cromatograma de cido p-hidroxibenzoico a una concentracin 0,05 mgmL y -1 un flujo de fase mvil 0,2 mLmin .
-1
17
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
Figura 7. Ampliacin del cromatograma de cido p-hidroxibenzoico a una concentracin 0,05 mgmL -1 y un flujo de fase mvil 0,2 mLmin .
-1
Unidades de Absorbancia
Tiempo (minutos)
-1
Figura 8. Cromatograma de cido p-hidroxibenzoico a una concentracin 0,05 mgmL con un flujo de -1 fase mvil 0,4 mLmin .
Pico Resultado (nmero) (%) 1,01 1 1,15 2 85,16 3 2,91 4
tR (min) 8,49 8,83 10,49 13,73
Cuentas de rea ( 106) 2,88 3,27 241,61 8,28
-1
Tabla 2. Resultados del cromatograma de cido p-hidroxibenzoico a una concentracin 0,05 mgmL y -1 un flujo de fase mvil 0,4 mLmin .
18
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
Figura 9. Ampliacin del cromatograma de cido p-hidroxibenzoico a una concentracin 0,05 mgmL -1 y un flujo de fase mvil 0,4 mLmin .
-1
Unidades de Absorbancia
Tiempo (minutos)
Figura 10. Cromatograma de cido p-hidroxibenzoico a una concentracin 0,05 mgmL con un flujo -1 de fase mvil 0,6 mLmin .
-1
Pico Resultado (nmero) (%) 1 1,05 2 90,15 3 1,59 4 2,82
tR (min) 5,04 7,02 9,24 10,58
Cuentas de rea ( 106) 1,92 165,05 2,9 5,15
-1
Tabla 3. Resultados del cromatograma de cido p-hidroxibenzoico a una concentracin 0,05 mgmL y -1 un flujo de fase mvil 0,6 mLmin .
19
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
Figura 11. Ampliacin del cromatograma de cido p-hidroxibenzoico a una concentracin 0,05 mgmL -1 y un flujo de fase mvil 0,6 mLmin .
-1
Unidades de Absorbancia
Tiempo (minutos)
Figura 12. Cromatograma de cido p-hidroxibenzoico a una concentracin 0,05 mgmL con un flujo -1 de fase mvil 0,8 mLmin .
-1
Pico Resultado (nmero) (%) 1 1,19 2 1,06 3 95,49 4 0,73
tR (min) 3,83 4,52 5,43 8,28
Cuentas de rea ( 106) 1,64 1,47 131,78 1,01
Tabla 4. Resultados del cromatograma de cido p-hidroxibenzoico a una concentracin 0,05 mgmL y -1 un flujo de fase mvil 0,8 mLmin .
-1
20
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
Figura 13. Ampliacin del cromatograma de cido p-hidroxibenzoico a una concentracin 0,05 mgmL -1 y un flujo de fase mvil 0,8 mLmin .
-1
Unidades de Absorbancia
Tiempo (minutos)
Figura 14. Cromatograma de cido p-hidroxibenzoico a una concentracin 0,05 mgmL con un flujo -1 de fase mvil 1 mLmin .
-1
Pico Resultado (nmero) (%) 1 0,8 2 98,64 3 0,55 4 0,8
tR (min) 4,07 4,84 6,9 4,07
Cuentas de rea ( 106) 0,85 104,61 0,59 0,85
Tabla 5. Resultados del cromatograma de cido p-hidroxibenzoico a una concentracin 0,05 mgmL y -1 un flujo de fase mvil 1 mLmin .
-1
21
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
Figura 15. Ampliacin del cromatograma de cido p-hidroxibenzoico a una concentracin 0,05 mgmL -1 y un flujo de fase mvil 1 mLmin .
-1
Una vez triangulado el pico del cido p-hidroxibenzoico en los cromatogramas ampliados obtenidos con cada flujo de fase mvil, se procede al clculo matemtico de N y H. Los resultados obtenidos se muestran en la Tabla 6.
F (mLmin-1 ) 0,2 0,4 0,6 0,8 1 P (bar) 63 103 141 175 219 t R (min) 15,21 10,59 7,02 5,43 4,84 t R (mm) 524,68 351,38 235,2 179,29 162,67 h' (mm) 76,5 67 70,5 68,5 64,5 h'1/2 (mm) 38,25 33,5 35,25 34,25 32,25
b (mm) 1/2 (mm)
N (adim) 10.590 10.687 12.265 8.061 9.117
H (m) 23,6 23,4 20,4 31 27,4
h (adim) 4,72 4,68 4,07 6,2 5,48
Cuentas de area ( 106 ) 472,42 241,61 165,05 131,78 104,61
24 15 11 9,5 7
12 8 5 4,7 4
Tabla 6. Clculo matemtico de algunos de los parmetros cromatogrficos que influyen en la eficiencia del pico, obtenida mediante el sistema de triangulacin de picos, en los cromatogramas ampliados.
Nota importante. Los valores que se muestran en la Tabla 6, se han obtenido como resultado de la triangulacin de cada uno de los picos de cido p-hidroxibenzoico en las diferentes velocidades de fase mvil, una vez ampliado el cromatograma (Figs. 7, 9, 11, 13 y 15), para mayor comodidad en el tratamiento de las medidas. Cualquier alteracin de la imagen que pudiera modificar estas medidas, repercutira en los resultados. Se recomienda, por tanto, que la impresin en papel se haga conservando el tamao del cromatograma. Con los resultados obtenidos, se procede a realizar las diferentes representaciones grficas: 1. Curva de van Deemter. HETP (H) frente a flujo de fase mvil (u), en (mLmin -1).
22
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
33
H
h 28
23
18 0 0,2 0,4 0,6 0,8 1 1,2 Flujo de fase mvil (mLmin -1 )
Figura 16. Representacin grfica de la ecuacin de van Deemter.
Segn se observa en la Fig. 16, la mxima eficiencia (menor valor de H y mayor valor de N) para la separacin de cido p-hidroxibenzoico, en las condiciones experimentales descritas, se alcanza a valores de flujo de fase mvil de 0,6 mLmin -1. Ya se ha comentado que, por razones de ahorro de tiempo y disolvente, se suele trabajar a valores un poco ms altos. Los valores en color azul corresponden a los datos experimentales sin ajustar; la curva en color rojo representa el mejor ajuste de los datos experimentales obtenidos. Por razones obvias, siempre se expresarn los valores experimentales que se obtengan sin ningn tipo de modificaciones. Los valores experimentales, en la generalidad de los casos, siempre sufren una dispersin que hace que no se ajusten obligatoriamente a las grficas tericas. El valor de esta variacin experimental es tan necesario y valioso como la exacta interpretacin de los mismos. Adems, para una prctica de iniciacin a la cromatografa, como para cualquier otra tcnica, estas desviaciones experimentales tienen un valor sicolgico aadido: el alumno que por primera vez realiza la experimentacin no debe desmoralizarse si sus datos no proporcionan una curva perfecta. 2. Presin en cabeza de columna (P), en (bar), frente a flujo de fase mvil (u), en (mLmin -1).
23
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
250 200
Presin (bar)
150 100 50 0 0 0,2 0,4 0,6
y = 209,86x + 11,905 R2 = 0,99
0,8
1,2
Flujo de fase mvil (mLmin -1 )
Figura 17. Variacin de la presin en cabeza de columna respecto al flujo de fase mvil.
La presin en cabeza de columna es directamente proporcional al flujo de fase mvil, segn se muestra en la Fig. 17. En color azul se representan los resultados experimentales. En color rojo se representa la recta, obtenida por regresin lineal, de los datos experimentales. Como puede observarse, los resultados experimentales se ajustan a una recta con un alto valor de coeficiente de regresin, cuya ecuacin tambin se muestra en la Fig. 17. 3. Tiempo de retencin (tR) del cido p-hidroxibenzoico, en (min) y (mm), frente a flujo de fase mvil (u), en (mLmin -1).
16 12
t R (min)
8 4 0 0 0,2 0,4 0,6 0,8
-1
1,2
Flujo de fase mvil (mLmin )
Figura 18. Variacin del tiempo de retencin (en min) en funcin del flujo de fase mvil.
24
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
600 500
t R (mm)
400 300 200 100 0 0 0,2 0,4 0,6 0,8 1 1,2 Flujo de fase mvil (mLmin -1 )
Figura 19. Variacin del tiempo de retencin (en mm) en funcin del flujo de fase mvil.
El tiempo de retencin, tanto expresado en min (Fig. 18) como en mm (Fig. 19) no es directamente proporcional al flujo de fase mvil, puesto que la retencin de un soluto y sus distintos equilibrios entre la fase estacionaria y la fase mvil no slo dependen de la velocidad de flujo de sta ltima sino de muchos ms parmetros, segn se ha comentado previamente. 4. Tiempo de retencin (tR) del cido p-hidroxibenzoico, en (min) y (mm) frente a presin (P), en (bar).
16 12
t R (min)
8 4 0 0 50 100 150 200 250 Presin (bar)
Figura 20. Variacin del tiempo de retencin (en min) en funcin de la presin en cabeza de columna.
25
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
600 500 400
t R (mm)
300 200 100 0 0 50 100 150 200 250 Presin (bar)
Figura 21. Variacin del tiempo de retencin (en mm) en funcin de la presin en cabeza de columna.
Ya que la presin en cabeza de columna y el flujo de fase mvil son directamente proporcionales, segn se observ en la Fig.17, la expresin de tiempo de retencin, tanto en min (Fig. 20) como en mm (Fig.21), en funcin de la presin en cabeza de columna, tampoco es directamente proporcional. En la salida de un soluto de la columna intervienen muchos ms factores que la mera velocidad de arrastre ocasionada por la fuerza (presin) de la fase mvil. 5. Respuesta del detector (cuentas de rea) frente a anchura de pico en la base (b), en (mm) y frente a flujo de fase mvil (u), en (mLmin -1).
500 400 300 200 100 0 0 5 10 15 wb (mm) 20 25 30
Cuentas de rea (10 )
y = 22,207x - 72,254 R2 = 0,988
Figura 22. Variacin de las cuentas de rea en funcin de la anchura del pico.
26
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
500
Cuentas de rea (10 )
400 300 200 100 0 0 0,2
=-1154,1x - 1.154,1x + 703,23 yy= + 703,23
R2 = 1
y = -151,1x + 254,7 R2 = 0,99 0,4 0,6 0,8
-1
1,2
Flujo de la fase mvil (mLmin )
Figura 23. Variacin de las cuentas de rea en funcin del flujo de fase mvil.
Las cuentas de rea del pico, expresin directa de la respuesta del detector, nos pueden dar una idea de su anchura en la base ( b), aunque no siempre suceda as (pensemos en un pico muy alto y ancho en la base pero de alta eficiencia). Segn se muestra en la Fig. 22 en color azul, las cuentas de rea del pico son directamente proporcionales a su anchura en la base (b); los resultados se ajustan a una recta (representada en color rojo) cuyo coeficiente de regresin est prximo a la unidad. Si observamos ms detenidamente, las cuentas de rea no varan en exceso para valores de anchura en la base entre 7 y 11 mm pero si lo hacen en mayor proporcin para valores de anchura entre 11 y 24 mm. Existe un agrupamiento de tres puntos para los menores valores de anchura y una mayor distancia entre los dos puntos que tienen mayor anchura de pico en la base. Cuando se representan de forma grfica las cuentas de rea frente al flujo de fase mvil (Fig. 23 en color azul), se observa la misma conducta comentada anteriormente. Esto es, el ensanchamiento de un pico y por tanto el valor de sus cuentas de rea aumenta proporcionalmente a medida que disminuye el flujo de fase mvil para valores de ste entre 0,2 y 0,4 mLmin-1. El valor de la pendiente de la recta obtenida por regresin lineal, representado en la Fig. 23 en color rojo, es de 1.154,1. Para valores de flujo de fase mvil entre 0,6 y 1,0 mLmin -1, el valor de las cuentas de rea no vara en la misma proporcin que para valores de flujo menores. Los valores a los flujos ms altos se ajustan a otra recta cuyo valor de pendiente (151,1) es cien veces menor. De alguna manera se estara confirmando lo explicado anteriormente y observado en la Fig. 22. Existe un agrupamiento de valores de cuentas de rea a velocidades de flujo bajas y de anchura en la base altas por un lado y valores de cuentas de rea a velocidades de flujo altas y anchura en la base bajas, por otro. En cualquier caso, las cuentas de rea de un pico no son estrictamente proporcionales al flujo de fase mvil ya que en la retencin de un soluto no slo influye ste y el
27
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
ensanchamiento de banda no es estrictamente proporcional al tiempo de permanencia en la fase estacionaria. 6. Tiempo de retencin (tR) del cido p-hidroxibenzoico, en (min) frente a anchura de pico (b), en (mm). Abundando un poco ms en la explicacin anterior, cuando analizamos los resultados mostrados en la Fig. 24 se observa lo siguiente. Valores de tiempo de retencin altos proporcionan picos de gran anchura, mientras que picos de menor tiempo de retencin tienen valores menores de anchura en la base. Los tres valores de la izquierda (tiempos de retencin cortos) estn ms juntos entre s; los otros dos valores (tiempos de retencin mayores) que dan picos ms anchos en la base, estn ms alejados entre s. En color azul se representan los resultados experimentales sin ningn tipo de ajuste. En color rojo se representa la recta, obtenida mediante regresin lineal, de los datos experimentales. Tambin se puede ver en la Fig. 24 la ecuacin de la recta obtenida mediante este procedimiento.
16
12
t R (min)
y = 0,6418x + 0,0815 8 R2 = 0,9798
0 0 5 10 15 wb (mm) 20 25 30
Figura 24. Variacin del tiempo de retencin en funcin de la anchura del pico en la base.
7. Eficiencia del pico, medida como nmero de platos tericos (N), frente a respuesta del detector en (cuentas de rea) y frente a anchura de pico en la base (b), en (mm). La eficiencia, expresada como N, no es proporcional al valor de cuentas de rea del pico cromatogrfico (Fig. 25 en color azul). Los valores no se ajustan a una recta (representada en color rojo) pues, como se observa, el valor de R2 es muy bajo. Dicho de forma fcil, la eficiencia de un pico es una conjugacin de dos factores que deben caminar juntos, tiempo de retencin y anchura en la base; recordemos ahora la expresin de N:
28
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
N = 16 (tR / b)2 Segn se mostr en la Fig. 24, aunque proporcionales, no lo son de forma estricta el tiempo de retencin y la anchura.
N (nmero de platos tericos10 )
30 25 20 15 10 5 0 0 100 200 300
6
y = 0,0035x + 9,3603 R2 = 0,1049
400
500
Cuentas de rea (10 )
Figura 25. Variacin de la eficiencia, expresada como nmero de platos tericos (N) en funcin de las cuentas de rea del pico.
Tambin es cierto que la triangulacin de picos que hace el software no es idntica en todos los casos y depende mucho de su forma. Aunque las cuentas de rea sean una medida de la anchura en la base del pico y en el clculo de N se utilice la proporcin (tR / b), la eficiencia no es proporcional a las cuentas de rea porque en la eficiencia de un pico intervienen multitud de factores. Baste ahora recordar que la expresin grfica de la ecuacin de van Deemter (Fig. 16), da una curva sigmoidea. Esta idea tambin se justifica al observar los resultados mostrados en la Fig. 26. La eficiencia no es funcin lineal de la anchura de un pico en su base (b), aunque el cromatografista tienda siempre a optimizar las separaciones cromatogrficas sobre la base de obtencin de picos estrechos.
29
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
30
N (nmero de platos tericos10 )
25 20 y = 0,086x + 9,0004 15 10 5 0 0 5 10 15 wb (mm) 20 25 30 R2 = 0,1259
Figura 26. Variacin de la eficiencia, expresada como nmero de platos tericos (N) en funcin de la anchura del pico en la base.
El rango de variacin en el valor de N oscila entre 8.061 y 12.265, mientras que el valor de b oscila entre 7 y 24 mm. Es decir, cuando el valor de rea disminuye unas tres veces, el valor de eficiencia no se multiplica por tres.
BIBLIOGRAFA
Dal Nogare, S. y Chiu, J. 1962. A study of the performance of packed Gas Chromatography columns. Anaytical Chemistry, 34: 890-896. Giddings, J. C. 1965. Dynamics of Chromatography. Part. I: Principles and Theory. (Chromatographic Science Series, vol.1). Marcel Dekker, New York. Horvth. Cs., Lin, H. J. 1976. Movement and band spreading of unsorbed solutes in liquids chromatography. Journal of Chromatography, 126: 401-420. Knox, J. H. 1977. Practical aspects of LC theory. Journal of Chromatographic Science, 15: 352-364. Martin, A. J. P. y Synge, R. L. M. 1941. A new form of chromatogram employing two liquid phases. Biochemical Journal, 35: 13581360. Miyabe, K. 2007. New moment equations for chromatography using various stationary phases of different structural characteristics. Analytical Chemistry, 79: 74577472. 30
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
Tswett, M. 1906. Fiziko-khimicheskoe stroenie khlorofil. Berichte der Deutschen Botanischen Gesellschaft, 24: 384-393. van Deemter, J. J., Zuiderweg, F. J. y Klinkenberg, A. 1956. Longitudinal diffusion and resistance to mass transfer as causes of non ideality in chromatography. Chemical Engineering Science, 5: 271-289.
BIBLIOGRAFA DE CONSULTA
Dolan, J. W. y Snyder, L. R. 1989 Troubleshooting LC Systems: A Comprehensive Approach to Troubleshooting LC Equipment and Separations. Humana Press, Totowa, New Jersey. Dong, M.W. 2006. Modern HPLC for Practicing Scientists. John Wiley and Sons, New York. Garca de Marina, A. y del Castillo, B. 1988. Cromatografa Lquida de Alta Resolucin. Ed. Limusa, Mjico. Lloyd, R., Snyder, L. R., Glajch, J. L. y Kirkland, J. J. 1997. Practical HPLC Method Development, 2nd Ed. John Wiley and Sons, New York. Miller, J.M. 1988. Chromatography: Concepts and Contrasts. John Wiley and Sons, New York. Snyder, L. R. 1997. HPLC Method Development. John Wiley and Sons, New York. Snyder, L. R. y Dolan, J. W. 2007. High-Performance Gradient Elution: The Practical Application of the Linear-Solvent-Strength Model. John Wiley and Sons, Hoboken, New Jersey. Snyder, L. R., Kirkland, J. J. y Dolan, J. W. 2010. Introduction to Modern Liquid Chromatography, 3rd Ed., John Wiley and Sons, New York.
RECURSOS ELECTRNICOS
Shula Levin's WebSite of HPLC and LC-MS. Consultada: 3 septiembre 2011. Disponible en: http://www.forumsci.co.il/HPLC/program.html Study HPLC. Consultada: 3 septiembre 2011. Disponible en: http://www.studyhplc.com/index.php
31
Reduca (Biologa). Serie Tcnicas y Mtodos. 4 (3): 1-32, 2011.
ISSN: 1989-3620
LCGCs Chrom Academy. Consultada: 3 septiembre 2011. Disponible en: http://www.chromacademy.com/ Chemguide. Consultada: 3 septiembre 2011. Disponible en: http://www.chemguide.co.uk/ HPLC. Consultada: 3 septiembre 2011. Disponible en: http://www.separationsnow.com/coi/cda/list.cda?catId=2737&type=Link&sort= az&chId=4
Recibido: 14 junio 2010. Aceptado: 3 de agosto 2011.
32
Das könnte Ihnen auch gefallen
- Práctica 2A Sintesis y Caracterización de Un Complejo de CobaltoDokument6 SeitenPráctica 2A Sintesis y Caracterización de Un Complejo de CobaltoJuanpa MosqueraNoch keine Bewertungen
- Caso HARVARD 1Dokument3 SeitenCaso HARVARD 1Luis Estrada0% (2)
- Determinación Del Grado de Disociación, Del Coeficiente de Actividad Iónica Medio y de Las Constantes Del Equilibrio de Disociación (Ka y KC) de Un Ácido Débil Por Medidas de ConductividadDokument12 SeitenDeterminación Del Grado de Disociación, Del Coeficiente de Actividad Iónica Medio y de Las Constantes Del Equilibrio de Disociación (Ka y KC) de Un Ácido Débil Por Medidas de ConductividadCarolinaQuimbayaNoch keine Bewertungen
- Determinacion de AlcalinidadDokument4 SeitenDeterminacion de Alcalinidadjose jilNoch keine Bewertungen
- Guia IR Org III 2020 PDFDokument12 SeitenGuia IR Org III 2020 PDFValentina ReyNoch keine Bewertungen
- Cuestionario Karl FischerDokument4 SeitenCuestionario Karl FischerJesus VillanuevaNoch keine Bewertungen
- La Inclusión Como Posibilidad. Kaplan CarinaDokument77 SeitenLa Inclusión Como Posibilidad. Kaplan Carinamemmomiriam100% (4)
- Informe ChalconasDokument3 SeitenInforme ChalconasAndrés OrtizNoch keine Bewertungen
- Determinación de La Concentración de Calcio y Cobre Por Una Titulación FotométricaDokument13 SeitenDeterminación de La Concentración de Calcio y Cobre Por Una Titulación Fotométricavanessa lopezNoch keine Bewertungen
- Persulfato TerminadoDokument13 SeitenPersulfato TerminadoJonathan SuazoNoch keine Bewertungen
- ENTREGADO Práctica 2, Preparación de Benzoe Por Catálisis Con Vitamina B A Partir de BenzaldehídoDokument5 SeitenENTREGADO Práctica 2, Preparación de Benzoe Por Catálisis Con Vitamina B A Partir de BenzaldehídoLuis IslasNoch keine Bewertungen
- 9 Constantes de EstabilidadDokument14 Seiten9 Constantes de EstabilidadAleiozNoch keine Bewertungen
- Experimento 10 PDFDokument5 SeitenExperimento 10 PDFLuïz A. Pinto Jr.Noch keine Bewertungen
- AnaliticaDokument1 SeiteAnaliticaSayuriNoch keine Bewertungen
- TALLER No. 1 EJERCICIOS Soluciones, Titulaciones Directas y Por Retroceso PDFDokument4 SeitenTALLER No. 1 EJERCICIOS Soluciones, Titulaciones Directas y Por Retroceso PDFYulieth PedrazaNoch keine Bewertungen
- Ejercicio de IR y CromatografiaDokument13 SeitenEjercicio de IR y CromatografiaKelly CamargoNoch keine Bewertungen
- Calcio AphaDokument3 SeitenCalcio AphaRocio BedogniNoch keine Bewertungen
- Evaluacion Final AI I, 5 Preguntas Selección MultipleDokument2 SeitenEvaluacion Final AI I, 5 Preguntas Selección MultiplejhonjpgNoch keine Bewertungen
- Electrogravimetria y ColumbimetríaDokument5 SeitenElectrogravimetria y Columbimetría05-FB-HU-EDISON PEREZ PAUCARNoch keine Bewertungen
- Volumetría Redox II - Titulaciones Con Permanganato Mediante Potenciometría PDFDokument2 SeitenVolumetría Redox II - Titulaciones Con Permanganato Mediante Potenciometría PDFMardabNoch keine Bewertungen
- Recuperacion de Reactivos Del Proceso de Curtiembre de CueroDokument2 SeitenRecuperacion de Reactivos Del Proceso de Curtiembre de CueroVivian Vertiz100% (1)
- Métodos Analíticos para La Determinación de Bisfenol A en Los AlimentosDokument41 SeitenMétodos Analíticos para La Determinación de Bisfenol A en Los AlimentosJonathan R Coa Nin100% (3)
- Síntesis de Colorantes Organicos: Fenolftaleína, Anaranjado de MetiloDokument16 SeitenSíntesis de Colorantes Organicos: Fenolftaleína, Anaranjado de MetiloCarlos Ruben Suarez GavidiaNoch keine Bewertungen
- Ensayos PreliminaresDokument4 SeitenEnsayos PreliminaresDaniloRojas100% (1)
- HPLC - Practicas de Laboratorio y Cuestiones Teorico-Practicos Cuarta ParteDokument11 SeitenHPLC - Practicas de Laboratorio y Cuestiones Teorico-Practicos Cuarta ParteGiancarlo DlcNoch keine Bewertungen
- Informe Final de Sintesis Quimica OrganicaDokument4 SeitenInforme Final de Sintesis Quimica OrganicaMaría Paula RincónNoch keine Bewertungen
- Conductancia de Los ElectrolitosDokument11 SeitenConductancia de Los ElectrolitosCamisnzNoch keine Bewertungen
- Nomenclatura de AlcoholesDokument9 SeitenNomenclatura de AlcoholesCristian Edwin Machaca RamosNoch keine Bewertungen
- Fase Estacionarias Quirales .Dokument25 SeitenFase Estacionarias Quirales .JuanAmaya100% (1)
- Ejercicios de Compuestos FenolicosDokument5 SeitenEjercicios de Compuestos FenolicosAyazo Lopez DaladielNoch keine Bewertungen
- Guia de Ejercicios PotenciometriaDokument7 SeitenGuia de Ejercicios PotenciometriaNICOLAS ANDRES RUBILAR CASTILLONoch keine Bewertungen
- Ejercicios U I Analisis InstrumentalDokument4 SeitenEjercicios U I Analisis InstrumentalchorvoNoch keine Bewertungen
- Informe 3 CromatografiaDokument5 SeitenInforme 3 CromatografiaMARIA ISABEL ROMERO ESCOBAR100% (1)
- Practica N°5 Lab. AnaliticaDokument7 SeitenPractica N°5 Lab. Analiticalili4614Noch keine Bewertungen
- Manual LaboratorioDokument43 SeitenManual Laboratoriopaaaz19Noch keine Bewertungen
- Determinación Espectrofotométrica de HierroDokument6 SeitenDeterminación Espectrofotométrica de HierroValentina LunaNoch keine Bewertungen
- TP 1 y 2 Preparacion y Normalizacion de HCL y Mezclas AlcalinasDokument5 SeitenTP 1 y 2 Preparacion y Normalizacion de HCL y Mezclas AlcalinasLuis PeredoNoch keine Bewertungen
- Problemas de Fugacidad de MezclasDokument3 SeitenProblemas de Fugacidad de MezclasEzequiel García PalomoNoch keine Bewertungen
- Taller Disoluciones y DilucionesDokument1 SeiteTaller Disoluciones y DilucionesYenifer Alejandra Diaz Chala0% (1)
- Informe 10 - Quimica Analitica CuantitativaDokument16 SeitenInforme 10 - Quimica Analitica CuantitativaRAMOS OLLACHICA MARYORI JENNIFERNoch keine Bewertungen
- Sintesis de Cloruro de IsopropiloDokument8 SeitenSintesis de Cloruro de Isopropiloyaye_lopezNoch keine Bewertungen
- Determinación de La Constante de Equilibrio de Un IndicadorDokument5 SeitenDeterminación de La Constante de Equilibrio de Un IndicadorMaryjoseLeónNoch keine Bewertungen
- Determinacion de BicarbonatosDokument3 SeitenDeterminacion de BicarbonatosCgamez 123Noch keine Bewertungen
- Normalización de Área EJEMPLODokument3 SeitenNormalización de Área EJEMPLOAlejandra VillamizarNoch keine Bewertungen
- Titulaciones CoulombimetricasDokument6 SeitenTitulaciones CoulombimetricasNatalia ValenciaNoch keine Bewertungen
- Enunciado PEC1!17!18Dokument11 SeitenEnunciado PEC1!17!18gau3koNoch keine Bewertungen
- Titulacion Acido BaseDokument3 SeitenTitulacion Acido BaseAlexander MeraNoch keine Bewertungen
- Practica Nº7Dokument18 SeitenPractica Nº7Angela Chumioque GarciaNoch keine Bewertungen
- Informe Analisis InstrumentalDokument18 SeitenInforme Analisis InstrumentalCatalina Andrea Constanzo SánchezNoch keine Bewertungen
- Acetil Acetonatos 1Dokument10 SeitenAcetil Acetonatos 1Luis FelipeNoch keine Bewertungen
- Reporte Fisico QuimicaDokument8 SeitenReporte Fisico QuimicaFelipe VilchesNoch keine Bewertungen
- Ferroceno ListoDokument13 SeitenFerroceno ListoJonathan SuazoNoch keine Bewertungen
- BENZOATODokument16 SeitenBENZOATOLuis BlNoch keine Bewertungen
- Informe Cromatografía de GasesDokument3 SeitenInforme Cromatografía de GasesPAOLA ANDREA SUAZA CARDONANoch keine Bewertungen
- Titulacion PotenciometricaDokument19 SeitenTitulacion PotenciometricaDiana Gabriela NinaNoch keine Bewertungen
- Análisis de Nitratos, Método de La BrucinaDokument5 SeitenAnálisis de Nitratos, Método de La BrucinaAida Jimenez100% (1)
- 6-2 Metodos Electroanaliticos v10Dokument75 Seiten6-2 Metodos Electroanaliticos v10Juan Paco PedroNoch keine Bewertungen
- La nanotecnología: El mundo de las máquinas a escala nanométricaVon EverandLa nanotecnología: El mundo de las máquinas a escala nanométricaNoch keine Bewertungen
- Cálculo de La Eficiencia y Representación GráficaDokument32 SeitenCálculo de La Eficiencia y Representación GráficaVictor Martinez MartinezNoch keine Bewertungen
- Curso de Cromatografia de Liquidos de AlDokument32 SeitenCurso de Cromatografia de Liquidos de AlMary SaenzNoch keine Bewertungen
- Analisis InstrumentalDokument7 SeitenAnalisis InstrumentalAliris Hernandez carreazoNoch keine Bewertungen
- Laboratorio Quimica 6Dokument10 SeitenLaboratorio Quimica 6Claudio GuerraNoch keine Bewertungen
- Manual Seguridad QuimicaDokument52 SeitenManual Seguridad QuimicaKristhian Castillo VillotaNoch keine Bewertungen
- Cromatografia de Gases Instrumentacion PDFDokument49 SeitenCromatografia de Gases Instrumentacion PDFalextm89Noch keine Bewertungen
- Ley 55 de 1993Dokument29 SeitenLey 55 de 1993Diego Fernando GalloNoch keine Bewertungen
- BDO Reporte Sectorial 2Dokument53 SeitenBDO Reporte Sectorial 2Silene SalazarNoch keine Bewertungen
- Técnicas Analíticas en Un Laboratorio FarmacéuticoDokument93 SeitenTécnicas Analíticas en Un Laboratorio Farmacéuticoalextm89100% (1)
- Validacion Por HPLCDokument66 SeitenValidacion Por HPLCalextm89Noch keine Bewertungen
- Cromatografia de Gases Instrumentacion PDFDokument49 SeitenCromatografia de Gases Instrumentacion PDFalextm89Noch keine Bewertungen
- Extraccion Por Solvente PDFDokument31 SeitenExtraccion Por Solvente PDFRoss MyNoch keine Bewertungen
- Brochure Academic ManagerDokument10 SeitenBrochure Academic ManagerCrhistian DiazNoch keine Bewertungen
- Algunas Reflexiones Sobre La Didáctica de La Lengua Oral: Mercé PujolDokument8 SeitenAlgunas Reflexiones Sobre La Didáctica de La Lengua Oral: Mercé PujolSebastian VillaNoch keine Bewertungen
- Copia de Maria Elisa PDFDokument11 SeitenCopia de Maria Elisa PDFmaria pinedaNoch keine Bewertungen
- La Cultura de La Autoformación PDFDokument14 SeitenLa Cultura de La Autoformación PDFEdward GamerNoch keine Bewertungen
- COAR Perfiles de DocentesDokument13 SeitenCOAR Perfiles de Docenteswilliamgem6925100% (1)
- Juan Carlos Del Bello UNRN PDFDokument43 SeitenJuan Carlos Del Bello UNRN PDFRomina DécimaNoch keine Bewertungen
- Matriz Efi-EfeDokument5 SeitenMatriz Efi-EfeJose CaceresNoch keine Bewertungen
- Prezi Caro 3Dokument1 SeitePrezi Caro 3chonnyNoch keine Bewertungen
- Tarea 7 Salvatore DeliaDokument6 SeitenTarea 7 Salvatore DeliaJoseNoch keine Bewertungen
- Acceso A Internet en Estudiantes de U.S.F.X.ChDokument8 SeitenAcceso A Internet en Estudiantes de U.S.F.X.ChErmelinda FuentesNoch keine Bewertungen
- Actividad de Contexto - La Importancia de La Gestion de La Informacion en La EmpresaDokument4 SeitenActividad de Contexto - La Importancia de La Gestion de La Informacion en La EmpresaJenniffer Espinosa MolinaNoch keine Bewertungen
- PDFDokument348 SeitenPDFLeidy RubioNoch keine Bewertungen
- Titulaciones Acceso Opos Docente AndaluciaDokument5 SeitenTitulaciones Acceso Opos Docente AndaluciaFrancisco SaladoNoch keine Bewertungen
- BenderskyDokument2 SeitenBenderskyvaninabredaelNoch keine Bewertungen
- Carta Estudiantes Facultad de Ciencias SocialesDokument1 SeiteCarta Estudiantes Facultad de Ciencias Socialessantiago robledo yepesNoch keine Bewertungen
- Sanciones Impuestas Por Prestar El Servicio Educativo Superior Universitario Sin Contar Con La Licencia de SUNEDUDokument3 SeitenSanciones Impuestas Por Prestar El Servicio Educativo Superior Universitario Sin Contar Con La Licencia de SUNEDUAgencia Andina50% (2)
- Tomo V UmbvDokument61 SeitenTomo V UmbvAlexander González Fernández100% (1)
- El Paper Como Herramienta Académica para El Empoderamiento PedagógicoDokument2 SeitenEl Paper Como Herramienta Académica para El Empoderamiento PedagógicoDavid Auris VillegasNoch keine Bewertungen
- Actividad La Lengua Como Instrumento de Comunicación Derecho (Velasquez)Dokument2 SeitenActividad La Lengua Como Instrumento de Comunicación Derecho (Velasquez)Mayela VelasquezNoch keine Bewertungen
- Anexo 8 A-B PDFDokument4 SeitenAnexo 8 A-B PDFRuth Vasquez NoblecillaNoch keine Bewertungen
- PDF 20230722 195441 0000Dokument12 SeitenPDF 20230722 195441 0000luis galanNoch keine Bewertungen
- Documentos de AdmisiónDokument2 SeitenDocumentos de AdmisiónKuuzzed LeoNoch keine Bewertungen
- Asignatura Sociologia Militar UNEDDokument5 SeitenAsignatura Sociologia Militar UNEDRosaEsterValenciaNoch keine Bewertungen
- PagosBancoDeLaNacionDokument6 SeitenPagosBancoDeLaNacionFarhansyahNoch keine Bewertungen
- Convocatoria y Bases Del Congreso Virtual. Cri - Uptamca 2020Dokument5 SeitenConvocatoria y Bases Del Congreso Virtual. Cri - Uptamca 2020ctrujillorendonNoch keine Bewertungen
- Guia 6801 2021Dokument15 SeitenGuia 6801 2021Antonio Garcia GomezNoch keine Bewertungen
- Https:servicios-Fscu - Ucsc.cl:application:docs:formulario Solicitud de Postergacion CuotaDokument1 SeiteHttps:servicios-Fscu - Ucsc.cl:application:docs:formulario Solicitud de Postergacion CuotaCarlos Ignacio CidNoch keine Bewertungen
- Master Cirugía VeterinariaDokument11 SeitenMaster Cirugía VeterinariaDavid LozanoNoch keine Bewertungen