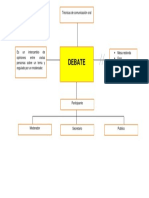
Beruflich Dokumente
Kultur Dokumente
Enzimas Bioquimica (Javier Campoverde)
Hochgeladen von
Javier Jimenez0 Bewertungen0% fanden dieses Dokument nützlich (0 Abstimmungen)
291 Ansichten74 SeitenOriginaltitel
enzimas bioquimica (Javier Campoverde)
Copyright
© © All Rights Reserved
Verfügbare Formate
DOCX, PDF, TXT oder online auf Scribd lesen
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
© All Rights Reserved
Verfügbare Formate
Als DOCX, PDF, TXT herunterladen oder online auf Scribd lesen
0 Bewertungen0% fanden dieses Dokument nützlich (0 Abstimmungen)
291 Ansichten74 SeitenEnzimas Bioquimica (Javier Campoverde)
Hochgeladen von
Javier JimenezCopyright:
© All Rights Reserved
Verfügbare Formate
Als DOCX, PDF, TXT herunterladen oder online auf Scribd lesen
Sie sind auf Seite 1von 74
BIOQUMICA
UNIVERSIDAD TECNICA DE MACHALA
FACULTAD DE CIENCIAS QUIMICAS Y DE LA SALUD
BIOQUMICA
ENZIMAS
1
BIOQUMICA
ENZIMAS
INTRODUCCION:
LA ENZIMA COMO UNIDAD FUNDAMENTAL DE VIDA
Cada clula y cada tejido tienen su actividad propia, lo que comporta continuos
cambios en su estado bioqumico, en la base de la cual estn las enzimas, que
tienen el poder de catalizar, facilitar, y agilizar determinados procesos sintticos y
analticos. Los propios genes son reguladores de la produccin de las enzimas;
por tanto, genes y enzimas pueden ser considerados como las unidades
fundamentales de la vida.
Este concepto poco difundido casi hasta el siglo XX, se ha desarrollado y
concretado cada vez ms, y constituye un componente esencial de diversas
disciplinas: la microbiologa, la fisiologa, la bioqumica, la inmunologa y
la taxonoma, formando adems parte del campo aplicado, en gran variedad
de industrias. El rasgo particular de las enzimas es que pueden catalizar procesos
qumicos a baja temperatura, compatible con la propia vida, sin el empleo de
sustancias lesivas para los tejidos. La vida es, en sntesis, una cadena de
procesos enzimticos, desde aquellos que tienen por sustratos los materiales ms
simples, como el agua (H2O) y el anhdrido carbnico (CO2), presentes en los
vegetales para la formacin de hidratos de carbono, hasta los ms complicados
que utilizan sustratos muy complejos.
La formacin de los prtidos, los glcidos y los lpidos es un ejemplo tpico: Son a
la vez degradados y reconstruidos por otras reacciones enzimticas, produciendo
energa a una velocidad adecuada para el organismo, sin el gasto energtico que
exigen los mtodos qumicos de laboratorio.
LAS ENZIMAS
Los enzimas son protenas que catalizan
reacciones qumicas en los seres vivos. Los
enzimas son catalizadores, es decir, sustancias
que, sin consumirse en una reaccin,
aumentan notablemente su velocidad. No
hacen factibles las reacciones imposibles, sino
que solamente aceleran las que
espontneamente podran producirse. Ello
hace posible que en condiciones fisiolgicas
tengan lugar reacciones que sin catalizador
requeriran condiciones extremas de presin,
temperatura o pH.
2
BIOQUMICA
ENZIMAS
IMPORTANCIA BIOMDICA DE LAS ENZIMAS
Sin enzimas, no sera posible la vida que conocemos. Igual que la biocatlisis que
regula la velocidad a la cual tienen lugar los procesos fisiolgicos, las enzimas
llevan a cabo funciones definitivas relacionadas con salud y la enfermedad. En
tanto que, en la salud todos los procesos fisiolgicos ocurren de una manera
ordenada y se conserva la homeostasis, durante los estados patolgicos, esta
ltima puede ser perturbada de manera profunda. Por ejemplo, el dao tisular
grave que caracteriza a la cirrosis heptica puede deteriorar de manera notable
la propiedad de las clulas para producir enzimas que catalizan procesos
metablicos claves como la sntesis de urea. La incapacidad celular para convertir
el amoniaco txico a urea no txica es seguida por intoxicacin con amoniaco y
por ultimo coma heptico. Un conjunto de enfermedades genticas raras, pero con
frecuencia debilitantes y a menudo mortales, proporciona otros ejemplos
dramticos de las drsticas consecuencias fisiolgicas que pueden seguir al
deterioro de la actividad enzimtica, inclusive de una sola enzima.
Despus del dao tisular grave (por ejemplo, infarto del miocardio o pulmonar,
trituracin de un miembro) o siguiendo a multiplicacin celular descontrolada (por
ejemplo, carcionoma prosttico), las enzimas propias de tejidos especficos pasan
a la sangre. Por lo tanto, la determinacin de estas enzimas intracelulares en el
suero sanguneo proporciona a los mdicos informacin valiosa para el
diagnstico y el pronstico.
CARACTERSTICAS DE LAS ENZIMAS
Desde el punto de vista qumico, las enzimas estn formadas de carbono
(C), Hidrgeno (H), oxigeno (O), Nitrgeno (Ni), y Azufre (S) combinados, pero
siempre con peso molecular bastante elevado y comn propiedades catlicas
especficas. Su importancia es tal que puede considerarse la vida como un "orden
sistemtico de enzimas funcionales". Cuando este orden y su sistema funcional
son alterados de algn modo, cada organismo sufre ms o menos gravemente y el
trastorno puede ser motivado tanto por la falta de accin como por un exceso de
actividad de enzima.
Las enzimas son catalizadores de naturaleza protenica que regulan la velocidad a
la cual se realizan los procesos fisiolgicos, producidos por los organismos vivos.
En consecuencia, las deficiencias en la funcin enzimtica causan patologas.
Las enzimas, en los sistemas biolgicos constituyen las bases de las complejas y
variadas reacciones que caracterizan los fenmenos vitales. La fijacin de la
energa solar y la sntesis de sustancias alimenticias llevadas a cabo por los
vegetales dependen de las enzimas presentes en las plantas. Los animales, a su
vez, estn dotados de las enzimas que les permiten aprovechar los alimentos con
3
BIOQUMICA
ENZIMAS
fines energticos o estructurales; las funciones del metabolismo interno y de la
vida de relacin, como la locomocin, la excitabilidad, la irritabilidad, la divisin
celular, la reproduccin, etc. Estn regidas por la actividad de innumerables
enzimas responsables de que las reacciones se lleven a cabo en condiciones
favorables para el individuo, sin liberaciones bruscas de energa a temperaturas
fijas en un medio de pH, concentracin salina, etc.; prcticamente constante.
A diferencia de un catalizador inorgnico que interviene en numerosas reacciones
las enzimas producidas por los organismos vivos habitualmente solo catalizan un
tipo de reaccin o solo una reaccin determinada; la especificidad de las enzimas
es tan marcadas que en general actan exclusivamente sobre sustancias que
tienen una configuracin precisa; por ejemplo, si solo atacan a los aminocidos
que tienen su carbono a , asimtrico, con estructura L-, no muestran la menor
actividad sobre formas idnticas de dichos aminocidos, pero que sean del tipo D-.
En los sistemas biolgicos se llevan a cabo diversas reacciones a partir de la
misma sustancia; por ejemplo algunos microorganismos convierten la glucosa en
alcohol y bixido de carbono, al paso que otros grmenes la convierten en cido
lctico o cido pirvico o acetaldehdo. Esto quiere decir que la glucosa puede
descomponerse en distintos productos y aunque todas las posibilidades son
tericas y prcticamente posibles la presencia de ciertas enzimas favorece uno de
los caminos que llevan a la acumulacin de determinados compuestos.
Las enzimas, por lo tanto, se consideran como catalizadores altamente especficos
que:
Modifican la velocidad de los cambios promovidos por ellas.
Determinan que sustancias particulares, de preferencia a otras distintas son las
que van a sufrir los cambios.
Impulsan dentro de los distintos cambios posibles que pueda seguir una sustancia,
cul de ellos en especial, ser el utilizado.
Las enzimas representan las sustancias encargadas de graduar la velocidad de
una reaccin determinada en el interior de las clulas; como en las diversas
clulas se realizan infinidad de reacciones, ya que en una de ellas se encuentran
varios miles de sustancias, se deduce, tambin, la presencia de varios miles de
enzimas. Es posible, por lo tanto, que la mayor parte de esta estructura protenica
celular est formada por enzimas, encargadas de las diversas funciones de
sntesis, degradacin, oxidacin, etc. caractersticas de la actividad vital de los
distintos organismos.
PROPIEDADES DE LAS ENZIMAS
Las enzimas son catalizadores proteicos que incrementan la rapidez de una
reaccin y que no se consumen durante una reaccin que catalizan.
4
BIOQUMICA
ENZIMAS
A. Sitios activos.
Las molculas
enzimticas
contienen un saco
o surco especial
denominado sitio
activo. El sitio
activo contiene
cadenas laterales
de aminocidos
que crean una
superficie natural
complementaria con el sustrato. El sitio activo fija al sustrato y forma un
complejo de enzima y sustrato(ES), este ES se convierte en complejo de
enzima y producto (EP), que se disocia ulteriormente en estos dos
componentes.
B. Eficiencia cataltica.
La mayor parte de las reacciones que se catalizan por enzimas son
altamente eficiente, y proceden con una rapidez de 10
3
a 10
8
veces mayor
que las reacciones no catalizadas. De manera caracterstica cada molcula
enzimtica es capaz de transformar de 100 a 1000 molculas de sustrato
en producto cada segundo. El nmero de molculas de sustrato que se han
convertido en producto por molcula enzimtica por segundo se denomina
nmero de recambio.
C. Especificidad
Las enzimas son altamente especficas, y entran en interaccin con uno o
ms sustratos y catalizan solo un tipo de reaccin qumica
D. Cofactores.
Algunas enzimas se relacionan con un cofactor no protenico que se
necesita para la actividad enzimtica. Entre los factores que se encuentran
de manera ms frecuente estn iones metlicos como Zn
2+
y Fe
++
, y
molculas orgnicas conocidas como coenzimas, que son a menudo
sustancias derivadas de vitaminas. Por ejemplo la coenzima NAD
+
contiene
niacina, la llamada FAD contiene riboflavina, y la coenzima A contiene cido
pantotico.
Se llama holoenzima a la enzima con su cofactor. El termino apoenzima se
refiere a la porcin protenica de la holoenzima.
5
BIOQUMICA
ENZIMAS
En ausencia del cofactor apropiado, la apoenzima no manifiesta ninguna
actividad biolgica de manera caracterstica. El grupo prosttico es una
coenzima firmemente unidad a la enzima, que no se disocia de ella
(ejemplo, la biotina que se encuentra en las carboxilasas.)
E. Regulacin.
La actividad enzimtica puede ser regulada; esto es, las enzimas se activan
o se inhiben, de modo que la tasa de formacin del producto en particular
satisface las necesidades de la clula.
F. Localizacin dentro de la clula.
Muchas enzimas estn localizadas en organelos especficos dentro de la
clula. Esta distribucin en compartimientos sirve para aislar el sustrato o al
producto de la reaccin de otras reacciones competitivas. Esto ofrece un
ambiente favorable para la reaccin y organiza a las miles de enzimas que
se encuentran dentro de la clula para que efecten sus funciones
inherentes. (PAMELA C. CHAMPE, PhD BIOQUIMICA 3
era
edicin pg.62-
63).
Las propiedades de las enzimas derivan del hecho de ser protenas y de actuar
como catalizadores. Como protenas, poseen una conformacin natural ms
estable que las dems conformaciones posibles. As, cambios en la
conformacin suelen ir asociados en cambios en la actividad cataltica. Los
factores que influyen de manera ms directa sobre la actividad de un enzima son:
pH
temperatura
cofactores
1. EFECTO DEL pH SOBRE LA ACTIVIDAD ENZIMTICA
Los enzimas poseen grupos qumicos ionizables
(carboxilos -COOH; amino -NH
2
; tiol -SH; imidazol,
etc.) en las cadenas laterales de sus aminocidos.
Segn el pH del medio, estos grupos pueden tener
carga elctrica positiva, negativa o neutra. Como la
conformacin de las protenas depende, en parte, de
sus cargas elctricas, habr un pH en el cual la
conformacin ser la ms adecuada para la actividad
cataltica. Este es el llamado pH ptimo.
6
BIOQUMICA
ENZIMAS
La mayora de los enzimas son muy
sensibles a los cambios de pH.
Desviaciones de pocas dcimas por
encima o por debajo del pH ptimo
pueden afectar drsticamente su
actividad. As, la pepsina gstrica tiene
un pH ptimo de 2, la ureasa lo tiene a
pH 7 y la arginasa lo tiene a pH 10
(Figura de la izquierda). Como ligeros
cambios del pH pueden provocar la
desnaturalizacin de la protena, los
seres vivos han desarrollado sistemas
ms o menos complejos para
mantener estable el pH intracelular: Los amortiguadores fisiolgicos.
2. EFECTO DE LA TEMPERATURA SOBRE LA ACTIVIDAD ENZIMTICA
En general, los aumentos de temperatura aceleran las reacciones qumicas: por
cada 10C de incremento, la velocidad de reaccin se duplica. Las reacciones
catalizadas por enzimas siguen esta ley
general. Sin embargo, al ser protenas, a
partir de cierta temperatura, se empiezan a
desnaturalizar por el calor. La temperatura a
la cual la actividad cataltica es mxima se
llama temperatura ptima (Figura de la
derecha). Por encima de esta temperatura, el
aumento de velocidad de la reaccin debido a
la temperatura es contrarrestado por la
prdida de actividad cataltica debida a la
desnaturalizacin trmica, y la actividad
enzimtica decrece rpidamente hasta anularse.
3. EFECTO DE LOS COFACTORES SOBRE LA ACTIVIDAD ENZIMTICA
A veces, un enzima requiere para su funcin la presencia de sustancias no
proteicas que colaboran en la catlisis: los cofactores. Los cofactores pueden ser
iones inorgnicos como el Fe
++
, Mg
++
, Mn
++
, Zn
++
etc. Casi un tercio de los
enzimas conocidos requieren cofactores. Cuando el cofactor es una molcula
7
BIOQUMICA
ENZIMAS
orgnica se llama coenzima. Muchos de estas coenzimas se sintetizan a partir de
vitaminas. En la figura inferior podemos observar una molcula
de hemoglobina (protena que transporta oxgeno) y su coenzima (el grupo hemo).
Cuando los cofactores y las coenzimas se encuentran unidos covalentemente al
enzima se llaman grupos prostticos. La forma catalticamente activa del enzima,
es decir, la enzima unida a su grupo prosttico, se llama holoenzima. La parte
proteica de un holoenzima (inactiva) se llama apoenzima, de forma que:
ASPECTOS GENERALES SOBRE LAS ENZIMAS
Prcticamente todas las reacciones qumicas que tienen lugar en los seres vivos
estn catalizadas por enzimas. Los enzimas son catalizadores especficos: cada
enzima cataliza un solo tipo de reaccin, y casi siempre acta sobre un nico
sustrato o sobre un grupo muy reducido de ellos. En una reaccin catalizada por
un enzima:
1. La sustancia sobre la que acta el enzima se llama sustrato.
2. El sustrato se une a una regin concreta de la enzima, llamada centro
activo. El centro activo comprende (1) un sitio de unin formado por los
aminocidos que estn en contacto directo con el sustrato y (2) un sitio
apoenzima + grupo prosttico= holoenzima
8
BIOQUMICA
ENZIMAS
cataltico, formado por los aminocidos directamente implicados en el
mecanismo de la reaccin
3. Una vez formados los productos el enzima puede comenzar un nuevo ciclo
de reaccin
Las enzimas, a diferencia de los catalizadores inorgnicos catalizan reacciones
especficas. Sin embargo hay distintos grados de especificidad. El enzima
sacarosa es muy especfico: rompe el enlace -glucosdico de la sacarosa o de
compuestos muy similares. As, para el enzima sacarosa, la sacarosa es
su sustrato natural, mientras que la maltosa y la isomaltosa son sustratos
anlogos. El enzima acta con mxima eficacia sobre el sustrato natural y con
menor eficacia sobre los sustratos anlogos. Entre los enzimas poco
especficos estn las proteasas digestivas como la quimotripsina, que rompe los
enlaces amida de protenas y pptidos de muy diverso tipo.
MODO DE ACCIN DE LAS ENZIMAS
En las reacciones espontneas, los productos finales tienen menos energa libre
comienzo de la reaccin requiere un aporte inicial de energa. Esta energa inicial
que hay que suministrar a los reactantes para que la reaccin transcurra se
llama energa de activacin (E
a
). Cuanto menor es la E
a
ms fcilmente transcurre
la reaccin.
1.- El enzima y su
sustrato
2.- Unin al centro
activo
3.- Formacin de
productos
9
BIOQUMICA
ENZIMAS
La accin de los catalizadores consiste, precisamente, en disminuir la
E
a
(Figura superior derecha). Los enzimas son catalizadores especialmente
eficaces, ya que disminuyen la E
a
an ms que los catalizadores inorgnicos. Por
ejemplo, la descomposicin del agua oxigenada (H
2
O
2
) para dar H
2
O y O
2
puede
ocurrir sin catalizador, con un catalizador inorgnico (platino), o con un enzima
especfico (catalasa). Las respectivas E
a
para cada proceso son 18, 12 y 6
Kcal/mol. As, se puede calcular que el platino acelera la reaccin 20.000 veces,
mientras que la catalasa la acelera 370.000 veces.
Para que una reaccin qumica tenga lugar, las molculas de los reactantes deben
chocar con una energa y una orientacin adecuadas. La actuacin del enzima (1)
permite que los reactantes (sustratos) se unan a su centro activo con una
orientacin ptima para que la reaccin se produzca y (2) modifica las
propiedades qumicas del sustrato unido a su centro activo, debilitando los enlaces
existentes y facilitando la formacin de otros nuevos (Figuras inferiores):
Hay dos modelos sobre la forma en que el sustrato se une al centro activo del
enzima:
Perfil energtico de una reaccin
espontnea
Perfil energtico de una reaccin
catalizada
10
BIOQUMICA
ENZIMAS
el modelo llave-cerradura
el modelo del ajuste inducido
MODELO LLAVE-CERRADURA
El modelo llave-cerradura supone que la estructura del sustrato y la del centro
activo son complementarias, de la misma forma que una llave encaja en una
cerradura. Este modelo es vlido en muchos casos, pero no es siempre correcto.
MODELO DEL AJUSTE INDUCIDO
En algunos casos, el centro activo adopta la
conformacin idnea slo en presencia del sustrato. La
unin del sustrato al centro activo del enzima
desencadena un cambio conformacional que da lugar a
la formacin del producto. Este es el modelo del ajuste
inducido (Figura de la derecha.). Sera algo as como un
cascanueces, que se adapta al contorno de la nuez.
REGULACIN DE LA ACTIVIDAD ENZIMTICA
Una molcula de enzima no tiene por qu actuar siempre a la misma velocidad. Su
actividad puede estar modulada por:
11
BIOQUMICA
ENZIMAS
cambios en el pH
cambios en la temperatura
presencia de cofactores
las concentraciones del sustrato y de los productos finales
presencia de inhibidores
modulacin alosterico
modificacin covalente
activacin por protelisis
isoenzimas
EFECTO DE LAS CONCENTRACIONES SOBRE LA ACTIVIDAD ENZIMTICA
La velocidad de una reaccin enzimtica depende de la
concentracin de sustrato. La Figura de la derecha
muestra la velocidad de una reaccin enzimtica a 6
concentraciones distintas de sustrato.
Adems, la presencia de los productos finales puede
hacer que la reaccin sea ms lenta, o incluso invertir su
sentido (Figura inferior).
INHIBICIN DE LA ACTIVIDAD ENZIMTICA
12
BIOQUMICA
ENZIMAS
Cualquier sustancia que pueda disminuir la velocidad de una reaccin catalizada
por enzimas se denomina inhibidor. Los inhibidores reversibles se fijan a las
enzimas mediante enlaces no covalentes. La dilucin del complejo de enzima e
inhibidor da por resultado disociacin del inhibidor enlazado de manera reversible,
y recuperacin de la actividad enzimtica. Ocurre inhibicin irreversible cuando
una enzima inhibida no recupera la actividad con la dilucin del complejo de
enzima e inhibidor. Las dos clases de inhibicin que se encuentran ms a menudo
son competitiva y no competitiva.
A. Inhibicin competitiva:
La inhibicin de esta clase se produce cuando el inhibidor se fija de
manera reversible al mismo sitio que ocupara normalmente el
sustrato y, en consecuencia, compite con el sustrato para ocupar ese
sitio.
1. Efecto sobre la V
mx
: el (S) en cantidad creciente invierte el
efecto de un inhibidor competitivo. A concentracin suficiente
elevada del sustrato, la velocidad de la reaccin alcanza la
V
mx
observada en ausencia de inhibidor (fig. 5-12).
2. Efecto sobre la K
m
: un inhibidor competitivo incrementa la K
m
aparente para un sustrato determinado. Esto significa que en
presencia de un inhibidor competitivo, se requiere ms
sustrato para lograr V
mx.
Inhibidor competitivo Inhibidor no competitivo
13
BIOQUMICA
ENZIMAS
3. Efecto sobre la grfica de Lineweaver-Burke: la inhibicin
competitiva manifiesta el trazo caracterstico de la grfica de
lineweaver-burke en el que las curvas de las reacciones
inhibida y no inhibida entran en interseccin sobre el eje Y a
1/V
max
(V
max
se conserva sin cambios). Las reacciones inhibida
y no inhibida efectan intersecciones diferentes sobre el eje x,
lo que indica que la K
m
aparente est aumentada en presencia
del inhibidor competitivo (fig.5-12).
4. Los frmacos llamados estatinas son ejemplos de
inhibidores competitivos: los agentes antihiperlipidemicos
de este grupo inhiben de manera competitiva la primera etapa
programada de la sntesis del colesterol. Esta reaccin es
catalizada por la reductasa de la hidroximetilglutaril-CoA
(reductasa de la HMG-CoA) Las estatinas, como la atorvastina
y la sinvastina son anlogos estructurales del sustrato natural
para esta enzima y compiten con eficacia para inhibir a la
reductasa de la HMG-CoA. Al hacerlo inhiben la sntesis de
novo del colesterol, y de esta manera disminuye las
concentraciones plasmticas de este.
14
BIOQUMICA
ENZIMAS
B. INHIBICION NO COMPETITIVA:
La inhibicin de este tipo se reconoce por su efecto caracterstico
sobre la V
max.
Ocurre inhibicin no competitiva cuando el inhibidor y
el sustrato se fijan en sitios diferentes de la enzima. El inhibidor no
competitivo puede fijarse a la enzima libre o al complejo ES, y de
esta manera impide que ocurra la reaccin.
1. Efecto sobre la V
max
: la inhibicin no competitiva no puede
quedar superada por el incremento de la concentracin del
sustrato. Por este motivo, los inhibidores no competitivos
disminuyen la V
max
de la reaccin.
2. Efecto sobre la K
m
: los inhibidores no competitivos no
interfieren con la fijacin del sustrato a la enzima. Por este
motivo la enzima manifiesta la misma K
m
en presencia o en
ausencia de un inhibidor de este tipo.
3. Efecto sobre la grfica de Lineweaver-Burke: la inhibicin
no competitiva se distingue con facilidad de la competitiva al
proyectar 1/V
0
contra 1/(S) y al observar que la V
max
disminuye
en presencia del inhibidor no competitivo, en tanto que K
m
persiste sin cambios.
4. Ejemplos de inhibidores no competitivos: algunos
inhibidores actan formando enlaces covalentes con grupos
especficos de enzimas. Por ejemplo, el plomo forma enlaces
covalentes con las cadenas laterales del sulfihidrilo de la
cistena en las protenas. La fijacin de este metal pesado
produce inhibicin competitiva. La ferroquelatasa, enzima que
cataliza la insercin del Fe
2+
en la protoporfirina es un ejemplo
de enzima sensible a la inhibicin por el plomo. Otros
ejemplos de inhibidores no competitivos son ciertos
insecticidas que producen efectos neurotxicos como
consecuencia de su fijacin irreversible sobre el sitio cataltico
de la enzima acetilcolinesterasa (enzima que segmenta al
neurotransmisor acetilcolina).
C. Inhibidores enzimticos como frmacos.
Por lo menos la mitad de los frmacos vendidos actan como
inhibidores enzimticos. Por ejemplo, los ampliamente prescritos
antibiticos lactamicos beta, como penicilina y amoxicilina, inhiben a
las enzimas que participan en la sntesis de la pared celular
bacteriana. Los frmacos pueden actuar tambin al inhibir las
reaccio9nes extracelulares. Ilustren este caso los inhibidores de la
15
BIOQUMICA
ENZIMAS
enzima conversora de angiotensina (ACE). Disminuyen la presin
arterial al bloquear a la enzima que segmenta a la angiotensina I
para que forme a la poderosa sustancia vasoconstrictora
angiotensina II. Estos frmacos que son captoprilo, enalaprilo, y
lisinoprilo producen vasodilatacin y reduccin resultante de la
presin arterial. (PAMELA C. CHAMPE, PhD BIOQUIMICA 3
era
edicin pg. 68-69-70).
LA ESTRUCTURA ENZIMTICA
Por su estructura y composicin qumica puede afirmarse que el origen de las
enzimas est vinculando al origen de las sustancias proteicas. Al hablar del origen
de la vida se ha citado el xito de los experimentos realizados en el laboratorio
para la produccin de aminocidos; estos aminocidos son los que precisamente
constituyen la base del edificio proteico. Tambin en el laboratorio se ha intentado
la sntesis de protenas a partir de aminocidos.
La sede de las enzimas es el citoplasma. Los cloroplastos vegetales contienen
una amplia gama enzimas encargadas de la funcin cloroflica, proceso que a
travs de reacciones qumicas complejas y encadenadas transforman compuestos
inorgnicos, como el agua, y el anhdrido carbnico, en sustancias complejas
adecuadas para ser entre otras cosas el alimento fundamental de los animales.
16
BIOQUMICA
ENZIMAS
En las mitocondrias existe un sistema de transporte de electrones que determinan
importantes fenmenos de xido reduccin, durante los cuales se forman notables
cantidades de ATP, que es un compuesto altamente energtico del que depende
la mayor parte de metabolismo, y coma, por tanto el trabajo de las clulas; en las
mitocondrias se produce el metabolismo enzimtico de los cidos grasos, los
cuales son en parte elaborados tambin en el citoplasma.
En los ribosomas tiene lugar concretamente todas las sntesis de las sustancias
proteicas, mientras que en los lisosomas se producen enzimas hidrolticos
cuya misin escindir, con la intervencin del agua, molculas grandes en otras
menores, que pueden a su vez ser utilizadas por las clulas; en cambio, las
enzimas glucolticos estn difundidos en el citoplasma.
La localizacin de las sedes de las distintas operaciones enzimticas antes
mencionadas ha sido posible a travs del sistema de ruptura de las clulas y de la
separacin de los distintos componentes mediante centrifugacin diferencial del
homogeneizado de estas la ruptura celular y la subdivisin de los componentes
subcelulares se realizan actualmente utilizando los tejidos, por ejemplo con saltos
bruscos desde temperaturas inferiores a 0 C hasta temperaturas ms elevadas
con cambios de presin osmtica o mediante ultrasonidos.
NATURALEZA QUMICA DE LAS ENZIMAS
Existen numerosas razones para afirmar que las enzimas son protenas. La
Ms importantes son las siguientes:
a. El anlisis de las enzimas obtenidas en forma ms pura, cristalizada,
demuestra que son protenas.
b. Las enzimas son inactivadas a altas temperaturas y, en general, la cintica de
la desnaturalizacin trmica de las enzimas da resultados muy parecidos a los
de la desnaturalizacin trmica de las protenas; por ejemplo el Q10 de la
mayora de las reacciones qumicas es de 2 a 3, y, en el caso de las enzimas,
a temperaturas elevadas, alrededor de 60 a 70 C, la actividad neta aumenta
varios cientos, como sucede con la velocidad de la desnaturalizacin trmica
de las protenas.
c. Las enzimas son activadas en una zona muy restringida de pH, y presenta un
punto ptimo de pH donde su actividad es mayor. Las protenas en su punto
isoelctrico, muestran propiedades parecidas desde el punto de vista
de viscosidad, solubilidad, difusin, etc., que resulta del todo similares a las
propiedades de este tipo que muestran las enzimas.
d. Todos los agentes que desnaturalizan a las protenas tambin destruyen o
inactivan a las enzimas, ya sea el calor, los cidos fuertes, o
los metales pesados que pueden combinarse con ellas.
17
BIOQUMICA
ENZIMAS
e. Los problemas de solubilidad y de precipitacin son comunes a las protenas y
las enzimas; en general, son solubles en agua o soluciones salinas, insolubles
en alcohol, precipitan con determinadas concentraciones de sales neutras, etc.
COMPOSICIN QUMICA DE LAS ENZIMAS
Los conocimientos sobre la composicin qumica de las enzimas
constituyeron materia de numerosas controversias hasta 1926, cuando J.B
Sumner (1887-1955) consigui cristalizar la ureasa, enzima que transforma la urea
en anhdrido carbnico y amoniaco, y demostrar que era una sustancia proteica.
A, partir de entonces fueron aisladas otras enzimas en forma pura, cristalina, y el
anlisis demostraba siempre la presencia de una protena, simple o conjugada.
Cuando los anlisis qumicos demuestran que la enzima es una protena
conjugada, pueden distinguirse en dos partes bien diferenciados:
El grupo prosttico (Coenzima)
La protena (Apoenzima)
En algunas enzimas oxidantes fue observada la presencia de la cromoprotenas,
en las cuales el grupo prosttico est representado por un compuesto que
contiene Fe y otro elemento, el cual desempea un papel importante en la
combinacin de la protena con el sustrato; otras veces este grupo prosttico es
derivada de vitaminas (como la vitamina B); 4en muchos casos resulta fcil de
separar de la molcula proteica. No obstante una vez separadas, las dos unidades
no muestran actividad enzimtica; por tanto el grupo proteico (coenzima) y el
grupo proteico (apoenzima) han de estar ntimamente ligados entre s para ser
operativos. Por consiguiente, de las enzimas pueden distinguirse los formados por:
Solo protenas, que difieren entre s por la secuencia con que los aminocidos
estn combinados, como la ureasa y las enzimas digestivas (la pepsina y la
tripsina)
Los conjugados, separados en dos entidades qumicas bien definidas: la coenzima
y la apoenzima.
Despus del descubrimiento de Sumner, el nmero de las enzimas y el estudio de
sus actividades qumicas proporcionaron un notable impulso en la enzimologa, y
la gran cantidad de las enzimas que rpidamente se acumulaban determinaron la
necesidad de utilizar una clasificacin o nomenclatura para evitar errores y facilitar
la comprensin de futuros investigadores.
NOMENCLATURA Y CLASIFICACIN DE LAS ENZIMAS
18
BIOQUMICA
ENZIMAS
Cien aos atrs solo se conocan enzimas, muchas de estas, catalizaban la
hidrlisis de enlaces covalentes. Algunas enzimas, de manera especial las que
fueron descubiertas en un principio, recibieron nombres ligados ms bien a su sitio
de procedencia anatmica que no siguen ninguna regla ni sistema; tal es el caso
de la ptialina de la saliva, que ataca al almidn de la pepsina del estmago y de la
tripsina del pncreas, que atacan protenas; de la renina, que coagula la leche; de
la papana, enzima proteoltica que se encuentra en la papaya y de las catepsinas,
tambin proteasas, que se encuentran en las clulas. Las enzimas relacionadas
con la coagulacin de la sangre, como son la trombina, la plasmina, el
plasmingeno, etc. reciben tambin nombres sistematizados.
Al descubrir nuevas enzimas y proceder a su caracterizacin estricta se aplicaron
reglas de nomenclatura basadas en el nombre del sustrato atacado, o en el tipo
general de sustrato, o en la reaccin catalizada y se ha aadido
convencionalmente, la terminacin -asa. Por ejemplo: las lipasas (hidrolizan lpidos
o grasas), las amilasas (hidrolizan almidn), las proteasas (hidrolizan protenas),
las esterasas (basado en la unin general de tipo ster presentes en muchas
sustancias), colesterol estrerasa (si la esterasa es especfica de los esteres de
colesterol) y acetilcolina esterasa (si la esterasa de la acetilcolina). Otros ejemplos:
Las fosfatasas son enzimas que atacan las uniones ster, pero en este caso,
toman su nombre del grupo vecino a la unin que van a atacar, de manera que se
denominan fosfatasas (cuando quitan una molcula de monofosfato),
pirofosfatasas (cuando quitan el cido fosfrico como esteres dobles (pirofosfatos),
o triples, etc.) De la misma manera, las carbohidrasas se denominan as
genricamente, pero pueden comprender enzimas con nombres proveniente del
sustrato particular sobre el que actan como la amilasa que ataca al almidn y la
celulosa que acta sobre la celulosa y, en otras ocasiones, se denominan de
acuerdo con la unin atacada, como la b -glucosidasa que acta sobre las uniones
b -glucosdicas. Los ejemplos se pueden extender a todos los terrenos de la
actividad enzimtica, como en las enzimas proteolticas, las fosforilasas, las
nucleasas, etc.
Esta manera de llamarlas, se demostr que era inadecuada porque al descubrirse
varias enzimas, notaron que varias enzimas catalizaban reacciones diferentes del
mismo sustrato, por ejemplo, oxidacin o reduccin de la funcin alcohol de
un azcar.
Aunque el sufijo asa contina en uso; actualmente, al nombrar a las enzimas, se
enfatiza el tipo de reaccin catalizada. Por ejemplo: las hidrogenasas catalizan la
eliminacin de hidrogeno y las transferasas, reacciones de transferencia de grupo.
Con el descubrimiento de ms y ms enzimas, surgieron ambigedades y con
frecuencia no estaba claro cul era la enzima que un investigador deseaba
estudiar. Para remediar esta deficiencia, la Comisin para el estudio de las
enzimas, que constituye con respecto a los sistemas anteriores un punto de vista
19
BIOQUMICA
ENZIMAS
ms uniforme, preciso y descriptivo; est formada por la Unin Internacional de
Bioqumica (IUB) adopto, en 1964, un sistema complejo pero inequvoco de la
nomenclatura enzimtica basado en el mecanismo de reaccin.
El sistema se basa en la reaccin qumica catalizada que es la propiedad
especfica que caracteriza a cada enzima las cuales se agrupan en clases, porque
catalizan procesos semejantes, y en subclases que especifican con mayor
exactitud la reaccin particular considerada. En general, las enzimas reciben un
nombre de acuerdo con el sustrato o los sustratos que participan en la reaccin
seguido por el tipo de reaccin catalizada y, por fin, la terminacin -asa. A menudo
los nombres as obtenidos resultan largos y complejos, por lo que es muy difcil
que en la prctica se pueda excluir el uso de los nombres triviales, consagrados
por la costumbre. Sin embargo, con fines de sistematizacin, se reconoce la
necesidad de aceptar el nuevo sistema.
Aunque su claridad y carencia de ambigedad recomiendan al sistema de
nomenclatura IUB para trabajos de investigacin, nombres ms ambiguos, pero
bastante ms cortos persisten en libros de texto y en el laboratorio clnico. Por
esta razn, a continuacin solo se presenta principios generales del sistema IUB:
1. Las reacciones y las enzimas que las catalizan se dividen en 6 clases
principales, cada una con 4 a 13 subclases.
2. El nombre de la enzima tiene 2 partes: la primera es el nombre del o los
sustratos; la segunda, con terminacin asa, indica el tipo de reaccin
catalizada.
3. Informacin adicional, si es necesario aclarar la reaccin, puede seguir el
parntesis. Por ejemplo: la enzima que cataliza L-malato + NAD= = piruvato +
CO2 NADH + H=, se denomina como 1.1.1.37 L-malato: NAD+ oxidorreductasa
(descarboxilante).
4. Cada enzima tiene un numero clave (E.C.) que caracteriza al tipo de reaccin
segn la clase (primer digito), subclase (segundo digito) y subclase (tercer
digito). El cuarto digito es para la enzima especfica. As, E.C. 2.7.1.1 denota la
clase 2 (una transferasa), subclase 7 (transferencia de fosfato), sub-clase 1
(una funcin alcohol como aceptor de fosfato). El ltimo digito denota a la
enzima hexocinasa o ATP: D-hexosa-6-fosforotransferasa, enzima que cataliza
la transferencia de fosfato desde el ATP al grupo hidroxilo de carbono 6 de la
glucosa.
Al final de sus y trabajos, clasifico las enzimas en seis grupos principales,
correspondientes por sus trminos a las raciones que cada enzima ejerce sobre el
sustrato. Estos grupos se subdividen en otro, segn el tipo de sustrato y los
tomos concretos que son sensibles a sus acciones. Estos seis grupos son los
siguientes:
20
BIOQUMICA
ENZIMAS
1. Oxidoreductasas
2. Transferasas
3. Hidrolasas
4. Isomerasas
5. Liasas
1. Oxido-reductasas: Son las
enzimas relacionadas con las
oxidaciones y las reducciones
biolgicas que intervienen de
modo fundamental en los
procesos de respiracin y
fermentacin. Las
oxidoreductasas son
importantes a nivel de algunas
cadenas metablicas, como la
escisin enzimtica de la
glucosa, fabricando tambin el
ATP, verdadero almacn de energa. Extrayendo dos tomos de hidrgeno,
catalizan las oxidaciones de muchas molculas orgnicas presentes en el
protoplasma; los tomos de hidrgeno tomados del sustrato son cedidos a algn
captor.
En esta clase se encuentran las siguientes subclases principales:
Deshidrogenasas y oxidasas. Son ms de un centenar de enzimas en cuyos
sistemas actan como donadores, alcoholes, oxcidos aldehdos, cetonas,
aminocidos, DPNH2, TPNH2, y muchos otros compuestos y, como receptores,
las propias coenzimas DPN y TPN, citocromos, O2, etc.
2. Las Transferasas: Estas enzimas catalizan la transferencia de una parte de la
molcula (dadora) a otra (aceptora). Su clasificacin se basa en la naturaleza
qumica del sustrato atacado y en la del aceptor. Tambin este grupo de enzimas
actan sobre los sustratos ms diversos, transfiriendo grupos metilo, aldehdo,
glucosilo, amina, sulfat, sulfrico, etc.
Un ejemplo es la glucoquinasa, que cataliza la
reaccin representada en la Figura de la derecha:
glucosa + ATP
ADP + glucosa-6-fosfato
21
BIOQUMICA
ENZIMAS
3. Las Hidrolasas: Esta clase de enzimas actan normalmente sobre las grandes
molculas del protoplasma, como son la de glicgeno, las grasas y las protenas.
La accin cataltica se expresa en la escisin de los enlaces entre tomos de
carbono y nitrgeno (C-Ni) o carbono oxigeno (C-O); Simultneamente se obtiene
la hidrlisis (reaccin de un compuesto con el agua) de una molcula de agua. El
hidrgeno y el oxidrilo resultantes de la hidrlisis se unen respectivamente a las
dos molculas obtenidas por la ruptura de los mencionados enlaces. La
clasificacin de estas enzimas se realiza en funcin del tipo de enlace
qumico sobre el que actan.
A este grupo pertenecen protenas muy conocidas: la pepsina, presente en el jugo
gstrico, y la tripsina y la quimotripsina, segregada por el pncreas. Desempean
un papel esencial en los procesos digestivos, puesto que hidrolizan enlaces
ppticos, estricos y glucosdicos.
Un ejemplo es la lactasa, que cataliza la reaccin:
lactosa + agua
glucosa + galactosa
4. Las isomerasas: Transforman ciertas sustancias en otras ismeras, es decir,
de idntica formula emprica pero con distinto desarrollo. Son las enzimas que
catalizan diversos tipos de isomerizacin, sea ptica, geomtrica, funcional, de
posicin, etc. Se dividen en varias subclases.
Las racemasas y las epimerasas actan en la racemizacin de los aminocidos y
en la epimerizacin de los azcares. Las primeras son en realidad pares de
enzimas especficas para los dos ismeros y que producen un
solo producto comn. Las isomerasas cis trans modifican la configuracin
geomtrica a nivel de un doble ligadura. Las xido reductasas intermoleculares
catalizan la interconversin de aldosas y cetosas, oxidando un grupo CHOH y
reduciendo al mismo tiempo al C = O vecino, como en el caso de la triosa fosfato
isomerasa, presente en el proceso de la gluclisis ; en otros casos cambian de
lugar dobles ligaduras, como en la (tabla) isopentenil fosfato isomerasa,
indispensable en el cambio biosintico del escaleno y el colesterol. Por fin las
transferasas intermoleculares (o mutasas) pueden facilitar el traspaso de grupos
acilo, o fosforilo de una parte a otra de la molcula, como la lisolecitina acil mutasa
que transforma la 2 lisolecitina en 3 lisolecitina, etc. Algunas isomerasa actan
realizando inversiones muy complejas, como transformar compuestos aldehdos
en compuestos cetona, o viceversa. Estas ltimas desarrollan una oxido reduccin
dentro de la propia molcula (oxido reductasa intermoleculares) sobre la que
22
BIOQUMICA
ENZIMAS
actan, quitando hidrgeno, a algunos grupos y reduciendo otros; actan
ampliamente sobre los aminocidos, los hidroxcidos, hidratos de carbono y sus
derivados.
Son ejemplos la fosfotriosa isomerasa y la fosfoglucosa isomerasa, que catalizan
las reacciones representadas en la tabla inferior:
fosfotriosa isomerasa fosfoglucosa isomerasa
gliceraldehdo-3-
fosfato
dihidroxiacetona-
fosfato
glucosa-
6-fosfato
fructosa-6-
fosfato
5. Las Liasas: Estas enzimas escinden (raramente construyen) enlaces entre
tomos de carbono, o bien entre carbono y oxgeno, carbono y nitrgeno, y
carbono y azufre. Los grupos separados de las molculas que de sustrato son casi
el agua, el anhdrido carbnico, y el amoniaco. Algunas liasas actan sobre
compuestos orgnicos fosforados muy txicos, escindindolos; otros separan el
carbono de numerosos sustratos.
Un ejemplo es la acetacetato descarboxilasa, que cataliza la reaccin:
cido acetactico
CO
2
+ acetona
6. Las Ligasas: Es un grupo de enzimas que permite la unin de dos
molculas, lo cual sucede simultneamente a la degradacin del ATP, que,
en rigor, libera la energa necesaria para llevar a cabo la unin de las
23
BIOQUMICA
ENZIMAS
primeras. Se trata de un grupo de enzimas muy importantes y recin
conocidas, pues antes se pensaba que este efecto se llevaba a cabo por la
accin conjunta de dos enzimas, una fosfocinasa, para fosforilar a una
sustancia A (A + ATP A - + ADP) y una transferasa que pasara y unira
esa sustancia A, con otra, B (A - + B A B + Pi). A este grupo pertenecen
enzimas de gran relevancia reciente, como las aminocido ARNt Ligasas
conocidas habitualmente con el nombre de sintetasas de aminocidos
ARNt o enzimas activadoras de aminocidos que representan el primer
paso en el proceso biosinttico de las protenas, y que forman uniones C-O;
las cido-tiol ligasas, un ejemplo tpico de las cuales es la acetil coenzima.
A sintetasa, que forma acetil coenzima. A partir de cido actico y coenzima
A; las ligasas cido amoniaco (glutamina sintetasa), y las ligasas cido-
aminocido o sintetasas de pptidos, algunos de cuyos ejemplos ms
conocidos son la glutacin sintetasa, la carnosina sintetasa, etc.
La accin de estas enzimas se manifiesta con la formacin de enlaces entre
tomos de carbono y oxigeno de diversas molculas, o bien entre carbono y
azufre, carbono y nitrgeno y carbono y carbono. Las ligasas utilizan siempre,
para el proceso de reaccin, la energa proporcionada por el ATP o compuestos
homlogos que son degradados, Por consiguiente las enzimas de esta clase son
los nicos que intervienen en reaccin no espontnea desde un punto de vista
termodinmico; Actan sobre los sustratos ms diversos y revisten particular
importancia en el metabolismo de los cidos nucleicos.
Estas reacciones enzimticas se desarrollan en dos tiempos: en el primero se
forma un complejo intermedio con potencia energtica muy alta-, en el segundo
utilizan la energa obtenida para realizar la reaccin de sntesis.
Un ejemplo es la piruvato carboxilasa, que cataliza la reaccin:
piruvato + CO
2
+ ATP
oxaloacetato + ADP + P
i
24
BIOQUMICA
ENZIMAS
GRUPO ACCIN EJEMPLOS
1. Oxidoreductasas Catalizan reacciones de xido
reduccin. Tras la accin catlica
quedan modificados en su grado de
oxidacin por lo que debe ser
transformados antes de volver a
actuar de nuevo.
Dehidrogenasas
Aminooxidasa
Deaminasas
Catalasas
2. Transferasas Transfieren grupos activos (obtenidos
de la ruptura de ciertas molculas) a
otras sustancias receptoras. Suelen
actuar en procesos de
interconversiones de azucares, de
aminocidos, etc.
Transaldolasas
Transcetolasas
Transaminasas
3. Hidrolasas Verifican reacciones de hidrlisis con
la consiguiente obtencin de
monmeros a partir de polmeros.
Suele ser de tipo digestivo, por lo que
normalmente actan en primer lugar
Glucosidasas
Lipasas
Peptidasas
Esterasas
Fosfatasas
4. Isomerasas Actan sobre determinadas
molculas obteniendo de ellas sus
ismeros de funcin o de posicin.
Suelen actuar en procesos de
interconversin
Isomerasas de
azcar
Epimerasas
Mutasas
5. Liasas Realizan la degradacin o sntesis
(entonces se llaman sintetasas) de
los enlaces denominados fuertes sin
ir acoplados a sustancias de
alto valor energtico.
Aldolasas
Decarboxilasas
6. Ligasas Realizan la degradacin o sntesis de
los enlaces fuertes mediante el
acoplamiento a sustancias ricas en
energa como los nucleosidos del
ATP
Carboxilasas
Peptidosintetasas
EFECTO DE LA MODIFICACIN COVALENTE SOBRE LA ACTIVIDAD
ENZIMTICA
Otros enzimas pasan de una forma menos activa a otra ms activa unindose
covalentemente a un grupo qumico de pequeo tamao como el P
i
o el AMP.
Tambin se da el caso inverso, en el que un enzima muy activo se desactiva al
liberar algn grupo qumico. En las enzimas de las vas degradativas del
metabolismo, la forma fosforilada es ms activa que la no fosforilada, mientras que
25
BIOQUMICA
ENZIMAS
en las vas biosintticas ocurre lo contrario. En las figuras inferiores se ilustra la
activacin de una protena por fosforilacin.
ACTIVACIN PROTEOLTICA DE LA ACTIVIDAD ENZIMTICA
Algunos enzimas no se
sintetizan como tales, sino
como protenas
precursoras sin actividad
enzimtica. Estas
protenas se
llaman proenzimas o
zimgenos. Para
activarse, los zimgenos
sufren un ataque
hidroltico que origina la
liberacin de uno o varios
pptidos. El resto de la
molcula proteica adopta la conformacin y las propiedades del enzima activo.
Muchos enzimas digestivos se secretan en forma de zimgenos y en el tubo
digestivo se convierten en la forma activa. Es el caso de la -quimotripsina, que se
sintetiza en forma de quimotripsingeno (Figura superior). Si estos enzimas se
sintetizasen directamente en forma activa destruiran la propia clula que las
produce. As, la tripsina pancretica (una proteasa) se sintetiza como tripsingeno
(inactivo). Si por alguna razn se activa en el propio pncreas, la glndula sufre un
proceso de autodestruccin (pancreatitis aguda), a menudo mortal.
Elementos de la reaccin El enzima no fosforilado es inactivo El enzima fosforilado es activo
26
BIOQUMICA
ENZIMAS
PARTES DEL SISTEMA ENZIMATICO
Los sistemas enzimticos en general, estn formados por la enzima propiamente
dicha (apoenzima), el sustrato o los sustratos un grupo proteico (o coenzimas) y
sustancias activadoras. La estructura formada por la apoenzima y la coenzima se
denomina holoenzima; con cierta frecuencia se reconocen sistemas enzimticos
que no tienen grupo prosttico o activadores reconocidos.
Apoenzima: concepto del centro activo
La apoenzima es la enzima propiamente dicha, de naturaleza proteica formada por
cadenas de polipptidos, con peso molculas elevado, no dializable y termolbil.
Las estudiadas analticamente hasta ahora, han sido, por razones tcnicas de
peso molecular bajo, 12 a 24 000, tienen una sola cadena polipeptidica
(ribonucleasa, papana, tripsina, pepsina, etc.) excepto uno o dos casos (a -
quimotripsina y aldolasa) que tienen dos.
El anlisis de los aminocidos que componen a diversas enzimas demuestran que
tienen una estructura similar a la de cualquier protena; existen, de hecho unos
cuantos casos en los que se ha determinado su secuencia completa, es decir, el
orden en el que estn dispuestos todos ellos en la cadena. El anlisis de la
estructura secundaria de la protena, sea el modo como la cadena peptdica se
dispone a lo largo de su eje mayor y el de la estructura terciaria, sea la forma en
que la cadena se pliega y se acomoda para formar una estructura tridimensional
se conoce muy mal para todas las enzimas. Solo en el caso de la lisozima (enzima
presente en las lgrimas donde funciona como un antisptico suave y que tiene la
capacidad de atacar a los polisacridos que forman la pared de diversas bacterias)
se ha determinado la estructura tridimensional de una enzima; para este fin se
aplican las tcnicas de cristalografa de rayos x, con una solucin de dos , lo que
demostr que la lisozima es una protena con su cadena de 129 aminocidos
ampliamente plegada y en la que se reconoce una hendidura representante del
centro activo donde se acomodan muy bien los inhibidores ciertos compuestos
del tipo de carbohidratos que nulifican su actividad enzimtica. Se ha
demostrado, en este caso, que es cierta regla general de que el modo como se
ordenan y disponen los aminocidos determina el arreglo espacial que permite a
las otras partes del sistema enzimtico sustratos, cofactores, iones, etc.
adaptarse, en el espacio, en forma adecuada, para que se lleve a cabo la accin
cataltica. Por lo tanto, las estructuras indispensables que permiten la combinacin
con el sustrato y que confieren propiedades enzimticas a la molcula se
denominan "centro activo". Se acepta que el centro activo no es una parte muy
grande de la enzima completa y, en ciertos sistemas estudiados por medio de
bloqueos qumicos no parece constituir una zona de ms de 20 de dimetro. Es
muy posible que el centro activo est formado por la contribucin de grupos
funcionales de aminocidos situados en distintas cadenas o en diferentes
27
BIOQUMICA
ENZIMAS
repliegues de una cadena, asiendo aparecer a dichos grupos muy distantes entre
ellos si se considera el orden que guardan a lo largo de la cadena polipeptidica.
Un caso muy ilustrativo sobre lo que significa la estructura del centro activo desde
el punto de vista de la composicin de los aminocidos es el de la triptfano
pirrolasa, enzima ampliamente estudiada en bacterias desde el punto de vista de
la bioqumica gentica. En ella, la modificacin de algunos aminocidos produce
perdida de la actividad enzimtica, que se recupera si vuelve a incluirse los
aminocidos en el orden original; sin embargo, se pueden reemplazar dos de ellos
por otros completamente distintos, y la enzima vuelve a ser totalmente activa. Es
posible que con estos nuevos aminocidos se consigan tambin las condiciones
de distribucin espacial de grupos funcionales y estructuras necesarias para la
actividad enzimtica.
El concepto de arreglo tridimensional adecuado de los aminocidos que forman la
cadena polipeptidica de la enzima para lograr la actividad funcional correcta
permite entender numerosos fenmenos: la necesidad de que la molcula proteica
ntegra est preservada en su forma; el hecho de que la desnaturalizacin de la
enzima al permitir la separacin de los pliegues, conduce a la perdida de la
actividad enzimtica; que al calentar una enzima con su sustrato (por ejemplo, la
invertasa con sacarosa, la transaminasa con cido a -cetoglutrico), se impide una
desnaturalizacin que sin ellos se producira, pues es posible que el propio
sustrato contribuya a sostener y reforzar la aproximacin de los pliegues de la
cadena, etc.
Tambin se entiende por qu al atacar la ribonucleasa con pepsina y romper una
sola unin peptdica que separa un tetrapeptido del extremo con grupo carboxilo
libre se pierde la actividad, mientras que si solo se quita los tres ltimos disminuye
su accin sugiriendo as la importancia del residuo de cido asprtico para
sostener el centro activo en condiciones de eficiencia, o lo que es ms probable,
para formar parte del propio centro activo. Si se parte la ribonucleasa entre los
aminocidos 20 y 21, y se separan los dos fragmentos, ninguno es activo, pero
basta mezclarlos para que se unan en tal forma que se restablece la actividad,
aunque un poco menor que la originalmente observada.
El estudio detallado de la estructura del centro activo se hace por medio de
inhibidores o de reactivos que se combinan de modo especfico, con algunos de
los aminocidos del centro activo tales como el diisopropilfluorofosfato (DFP), que
se combina con el OH del aminocido Serina, en diversas esterasas, peptidasas,
etc. , e inactiva el centro activo del que forman parte dicho aminocido; este
inhibidor, an a concentraciones de 10-10 M, inhibe a la acetilcolinesterasa;
mucho de los derivados del DFP se utilizan como gases de guerra o como
insecticidas (parathion), y su utilidad se debe, en rigor a su capacidad para destruir
funcionalmente ciertas enzimas.
28
BIOQUMICA
ENZIMAS
La unin del DFP al aminocido cedina es muy estrecha y a permitido el anlisis
de los aminocidos vecinos a l, haciendo un estudio de su ordenamiento en el
centro activo. La secuencia de los centros activos de diversas enzimas hidrolticas
sensibles al DFP, se demuestran que la mayora tienen cerina y adems un
aminocido dicarboxlico (asprtico o glutmico) y en el otro un aminocido neutro
(alanina o glicina). Tambin se ha demostrado que la histidina, cuando menos
para el caso de la quimotripsina, forma parte del centro activo aun cuando el
anlisis de la secuencia no demuestra que exista cerca de la cerina ninguna
histidina; se trata, por lo tanto, de otro ejemplo de una aminocido, alejado e otro,
y en distinto pliegue de la cadena, que integra el centro activo.
Teniendo en cuenta estos hechos, se deduce, por lo tanto, que la actividad de la
enzima depende en parte de la disposicin o arreglos de los aminocidos y grupos
prostticos en determinada regin de la protena. Los aminocidos que componen
a las protenas pueden tener moderadas actividades catalticas, aunque de
ninguna manera comparable en su magnitud, cuando se les considera en forma
aislada, a las que muestran la gran molcula proteica. De hecho para muchos
sistemas enzimticos se han ideado modelos anlogos, sea sustancias qumicas
sencillas que suelen reproducir los efectos ocasionados por la enzima, tal es el
caso de los anlogos, a base de piridoxsal que representan la parte activa de
enzimas descarboxilantes y transaminantes. Esto no significa que
necesariamente, en el estado natural, la enzima funcione como lo hace el anlogo
pues muchos sistemas pudieran tener otro mecanismo de operacin; la hidrlisis
del almidn lo mismo se logra con la adicin del cido que con la enzima
especfica amilasa, aun cuando en el primer caso se atacan indiscriminadamente
numerosas uniones glucosdicas, y con la enzima, en cambio solo se desprenden,
uno tras otro fragmentos de dos unidades de glucosa de los extremos de las
ramificaciones.
Conformacin de la enzima y propiedades del centro activo. La propiedad
cataltica de las enzimas parece depender de la facilidad con la que ayudan a que
se pongan en contacto las sustancias reaccionantes para dar el producto o los
productos de la reaccin. Esto implica que el sistema enzimtico tenga una
conformacin especial sea, una disposicin adecuada de os grupos funcionales
aminocidos de la apoenzima y grupos prostticos, cuando existen estos y de
las molculas mismas de los sustratos que se unirn a aquellos y permitirn que
se lleve a cabo la reaccin qumica. Este acercamiento de las sustancias
reaccionantes de los grupos prostticos y los grupos funcionales fue las razn
del modelo de Ehrlich, conocido clsicamente como de la "llave y la cerradura".
As la enzima sera un molde tridimensional en negativo, de la estructura tambin
tridimensional, en positivo de los reaccionantes que se adaptaran perfectamente a
ala disposicin de la enzima. Sin embargo ha sido necesario reconsiderar esta
29
BIOQUMICA
ENZIMAS
situacin y sugerir de acuerdo con Koshland la teora de un "acomodo
inducido".
As las enzimas pueden sufrir un cambio en su estructura desde el momento en
que entran en contacto con los reaccionantes, sustratos y cofactores, y es posible
que todos ellos modifiquen el arreglo tridimensional de la enzima; la enzima los
recibe en un orden determinado y cada uno de ellos al unirse a la enzima modifica
su estructura. La nueva analoga es la del "guante y la mano"; aquel no representa
una estructura de negativo tridimensional mientras no se halla la mano en el, ya
que antes pueden tener diversas formas y disposiciones, una vez que ha entrado
la mano - que a su vez tambin puede adoptar distintas posiciones se ponen en
contacto todas las partes correspondientes, es decir, en el caso de la enzima, las
partes reactivas del sistema enzimtico, con las partes reaccionantes, osea los
sustratos. Se ha preservado con esta nueva idea, el aspecto de la armona
estructural entre el sustrato y la enzima pero se introduce el nuevo concepto de
que es necesario provocar un cambio en la estructura proteica que favorezca la
colocacin adecuada de todos los elementos que interviene en la reaccin
enzimtica. Los cambios de la estructura proteica se denominan
"conformacionales". El cambio en la disposicin tridimensional puede hacerse a
distancia y en muchas ocasiones la unin del sustrato a una parte de la enzima
modifica otras zonas de ella y an su estructura completa, debido a plegamientos
que acercan o alejan diversos grupos colocados a lo largo del pptido que forma la
enzima. Esta alteracin mltiple y de tipo flexible, permite entender mejor el
proceso de entrada ordenada de los sustratos, y los cofactores y la reaccin en la
que se participan. Tambin permiten comprender porque un sustrato entra a una
enzima y es atacado y uno que no lo es an muy parecido a l, puede quedar
excluido del centro activo.
Se ejemplifican estas ideas en A se encuentra la enzima en una forma desplegada
con ciertos grupos reactivos (+) y (-), colocados en una zona de la superficie de la
enzima. La entrada de un cofactor F1, modifica una parte del sistema (B); se
introduce en el sistema un nuevo arreglo a base de la reactividad de tipo
electrnico entre la zona (+) y una parte del cofactor F1, recin introducido; por fin
la entrada de un nuevo reaccionate F2 modifica la parte terminal de la enzima de
manera que permite la entrada del otro reaccionante (sustrato) que se acomoda
en un lugar preparado previamente por los reaccionantes F1 y F2, y permite de
esta manera echar a andar la reaccin cataltica. Los cambios conformacionales,
se pueden demostrar con diversos mtodos algunos de tipo fsico, como son las
modificaciones en la rotacin ptica o en el patrn de sedimentacin en el campo
gravitacional de la ultracentrfuga, o qumicos como el aumento o la disminucin
de la actividad enzimtica bajo la influencia de cambios trmicos o la adicin de
agentes desnaturalizantes. Basten unos cuantos ejemplos: la transaminasa a -
30
BIOQUMICA
ENZIMAS
cetoglutrica se pude calentar a 65 C. en presencia de su sustrato sin que se
afecte, al paso que la enzima sola es rpidamente degradada, cambia de
configuracin y se precipita; la miosina, protena muscular contrctil, en presencia
de ATP hace ms notable su forma de espiral y permite el reconocimiento de
aminocidos previamente ocultos en sus pliegues; la D-amino oxidasa, al unirse a
su cofactor, el FAD, pasa de la forma espiral en a -hlice, a una disposicin
irregular distribuida al azar.
COENZIMA Y GRUPOS PROSTTICOS
Una coenzima es una molcula orgnica pequea necesaria para la actividad de una
enzima. Las coenzimas son cofactores de naturaleza orgnica.
Una coenzima es un cofactor de naturaleza orgnica. Las coenzimas son necesarias
para la actividad de muchas enzimas. La tetrahidrobiopterina, el ATP, el GTP, el
NAD, la coenzima A o la coenzima Q son algunos ejemplos de coenzimas. Muchas
coenzimas son vitaminas o derivados de ellas especialmente de la vitamina B.
Normalmente sufren reacciones de oxidacin, reduccin y transferencia de grupos
qumicos. Las coenzimas sufren las transformaciones qumicas necesarias para la
catlisis enzimtica evitando que la enzima las sufra. De este modo la enzima queda
intacta y puede llevar a cabo otro ciclo de reacciones simplemente cambiando la
coenzima.
Las coenzimas tienen un papel fundamental en el metabolismo y en la fisiologa del
organismo y, de hecho, hay muchas enfermedades producidas por defectos en
coenzimas. Algunos ejemplos de este tipo de enfermedades son la fenilcetonuria en
la que existe un defecto de tetrahidrobiopterina o la pelagra que se produce por un
dficit de NAD (Nicotinamida Adenina Di nucletido).
MECANISMO DE ACCIN DE LAS COENZIMAS
El mecanismo de accin bsico de las coenzimas es el siguiente:
1. La coenzima se une a una enzima.
2. La enzima capta su sustrato especfico.
3. La enzima ataca a dicho sustrato, transfiriendo algunos de sus electrones.
En realidad la unin de sustrato y enzima produce una nueva sustancia.
Esta sustancia es inestable, lo que provoca su separacin en diferentes
partes: enzima, producto, y la forma reducida de la coenzima, que se
31
BIOQUMICA
ENZIMAS
qued con algunos electrones (al oxidar el sustrato sta se reduce) por
presentar mayor fuerza de atraccin molecular.
4. La enzima cede a la coenzima dichos electrones provenientes del sustrato.
5. La coenzima acepta dichos electrones y se desprende de la enzima.
6. La coenzima reducida va a la cadena de transporte de electrones, en la
cual se genera ATP y H2O (respiracin celular), al "dejar" all sus
electrones sta mediante unas lanzaderas, vuelve a su estado inicial.
Este ltimo paso es esencial para no agotar la dotacin de coenzimas de una
clula ya que las enzimas junto con las que acta no pueden realizar la reaccin
qumica sin el concurso de su coenzima.
Algunas coenzimas estn fuerte y permanentemente unidas a su enzima,
constituyendo en la prctica un grupo prosttico; tal es el caso del FMN a la
enzima NADH deshidrogenasa o el FAD a la succinato deshidrogenasa.
Cada coenzima est especializada en aceptar y transportar un tipo de tomos
determinado; unos aceptan hidrgenos, otros grupos acetilo, amino, etc. No
obstante, las coenzimas no son nada especficas respecto a las enzimas a las que
se unen, de modo que una misma coenzima puede unirse a un gran nmero de
enzimas distintas y es por ello que el nmero de coenzimas diferentes es
relativamente bajo.
PRINCIPALES COENZIMAS:
Coenzima A.
FAD (flavn-adenn dinucletido): transferencia de electrones y protones.
FMN (flavn mononucletido): transferencia de electrones y protones.
NAD
+
(nicotn-adenn dinucletido): transferencia de electrones y protones.
NADP
+
(nicotn-adenn dinucletido fosfato):
Coenzima A: transferencia de grupos acetilo (por ejemplo, en
la descarboxilacion del cido pirvico) y de grupos acilo en general.
Coenzima Q: transferencia de electrones en la cadena respiratoria.
32
BIOQUMICA
ENZIMAS
Coenzima B
12
: transferencia de grupos metilo o hidrgenos entre molculas.
TPP (pirofosfato de tiamina): transferencia de grupos aldehdo; forma parte,
entre otros, del complejo piruvato deshidrogenasa.
Vitamina C
PLP (fosfato de piridoxal): transferencia de grupos amino.
PMP (fosfato de piridoxamina): transferencia de grupos amino.
FH
4
(cido tetrahidroflico): transferencia de
grupos formilo, metenilo y metileno.
Biocitina: transferencia de dixido de carbono.
cido lipoico: transferencia de hidrgenos, grupos acilo y metilamina.
Aparte del sustrato, cuya transformacin ser condicionada por la enzima, existe
otra parte del sistema enzimtico, de peso molculas bajo y por lo tanto dializable,
termostable y en general, no proteica, adherida de ms o menos laxa a la
apoenzima y a la cual se le llama grupo prosttico, si est muy ntimamente ligada
a la apoenzima como es el caso del ncleo porfirnico de numerosas oxidasas o
la estructura flavnica de la deshidrogenasa succnica o coenzima cuando la
unin es dbil y se separan fcilmente, como por ejemplo el DPN y el TPN que
asisten a las funciones de varias deshidrogenasas. Es muy grande la importancia
del grupo prosttico o de la coenzima desde el punto de vista funcional pues
suelen ceder y recibir alternadamente parte de los productos de la reaccin. Por
ejemplo en las reacciones de xido reduccin los hidrgenos desprendidos de
un sustrato deben ser captados por una sustancia con lo que se expulsa al
sustrato oxidado y es posible recibir una nueva molcula del sustrato con
hidrgenos. Tal sustancia es una coenzima, como el DPN, el TPN, el FAD, etc.,
que, a su vez, suele cederlos a una tercera sustancia o, cuando las reacciones
son reversibles los pasan al sustrato oxidado para reducirlo. Algunos autores
denominan cosustratos a estos agrupamientos coenzimticos para hacer nfasis
en su carcter reversible, no cataltico y equimolecular con respecto al sustrato.
Una proporcin de las vitaminas forman parte de molculas ms complejas que
funcionan como coenzimas en diversas reacciones.
Muchas enzimas requieren una coenzima
Muchas enzimas que catalizan la transferencia de grupos y otras reacciones
requieren, adems de su sustrato, una segunda molcula orgnica conocida como
coenzima sin la cual son inactivas. Para distinguirlas de iones metlicos
activadores y de las enzimas mismas, las coenzimas se definen como compuestos
orgnicos termoestable, de peso molecular bajo, requeridas para la actividad de
las enzimas. La mayor parte de las coenzimas se unen a las enzimas
33
BIOQUMICA
ENZIMAS
por fuerza no covalentes. Las que forman enlace covalentes con las enzimas se
denominan tambin grupos prostticos.
Entre las reacciones que requieren coenzimas estn las oxido reducciones, las
reacciones de transferencia de grupo e isomerizacin y las reacciones que forman
enlaces covalentes (claves 1, 2,5 y 6; IUB). Las reacciones lticas que comprenden
reacciones hidrolticas catalizadas por enzimas digestivas no requieren de
coenzimas.
Las coenzimas pueden considerarse como segundo sustrato
La coenzima puede considerarse como un segundo sustrato o cosustratos por dos
razones. En primer lugar, los cambios qumicos en la coenzima compensan
exactamente a los que realizan en el sustrato. Por ejemplo, en las reacciones u
oxido reduccin (deshidrogenasa), una molcula de sustrato es oxidasa y una
molcula de coenzima es reducida.
Una segunda razn para dar igual nfasis a las reacciones de la coenzima es que,
en realidad, este aspecto de la reaccin es el que puede ser de significado
fisiolgico fundamental. Por ejemplo, la importancia de la capacidad del msculo
que trabaja en condiciones anaerobias para convertir el piruvato en lactato no
reside en el piruvato ni en el lactato.
La reaccin sirve solamente para oxidar la coenzima reducida NADH a NAD+. Sin
NAD+ la gluclisis no puede continuar y la sntesis anaerobias de ATP (y por
tanto, el trabajo) tiene que cesar. En condiciones anaerobias, la reduccin del
piruvato en lactato reoxida al NADH y permite la sntesis de ATP. Otras reacciones
pueden servir igualmente bien. Por ejemplo, en las bacterias o levaduras que
crecen en medio anaerobio, algunos metabolitos derivados del piruvato son
utilizados como oxidante para el NADH y son reducidos en el proceso.
Las coenzimas funcionan como reactivos en la transferencia de grupos
Las reacciones bioqumicas de transferencia de grupo del tipo.
D G + A = A G + D
En la cual un grupo funcional, G es transferido de una molcula donadora, D-G, a
una molcula aceptora, A, por lo general comprende la participacin de una
coenzima como ltimo aceptor (por ejemplo, reacciones de hidrogenacin) o como
portador intermediario del grupo (por ejemplo, reacciones de transaminacin). El
esquema siguiente muestra el ltimo concepto.
D-H CoE A-G
D CoE-G A
34
BIOQUMICA
ENZIMAS
Aunque estos sugiere la formacin de un complejo sencillo CoE-G, durante el
curso de la reaccin global, pueden intervenir varios complejos intermediarios
CoE-G en una reaccin particular (por ejemplo, transaminacin).
Cuando el grupo transferido es el hidrgeno, es costumbre representar slo la
"mitad izquierda de la reaccin":
D-H CoE
D CoE-H
Que esto representa en realidad slo un caso especial de la transferencia general
de grupos puede apreciarse mejor en trminos de las reacciones que ocurren en
las clulas intactas. Se pueden representar de la siguiente manera:
D-H CoE A-H
D CoE-H A
Las coenzimas pueden clasificarse de acuerdo al grupo cuya transferencia
facilitan. Basndose en este concepto podra clasificarse a las coenzimas como
sigue:
Para la transferencia de grupos distintos del hidrgeno:
Fosfatos de azcares
CoASH
Pirofosfato de tiamina.
Fosfato de piridoxal
Coenzimas del folato
Biotina
Coenzimas de cobamida (B12)
cido lipoico
Para la transferencia del hidrgeno:
NAD+, DADP+
FMN, FAD.
cido lipoico
Coenzima Q.
-Muchas coenzimas derivan de vitamina B y del monofosfato de adenosina
Las vitaminas B forman parte de la estructura de numerosas coenzimas. Las
vitaminas B; nicotinamida, tiamina, riboflavina y cido pantotnico son
constituyentes esenciales de las coenzimas para las oxidaciones y las reducciones
biolgicas y las coenzimas cido flico y cobamida funcionan en
35
BIOQUMICA
ENZIMAS
el metabolismo de compuestos de un solo carbono. Numerosas coenzimas
contienen adenina, ribosa y fosfato y se derivan del monofosfato de adenosina
AMP. Los ejemplos incluyen NAD+ y NADP+
ACTIVADORES
Las enzimas son catalizadores orgnicos que disminuyen la barrera denominada
energa de activacin; y por tanto facilitan el que se inicie una reaccin. Este
proceso implica el trabajo necesario para poner a dos molculas en un contacto lo
suficientemente estrecho como para que reaccionen; adems, el trabajo debe
realizarse sobre la unin qumica una con covalencia en sentido estricto para
que pueda romperse y formar otros compuestos. Las enzimas, como muchos
catalizadores, son partculas de gran superficie y muestran que tienen capacidad
para atraer y captar diversas molculas. Cualquier factor que permita por una
parte atraer al sustrato a su centro activo se pude considerar como un activador,
adems algo que permita la rpida salida de los productos tambin pude
considerarse como un activador. As se reconocen diversas posibilidades:
Activacin inica. Numerosos metales mono divalentes son necesarios para la
actividad enzimtica de diversos sistemas. Destacan entre ellos los siguientes: K+,
Mn++, Mg++, Ca++, Fe+++, Cu+, Cu++, etc. A menudo el metal, a estas
condiciones, es el centro que permite la unin conjunta del sustrato, de la
coenzima y de la misma apoenzima con la que forma quelatos (de chelos, garra;
complejos moleculares sostenidos por un metal) al unirse con grupos cargados
elctricamente. Muy amenudo se demuestra que es posible sustituir
los metales divalentes entre ellos, sin grandes modificaciones de la velocidad de la
reaccin.
Los metales como el hierro, el cobre y el molibdeno, actan a menudo como
transportadores de electrones y no se les puede considerar activadores en el
sentido estricto pues forman parte integral del grupo prosttico. Algunos aniones
tambin son necesarios para la actividad de ciertas enzimas; bien conocido es el
caso del Cl-, el que puede sustituirse, aun cuando con baja de la velocidad, por Br-
, para la amilasa salival; o el propio radical fosfato que se requiere en reacciones
de fosforilacin.
Activacin por el grupo prosttico. En determinadas reacciones estos son
indispensables para el trabajo de la enzima y constituyen, en rigor, la parte
funcional activa del sistema.
36
BIOQUMICA
ENZIMAS
Activacin de la apoenzima. Consiste en la obtencin de una correcta estructura
del centro activo de la protena con actividad enzimtica, ya referido
anteriormente.
Integridad de los grupos funcionales del centro activo. Destaca la relacionada
con los grupos sulfhidrilo, -SH. Cualquier alteracin qumica que los destruya,
bloquee u oxide a disulfuro, -S-S-, puede inactivar a las enzimas. Esto puede
suceder incluso en las suaves condiciones del trabajo celular por exposicin a
agentes oxidantes o al oxigeno mismo, aunque puede lograrse por el efecto de
sustancias que los ataquen y que combinen con ellos como la yodacetamida. En
otras ocasiones la destruccin de los grupos SH, aun la distancia del centro
activo modifica de tal manera la estructura tridimensional de la enzima que el
centro activo se deforma al grado de que no puede llevar a efecto su accin sobre
las sustancias reaccionantes. Existen otros grupos funcionales cuyo bloqueo
acaba por completo con la actividad enzimtica; en tal caso estara la accin de
inhibidores o venenos enzimticos.
Medida de la actividad enzimtica. Aparte del problema de medir las
pequesimas cantidades de enzimas presentes en los tejidos; muy pocas de ellas
poseen caractersticas qumicas o espectroscpicas particulares que permita
medirlas directamente. En general, las enzimas se cuantean siguiendo la actividad
de la reaccin que catalizan y se aceptan, en principio que dicha actividad es
proporcional a la cantidad de enzima presente. Como la actividad de unas
enzimas slo rara vez se puede expresar en relacin a su peso absoluto o a la
molaridad de la enzima, lo habitual es expresarla en "unidades" fijadas de modo
convencional con relacin a la protena presente en la preparacin.
La actividad enzimtica se mide por la desaparicin del sustrato o la aparicin de
alguno de los productos de la reaccin, siguiendo dichos cambios en el tiempo.
Sin embargo, las condiciones del sistema no son uniformes a lo largo del tiempo:
el grado de saturacin de la enzima con el sustrato cambia constantemente, los
productos que aparecen suelen inhibir a la enzima o se presentan modificaciones
del pH que afectan a la reaccin, etc. Para evitar estos problemas se hace la
medida de la velocidad inicial, tomando en cuenta solo el comienzo, en forma de
lnea recta de la grfica, lo que sucede en general cuando se ha consumido no
ms de una cuarta parte del sustrato.
La actividad puede expresarse, una vez determinada la reaccin, en relacin con
el tiempo empleado por la enzima para producir un cambio determinado; mientras
mayor sea el tiempo, la actividad de la enzima es menor. Por lo tanto, la recproca
del tiempo (la inversa del tiempo sea el valor que resulta de dividir la unidad
sobre el tiempo, 1/T) es una medida de la actividad enzimtica.
37
BIOQUMICA
ENZIMAS
LAS ENZIMAS SON CATALIZADORES ESTEREOESPECFICOS
Casi todos los sustratos forman por lo menos tres enlaces con las enzimas. Esta
adherencia en tres puntos puede conferir asimetra a una molcula por otro lado
simtrica. La figura * muestra una molcula de sustrato, representada como
un tomo de carbono que tiene tres grupos diferentes, prximos a adherirse en
tres puntos a un sitio de la enzima. Si el sitio puede ser alcanzado slo desde un
lado y nicamente los tomos complementarios y los silios pueden interactuar
(ambos suposiciones vlidas para las enzimas reales), la molcula se unir slo
en una forma. La reaccin misma puede estar confinada a los tomos unidos en
los sitios 1 y 2 an, cuando los tomos 1 y3 sean idnticos. Girando mentalmente
la molcula de sustrato en el espacio, ntese que puede adherirse en tres puntos
a un costado del sitio planear con una sola orientacin. En consecuencia, los
tomos 1 y 3 aunque sean idnticos vienen a ser distintos cuando el sustrato est
adherido a la enzima. Por tanto, un cambio qumico puede afectar el tomo uno
(pero no al tomo tres) o viceversa. Esto puede explicar por qu la reduccin,
catalizada enzimticamente de la molcula del piruvato pticamente inactiva,
forma L- y no D,L-lactato.
ESPECIFICIDAD ENZIMTICA
Los distintos grupos de enzimas muestran variaciones considerables en su grado
de especificidad. Algunas de ellas muestran requerimientos estrictos tanto para el
sustrato (o los sustratos si se trata de reacciones biomoleculares) como para el
tipo de unin qumica sobre el que van a actuar; pequeos cambios en cualquiera
de ellos bastan para inactivar la reaccin; tal es el caso de la mayora de las
enzimas. En otras ocasiones, la deshidrogenasa alcohlica, que funciona con DPN
como coenzima, es absolutamente especfica para el DPN, pero pude actuar
sobre diversos alcoholes aparte del etlico que es su sustrato caracterstico. Asi
mismo, las enterasas, las fosfatasas y ciertas peptidasas a menudo solo son
especficas para el tipo de unin atacada ster, peptdica, etc. y no
requieren estructuras definidas en el sustrato, a ambos lados de la unin. Hay
ejemplo de especificidad doble: la xantina oxidasa, altamente especfica para la
xantina a la que convierte en cido rico, y por otro lado muy activa, pero en forma
inespecfica, al mostrar gran capacidad para mostrar la activacin de gran
variedad de aldehdos.
El requisito de estreo especificidad para los sustratos es muy importante. Las
enzimas que habitualmente atacan a los azcares naturales con configuracin D-,
no lo hacen sobre sus ismeros artificiales L-; las enzimas tan activas en
la naturaleza sobre los aminocidos comunes tipo L- so inactivas para los
38
BIOQUMICA
ENZIMAS
aminocidos artificiales (o muy raros en los organismos vivos) de tipo D-. Esto es
tan absoluto que cuando existen mezclas racmicas de ismeros D- y L-,
un mtodo conveniente de separarlas, es el de dejar que actu sobre ellas una
enzima que degradar exclusivamente a uno de los dos ismeros dejando al otro
intacto.
Cuando el sustrato es simtrico y el producto es asimtrico, la enzima provoca,
especficamente, la formacin de uno solo de los productos asimtricos, aquel
para el que la enzima es activa; tal es el caso de la deshidrogenasa lctica que, al
actuar sobre el cido pirvico (simtrico) produce exclusivamente cido D-lctico y
no cido L-lctico, y el de la deshidrogenasa glutmica que al atacar el cido a -
cetoglutrico produce solo cido L-glutmico:
CH3CH3
| |
C = O HCOH
| |
COOH COOH
cido pirvico cido D-lctico
Existen otras formas de isomerismo geomtrico aparte del isomerismo D-, L-,
susceptibles de ser reconocidas por enzimas. Tal es la situacin de los ismeros
cis trans en que solo uno de los tipos del par es atacado. La fumarasa introduce
una molcula de agua en el cido fumrico trans, pero el ismero cis, o sea el
cido maleico, no es atacado.
H C COOH H C COOH
HOOC C H H C COOH
cido fumrico (trans) cido maleico (cis)
Las enzimas tambin pueden distinguir molculas que desde el punto de vista
estructural, como compuestos qumicos, son idnticas. Por ejemplo, la glicerol
cinasa, por medio de ATP, convierte al glicerol en L-glicerol 3- fosfato, sea
produce su fosforilacin, pero exclusivamente en la posicin 3, hecho que se ha
demostrado con glicerol marcado con C radiactivo, C14, en las dos posiciones
posibles 1 y 3.
Los mismo sucede con el cido ctrico que al ser oxidado y descarboxilado hasta
producir cido a -cetoglutrico adquiere un grupo C=O, en uno de los lados de la
molcula, qumicamente simtrica. Esta capacidad de la enzima para reconocer el
sustrato obedece a que debe tener por lo menos tres grupos qumicos orientados
39
BIOQUMICA
ENZIMAS
en el espacio de tal modo que el sustrato, aunque en apariencia simtrica, solo
puede adaptarse por completo a la enzima en una sola posicin. De todo esto se
desprende por el sustrato a los sustratos necesitan tener un patrn peculiar de
grupos qumicos, especficos para cada enzima particular, de modo que se adapte
perfectamente a su centro activo; mientras mayor y ms complejo sea este
requerimiento mayor ser la especificidad de la enzima.
ISOENZIMAS O ISOZIMAS
Deshidrogenasa Lctica LDH1 (MMMM)
Isozimas o Isoenzimas son protenas
con diferente estructura pero que
catalizan la misma reaccin. Con
frecuencia, las isoenzimas son
oligomeros de diferentes cadenas
peptdicas, y usualmente difieren en
los mecanismos de regulacin y en
las caractersticas cinticas.
Desde el punto de vista fisiolgico,
la existencia de isoenzimas permite
que haya enzimas similares con
diferentes caractersticas,
personalizadas de acuerdo a los
requerimientos especficos del tejido
o a determinadas condiciones metablicas.
Un ejemplo de las ventajas que ofrecen las isoenzimas al permitir un ajuste fino
del metabolismo, en diferentes condiciones metablicas y en diferentes rganos,
es el siguiente:
Glucoquinasa y Hexokinasa son ejemplos tpicos de isoenzimas. De hecho, hay
cuatro Hexoquinasas: I, II, III y IV. Hexokinasa I est presente en todos los tejidos,
y la Hexoquinasa IV, tambin conocida como Glucoquinasa, est presente
principalmente en el hgado, el pncreas y el cerebro.
Ambas enzimas catalizan la fosforilacin de la glucosa:
Glucosa + ATP Glucosa 6 (P) + ADP
40
BIOQUMICA
ENZIMAS
Hexokinasa I tiene un bajo Km y es inhibida por Glucosa 6 (P). Glucokinasa no es
inhibida por Glucosa 6 (P) y tiene un alto Km. Estos dos hechos indican que la
actividad de Glucoquinasa depende de la disponibilidad de substrato y no de la
demanda del producto.
Debido a que la Glucoquinasa no es inhibida por Glucosa 6 (P). En condiciones en
que la concentracin de glucosa es alta, esta enzima continua fosforilando
glucosa, la cual puede ser usada para la sntesis de glucgeno en el hgado.
Adems, debido a que la Glucoquinasa tiene un alto Km, su actividad no
compromete el suministro de glucosa a otros rganos; en otras palabras, ya que la
Glucoquinasa no es inhibida por glucosa 6 (P), si esta enzima tuviera un bajo Km,
continuara convirtiendo glucosa a glucosa 6 (P) en el hgado, haciendo que la
glucosa no estuviera disponible para otros rganos (recuerde que despus de las
comidas, la glucosa llega primero al hgado antes que a los otros rganos, a travs
del sistema porta.)
Debido a que las isoenzimas tienen diferente distribucin tisular, su estudio es un
importante instrumento en la determinacin del dao sufrido por rganos
especficos.
Ejemplos del uso diagnstico de isoenzimas son el estudio de la Lactato
Deshidrogenasa y de la Creatina quinasa
Deshidrogenasa Lctica (LDH)
Esta enzima est formada por la asociacin de cinco cadenas peptdicas de 2
diferentes tipos de monmeros: M y H.
Las variantes encontradas en el ser humano son:
LDH1: M M M (abundante en el corazn, el cerebro y los eritrocitos; alrededor del
33 % de la LDH en el suero humano es de este tipo)
LDH2: M M M H (abundante en el corazn, el cerebro y los eritrocitos; alrededor
del 45 % de la LDH en el suero humano es de este tipo)
LDH3: M M H H (abundante en el cerebro, los riones y los pulmones; constituye
alrededor del 18 % de la LDH en suero humano)
LDH4: M H H H ((abundante en el hgado, musculo esqueltico y el tejido renal;
constituye alrededor del 3 % de la LDH srica)
LDH5: H H H H ((abundante en el tejido heptico, musculo esqueltico y el ileum;
apenas hasta 1 % de la LDH del suero humano es LDH5)
41
BIOQUMICA
ENZIMAS
En el infarto del miocardio, la LDH total en suero aumenta, y debido a que el
musculo cardiaco contiene ms LDH1 que LDH2, el nivel de LDH1 en suero se
hace mayor que el de LDH2 entre 12 y 24 horas despus del infarto, por lo que el
radio LDH1/LDH2 se hace mayor y se mantiene invertido durante varios das.
Se observa un aumento de LDH5 en diversas patologas hepticas como la
cirrosis, hepatitis y otras. Un aumento de LDH5 durante una enfermedad cardiaca
sugiere congestin heptica secundaria.
Creatina Kinasa:
Creatina Kinasa (CK), tambin conocida como Creatina fosfoquinasa (CPK) es
otro ejemplo de isoenzimas cuyo estudio es til para el diagnstico. Hay tres
isoenzimas de CK formadas cada una por la combinacin de diferentes
subunidades:
CK1 (BB) abunda en el cerebro y en la musculatura lisa (esta prcticamente
ausente del suero)
CK2 (MB) abunda en el corazn y aparece en ciertas cantidades en el musculo
esqueltico (prcticamente est ausente del suero)
CK3 (MM) abunda en el musculo esqueltico y el cardiaco y constituye
prcticamente el 100 % de la CK srica.
Creatina Kinasa CK3
Estas isoenzimas pueden diferenciarse en base a su diferente movilidad
electrofortica.
42
BIOQUMICA
ENZIMAS
Los estudios de CK son tiles fundamentalmente en el diagnstico de infarto del
miocardio, donde se constata un aumento de la variante MB, pero tambin puede
usarse para estudiar otras condiciones, como enfermedades y traumas
musculares (MM y MB) y traumas y ciruga del cerebro (BB).
CK2 aparece en el suero dentro de las 6 horas siguientes a un infarto del
miocardio y desaparece despus de 24 a 48 horas. La persistencia de CK2 en
suero indica extensin del infarto a otras reas o el desarrollo de otro infarto.
REGULACIN DE LA ACTIVIDAD ENZIMTICA POR MEDIO DE ISOENZIMAS
Algunos enzimas tienen distinta estructura molecular aunque su funcin biolgica
es similar. Se llamanisozimas o isoenzimas. Estas diferencias de estructura se
traducen en ligeros cambios en sus propiedades, de forma que cada isozima se
adapta perfectamente a la funcin que debe realizar. As, podemos observar la
existencia de isoenzimas en funcin de:
el tipo de tejido: Por ejemplo, el lactato deshidrogenasa presenta isozima
distintos en msculo y corazn.
el compartimento celular donde acta: Por ejemplo, la malato
deshidrogenasa del citoplasma es distinta de la de la mitocondria.
El momento concreto del desarrollo del individuo: Por ejemplo, algunos enzimas
de la glicolisis del feto son diferentes de los mismos enzimas en el adulto.
CINTICA DE LAS REACCIONES ENZIMTICAS
Aunque las leyes generales de la catlisis debieran ser vlidas para las enzimas,
el hecho de que stas sean sustancias complejas, de alto peso molecular, de
tamao coloidal y de composicin difcil de precisar, impide la aplicacin de dichas
leyes de una manera estricta; por ejemplo, su tamao coloidal puede causar
fenmenos de adsorcin o diversas reacciones debidas a sus numerosas cargas
elctricas. No obstante, los factores que afectan la velocidad de la reaccin
enzimtica son los ya sealados a propsito de las reacciones qumicas en
general, como la temperatura y las concentraciones de las sustancias
reaccionantes que, en este caso particular, son la enzima el sustrato. Adems
intervienen el PH medio donde se realiza la reaccin, la presencia de los
productos de la reaccin, y otros factores secundarios como las radiaciones y los
efectos xido reductores.
43
BIOQUMICA
ENZIMAS
CINTICA ENZIMTICA
La cintica enzimtica estudia la velocidad de las reacciones catalizadas por
enzimas. Estos estudios
proporcionan informacin
directa acerca del mecanismo
de la reaccin cataltica y de la
especificad del enzima. La
velocidad de una reaccin
catalizada por un enzima puede
medirse con relativa facilidad,
ya que en muchos casos no es necesario purificar o
aislar el enzima. La medida se realiza siempre en
las condiciones ptimas de pH, temperatura, presencia
de cofactores, etc., y se utilizan concentraciones
saturantes de sustrato. En estas condiciones, la
velocidad de reaccin observada es la velocidad
mxima (V
mx
). La velocidad puede determinarse bien
midiendo la aparicin de los productos o la
desaparicin de los reactivos.
Al seguir la velocidad de aparicin de producto (o de
desaparicin del sustrato) en funcin del tiempo se obtiene la llamada curva de
avance de la reaccin, o simplemente, la cintica de la reaccin. A medida que la
reaccin transcurre, la velocidad de acumulacin del producto va disminuyendo
porque se va consumiendo el sustrato de la reaccin (Figura de la derecha). Para
evitar esta complicacin se procede a medir la velocidad inicial de la reaccin (v
0
).
La velocidad inicial de la reaccin es igual a la pendiente de la curva de avance a
tiempo cero (Figura de la derecha). De esta forma, la medida de v
0
se realiza
antes de que se consuma el 10% del total del sustrato, de forma que
pueda considerarse la [S] como
esencialmente constante a lo largo del
experimento. Adems, en estas
condiciones no es necesario considerar
la reaccin inversa, ya que la cantidad
de producto formada es tan pequea que
la reaccin inversa apenas ocurre. De
esta forma se simplifican enormemente
las ecuaciones de velocidad.
44
BIOQUMICA
ENZIMAS
Para estudiar la cintica enzimtica se mide el efecto de la concentracin inicial de
sustrato sobre la velocidad inicial de la reaccin, manteniendo la cantidad de
enzima constante. Si representamos v
0
frente a [S]
0
obtenemos una grfica como
la de la Figura de la derecha. Cuando [S]
0
es pequea, la velocidad inicial es
directamente proporcional a la concentracin de sustrato, y por tanto, la reaccin
es de primer orden. A altas [S]
0
, el enzima se encuentra saturada por el sustrato, y
la velocidad ya no depende de [S]
0
. En este punto, la reaccin es de orden cero y
la velocidad es mxima (V
max
).
MODELO CINTICO DE MICHAELIS-MENTEN
Los estudios sistemticos del efecto de la concentracin
inicial del sustrato sobre la actividad enzimtica
comenzaron a realizarse a finales del siglo XIX. Ya en
1882 se introdujo el concepto del complejo enzima-
sustrato como intermediario del proceso de catlisis
enzimtica. En 1913, Leonor Michaelis (foto de la
izquierda) y Maud Menten (foto de la derecha)
desarrollaron esta teora y propusieron una ecuacin de
velocidad que explica el comportamiento cintico de los
enzimas.
Para explicar la relacin observada entre la velocidad inicial (v
0
) y la concentracin
inicial de sustrato ([S]
0
) Michaelis y Menten propusieron que las reacciones
catalizadas enzimticamente ocurren en dos etapas: En la primera etapa se forma
el complejo enzima-sustrato y en la segunda, el complejo enzima-sustrato da lugar
a la formacin del producto, liberando el enzima libre:
En este esquema, k
1
, k
2
y k
3
son las constantes cinticas individuales de cada
proceso y tambin reciben el nombre de constantes microscpicas de velocidad.
Segn esto, podemos afirmar que:
v
1
= k
1
[E] [S]
v
2
= k
2
[ES]
45
BIOQUMICA
ENZIMAS
v
3
= k
3
[ES]
Se puede distinguir entre enzima libre (E) y enzima unido al sustrato (ES), de
forma que la concentracin total de enzima, [E
T
], (que es constante a lo largo de la
reaccin) es:
[E
T
] = [E] + [ES]
Como [E] = [ET] - [ES], resulta que: v
1
= k
1
[S]
[E
T
] - k
1
[S] [ES]
Este modelo cintico adopta la hiptesis del
estado estacionario, segn la cual la
concentracin del complejo enzima-sustrato es
pequea y constante a lo largo de la reaccin
(Figura de la derecha). Por tanto, la velocidad de
formacin del complejo enzima-sustrato (v
1
) es
igual a la de su disociacin (v
2
+ v
3
):
v
1
= v
2
+ v
3
Adems, como [ES] es constante, la velocidad de formacin de los productos es
constante:
v = v
3
= k
3
[ES] = constante.
Como v
1
=v
2
+v
3
, podemos decir que:
k
1
[S] [E
T
] - k
1
[S] [ES] = k
2
[ES] + k
3
[ES]
Despejando [ES], queda
Que: , siendo , en donde la expresin
(k
2
+k
3
)/k
1
se ha sustituido por K
M
, o constante de Michaelis-Menten. Este enlace
nos aporta una explicacin sobre las razones que hacen de la K
M
un parmetro
cintico importante.
Por lo tanto, en el estado estacionario, la velocidad de formacin del producto es:
46
BIOQUMICA
ENZIMAS
v = v
3
= k
3
[ES] =
Para cualquier reaccin enzimtica, [E
T
], k
3
y K
M
son constantes. Vamos a
considerar dos casos extremos:
A concentraciones de sustrato pequeas ([S] << K
M
) v = (k
3
[E
T
]/K
M
) [S].
Como los trminos entre parntesis son constantes, pueden englobarse en
una nueva constante, k
obs
, de forma que la expresin queda reducida a: v =
k
obs
[S], con lo cual la reaccin es un proceso cintico de primer orden.
A concentraciones de sustrato elevadas ([S] >> KM), v = k
3
[E
T
]. La
velocidad de reaccin es independiente de la concentracin del sustrato, y
por tanto, la reaccin es un proceso cintico de orden cero. Adems, tanto
k
3
como [E
T
] son constantes, y nos permite definir un nuevo parmetro,
la velocidad mxima de la reaccin (V
mx
): V
max
= k
3
[E
T
], que es la
velocidad que se alcanzara cuando todo el enzima disponible se encuentra
unido al sustrato.
Si introducimos el parmetro V
max
en la ecuacin general de la velocidad, (la
frmula recuadrada anteriormente), obtenemos la expresin ms conocida de la
ecuacin de Michaelis-Menten:
47
BIOQUMICA
ENZIMAS
Hay enzimas que no obedecen la ecuacin
de Michaelis-Menten. Se dice que su
cintica no es Michaeliana. Esto ocurre con
los enzimas alosterico, cuya grfica v frente
a [S] no es una hiprbola, sino una
sigmoide (Figura de la derecha). En
la cintica sigmoidea, pequeas
variaciones en la [S] en una zona crtica
(cercana a la K
M
) se traduce en grandes
variaciones en la velocidad de reaccin.
CLCULO DE LA K
M
Y DE LA V
max
DE UN ENZIMA
La representacin grfica de la ecuacin de
Michaelis-Menten (v
0
frente a [S]
0
) es una
hiprbola (Figura de la izquierda). La V
max
corresponde al valor mximo al que tiende la
curva experimental, y la K
M
corresponde a la
concentracin de sustrato a la cual la velocidad
de la reaccin es la mitad de la V
max
.
Para determinar grficamente los valores
de K
M
y V
max
es ms sencillo utilizar
la representacin doble
recproca (1/v
0
frente a 1/[S]
0
), ya que es
una lnea recta. Esta representacin doble
recproca recibe el nombre
de representacin de Lineweaver-
Burk (Figura de la derecha). Es una recta
en la cual:
La pendiente es K
M
/V
max
48
BIOQUMICA
ENZIMAS
La abscisa en el origen (1/v
0
= 0) es -1/K
M
La ordenada en el origen (1/[S]
0
= 0) es 1/V
max
De esta forma, a partir de los datos experimentales se puede calcular
grficamente, los valores de K
M
y V
max
de un enzima para diversos sustratos.
ACTIVIDAD ENZIMTICA
Se define la unidad de actividad enzimtica (U) como la cantidad de enzima que
cataliza la conversin de 1 mol de sustrato en un minuto. La actividad especfica
es el nmero de unidades de enzima por miligramo de protena (U/mg prot) o por
mililitro de disolucin (U/ml).
Recientemente, el Sistema Internacional de unidades (SI) ha definido la unidad de
actividad enzimtica como la cantidad de enzima que transforma 1 mol de sustrato
por segundo. Esta unidad se llama katal(kat). Como 1 mol son 10
6
moles y 1
minuto son 60 segundos, resulta que 1 katal equivale a 60 x 10
6
U. Esta unidad es
muy grande, de forma que se utilizan frecuentemente los submltiplos como el
microkatal (kat, 10
-6
kat) o el nanokatal (nkat, 10
-9
kat).
Cuando se conoce el peso molecular del enzima puro y el nmero de centros
activos por molcula de enzima, las medidas de actividad enzimtica permiten
calcular el nmero de recambio del enzima, o sea, el nmero de reacciones
elementales que realiza el enzima por cada centro activo y por unidad de tiempo.
RELACIONES ENTRE LA ENZIMA Y EL SUSTRATO.
Es universalmente aceptado, que la enzima, como todo catalizador, participa de
una manera activa en la reaccin. Existen pruebas experimentales de esta
situacin cuando menos para algunos.
Un ejemplo bien conocido es el de la peroxidasa que, en presencia de perxido de
hidrgeno, H2O2, y un aceptor de hidrgeno adecuado, produce la reduccin del
H2O2, La peroxidasa en ausencia de H2O2 muestras unas bandas de absorcin
caractersticas en el espectro visible; cuando se combina con el H2O2, pero sin
que exista el aceptor de los hidrgenos, aparece una nueva distribucin de las
bandas. Si se permite el paso de los hidrgenos a un aceptor, automticamente
desaparecen las bandas nuevas y reaparecen las originales de peroxidasa.
Se acepta corrientemente una hiptesis propuesta por Michaelis para explicar la
actividad enzimtica, sobre la base de la informacin de un compuesto de la
enzima con el sustrato (complejo enzima sustrato), previamente al ataque del
sustrato por la enzima y a la liberacin de los productos de la reaccin.
49
BIOQUMICA
ENZIMAS
El desarrollo matemtico que permiti a Michaelis formular su hiptesis, estuvo
acorde con los datos experimentales obtenidos una vez vencidos los enormes
obstculos de orden tcnico para llevar a cabo la confirmacin de la teora en el
laboratorio.
Si se hace el estudio de la actividad de una enzima en relacin con la
concentracin de sustrato. En ella se registran, en las abscisas, la cantidad
creciente de sustrato y, en las ordenadas, la cantidad de uno de los productos de
la reaccin liberada de un tiempo dado, que expresa, en rigor, la actividad de la
enzima. La curva obtenida es la de una hiprbola rectangular, la cual tiene algunas
propiedades interesantes; por ejemplo, la velocidad lmite o velocidad mxima, es
el valor que trata de alcanzar la curva a medida que se aumenta el sustrato y que,
en la figura, est sealada con la lnea V. Existe un punto, fijado arbitrariamente,
en el que la mitad de la velocidad lmite corresponde a una concentracin
especfica del sustrato; esta concentracin de sustrato se representa
habitualmente como KM, y se denomina constante de Michaelis, valor
caracterstico para un par enzima sustrato y que, por lo tanto, es la
concentracin de sustrato con la cual se alcanza la mitad de la velocidad lmite o
velocidad mxima de la reaccin. Los resultados obtenidos experimentalmente
concuerdan con los derivados de modo matemtico, sobre la hiptesis de
formacin de un complejo enzima sustrato.
La constante de Michaelis, KM, indica en trminos generales, las relaciones de
afinidad entre el sustrato y la enzima; un KM, implica la necesidad de una alta
concentracin de sustrato que, al combinarse con una enzima, produzca la mitad
de la velocidad mxima, o sea, que la afinidad por la enzima y sustrato es pobre;
por el contrario, si la concentracin de sustrato que se requiere para alcanzar la
mitad de la velocidad es muy pequea (KM pequea), quiere decir que el sustrato
tiene una gran afinidad por la enzima.
En ocasiones, la misma enzima puede ser ms afn a un sustrato que a otro; por
ejemplo, la sacarosa es 16 veces ms activa para atacar a la sacarosa que a la
rafinosa. Se conocen con exactitud los valores de KM para muchos sustratos y
enzimas, con los siguientes: la pepsina, actuando sobre albmina, de huevo: KM
de 4.5. Por ciento; la tripsina sobre la casena: KM de 2 por ciento; la amilasa
sobre el almidn en presencia de Cl : KM de 0.4 por ciento; la sacarosa de
levadura, sobre la sacarosa: KM 0.016 a 0.04 M, etc.
La explicacin de la curva hiperblica que implica la formacin del complejo
enzima sustrato parece depender de la existencia fsica, en la enzima, de
determinados sitios donde se absorbe el sustrato para ser activado. Al principio de
la curva se puede aumentar la concentracin del sustrato y la enzima es capaz de
activarlo con toda eficiencia; pero como una vez activado el sustrato se separa en
forma de los productos, y la velocidad con la que stos se separan no es igual a la
velocidad con la que captado el sustrato, y en vista de la cantidad creciente del
50
BIOQUMICA
ENZIMAS
sustrato, la lnea obtenida no es una recta, sino la curva sealada. Cuando la
cantidad de sustrato ha sobrepasado la capacidad fsica de la enzima para
recibirlo y poder transformarlo, la curva alcanza una meseta, lo que significa que la
reaccin prosigue a la misma velocidad, independientemente de la cantidad de
sustrato adicionada. De acuerdo con los trminos ligados a la velocidad de
reaccin, expresados en la pgina 36, se encuentra que, al principio del
experimento, la reaccin depende exclusivamente de la concentracin del sustrato
y se trata de una reaccin de primer orden; al final de ella, cuando hay un exceso
de sustrato, la reaccin es independiente de la cantidad de sustrato y, por lo tanto,
es de orden cero.
Otra caracterstica en relacin con la finalidad de la enzima por el sustrato es la
comprendida en el llamado nmero de recambio, el cual representa los moles de
sustrato atacados por un mol de enzima en una unidad de tiempo determinada,
generalmente un minuto. Este nmero de recambio, en algunas ocasiones, es muy
elevado, como sucede con la catalasa que a 0 C., tiene un nmero de recambio
de 2.5 millones; es decir, un mol de enzima es capaz, en un minuto, de desdoblar
dos y medio millones de moles de H2O2; el citrocomo c, a 38 C, tiene un nmero
de recambio de 1.4 X 10
3
; la carboxilasa a 30 C., da un nmero de recambio de 1
X 10
3
, etc.
Mecanismo Ping Pong
En la transaminacin, la reaccin avanza a travs de los fenmenos alternos de
adicin de sustrato y liberacin de producto.
Iones sustrato
Estos facilitan la fijacin del sustrato y la catlisis por creacin de varias de
complejo de puente constituidos por un enzima, metal y sustrato en la que os
iones metlicos pueden actuar como catalizadores cidos generales o facilitar la
aproximacin de los reactantes.
ANTAGONISMO METABLICO (ANTI METABOLITOS)
Las enzimas pueden ser inhibidas por diversos compuestos, especialmente los
que presentan una estructura parecida al sustrato natural, como expres en el
caso del cido malnico y el cido succnico con respecto a la deshidrogenasa
succnica.
Esta inhibicin se denomina metabolitos las sustancias presentes o producidas en
el curso del metabolismo celular, y antimetabolitos las sustancias parecidas a
aqullos, y que impiden su aprovechamiento y utilizacin; en general, se trata de
sustancias que compiten, a nivel enzimtico, en vista de su parecido estructural,
con los metabolitos naturales.
51
BIOQUMICA
ENZIMAS
Numerosos hongos, actinomicetos, bacterias, etc., producen sustancias que
muestran actividad contra otros microorganismos. Estas sustancias se han
denominado antibiticos y, en principio, se deben considerar como antimetabolitos
que impiden, por razones de competencia, el crecimiento de determinadas formas
microbianas. En medicina ha resultado del mayor inters el aislamiento y la
actividad de los antibiticos, ya que en ciertas condiciones se usan para reprimir el
desarrollo de grmenes patgenos para los seres humanos.
El estudio de los antimetabolitos probablemente se inici al observar que
numerosas bacterias podan crecer en un medio que tuviera sulfanilamida, que
normalmente es un inhibidor de su crecimiento, siempre que se aadieran grandes
cantidades de cido p-aminobenzoico, una vitamina necesaria para
la nutricin celular. En vista del parecido estructural entre las dos molculas, la
sulfanilamida y el cido p-aminobenzoico, se acept que los fenmenos de
inhibicin tenan una base estructural.
Entre los antibiticos, existen algunos de gran utilidad teraputica, como la
penicilina, aislada de diversos hongos Pemicillium ; la estreptomicina, proveniente
de cultivos de Streptomyces griseus, y las tetraciclinas, sustancias que tienen
amplio campo de accin de diversas infecciones producidas por bacterias
grampositivas o gramnegativas. Qumicamente, son sustancias complejas
formadas por distintos grupos: por ejemplo, la estreptomicina contiene
glucosamina, estreptosa y estreptidina. Algunos antibiticos son pptidos, de tipo
bsico, aislados de bacterias, tales como la gramicidina y las tirocidinas. Un
ejemplo peculiar de antibitico producido por el hongo Pemicillium notatum es la
notatina, idntica a la enzima glucosa oxidasa que ataca a la glucosa permitiendo
su conversin a gluconolactona y cido glucnico; es posible que de esta manera
ejerza su accin de antibitico.
Muchos antimetabolitos suelen intervenir de modo especfico a nivel de las
coenzimas o de los grupos prostticos, cuando stos son del tipo de las vitaminas.
Se trata, por lo tanto, en estos casos, de anti vitaminas, muy comunes en las del
grupo B. As, la tiamina modificada en su estructura qumica para formar
piritiamina u oxitiamina, no participa en los procesos de descarboxilacion.
El cido piridn 3 sulfnico impide la accin de la vitamina natural parecida a l, o
cido nicotnico y perturba numerosas reacciones de deshidrogenacin. La
piridoxina es antiorganizada por la desoxipiridoxina y la biotina, de la misma
manera, por la destiobiotina. Se han preparado numerosas sustancias parecidas a
las bases pricas y pirimidnicas con la finalidad de bloquear los sistemas de
formacin de protena, que dependen de la presencia de cidos nucleicos que
contienen dichas bases, en el interior de las clulas; estos trabajos se han
planeado para deprimir la velocidad de desarrollo de clulas cancerosas. Entre las
sustancias obtenidas en fechas recientes se puede sealar el grupo del 5
fluorouracilo, que produce inhibicin tumoral por el siguiente mecanismo, que
52
BIOQUMICA
ENZIMAS
puede ser comn a un gran nmero de sustancias con estas propiedades : en el
tumor falta la enzima que destruye el antimetabolitos, en este caso el 5
fluorouracilo, el cual se vuelve muy agresivo hacia el tumor ya que no es
degradado por l; en cambio, dicha sustancia es menos txica para el tejido
normal que s est en posibilidad de destruirlo.
INHIBICIN ALOSTERICO
De gran importancia en el fenmeno de la actividad enzimtica es el hecho de
que, en las protenas, pueden existir dos (o cuando menos dos) sitios diferentes
desde el punto de vista estereo- especfico y que, adems, estn en lugares
distintos. Uno de estos sitios es el centro activo, donde el sustrato es atacado para
dar origen a los productos de la reaccin y por lo tanto donde reside el aspecto
funcional de la protena. El otro sitio denomina sitio alosterico y en l puede
acomodarse de manera complementaria - pero reversible - alguna sustancia
llamada efector alosterico ; al efectuarse esta unin se produce una alteracin
discreta de la estructura de la protena, la transicin alostrica, que modifica la
actividad biolgica de la protena, porque altera la distancia, las propiedades del
sitio activo.
Es muy importante que el efector alosterico normal no tiene relacin qumica o
metablica alguna con el sustrato de dicha enzima y que su accin tan especfica
se debe a que altera de tal modo la conformacin de la protena que modifica su
centro activo.
El efecto alosterico se ha estudiado de manera especial en bacterias, pero ocurre
tambin en animales superiores. En un principio se reconoci como un efecto
inhibidor que, por su caractersticas, fue denominado "por retro- alimentacin" o
"por producto final. En rigor, en las bacterias, es la regla que el metabolito
formado al final de un camino metablico, resulte un poderoso inhibidor de su
propia sntesis. Parte de la explicacin de este efecto (pg. 535) se debe a que
dicho metabolito inhibe especficamente a una sola enzima localizada en el
camino metablico que forma a dicha sustancia, y de manera curiosa, la enzima
sensible al metabolito final es la primera de este camino metablico.
En un ejemplo de camino A B C D E, siendo E el metabolismo final, ste inhibira a
la primera enzima la que forma B a partir de A. En este captulo en que se estudia
la regulacin metablica se analizan con detalle algunos de estos ejemplos y las
reacciones qumicas individuales afectadas. La inhibicin alostrica demuestra la
alta especializacin de las enzimas que reconocen tanto al sustrato como al
inhibidor, siendo muy especficas para ambos. Como qumicamente el sustrato y el
efector alosterico son muy distintos, se acepta que la unin con la enzima debe
efectuarse en sitios diferentes, lo que ha demostrado con mutantes bacterianas no
53
BIOQUMICA
ENZIMAS
sensibles al efector alosterico. Adems, no hay interaccin directa entre el sustrato
y el inhibidor puesto que los sitios receptores estn muy separados.
Las protenas alostricas pueden corresponder a polmeros, es decir, a molculas
compuestas de sub- unidades idnticas, con ejes de simetra definidos. El hecho
de que se agreguen las subunidades, por una parte, y el que al estar en forma
polimrica adopten diversas situaciones conformaciones, hace susceptibles a la
enzima a los inhibidores, o por el contrario, a recibir (fig. 3-10) al sustrato y llevar a
efecto su accin caracterstica. Ms an, para el caso de la
transcarbamilasa asprtica se ha demostrado que una subunidad se combina con
el sustrato y otra, distinta, con el inhibidor. Estos fenmenos adquieren una
importancia de tipo general, al demostrar que es factible modificar la accin de las
enzimas por cambios en la estructura cuaternaria de las protenas, basadas en la
asociacin y disociacin de subunidades. Algunos ejemplos particulares son los
siguientes: la deshidrogenasa glutmica, con peso molecular de cerca de 1 milln
puede partirse en subunidades de 250 000 por diversos agentes: DPN, ADP,
estrgenos tiroxina y ciertos aminocidos. Otro ejemplo es la carboxilasa de la
acetil coenzima. A, que es activada por la adicin de citrato, el cual cambia el
coeficiente de sedimentacin de la enzima de 18 S a 43 S, o sea la molcula pasa
a forma de polmero activo a partir de monmeros inactivos. Un caso ya clsico es
el de la fosforilasas inactiva que se convierte en activa cuando se fosforila; la
estructura inactiva est formada por 2 unidades y la activa por 4.
ENZIMAS DIGESTIVAS
Las enzimas adoptan una estructura
tridimensional que permite reconocer a
los materiales especficos sobre los que
pueden actuar (sustratos).
Cada una de las transformaciones, que
experimentan los alimentos en nuestro
sistema digestivo est asociada a un
tipo especfico de enzima. Estas
enzimas son las llamadas enzimas
digestivas.
Cada enzima acta sobre un solo tipo de
alimento, como una llave encaja en una
cerradura. Adems, cada tipo de enzima trabaja en unas condiciones muy
concretas de acidez, como se puede ver en el cuadro de abajo.
Ptialina, en la boca, para almidones
54
BIOQUMICA
ENZIMAS
Si no se dan estas condiciones, la enzima no puede actuar, las reacciones
qumicas de los procesos digestivos no se producen adecuadamente y los
alimentos quedan parcialmente digeridos.
LAS ENZIMAS Y LA DIGESTIN
Enzima Acta
sobre
Proporciona Se produce en Condiciones
para que acte
Ptialina Almidones. Mono y
disacridos
La boca (glndulas
salivares)
Medio
moderadamente
alcalino
Amilasa almidones y
azcares
Glucosa El estmago y pncreas Medio
moderadamente
cido
Pepsina protenas Pptidos y
aminocidos
El estmago Medio muy cido
Lipasa grasas cidos grasos
y glicerina
Pncreas e intestino Medio alcalino y
previa accin de
las sales biliares
Lactasa lactosa de
la leche
Glucosa y
galactosa
Intestino (su produccin
disminuye con el
crecimiento)
Medio cido
El proceso normal de digestin de los alimentos, mediante la accin de las
enzimas, da como resultado nutrientes elementales (aminocidos, glucosa, cidos
grasos, etc.) que asimilamos en el intestino y son aprovechados por el organismo.
Sin embargo, cuando las enzimas no pueden actuar o su cantidad es insuficiente,
se producen procesos de fermentacin y putrefaccin en los alimentos a medio
digerir. En este caso, son los fermentos orgnicos y las bacterias intestinales las
encargadas de descomponer los alimentos.
La diferencia es que en lugar de obtener exclusivamente nutrientes elementales,
como en el caso de la digestin propiciada por las enzimas, se producen adems
una gran variedad de productos txicos (indol, escatol, fenol, etc.). Estas
sustancias tambin pasan a la sangre, sobrecargando los sistemas de eliminacin
de txicos del organismo.
55
BIOQUMICA
ENZIMAS
No slo para provocar la digestin
ENZIMAS INTRACELULARES
Otras enzimas actan en el interior de las clulas, transformando los nutrientes
que les llegan a travs de la sangre en otras sustancias, como el cido oxalactico
o el pirvico, que forman parte del metabolismo celular.
Las enzimas intracelulares tambin son los responsables de los procesos de
degradacin celular. En estos procesos se obtienen nutrientes elementales a partir
de los materiales estructurales propios de las clulas cuando el aporte mediante la
dieta se interrumpe (por ejemplo, durante el ayuno), o cuando la clula no puede
utilizar los nutrientes de la sangre (por ejemplo, en la diabetes).
PARTICULARIDADES
Hay enzimas que necesitan la participacin de otros compuestos qumicos no
proteicos, denominados cofactores, para poder actuar realmente como enzimas.
Estos compuestos pueden ser: el grupo prosttico, como por ejemplo el grupo
hemo de la hemoglobina, o una coenzima, como la coenzima A o el fosfato de
piridoxal. A la parte proteica sin el cofactor se le llama apoenzima, y al complejo
enzima-cofactor holoenzima.
Tambin existen enzimas que se sintetizan en forma de un precursor inactivo
llamado proenzima. Cuando se dan las condiciones adecuadas en las que la
enzima debe actuar, se segrega un segundo compuesto que activa la enzima. Por
ejemplo: el tripsingeno segregado por el pncreas activa a la tripsina en el
intestino delgado, el pepsingeno activa a la pepsina en el estmago, etc.
56
BIOQUMICA
ENZIMAS
Las enzimas actan generalmente sobre un sustrato especfico, como la ureasa, o
bien sobre un conjunto de compuestos con un grupo funcional especfico, como la
lipasa o las transaminasas. La parte de la enzima que "encaja" con el sustrato
para activarlo es denominada centro activo, y es el responsable de
la especificidad de la enzima. En algunos casos, compuestos diferentes actan
sobre el mismo sustrato provocando una misma reaccin, por lo que se les
llama isoenzimas.
DIGESTIN, ENZIMAS
Las principales enzimas que intervienen en la dinmica digestiva son las
siguientes:
Principales enzimas digestivas
ENZIMA ORIGEN SUBSTRATO FUNCIN
CATALTICA O
PRODUCTOS
Amilasa salival
Glndulas
salivales
Almidn Hidroliza LOS
enlaces 1,4,
produciendo
dextrinas limitantes,
matotriosa y
maltosa.
Pepsinas
Estmago Protenas y
polipptidos
Rompen los
enlaces peptdicos
adyacentes a los
aminocidos
aromticos
Tripsina
Pncreas exocrino Protena y
polipptidos
Rompen los
enlaces peptdicos
adyacentes a la
arginina o lisina.
Quimotripsinas Pncreas exocrino Protena y
polipptidos
Rompen los
enlaces peptdicos
adyacentes a los
aminocidos
aromticos
Carboxipeptidasa Pncreas exocrino Protena y
polipptidos
Separa los
carboxiaminocidos
terminales
Lipasa pancretica Pncreas exocrino Triglicridos Monogliceridos y
57
BIOQUMICA
ENZIMAS
cidos grasos
Esterasa
pancretica
Pncreas exocrino Esteres de
colesterol
Colesterol
Amilasa pancretica Pncreas exocrino Almidn Igual que la amilasa
salival
Ribonucleasa Pncreas exocrino ARN Nucletidos
Desoxirribonucleasa Pncreas exocrino ADN Nucletidos
Enteropeptidasa Mucosa intestinal Tripsingeno Tripsina
Aminopeptidasas
Mucosa intestinal Polipptidos Separa el
aminocido N-
terminal del pptido
Dipeptidasas Mucosa intestinal Dipptidos Dos aminocidos
Maltasa Mucosa intestinal Maltosa,
maltotriosa
Glucosa
Lactasa Mucosa intestinal Lactosa Galactosa y glucosa
Sacarasa Mucosa intestinal Sacarosa Fructosa y glucosa
Dextrinasa limitante Mucosa intestinal Dextrinas
limitantes
Glucosa
Nucleasa y enzimas
relacionadas
Mucosa intestinal cidos
nucleicos
(ADN y ARN)
Pentosas y bases
pricas y
pirimdicas
Diversas peptidasas Citoplasma de las
clulas de la
mucosa
Di-, tri-, y
tetrapptidos
Aminocidos.
ENZIMAS EN EL DIAGNSTICO CLNICO
Las enzimas plasmticas se pueden clasificar en dos grupos principales.
En primer lugar se encuentra un grupo relativamente pequeo de enzimas que
secretan activamente hacia la sangre ciertos tipos de clulas.
Por ejemplo las clulas hepticas secretan cimgenos (precursores inactivos) de
las enzimas que participan en la coagulacin de la sangre. El segundo grupo est
constituido por gran nmero de especies enzimticas que descargan las clulas
durante su recambio normal. Estas enzimas funcionan casi siempre dentro de la
clula y carecen de utilidad fisiolgica en el plasma. En los individuos sanos las
58
BIOQUMICA
ENZIMAS
concentraciones de estas enzimas son bastante constantes, y representan un
estado sostenido en el que la tasa de descarga desde las clulas lesionadas hacia
el plasma se encuentra equilibrada por una tasa igual de remocin de la enzima
protenica desde el plasma. La presencia de actividad enzimtica elevada en el
plasma puede indicar la lesin tisular que se acompaa de aumento de la
descarga de enzimas intracelulares (fig. 5-20) (nota el plasma es liquido no celular
constituyente de la sangre. Las pruebas de laboratorio de la actividad enzimtica
se efectan ms a menudo con suero que se obtiene mediante configuracin de la
sangre entera despus que ha dejado coagular. El plasma es un lquido
fisiolgico, en tanto que el suero se prepara en laboratorios.)
A. ALTERACIN DE LAS CONCENTRACIONES DE ENZIMAS
PLASMTICAS EN LOS ESTADOS DE ENFERMEDAD.
Muchas enfermedades que producen lesin tisular tiene como
consecuencia aumento de la descarga de enzimas extracelulares
hacia el plasma. Las actividades de muchas de estas enzimas se
identifican de manera sistemtica con finalidad diagnosticas en las
enfermedades de corazn, hgado, musculo, esqueleto y otros
tejidos.
La magnitud de las actividades de una enzima especifica en el
plasma suele guardar correlacin con la extensin de la lesin tisular
de este modo a menudo es til determinar el grado de elementos de
la actividad de una enzima en particular en el plasma para valorar el
pronstico de pacientes.
B. ENZIMAS PLASMATICAS COMO INSTRUMENTOS
DIAGNOSTICOS
Algunas enzimas manifiestan actividades relativamente elevadas
nada ms en uno o unos cuantos tejidos. La presencia de
concentraciones incrementadas de estas enzimas en el plasma
59
BIOQUMICA
ENZIMAS
refleja, en consecuencia lesin del tejido correspondiente. Por
ejemplo, la enzima aminotransferasa de la alanina abunda en el
hgado. La aparicin de concentraciones elevadas de esta enzima en
el plasma indica posible lesin del tejido heptico. Los aumentos de
las concentraciones plasmticas de enzimas que tienen gran
distribucin tisular son indicaciones menos especficas del sitio en
que se encuentran las clulas daadas. Esta falta de especificidad
tisular limita el valor diagnstico de muchas enzimas plasmticas.
C. ISOENZIMAS Y ENFERMEDADES DEL CORAZON.
La mayor parte de las isoenzimas (llamadas tambin Isozimas) son
enzimas que catalizan la misma relacin. Sim embargo no tienen
necesariamente las mismas propiedades fsicas a causa de los
diferencias de la secuencia de aminocidos producida de manera
gentica. Por este motivo, las isoenzimas pueden contener nmeros
diferentes de aminocidos cargados y, por este motivo, se parece
entre s mediante electroforesis. Diferentes rganos contienen a
menudo proporciones caractersticas de isoenzimas distintas. El
patrn de isoenzimas que se encuentra en el plasma puede servir,
por este motivo como medio para identificar el sitio de la lesin
tisular. Por ejemplo, las concentraciones plasmticas de cinasa de la
creatina (CK) y de deshidrogenasa del lactato (LDH) se miden con
frecuencia para ser el diagnstico de infarto del miocardio. Tienen
utilidad particular es difcil interpretar el electrocardiograma, como en
los casos en que han ocurrido crisis previas de enfermedad del
corazn.
1. Estructura cuaternaria de las isoenzimas:
Muchas isoenzimas contienen subunidades diferentes en
diversas combinaciones. Por ejemplo, la cinasa de la creatina
se encuentra como 3 isoenzimas. Cada isoenzima es un
dmero compuesto por dos polipeptidos (denominados
subunidades BiN) enlazados en una de tres
combinaciones:CK1=BB, CK2= MB, y CK3= MM. Cada
isoenzima CK manifiesta una movilidad electrofortica
caracterstica.
2. Diagnstico de infarto del miocardio: el musculo
miocrdico es el nico tejido que contiene ms del 5% de la
actividad total del CK como la isoenzima CK2 (MB). La
aparicin de esta isoenzima hibrida en el plasma es
virtualmente especifica de infarto de miocardio. Despus de
un infarto agudo del miocardio, la isoenzima aparece entre 4 y
60
BIOQUMICA
ENZIMAS
8 horas despus de haberse iniciado el dolor torcico y
alcanza su actividad mxima en cerca de 24 horas (nota: la
actividad de deshidrogenasa del lactato se eleva tambin en
el plasma despus del infarto del miocardio y alcanza una
nivel de 36 a 40 horas despus de iniciarse los sntomas. Las
actividades LDH es, por este motivo de utilidad diagnostica en
los pacientes que ingresan en el hospital ms de 48 horas
despus de haber sufrido infarto, momento en el que la CK2
puede ofrecer resultado equivoco).
3. Marcadores de infarto del miocardio de aparicin ms
reciente: la troponina T y la troponina I son protenas
reguladoras que participan en la contractibilidad miocrdica.
Se descarga en el plasma como reaccin a la lesin cardiaca.
Las troponinas sricas elevadas son factores de prediccin
ms importantes de resultados adversados en los casos de
angina inestable y de infarto del miocardio que la prueba
ordinaria para determinar la CK2. ( PAMELA .C. CHAMPE ,
PhD bioqumica 3
era
edicin pg. 73-74-75)
COLISNESTERASA (esterasa de acetilcolina)
La colinesterasa del suero o plasmtica (CoP) es la inespecfica o
seudocolinesterasa o II frente a la genuina que es la contenida en los hemticos y
en el tejido nervioso. Normalmente de 2 a 4 U.* en unidades internacionales los
valores normales oscilan entre 1.900 y 3.800 Mu/ml.
1. En la miastenia grave, algunos autores registran valores altos.
2. En la miotonia congnita por el contrario cifras subnormales. Ambos
resultados no han podido ser comprobados por otros investigadores.
Disminuye:
1. En las hipoproteinemias e hipoalbuminemias (cirrosis, kala- azar, anemia
perniciosa, etc.). Suele encontrar un descenso del poder colinesterasico del
suero, exacto en los casos debidos a escape colinesterasico del suero,
excepto en los casos debidos a escape renal de la seroalbmina o sea con
albuminuria positiva.
2. Su utilizacin como prueba funcional heptica puede encontrarse en la
sesin correspondiente: la colinesterasa desciende en la insuficiencia
heptica, y su determinacin sirve para observar el pronstico en las
hepatopatas terminales graves. Tambin se utiliza en la monitorizacin de
los trasplantes de hgado.
3. Ciertos insecticidas inciden especficamente la actividad colinesterasica del
suero (insecticidas tipo alkil- fosfato).
61
BIOQUMICA
ENZIMAS
4. Existe una forma congnita de deficiencia de colinesterasa que puede
ocasionar apneas prolongadas por succinilcolina menos usada como
miorrelajantes despus de la anestesia. La colinesterasa baja y permite
identificar a los pacientes sensibles a la succinilcolina.
5. En la anemia perniciosa decrecen tanto la del plasma como la eritrocitaria.
6. En la triquinosis, descensos que pueden durar meses, especialmente los de
la eritrocitaria.
Aumenta:
1. En el sndrome nefrtico aumenta la colinesterasa (Vincent), a pesar de las
perdidas renales de protenas.
2. En los diabticos obesos es frecuente una hipercolinesterasemia.
3. En la esclerosis en placas se ha comprobado disminucin en la
desmielinizacion y aumentos notables en las formas progresivas (jones).
LIPASA EN SANGRE
Normalmente de 0 a 1 U/ml solo se considera claramente patolgicos los
resultados superiores a 2 U. En la tcnica clasificadamente usada, 1U equivale a
1 ml de solucin de N/20 de NaOH necesaria para neutralizar los cidos grasos
liberados en la hidrolisis de aceite de oliva por suero.
1. Aumenta la lipasemia:
a. En las pancreatitis agudas se alcanzan cifras de hasta 10
U/ml. La hiperlipasemia en estos casos perdura mucho ms
que la hiperamilasemia, de forma que normalizada esta puede
el diagnstico tardo confirmarse mediante la comprobacin
de una cifra de lipasa en sangre en la primera o en la segunda
y en ocasiones, hasta en la tercera semana de enfermedad.
b. En algunas pancreopatias crnicas, al revs de lo que sucede
con la amilasemia, se observa un franco aumento de la
lipasemia, especficamente en el cncer de cabeza de
pncreas, dato de gran valor para el diagnstico diferencial
con otras ictericias obstructivas. En los procesos pancreticos
de larga duracin pueden normalizarse la actividad lipoltica
del suero, y entonces esta no se eleva ni siquiera tras la
administracin de secretina y otros estimulantes, combinada
con la inyeccin de morfina para cerrar el esfnter de Oddi
(prueba funcional).
c. En algunas afecciones hepticas- ciertas ictericias
parenquimatosas, cirrosis heptica, as como casos de ulcus
duodenal aunque no de forma constante ni caracterstica,
62
BIOQUMICA
ENZIMAS
indicara una participacin pancretica concomitante o
secundaria.
2. Disminuye la lipasemia
a. Durante el embarazo como variacin fisiolgica, especialmente en
los ltimos meses, con pronta recuperacin despus del parto.
b. En el curso de la tuberculosis y otras enfermedades infecciosas.
c. Frecuentemente en la diabetes sacarina.
d. En el 56 % de casos de pancreatitis crnica. Pero en el 75 % en las
formas con insuficiencia exocronica marcada o despus de larga
evolucin ( Kehl).
LIPOPROTEINLIPASA
Valor normal:
+
-
4.6 umol FFS/ml/hora. Se encuentra disminuida en la aterosclerosis
coronaria (Breier) y coincide con el colesterol alto, HDL-col bajo y triglicridos
elevados.
AMILASA (diastasa) EN SANGRE
Normalmente 70-200 U/100 ml (mtodo Somogyi), equivalentes a 3-10U
Wohlgemuth por mililitro. Actualmente se tiende a expresar en unidades
internacionales, que oscilan en el adulto normal entre 230 y 3.500/100 ml (o sea
20 U/ml).hasta 160 U Ricel/l y 200UI/I con el mtodo nefelomtrico de Coleman.
1. Aumentos de la amilasemia* se observan:
a) En las pancreatitis agudas como hallazgo
caracterstico, excepto en los casos de necrosis
fulminante, que no permiten la elevacin de la
amilasemia. Cuando se produce hiperamilasemia, se
alcanza cifras elevadas que pueden llegar a 3.00 U o
ms, normalizndose a las 48 horas o como mximo a
los 4 o 6 das. Tambin en las pancreatitis secundarias
a hepatitis agudas por virus, lo cual tiene valor para
diagnosticar esta complicacin. Se han descrito
amilasemias por pancreatitis yatrgenas (en
tratamientos con macrlidos: erotromicina,
roxitromicina). Por el contrario las afecciones crnicas
del pncreas no suelen elevar la amilasemia, excepto
en los brotes agudos de una pancreatitis crnica, pero
a veces tambin en los tumores y quistes pancreticos.
b) En el ulcus gstrico penetrante en pncreas. En estos
casos, los aumentos son mucho menores que en la
pancreatitis aguda. En distintos procesos abdominales
63
BIOQUMICA
ENZIMAS
para pancreticos: gastritis, ulcus duodenal perforado,
peritonitis, obstruccin del intestino delgado, etc. Hay
discretas elevaciones de la diastasemia.
c) En los traumatismos pancreticos y en la obstruccin
del conducto pancretico o de la esfnter de Oddi por
litiasis o carcinoma (ampuloma). Hiperamilasemia
transitorias poscolangiopancreatografia.
d) En la parotiditis, sobre todo si es bilateral,
generalmente entre el quinto y sptimo da de
enfermedad. A veces el aumento se exagera por la
participacin pancretica. La litiasis salival con
obstruccin determina tambin hiperamilasemia.
e) En el curso de diversas infecciones-tiroides tifoidea,
tifus exantemtico, paludismo, neumona, sarampin,
meningitis meningococica- se observan a veces
aumentos moderados, posiblemente en relacin con
una afectacin toxica de pncreas.
f) En la insuficiencia renal pueden registrarse aumentos
moderados de la amilasemia cuando esta interceptada
la excrecin urinaria de la diastasa. La fraccin P3 de
la amilasa (isoamilasa P3) es la ms frecuentemente
elevada. En estos casos, la amilasuria es negativa.
g) La simple inyeccin morfina, codena y otros opiceos
puede ocasionar una elevacin, incluso marcada de la
amilasemia en individuos sanos o por lo menos sin
afeccin pancretica, posiblemente a consecuencia de
un espasmo a nivel del esfnter de Oddi(Gross).
h) En la insuficiencia cardiaca con uremia extrarenal y
trastornos electrolticos.
i) En los trastornos del sistema reticuloendotelial con
dficit de catabolismo del enzima.
j) En la macroamilasemia, una alteracin por
polimerizacin o formacin de complejos
macromoleculares con IgG, de origen incierto
(Horstmann). El gran tamao molecular impide el paso
a travs del filtro renal: amilasuria negativa.
k) En el embarazo ectpico.
l) Incluso en neoplasias pulmonares, ovricas o de colon.
2. Disminucin de la amilasemia:
a) En hepatopatas graves.
64
BIOQUMICA
ENZIMAS
b) En algunos casos de diabetes pancretica con esclerosis de la
glndula y en todas las destrucciones masivas del pncreas: por
pancreatitis crnica, fibrosis qustica avanzada, pancreatitis aguda
fulminante.
c) En el mongolismo de modo inconstante.
d) En grandes quemaduras.
e) En casos de insuficiencia cardiaca congestiva con anasarca.
f) A veces en la neumona.
g) En la tirotoxicosis severa.
h) En la toxemia del embarazo
TRIPSINA EN SUERO.
Recientemente se ha descrito una tcnica para la determinacin por RIA en el
suero de la tripsina inmunorreactiva (SIT). Valores normales: 10-57 ng/ml.
1. Se encuentra elevada:
a) En las pancreatitis agudas y en los brotes agudos de las pancreatitis
crnicas.
b) Inconstantemente en casos de coledocolitiasis e incluso en algunas
cirrosis, especialmente alcohlicas.
c) En el 50 % de casos de carcinoma pancretico.
d) Se ha descrito en la pancreatitis urliana (parotiditis) y en algunas
viriasis.
e) En los primeros meses o aos de nios con fibrosis qustica
(mucoviscidosis).
f) En la insuficiencia renal crnica.
2. Disminuye:
a) En la pancreatitis crnica avanzada con insuficiencia exocrina.
b) En el curso ulterior adolescentes y adultos- de la fibrosis qustica
(mucoviscidosis).
FOSFATASA ACIDA DEL SUERO (FAc).
Normalmente comprendida entre 0.5 y 5 U King-Armstrong, o inferior a 1.5 U
Bodansky. En unidades internacionales, la fosfatasa acida total no debe
sobrepasar las 11mU/ml y la prosttica 4mU/ml. Por el mtodo de Bessey-Lowry:
0,10-63 U/ml en el varn y 0,01-0,56 U/ml en la mujer.
El hecho de que las cifras sean sensiblemente iguales en la mujer y en el varn
nos habla a favor de que fisiolgicamente, el origen de esta fosfatasa no sea la
prstata, sino el hgado y bazo probablemente. Puede determinarse la fraccin
prosttica de la fosfatasa acida por la tcnica de Fihman y Lerner, basada en la
inhibicin por en L-tartrato de aquella.
65
BIOQUMICA
ENZIMAS
Patolgicamente:
1. El hallazgo de cifras elevadas de fosfatasa acida suele darse
como un sinnimo de carcinoma de prstata metastatizado
(ya que la fosfatasa acida originada en la prstata es vertida
en el sano directamente al semen y orina, y no a la sangre),
pero tambin los ndulos prostticos malignos, incluso
algunos casos de hipertrofia prosttica benigna o de
prostatitis, pueden hacerlo aunque con valores ms discretos.
Los valores que ya deben indicar sospecha clnica de
metstasis son de 3-5 U Bodansky (5-10 U King- Armstrong) y
son ya totalmente demostrativas las cifras por enzimas de 5
U Bodansky, o de 10 U King-Armstrong.
A veces (en especial en ancianos), a pesar de la existencia de
metstasis de origen prosttico, la cifra de fosfatasa acida no
esta elevada. En casi todos estos casos, tras 5 das de
inyeccin diaria de 25 mg de propionato de testosterona, se
comprueba su elevacin.
A parte este inters diagnstico, el grado de elevacin de
fosfatasa acida y su reduccin o persistencia con el
tratamiento constituyen un ndice pronstico, siendo su
acenso un signo de progresin de la enfermedad.
Conviene sealar que normalmente despus de manipular la
prstata por tacto rectal, puede elevarse la fosfatasemia
durante 24 horas. Se supone que en estos casos la glndula
tiene una estructura celular qustica. Si no aumenta la
fosfatasa su textura es probablemente fibrosa. Tambin puede
elevarse en la reseccin transuretral y en la biopsia.
2. En enfermedades seas de otro origen pueden registrarse
elevaciones de fosfatasa acida: hiperparatiroidismo primario y
metstasis carcinomatosas de diversas procedencias o
linfomatosas, excepcionalmente en el mieloma y en el
granuloma eosinofilo (histiocitos X) si est muy extendido.
Tambin en la enfermedad de paget y en la osteopetrosis, el
Ca urinario es bajo, hay ligeras elevaciones por actividad
osteoclastica (pero es mucho ms alta la F alcalina) y a veces
en la osteodistrofia renal, en la ontognesis imperfecta y en la
ostetis fibrosa qustica.
3. En la enfermedad de Gaucher y en la de Niemann-Pick,
igualmente se comprueban valores altos.
66
BIOQUMICA
ENZIMAS
4. Tambin en la embolia pulmonar y en otras lisis plaquetarias
(trombosis, trombopenia por destruccin, no por aplasia). As
tambin en la hiperplaquetosis (trombositosis y
trombositemia).
5. En hemopatas malignas: leucemias mieloides o linfoides o
crnicas, de clulas peludas, mielomonociticas. Pero tambin
en otras hemopatas: anemia megaloblastica, hemoltica,
policitemia, mononucleosis infecciosa.
FOSFATASA ALCALINA DEL SUERO (FAI O ALP)
La fosfatasa alcalina del suero procede principalmente de los huesos y tambin en
parte del hgado.
Aumenta normalmente la fosfatasemia en los periodos del crecimiento y
reparacin sea.
La cifra media normal de la fosfatasa alcalina es de 1.5 a 5 U Bodansky (4 a 3 U
King-Armstrong). Durante el embarazo aumenta la fosfatasemia hasta valores 3
veces superiores a lo normal al final del primer trimestre, normalizndose a las 6
semanas del parto, aunque puede persistir un ligero aumento durante todo el
periodo de lactancia.
1. Se registran aumentos de la fosfatasemia alcalina, patolgicos en los
siguientes casos:
a) En el hiperparatiroidismo primario donde los valores alcanzados son
superiores, en algunas ocasiones a 50 o 60 U Bodansky.
b) En la ostetis deformante o enfermedad de Paget, donde la fosfatasemia
alcanza valores mximos, hasta 200 U Bodansky.
c) En distintas neoplasis seas: en el carcinoma osteolitico matastasico
inconstantemente y sobre todo en los casos con metstasis hepticas.
d) En el cncer de prstata con metstasis seas, aunque aqu predomina
especialmente la elevacin de la fosfatasa acida.
e) En el mieloma mltiple, solo en algunos casos, casi siempre por
amiloidosis heptica secundaria.
f) En el raquitismo: ligeros aumentos en los casos leves y mucho mayores
-60U Bodansky o ms.
2. Disminucin de la fosfatasemia: ocurre en los siguientes casos:
a) En la hipofosfatasia, enfermedad rara de herencia recesiva, consistente
en un raquitismo congnito por disfermencia familiar. Aqu la fosfatasa
del suero est muy disminuida o ausente totalmente y aumenta la
fosfoetanolamina en la orina.
67
BIOQUMICA
ENZIMAS
b) En el hipotiroidismo infantil, con o sin cretinismo.
c) En el escorbuto excepto en la calcificasion de hemorragias.
d) En la enfermedad celiaca.
e) En la acondroplasia. (Alfonso Balcells 17
ava
edicin la clnica y el
laboratorio pg.124, 125, 126, 127, 128, 129,130-140)
RIBOZIMAS: el ARN como enzima
Las ribozimas son molculas de ARN que tienen la capacidad de actuar como
catalizadores, es decir, de acelerar reacciones qumicas especficas. Al igual que
las enzimas proteicas, poseen un centro activo que se une especficamente a un
sustrato y facilita su conversin en un
producto. Las ribozimas son menos verstiles
que las enzimas proteicas.
Anteriormente las protenas se consideraban
como las nicas macromolculas biolgicas
capaces de funcionar como catalizadores. El
descubrimiento de la actividad cataltica del
ARN ejerci un impacto profundo en el
pensamiento de os bioqumicos. Se han
descubierto algunas enzimas como
componentes del ARN como la telomerasa y
la RNasa P, enzimas que desprenden
nucletidos adicionales de los extremos 5 de
los precursores de tARN. Ms tarde se
demostr que la porcin de ARN RNasa P
tiene actividad catablica. El campo del ARN
cataltico (las ribozimas) se inici con todo
entusiasmo gracias al descubrimiento del
ARN que cataliza su propio autoempalme. Es
fcil entender la conexin entre este proceso
y el empalme del mARN por snRNP. Ms
recientemente se han demostrado que los
ARN pueden catalizar reacciones que
participan en la sntesis proteica. La
eficiencia cataltica de los ARN catalticos es
inferior al de las enzimas proteicas, y la
eficiencia cataltica de los sistemas de ARN que existen en la actualidad mejora
notablemente por la presencia de subunidades proteicas adems del ARN.
Recordemos que muchas coenzimas importantes incluyen una parte de adenosina
fosfato en su estructura. Los compuestos que tienen una importancia tan marcada
68
BIOQUMICA
ENZIMAS
en el metabolismo sin duda son de origen antiguo, otra evidencia que apoya el
concepto de un mundo basado en ARN.
Se sabe que existen varios grupos de ribozimas. En las ribozimas del grupo I hay
un requisito para una guanosina externa, la cual se enlaza covalentemente con el
sitio de empalme en el sitio de la excisin. Un ejemplo es el autoempalme que
tiene lugar en el pre-rARN del protozoario Tetrahymena La transesterificacin (de
esteres del cido fosfrico) que tiene lugar en este caso libera un extremo del
intrn. El extremo 3-OH libre del exn ataca el extremo 5 del otro exn, con lo
que provoca el empalme de ambos exones y libera el intrn. El extremo libre 3-OH
del intron ataca entonces a un nucletido que se encuentra a distancia de 15
residuos del extremo 5, de tal modo que cicliza el intrn y libera la secuencia
terminal 5. La precisin de esta secuencia de reacciones depende de
conformacin de pliegues del ARN, que permanecen con sus puentes de
hidrogeno internos durante el proceso. In vitro, este ARN cataltico puede actuar
muchas veces, y se regenera del modo usual para un catalizador verdadero. Sin
embargo, in vivo, solo parece actuar una vez, pues se autoempalma y deja de
funcionar.
Las ribozimas del grupo II presentan un mecanismo lariat de funcionamiento que
es facilitado por el snRNP. No hay requisito de un nucletido externo; el 2-OH de
una adenosina interna ataca el fosfato en el sitio del empalme 5. Evidentemente,
el ADN no puede actuar al mximo de este modo porque no tiene un grupo OH en
2.
El plegamiento del ARN es crucial para su actividad cataltica como ocurre en los
catalizadores proteicos. Se requiere un divalente (Mg
2+
o Mn
2+
); es muy probable
que los cierres metlicos estabilicen la estructura plegada y neutralicen algunas de
las cargas negativas sobre los grupos fosfato del ARN. Un catin divalente es
fundamental para el funcionamiento de las ribozimas ms pequeas que se
conocen, llamadas de cabeza de martillo, las cuales pueden tener actividad
cataltica con tan solo 43 nucletidos. (El nombre proviene del hecho que sus
estructuras se asemejan a la cabeza de un martillo cuando se muestran en
representaciones convencionales de estructuras secundarias con puentes de
hidrgeno). El plegamiento de ARN es tal que puede efectuarse cambios
conformacionales a gran escala con gran precisin. Se realizan cambios similares
a gran escala en el ribosoma en la sntesis proteica y en el espliceosoma en el
procesamiento ce mARN: observe que an quedan mquinas de ARN cuando las
protenas ya llevan a cabo gran parte del funcionamiento cataltico de las clulas.
La capacidad del ARN para experimentar los cambios conformacionales
necesarios a gran escala quiz desempee algn papel en el proceso. Una
aplicacin clnica recientemente propuesta de los ribosomas ha sido sugerida
69
BIOQUMICA
ENZIMAS
como consecuencia. Si se puede disear un ribosoma que pueda romper el
genoma del ARN del VIH, virus que provoca el SIDA esto constituira un gran
avance en el tratamiento de esta enfermedad. Varios laboratorios realizan
investigaciones sobre el tema.( MARY. K CAMOBELL bioqumica 4
ta
edicin
pg.314-315)
INHIBICIN DE ENZIMAS EN EL TRATAMIENTO DEL SIDA
Una estrategia clave en el tratamiento del sndrome de inmunodeficiencia
adquirida (SIDA) ha sido el desarrollo de inhibidores especficos que bloquean
selectivamente la accin de enzimas exclusivas del virus de inmunodeficiencia
humana (VIH), que causa el SIDA. Muchos laboratorios estn explorando este
enfoque de desarrollo de agentes teraputicos.
Una de las enzimas ms importantes
que se ha escogido como blancos es
la VIH proteasa, una indispensable
para la produccin de nuevas
partculas de virus en las clulas
infectadas. La VIH proteasa solo se
encuentra en este virus, y cataliza el
procesamiento de protenas virales en
la clula infectada. La VIH proteasa,
incluido su sitio activo se determin
mediante cristalografa de rayos X.
con esta estructura en mente, los
cientficos han diseado y sintetizado
compuestos que se unen al sitio
activo. Se mejor el diseo del
medicamento obteniendo las
estructuras de una serie de
inhibidores que se unen al sitio activo
de la VIH proteasa. Dichas estructuras
tambin se determinaron con
cristalografa de rayos X. en ltima
instancia el proceso llevo a varios compuestos que han comercializado diferentes
compaas farmacuticas. Estos inhibidores de VIH proteasa incluyen saquinavir
de Hoffman-LaRoche, ritonavir de Abbot, indinavir de Merck, viracept
Pharmaceuticals. (Estas compaas mantienen pginas bases muy informativas
en la World Wide Web).
70
BIOQUMICA
ENZIMAS
Los tratamientos del SIDA son ms eficaces cuando se usa una combinacin de
terapias medicamentosa s y los inhibidores de la VIH proteasa desempean un
papel importante. Se obtienen resultados especialmente prometedores cuando los
inhibidores de VIH proteasa forman parte de terapias medicamentosas para el
SIDA.
71
BIOQUMICA
ENZIMAS
GLOSARIO
Proenzima: Un zimgeno o proenzima es un precursor enzimtico inactivo,
es decir, no cataliza ninguna reaccin como hacen las enzimas. Para
activarse, necesita de un cambio bioqumico en su estructura que le lleve a
conformar un centro activo donde pueda realizar la catlisis. En ese
momento, el zimgeno pasa a ser una enzima activa. El cambio bioqumico
suele ocurrir en un lisosoma, donde una parte especfica de la enzima
precursora se escinde del resto para activarla. La cadena de
aminocidos que se libera por la activacin se llama pptido de activacin.
Coenzima: Las coenzimas son cofactores orgnicos
no proteicos, termoestables, que unidos a una apoenzima constituyen
la holoenzima o forma catalticamente activa de la enzima. Tienen en
general baja masa molecular (al menos comparada con la apoenzima) y
son claves en el mecanismo de catlisis, por ejemplo, aceptando o
donando electrones o grupos funcionales, que transportan de un enzima a
otro.
A diferencia de las enzimas, las coenzimas se modifican durante la reaccin
qumica; por ejemplo, el NAD
+
se reduce a NADH cuando acepta dos
electrones (y un protn) y por tanto se agota; cuando el NADH libera sus
electrones se recupera el NAD
+
, que de nuevo puede actuar como
coenzima.
Holoenzima: Una holoenzima es una enzima que est formada por
una protena (apoenzima) y un cofactor, que puede ser un ion o
una molcula orgnica compleja unida (grupo prosttico) o no
(una coenzima). En resumidas cuentas, es una enzima completa y activada
catalticamente.
Las apoenzimas son enzimas que carecen de los componentes qumicos
apropiados para realizar la actividad cataltica, por ello, se ayudan de otras
sustancias no proteicas, denominadas cofactores que, fijadas en su
superficie mediante enlaces covalentes o dbiles, le aportan a la enzima
los grupos y funciones qumicas que necesita. En estos casos, la parte
proteica de la enzima de denomina apoenzima y la fraccin no proteica es
el cofactor.
Hemoglobina: La hemoglobina es una heteroprotena de la sangre,
de masa molecular de 64.000 g/mol (64 kDa), de color rojo caracterstico,
que transporta el oxgeno desde los rganos respiratorios hasta los tejidos,
el dixido de carbono desde los tejidos hasta los pulmones que lo eliminan
72
BIOQUMICA
ENZIMAS
y tambin participa en la regulacin de pH de la sangre, en vertebrados y
algunos invertebrados.
La hemoglobina es una protena de estructura cuaternaria, que consta de
cuatro subunidades. Su funcin principal es el transporte de oxgeno. Esta
protena hace parte de la familia de las hemoprotenas, ya que posee un
grupo hemo
Sustrato: un Sustrato es una molcula sobre la que acta una enzima.
Las enzimas catalizan reacciones qumicas que involucran al sustrato o los
sustratos. El sustrato se une al sitio activo de la enzima, y se forma un
complejo enzima-sustrato. El sustrato por accin de la enzima es
transformado en producto y es liberado del sitio activo, quedando libre para
recibir otro sustrato.
Quimotripsina: La Quimotripsina es una enzima digestiva que puede
realizar protelisis. La quimotripsina se sintetiza por biosntesis
proteica como
un precursor denominado quimotripsingeno enzimticamente inactivo. Se
rompe por accin de la tripsina en dos partes que permanecen unidas por
un enlace S-S, y estas molculas de quimotripsingeno pueden activar a
otras eliminando dos pequeos pptidos en una trans-proteolisis.
La molcula resultante es una quimotripsina activa, una molcula
tripeptdica interconectada por enlaces disulfuro.
Apneas: Una apnea es el cese completo de la seal respiratoria (medida
por termistor, cnula nasal o neumotacgrafo) de al menos 10 segundos de
duracin.
Tetrahymena: Los Tetrahymena son un gnero de protozoos ciliados, que
se encuentran naturalmente en aguas dulces. Las especies T. termophila y
T. pyriformis son ampliamente empleadas como modelos de
investigaciones biomdicas
73
BIOQUMICA
ENZIMAS
BIBLIOGRAFIA:
Balcells, A. (1997). LA CLINICA Y LABORATORIO (17 ed., Vol. DECIMOSEPTIMA EDICION).
BARCELONA-MADRID, MADRID, ESPAA: MASSON,S.A. Recuperado el MARTES 3 de
DICIEMBRE de 2013
FARRELL, M. .. (200). BIOQUIMICA cuarta edicion (CUARTA ed., Vol. 4). (S. .O.FARREL,
Trad.) Mexico, MEXICO. Recuperado el JUEVES de DICIEMBRE de 2013
RODWEL. (1969). BIOQUIMICA DE HARPER 13 ava EDICION. s.d. Mexico: Laguna, jose ,
UNAM, Mexico Fournier S.A.
Weil, M. B. (2009). BIOQUIMICA ILUSTRADA (28 ed.). (D. r. muoz, Trad.) MEXICO:
McGRAW-HILL INTERAMERICANA EDITORES.S.A. de C.V. Recuperado el sabado de
noviembre de 2013
http://www.ehu.es/biomoleculas/enzimas/tema11.htm
http://www.diversidadmicrobiana.com/index.php?option=com_content&view=article
&id=453&Itemid=537
http://www.biologia.edu.ar/metabolismo/enzimas.htm
http://www.fbioyf.unr.edu.ar/evirtual/pluginfile.php/5982/mod_resource/content/0/Efec
tos_cooperativos.pdf
http://www.utmachala.edu.ec/bibliotecav/public/buscador/index
http://www.binasss.sa.cr/revistas/rmcc/rmedica/487/art4.pdf
http://medmol.es/glosario/81/
http://www.uned.es/pea-nutricion-y-dietetica-I/guia/guianutr/enzimas.htm.
http://www.profesorenlinea.cl/Ciencias/AlimentaMETABOLISMOyENZIMAS.htm
Das könnte Ihnen auch gefallen
- Taller 1 de Reconocimiento PDFDokument6 SeitenTaller 1 de Reconocimiento PDFJohn Alexander Delgado LeyvaNoch keine Bewertungen
- Normas de Servicio FarmaceuticoDokument63 SeitenNormas de Servicio FarmaceuticoAlejandra Gonzalez De RiveroNoch keine Bewertungen
- Taller 1 de ReconocimientoDokument6 SeitenTaller 1 de ReconocimientoJimmy DelgadoNoch keine Bewertungen
- Fase 2 Informe de Caracterizacion Del Servicio Farmaceutico HospitalarioDokument4 SeitenFase 2 Informe de Caracterizacion Del Servicio Farmaceutico HospitalarioeduinsonNoch keine Bewertungen
- Analisis de VulnerabilidadDokument39 SeitenAnalisis de VulnerabilidadMonik RENoch keine Bewertungen
- PROFESIOGRAMADokument8 SeitenPROFESIOGRAMAFLOR HUERTASNoch keine Bewertungen
- Inspire Oms 2018 PDFDokument308 SeitenInspire Oms 2018 PDFCarolina IllánNoch keine Bewertungen
- Evaluacion de PavimentosDokument58 SeitenEvaluacion de PavimentosAtalayaRimacJudithJeidy100% (1)
- Actividad 6 Desarrollo de Un CuentoDokument4 SeitenActividad 6 Desarrollo de Un CuentorafaelNoch keine Bewertungen
- Teoría Evolutiva de La EmociónDokument1 SeiteTeoría Evolutiva de La Emociónfernanda leonNoch keine Bewertungen
- EcotrashDokument16 SeitenEcotrashCbus Que Deberían MeterNoch keine Bewertungen
- Ensayo El Lider Tranformador 1Dokument6 SeitenEnsayo El Lider Tranformador 1Kassandra Solange Cevallos SánchezNoch keine Bewertungen
- Matriz PeyeaDokument43 SeitenMatriz PeyeaLeidy Marisol BURBANO ARGOTYNoch keine Bewertungen
- Formato ValidacionDokument9 SeitenFormato ValidacionCarmen JimenezNoch keine Bewertungen
- Linea de Tiempo Sobre AMBIENTAL HISTORIADokument7 SeitenLinea de Tiempo Sobre AMBIENTAL HISTORIAMayra Alejandra GelvesNoch keine Bewertungen
- Exercises and TestsDokument23 SeitenExercises and TestsJader Manjarrez MoralesNoch keine Bewertungen
- Taller SG-SSTDokument18 SeitenTaller SG-SSTJames ParkerNoch keine Bewertungen
- Carga FisicaDokument8 SeitenCarga FisicaLina Paola Trujillo VasquezNoch keine Bewertungen
- Tesis "Asociatividad Como Factor Principal en La Productividad de Las Mype Formales de HuancayoDokument72 SeitenTesis "Asociatividad Como Factor Principal en La Productividad de Las Mype Formales de HuancayoBrandwin LmNoch keine Bewertungen
- Actividad - Cuadro Comparativo - Katherine Gaviria PDFDokument6 SeitenActividad - Cuadro Comparativo - Katherine Gaviria PDFkatherine gaviriaNoch keine Bewertungen
- Ensayo Mercado de ValoresDokument1 SeiteEnsayo Mercado de ValoresEsther Elizabeth MorenoNoch keine Bewertungen
- Actividad 1 y 2 GERENCIA PRODUCCIÓN (NRC 9455) Febrero 6 GruposDokument143 SeitenActividad 1 y 2 GERENCIA PRODUCCIÓN (NRC 9455) Febrero 6 GruposWilson Joan CEPEDA MORANoch keine Bewertungen
- Taller Evaluacion Costo de CapitalDokument3 SeitenTaller Evaluacion Costo de CapitalMigdalia MolinaNoch keine Bewertungen
- Economía Social y SolidariaDokument3 SeitenEconomía Social y SolidariaDahiana Charry MartinezNoch keine Bewertungen
- Ensayo Comportamiento de Los Individuos en Las OrganizacionesDokument4 SeitenEnsayo Comportamiento de Los Individuos en Las Organizacionessandra patricia rodriguez vanegasNoch keine Bewertungen
- Casos en Colombia de Justo A Tiempo4Dokument1 SeiteCasos en Colombia de Justo A Tiempo4Zaida ReyesNoch keine Bewertungen
- Proceso para La Creación de Una Organización Social Rev1Dokument2 SeitenProceso para La Creación de Una Organización Social Rev1Christian VeraNoch keine Bewertungen
- Guion AuditoriaDokument9 SeitenGuion AuditoriaJackeline HERNANDEZ CIFUENTES100% (1)
- Matriz MorfologicaDokument1 SeiteMatriz MorfologicaLh MonteroNoch keine Bewertungen
- Tarea 4Dokument11 SeitenTarea 4Sebastian CorreaNoch keine Bewertungen
- 04-02-2019 112407 Am GUÍA DE PRÁCTICAS 2019-I OCLUSIÓNDokument46 Seiten04-02-2019 112407 Am GUÍA DE PRÁCTICAS 2019-I OCLUSIÓNMaria Claudia Leigh BalarezoNoch keine Bewertungen
- Validation BoardDokument2 SeitenValidation BoardcarlosNoch keine Bewertungen
- 1 AlginatosDokument31 Seiten1 AlginatosMiriam EstefaniNoch keine Bewertungen
- Trabajo Final Rse PDFDokument58 SeitenTrabajo Final Rse PDFMARIA CRISTINA LOPEZ VELASQUEZNoch keine Bewertungen
- Ejercicio Propuesto Estudio de Caso Empresarial para El Uso de Matrices InversasDokument6 SeitenEjercicio Propuesto Estudio de Caso Empresarial para El Uso de Matrices InversasGilson CarmonaNoch keine Bewertungen
- Actividad 1 - Introduccion de InvestigacionDokument7 SeitenActividad 1 - Introduccion de InvestigacionMaría Alejandra Serje OlarteNoch keine Bewertungen
- Enzimas y VitaminasDokument98 SeitenEnzimas y VitaminasJersonLimaymantaSalazarNoch keine Bewertungen
- Alternativas y Mécanismos para Resolución de ConflictosDokument1 SeiteAlternativas y Mécanismos para Resolución de ConflictoskarenNoch keine Bewertungen
- MENTEFACTODokument1 SeiteMENTEFACTOmaria angaritaNoch keine Bewertungen
- Proyecto en Empresa 2.0Dokument34 SeitenProyecto en Empresa 2.0chuliNoch keine Bewertungen
- Informe Final de AuditoriaDokument7 SeitenInforme Final de AuditoriaMiguel Angel Zuñiga LlamocaNoch keine Bewertungen
- Infografía 1Dokument1 SeiteInfografía 1Elizabeth ZambranoNoch keine Bewertungen
- Adm. F. Organigrama LilianaDokument5 SeitenAdm. F. Organigrama LilianaFARINCO INGENIERIANoch keine Bewertungen
- Propuesta de ValorDokument2 SeitenPropuesta de ValorRoger AsenciosNoch keine Bewertungen
- Actividad 2.Dokument13 SeitenActividad 2.Valerie Luna HernándezNoch keine Bewertungen
- Ensayo Cop 24Dokument2 SeitenEnsayo Cop 24Sandra Milena Rojas BuendiaNoch keine Bewertungen
- Marco de Referencia Discriminación YukpaDokument5 SeitenMarco de Referencia Discriminación YukpaAnonymous dZHZcqNoch keine Bewertungen
- Higiene. Phva..Dokument15 SeitenHigiene. Phva..Kardasian KatNoch keine Bewertungen
- Infografia FaDokument1 SeiteInfografia Fasilfredo barrios valleNoch keine Bewertungen
- Mentefacto ConceptualDokument4 SeitenMentefacto ConceptualRocio HernandezNoch keine Bewertungen
- Inmunidad Nivel 7Dokument27 SeitenInmunidad Nivel 7vicente figueroaNoch keine Bewertungen
- Etica y Trato Justo en La Administración de Recursos HumanosDokument7 SeitenEtica y Trato Justo en La Administración de Recursos HumanosErnesto RamirezNoch keine Bewertungen
- 105-5 Informe Auditoria-Inspeccion en SDokument3 Seiten105-5 Informe Auditoria-Inspeccion en SINGENEGREANUNoch keine Bewertungen
- Mapa Conceptual Comportamiento OrganizacionalDokument4 SeitenMapa Conceptual Comportamiento OrganizacionalMonica Marcela AArcosNoch keine Bewertungen
- Registro Nacional Desaparecidos 2014 PDFDokument37 SeitenRegistro Nacional Desaparecidos 2014 PDFLinda Mariana PachonNoch keine Bewertungen
- Estrategias Socioeducativas para El Tratamiento DrogasDokument15 SeitenEstrategias Socioeducativas para El Tratamiento Drogaskaweskar1973Noch keine Bewertungen
- ChuchaquiDokument3 SeitenChuchaquiAndres CarvajalNoch keine Bewertungen
- Enzima - Docx INFORMEDokument8 SeitenEnzima - Docx INFORMEMax WellsNoch keine Bewertungen
- ENZIMOLOGIA Trabajo 1Dokument13 SeitenENZIMOLOGIA Trabajo 1Oscar PerezNoch keine Bewertungen
- Inform 12 Intoxicacion Por EstañoDokument11 SeitenInform 12 Intoxicacion Por EstañoJavier JimenezNoch keine Bewertungen
- Para Hacer Los Tripticos de La Hepatitis ADokument2 SeitenPara Hacer Los Tripticos de La Hepatitis AJavier Jimenez100% (2)
- Farmacos AntipaludicosDokument85 SeitenFarmacos AntipaludicosJavier JimenezNoch keine Bewertungen
- Formas Farmacéuticas GasesosasDokument8 SeitenFormas Farmacéuticas GasesosasJavier Jimenez88% (8)
- HaemophilusDokument7 SeitenHaemophilusJavier JimenezNoch keine Bewertungen
- EPOCDokument2 SeitenEPOCJose Luis LeguiaNoch keine Bewertungen
- Trauma AcústicoDokument5 SeitenTrauma AcústicoValeyErickNoch keine Bewertungen
- Razonamiento Verbal TemarioDokument5 SeitenRazonamiento Verbal TemarioDebora Calderon HurtadoNoch keine Bewertungen
- Mozzi, Viviana Alejandra, Rese, Sandr (..) (2014) - Las Toxicomanias Una Aproximacion Posible en El Campo Del PsicoanalisisDokument4 SeitenMozzi, Viviana Alejandra, Rese, Sandr (..) (2014) - Las Toxicomanias Una Aproximacion Posible en El Campo Del PsicoanalisisBusNoch keine Bewertungen
- Clase 1Dokument22 SeitenClase 1Zato IchiNoch keine Bewertungen
- Universidad Nacional Autonoma de Nicaragua Facultad de Ciencias MédicasDokument42 SeitenUniversidad Nacional Autonoma de Nicaragua Facultad de Ciencias MédicasRicardo ZepedaNoch keine Bewertungen
- Qué Es La MenstruaciónDokument2 SeitenQué Es La MenstruaciónNoeldi RamosNoch keine Bewertungen
- Caso Clínico 1Dokument3 SeitenCaso Clínico 1Oscar HernándezNoch keine Bewertungen
- Resumen Problematica Familia Panameña. SCRDokument4 SeitenResumen Problematica Familia Panameña. SCRLaurys Caballero SaldañaNoch keine Bewertungen
- PEC 1 Neuropsicología Del LenguajeDokument8 SeitenPEC 1 Neuropsicología Del LenguajeFernando Rodríguez BogasNoch keine Bewertungen
- Células en Forma de HozDokument8 SeitenCélulas en Forma de HozJorman A Parra ANoch keine Bewertungen
- FLUJOGRAMAS viviENDADokument3 SeitenFLUJOGRAMAS viviENDAJuan Carlos Perez BlancoNoch keine Bewertungen
- Grupo 04. Psicología de La SaludDokument2 SeitenGrupo 04. Psicología de La SaludLuis Pablo Huaman RojasNoch keine Bewertungen
- Un Hospital, Un MundoDokument196 SeitenUn Hospital, Un Mundomarqo_021Noch keine Bewertungen
- Antropólogo en MarteDokument23 SeitenAntropólogo en MarteSmart DomNoch keine Bewertungen
- Espacios ConfinadosDokument5 SeitenEspacios ConfinadosOtero Valdiviezo RonaldNoch keine Bewertungen
- Importancia Del Trabajo en EquipoDokument3 SeitenImportancia Del Trabajo en Equipojose de jesusNoch keine Bewertungen
- Seguridad Ocupacional PDFDokument42 SeitenSeguridad Ocupacional PDFCarlos Alfredo Sierra AlarconNoch keine Bewertungen
- Ensayo de Lo Visto en Toda La Semana de ClasesDokument5 SeitenEnsayo de Lo Visto en Toda La Semana de ClasesLuis TrinidadNoch keine Bewertungen
- Carpeta de Recuperacion 3ero de Primaria Experiencias 3Dokument24 SeitenCarpeta de Recuperacion 3ero de Primaria Experiencias 3Distribuidoras AnaluzNoch keine Bewertungen
- GerminadorDokument5 SeitenGerminadorleida martinezNoch keine Bewertungen
- Bromatología de Las Frutas ExpoDokument25 SeitenBromatología de Las Frutas ExpoOl Keen100% (1)
- Tema 6 Rediseño Del UrbanismoDokument1 SeiteTema 6 Rediseño Del UrbanismoLisbeth Peña SoelNoch keine Bewertungen
- Hoja de Datos de Seguridad Fuel # 6Dokument11 SeitenHoja de Datos de Seguridad Fuel # 6Kenny Jesus Abreu ZarragaNoch keine Bewertungen
- Formato de Solicitud de Ingreso Al Cuerpo Medico Hsai Corta EstancaDokument4 SeitenFormato de Solicitud de Ingreso Al Cuerpo Medico Hsai Corta EstancaAnonymous bU2XQY100% (1)
- Apuntes de LegislacionDokument13 SeitenApuntes de LegislacionCamila De la TorreNoch keine Bewertungen
- Propiedades Del IG4Dokument5 SeitenPropiedades Del IG4bass2008Noch keine Bewertungen
- Parto PrematuroDokument9 SeitenParto PrematuroRusvel Soto MendozaNoch keine Bewertungen
- Teorias de La PersonalidadDokument8 SeitenTeorias de La PersonalidadAlberto2019100% (1)
- Notas Bloc de Notas Sin TítuloDokument5 SeitenNotas Bloc de Notas Sin Títulolaysha ruizNoch keine Bewertungen