Beruflich Dokumente
Kultur Dokumente
Informe 2 Ondas
Hochgeladen von
Joel CoaguilaOriginaltitel
Copyright
Verfügbare Formate
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
Verfügbare Formate
Informe 2 Ondas
Hochgeladen von
Joel CoaguilaCopyright:
Verfügbare Formate
Alumno(s):
Apellidos y Nombres Nota
Coaguila Cosi, Joel Enrique
Profesor:
Muoz Medina, Juan de la Cruz
Programa Profesional:
C-5
Grupo: N1
Fecha de entrega: 01 09
14 Mesa de Trabajo: N1
CURSO: ONDAS Y CALOR
CODIGO: PG1014
LABORATORIO N 02
Calor especifico de los
solidos
1.-INTRODUCCION:
Como estudiantes preocupados por el conocimiento de la fsica hemos elaborado este
informe, donde se presentaran conocimientos referentes a calor especifico, cantidad, de calor
cedido y absorbido, entre otros al igual que su definicin, objetivo, formulas y aplicaciones.
Para llegar a la consecucin de los principales objetivos se tomaron medidas con las
herramientas e instrumentos habilitados en el laboratorio. Luego de ello se precedi a realizar
las respectivas observaciones clculos y confrontacin de resultados. Incluyendo la
determinacin del error porcentual, hasta que por ltimo se llegase a una conclusin de lo
hecho en base a los objetivos planteados en el comienzo de este escrito
2.-OBJETIVOS:
Determinar el calor especfico de un cuerpo slido por el mtodo de las
mezclas.
Ser capaz de configurar e implementar equipos para toma de datos
experimentales y realizar un anlisis grfico utilizando como herramienta el software
PASCO Capston
Utilizar el software Data Studio para verificacin de parmetros estadsticos
respecto a la informacin registrada.
3.-ANALISIS DE TRABAJO SEGURO
Implementos de seguridad de uso obligatorio
LABORATORIO DE ONDAS Y CALOR
GRUPO I
PAGINA 1/
Tabla de Anlisis de Trabajo Seguro (ATS)
N TAREAS RIESGOS IDENTIFICADOS MEDIDAS DE CONTROL DEL
RIESGO
1
Recepcin e inspeccin de
Materiales.
Cada y daos de ruptura de equipos.
Organizar el grupo para una
adecuada recepcin del
Material e instrumento.
2
Toma de corriente al
momento de instalar el
Equipo.
Recibir una descarga elctrica al
momento de conectar la computadora
a la fuente de tensin.
Verificar el buen estado de los cables
antes de realizar el laboratorio.
3
Montaje del laboratorio
Daar algunos de los componentes por
una mala ejecucin.
Prestar atencin a las instrucciones
del profesor tambin se debe tener en
cuenta su correcta instalacin.
4
Trabajando con el sensor de
temperatura.
Ruptura del sensor como tambin
quemar por su mala aplicacin.
Hacer un ajuste seguro a las
Sensor de temperatura con la pinza
universal.
5
Toma de mediciones del
PASCO Capston
Generar mal los clculos.
Hacer los ajustes necesarios
verificando siempre nuestras
guas de trabajo
6
Orden y limpieza
Cadas y tropezones.
Tener la misma actitud para
Culminar el laboratorio.
LABORATORIO DE ONDAS Y CALOR
GRUPO I
PAGINA 1/
ADVERTENCIA
Leer detalladamente el procedimiento y verificar la correcta parametrizacin.
Identificar la polaridad de los conectores utilizados para no provocar sobre corriente o
cortocircuitos.
Antes de energizar el sistema, el profesor del curso debe verificar las conexiones y dar su
visto bueno.
4.-FUNDAMENTO TERICO:
Calor especfico:
El calor especfico (c) de una sustancia, es la cantidad de calor requerido para que un gramo de
dicha sustancia, eleve su temperatura en 1 C.
El calor ganado o perdido por un cuerpo es igual al producto de sus masas, su calor especfico y el
cambio de temperatura.
El mtodo ms comn usado en la determinacin de cambios de calor es el mtodo de las mezclas,
basado en el principio de la conservacin de la energa.
En el cual dos o ms sistemas que tienen temperaturas diferentes son puestos en contacto, de tal
forma que intercambien calor hasta que todos ellos adquieren la misma temperatura
(temperatura de equilibrio).
Como un resultado del intercambio, los cuerpos de ms alta temperatura cedern calor a los cuerpos
de temperatura ms baja, de manera que la cantidad de calor perdido por algunos cuerpos es igual a
la cantidad de calor ganado por los otros.
Un cuerpo de masa M, cuyo calor especifico c se desea determinar es calentado hasta alcanzar una
temperatura T y luego introducido rpidamente a un calormetro de masa
, cuyo calor especifico
el cual contiene en su interior una masa de agua
, todos estos a una temperatura inicia
. La
mezcla alcanzara una temperatura intermedia de equilibrio
.
c =
Que nos determina el calor especfico c del cuerpo. Este es el fundamento del mtodo de las
mezclas. Es necesario observar que este mtodo solo conduce a la determinacin del calor
especfico promedio en un intervalo de temperaturas un poco amplio.
LABORATORIO DE ONDAS Y CALOR
GRUPO I
PAGINA 1/
El calormetro:
El calormetro es un instrumento que sirve para medir las cantidades de calor suministradas o
recibidas por los cuerpos. Es decir, sirve para determinar el calor especfico de un cuerpo, as como
para medir las cantidades de calor que liberan o absorben los cuerpos. El tipo de calormetro de uso
ms extendido consiste en un envase cerrado y perfectamente aislado con agua, un dispositivo para
agitar y un termmetro. Se coloca una fuente de calor en el calormetro, se agita el agua hasta lograr
el equilibrio, y el aumento de temperatura se comprueba con el termmetro. Si se conoce la
capacidad calorfica del calormetro (que tambin puede medirse utilizando una fuente corriente de
calor), la cantidad de energa liberada puede calcularse fcilmente. Cuando la fuente de calor es un
objeto caliente de temperatura conocida, el calor especfico y el calor latente pueden ir midindose
segn se va enfriando el objeto. El calor latente, que no est relacionado con un cambio
de temperatura, es la energa trmica desprendida o absorbida por una sustancia al cambiar de un
estado a otro, como en el caso de lquido a slido o viceversa. Cuando la fuente de calor es una
reaccin qumica, como sucede al quemar un combustible, las sustancias reactivas se colocan en un
envase de acero pesado llamado bomba. Esta bomba se introduce en el calormetro y la reaccin se
provoca por ignicin, con ayuda de una chispa elctrica.
Figura (a). Calormetro
LABORATORIO DE ONDAS Y CALOR
GRUPO I
PAGINA 1/
El equivalente en agua:
Es un trmino frecuentemente en calorimetra. Es la masa de agua que requiere la misma cantidad
de calor para aumentar su temperatura en un grado como el que se requiere para aumentar
la temperatura del cuerpo en un grado. El equivalente del agua es el producto de la masa de un
cuerpo y la capacidad trmica del material del cuerpo.
Cuando un lquido contenido en un calormetro recibe calor (energa) la absorbe, pero tambin la
absorben las paredes del calormetro. Lo mismo sucede cuando pierde energa. Esta intervencin
del calormetro en el proceso se representa por su equivalente en agua: su presencia equivale a
aadir al lquido que contiene los gramos de agua que asignamos a la influencia del calormetro y
que llamamos "equivalente en agua". El "equivalente en agua" viene a ser "la cantidad de agua que
absorbe o desprende el mismo calor que el calormetro".
-D Q
perdido
= + D Q
ganado
5.-MATERIALES:
Figura 1. Computadora personal con programa PASCO Capston
LABORATORIO DE ONDAS Y CALOR
GRUPO I
PAGINA 1/
Figura 2. Interface 850 universal Interface Figura 3. Sensor de temperatura
Figura 4. Balanza Figura 5. Calormetro
Figura 6. Cuerpos metlicos Figura 7. Probeta graduada
LABORATORIO DE ONDAS Y CALOR
GRUPO I
PAGINA 1/
Figura 8. Vaso precipitado de 250ml Figura 9. Pinza universal
Figura 10. Nuez doble (3) Figura 11. Bases (2)
Figura 12. Varillas (3) Figura 13. Fuente de calor
LABORATORIO DE ONDAS Y CALOR
GRUPO I
PAGINA 1/
6.-PROCEDIMIENTO Y RESULTADOS
6.1 Experiencia del calor especifico de solidos
Ingrese el programa PASCO Capston, haga clic sobre el icono crear experimento y seguidamente
reconocer el sensor de temperatura previamente insertado ala interface USB link.
Seguidamente procedemos a configurar dicho sensor, para lo cual hacemos doble clic sobre el icono
CONFIGURACION y lo configuramos para que registre un periodo de muestreo de 10hz en C.
Luego presione el icono del SENSOR DE TEMPERATURA luego seleccione numrico y cambie a
2 cifras despus de la coma decimal, segn datos proporcionados por el fabricante el sensor mide
en el rango de -35 C a 135 C con un paso de 0.01 C.
Una vez calibrado el sensor arrastramos el icono Grafico sobre el icono sensor de temperatura y
seleccionamos la grfica temperatura vs. Tiempo, luego hacemos el montaje de la figura 14.
Figura 14. Primer montaje
Inicie la toma de datos introduciendo 200 ml de agua en el calormetro y oprimiendo el botn
inicio en la barra de configuracin principal de PASCO Capston. Utilice las herramientas
de anlisis del programa para determinar la temperatura inicial T
i
del sistema calormetro,
agitador y agua.
LABORATORIO DE ONDAS Y CALOR
GRUPO I
PAGINA 1/
1.- Al momento de medir la masa de agua que introducir en el matraz cuide de no mojar
la balanza.
Coloque en el vaso de precipitados 200 ml de agua, conjuntamente con el cuerpo y usando el
mechero calintelo hasta que el agua hierva, de esta forma la temperatura T del cuerpo ser la
misma que la del agua hirviendo (100 C aproximadamente).
Oprima el botn inicio en la barra de configuracin principal de PASCO Capston.
2.- Rpida y cuidadosamente introduce el cuerpo dentro del calormetro, agite el
agua con el fin de crear corrientes de conveccin y distribuir el aumento de temperatura a
todo el recipiente.
Utilice las herramientas de anlisis del programa para determinar la temperatura ms alta
registrada. Esta ser la temperatura de equilibrio T
Eq
.
Repita el proceso hasta completar 2 mediciones, con 3 cuerpos metlicos diferentes y
llene las tablas 1 al 3
Datos tericos tiles
c
Al
= 0.2250 cal/g C Aluminio c
Cu
= 0.0931 cal/g C Cobre
c
Fe
= 0.1146 cal/g C Hierro c
Pb
= 0.0320 cal/g C Plomo
c
Cb
= 0.0577 cal/g C Estao
c
Cu.Zn= 0.086 cal/g.C
Bronce
e
TABLA N 1
LABORATORIO DE ONDAS Y CALOR
GRUPO I
PAGINA 1/
Clase de metal usado
Hierro,
Fe
Calor especifico
terico (cal/g C)
0.1146 cal/g C
Medicin 1 2
Capacidad calorfica del
calormetro C
19,35cal/g 19,35cal/g
Masa del cuerpo metlico M
59,6 g 59,6 g
Masa de agua
200 g 200 g
Temperatura inicial del
sistema T
i
19.6 C 25.5 C
Temperatura inicial del cuerpo
caliente T
92,1 C 92,1 C
Temperatura de equilibrio T
Eq
21,8C 27.4 C
Calor especifico experimental
0.1151 cal/g C 0.1081 cal/g C
|
|
Error porcentual
0.43% 5.67%
2.1 MEDICION N1
c =
| |
| 0.43%
Figura 15. Temperatura inicial del cuerpo caliente T
LABORATORIO DE ONDAS Y CALOR
PAGINA
GRUPO I
Figura 16. Temperatura de equilibrio T
Eq
2.2 MEDICION N2
c =
| |
| 5.67%
LABORATORIO DE ONDAS Y CALOR
GRUPO I
PAGINA 1/
TABLA N 2
2.3 MEDICION N1
c =
| |
| 4,30%
LABORATORIO DE ONDAS Y CALOR
GRUPO I
PAGINA 1/
Clase de metal usado
Bronce,
Cu.Zn
Calor especifico
terico (cal/g C)
0.086 cal/g.C
Medicin 1
Capacidad calorfica del
calormetro C
19,35cal/g
Masa del cuerpo metlico M
63,75 g
Masa de agua
200 g
Temperatura inicial del
sistema T
i
19.6 C
Temperatura inicial del cuerpo
caliente T
92,3 C
Temperatura de equilibrio T
Eq
21,3C
Calor especifico experimental
0.0823 cal/g C
|
|
Error porcentual
4,30%
Figura 17. Temperatura inicial del cuerpo caliente T
Figura 18. Temperatura de equilibrio T
Eq
LABORATORIO DE ONDAS Y CALOR
GRUPO I
PAGINA 1/
TABLA N 3
2.4 MEDICION N1
c =
| |
| 1,29%
LABORATORIO DE ONDAS Y CALOR
GRUPO I
PAGINA 1/
Clase de metal usado
Aluminio,
Al
Calor especifico
terico (cal/g C)
0.2250 cal/g.C
Medicin 1
Capacidad calorfica del
calormetro C
19,35cal/g
Masa del cuerpo metlico M 25,86 g
Masa de agua 200 g
Temperatura inicial del
sistema T
i
19.6 C
Temperatura inicial del cuerpo
caliente T
92,2 C
Temperatura de equilibrio T
Eq
21,5C
Calor especifico experimental
0,2279 cal/g C
|
|
Error porcentual
1,29%
Figura 19. Montaje ya armado
Figura 20. Realizando las pruebas Correspondientes
Figura 21. Resultados Finales
LABORATORIO DE ONDAS Y CALOR
GRUPO I
PAGINA 1/
7.-CUESTIONARIO
Sobre la experiencia del calor especifico de slidos
Podras determinar el calor especfico de las muestras usadas en este experimento
enfriando el metal a la temperatura del hielo en vez de calentarlo como se hizo en la
experiencia? Explica
S, porque el slido a temperatura del hielo y el agua no estn a la misma temperatura, por
lo tanto existe un intercambio de temperatura entre los dos materiales, esto ayuda a saber el
calor especfico del slido.
Podras determinar el calor especfico de unas sustancias desconocidas sin necesidad
de hacer uso de una sustancia de referencia como el agua? Explica
S se puede determinar, siempre y cuando sabiendo el calor especfico de la sustancia que
sustituya al agua y que exista una diferencia de temperatura entre los dos materiales.
Si se duplicara el espacio entre las paredes de los recipientes del calormetro Variara
el intercambio de calor?, esplique sus repuestas.
No, porque para que haya un intercambio de temperatura solo tiene que estar presente una
diferencia de temperaturas ms no el rea o volumen del recipiente que los contiene.
Qu viene a ser la energa calorfica absorbida por una sustancia cuando la
temperatura es incrementada ?
Viene a ser la capacidad calorfica que necesita una sustancia para aumentar su
temperatura.
Cunto es el equivalente en agua del calormetro?
Se podra decir que es la capacidad calorfica K = 19,35 cal/g.C
LABORATORIO DE ONDAS Y CALOR
GRUPO I
PAGINA 1/
LABORATORIO DE ONDAS Y CALOR
Qu evidencia dan los resultados de esta experiencia para justificar que el agua tiene
un calor especfico ms alto que el material considerado?
Si la temperatura del rollo de cobre hubiera sido 900
O
C Cul hubiera sido la
temperatura de equilibrio de la mezcla?
Qu porcentaje de error has introducido al depreciar el equivalente en agua del
termmetro? Demuestra tu respuesta.
Cmo podras medir la temperatura de una estrella?
Se puede calcular la temperatura de una estrella, se necesita un avin de reaccin, un
telescopio, detector de calor y un disco de diamante grueso de un papel. El avin vuela tan
alto saliendo de la contaminacin de la atmosfera, el telescopio comienza explorar el cielo
justo antes de enfocarse en la estrella, insertan el disco de diamante en el telescopio , as se
determina la temperatura de una estrella ya que el disco de diamante es muy sensible a los
cambio de temperatura.
Das könnte Ihnen auch gefallen
- Manual Instrucciones CTA Modelos DAn PDFDokument26 SeitenManual Instrucciones CTA Modelos DAn PDFJoel CoaguilaNoch keine Bewertungen
- K434109 - Plano Electrico BM PDFDokument243 SeitenK434109 - Plano Electrico BM PDFJoel CoaguilaNoch keine Bewertungen
- Previo 6Dokument11 SeitenPrevio 6Joel CoaguilaNoch keine Bewertungen
- Introduccion FP1Dokument18 SeitenIntroduccion FP1Joel CoaguilaNoch keine Bewertungen
- Guia 02 Metodos Matematicos: Broncano Torres Juan CarlosDokument5 SeitenGuia 02 Metodos Matematicos: Broncano Torres Juan CarlosJuan Carlos BroncanotorresNoch keine Bewertungen
- Grado 6 Segundo PeriodoDokument9 SeitenGrado 6 Segundo PeriodonelcyNoch keine Bewertungen
- Informe 7 Sistemas DigitalesDokument7 SeitenInforme 7 Sistemas DigitalesEdwin CabreraNoch keine Bewertungen
- Teléfono DescompuestoDokument3 SeitenTeléfono DescompuestoAndrés AsturiasNoch keine Bewertungen
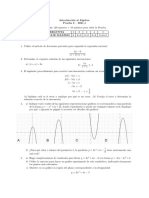
- Intro Algebra Prueba 2 - 2021 - 1Dokument1 SeiteIntro Algebra Prueba 2 - 2021 - 1Javier UrmenetaNoch keine Bewertungen
- E Inferencial3Dokument4 SeitenE Inferencial3Franklin Daniel Carbajal OsisNoch keine Bewertungen
- Organismos Internacionales A Los Que Pertenece VenezuelaDokument5 SeitenOrganismos Internacionales A Los Que Pertenece VenezuelaM̦̻̙i͓͙̝t̡͎̺c͔͜h͙̫͎e̻̘͕l͍̝͇l̡͚͉ S͛aͣlaͣzaͣrͬ100% (1)
- NIVELES de TRANSTEXTUALIDAD Lectoescritura. Trabajo FinalDokument7 SeitenNIVELES de TRANSTEXTUALIDAD Lectoescritura. Trabajo Finaljacqueline bacaNoch keine Bewertungen
- Ejercicio Entregable SemanaDokument9 SeitenEjercicio Entregable SemanaXimena PreciadoNoch keine Bewertungen
- Actividad Probatoria en Fase Administrativa TributariaDokument13 SeitenActividad Probatoria en Fase Administrativa TributariaJaime RodrigoNoch keine Bewertungen
- Arbol ACHSDokument3 SeitenArbol ACHSjaviera paz parra henríquez88% (8)
- Economía FreakDokument3 SeitenEconomía FreakAgustínNoch keine Bewertungen
- ARTI. El Papiro de Turin PDFDokument12 SeitenARTI. El Papiro de Turin PDFAR MagoNoch keine Bewertungen
- Tipos de Respuesta Inflamatoria-Act 2-FisiopatologiaDokument6 SeitenTipos de Respuesta Inflamatoria-Act 2-FisiopatologiaNancy Gocobachi PerezNoch keine Bewertungen
- Solucionario de Calculo 3 de MitaccDokument93 SeitenSolucionario de Calculo 3 de MitaccMoises Apz Qmc50% (2)
- Escala Abreviada de DesarrolloDokument63 SeitenEscala Abreviada de DesarrolloJoaquin Enrique Sepulveda Aravena100% (1)
- Papá y Mamá Se SeparanDokument1 SeitePapá y Mamá Se SeparaninesvictoriaNoch keine Bewertungen
- Física General (Libro Completo) PDFDokument199 SeitenFísica General (Libro Completo) PDFd-fbuser-3219414169% (16)
- Laboratorio 04 Fisica III AñadidoDokument13 SeitenLaboratorio 04 Fisica III AñadidoPedro RosalesNoch keine Bewertungen
- Programa Curricular de Educacion Primaria Parte 1Dokument233 SeitenPrograma Curricular de Educacion Primaria Parte 1Cecoosdes UniNoch keine Bewertungen
- Unidad VII - Fundamentos Filosóficos e Históricos de La EducaciónDokument4 SeitenUnidad VII - Fundamentos Filosóficos e Históricos de La EducaciónDjerico DumayNoch keine Bewertungen
- Capìtulo 9 Schey Procesos de Deformaciòn VolumètricaDokument55 SeitenCapìtulo 9 Schey Procesos de Deformaciòn VolumètricaMiguel Angel López Navarrete100% (1)
- Comparar y Contrastar La Política Exterior de Hitler y Mussolini Hasta El Estallido de La Segunda Guerra MundialDokument1 SeiteComparar y Contrastar La Política Exterior de Hitler y Mussolini Hasta El Estallido de La Segunda Guerra MundialBryan Locotronic Toala100% (1)
- El Principio de Las Activaciones ProfeticasDokument10 SeitenEl Principio de Las Activaciones Profeticaszayd ricardo salek jimenezNoch keine Bewertungen
- Resumen Tercer GradoDokument2 SeitenResumen Tercer GradoMAGM GMNoch keine Bewertungen
- 5) Zapatos de DescargaDokument10 Seiten5) Zapatos de DescargaMai PyonNoch keine Bewertungen
- Tarea 1 Redes de DispositivosDokument3 SeitenTarea 1 Redes de DispositivosLuis Berrezueta100% (1)
- Pauta de Guía de Ejercicios Ingeniería Económica 2014 (I)Dokument11 SeitenPauta de Guía de Ejercicios Ingeniería Económica 2014 (I)MarkTweinNoch keine Bewertungen
- Act 1Dokument4 SeitenAct 1Grisel HernándezNoch keine Bewertungen