Beruflich Dokumente
Kultur Dokumente
Determinacion Gravimetrica de So3 en Yeso
Hochgeladen von
Carlitos Guerra0 Bewertungen0% fanden dieses Dokument nützlich (0 Abstimmungen)
2K Ansichten10 SeitenCopyright
© © All Rights Reserved
Verfügbare Formate
PDF, TXT oder online auf Scribd lesen
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
© All Rights Reserved
Verfügbare Formate
Als PDF, TXT herunterladen oder online auf Scribd lesen
0 Bewertungen0% fanden dieses Dokument nützlich (0 Abstimmungen)
2K Ansichten10 SeitenDeterminacion Gravimetrica de So3 en Yeso
Hochgeladen von
Carlitos GuerraCopyright:
© All Rights Reserved
Verfügbare Formate
Als PDF, TXT herunterladen oder online auf Scribd lesen
Sie sind auf Seite 1von 10
DETERMINACION GRAVIMETRICA DE SO3 EN YESO
Departamento de Qumica, Facultad de Ciencias Exactas y Naturales, Universidad
de Nario.
Realizado 23 de Octubre de 2009; entregado 3 de Noviembre de 2009
RESUMEN
Se determin la cantidad de SO3 presente en una muestra de 0.540g de yeso comercial,
para ello se emple el mtodo de anlisis gravimtrico por precipitacin, donde se utiliz
como disolvente una solucin de HCl 2M y como agente precipitante una solucin de BaCl2
0.5M. El porcentaje de SO3 presente en la muestra se calcul a partir de la masa de BaSO4
obtenida, en ello se encontr que este tuvo un valor de
-------------------------------------------------
Palabras clave: Anlisis gravimtrico por precipitacin, yeso, SO3, BaCl2.
INTRODUCCION
Dentro del anlisis qumico cuantitativo, el cual engloba un conjunto de tcnicas y
procedimientos empleados para determinar y cuantificar la composicin qumica de una
sustancia, es muy importante resaltar los mtodos gravimtricos de anlisis, donde se
determina la cantidad de una sustancia presente en una muestra, eliminando todas las
sustancias que interfieren y convirtiendo el constituyente o componente deseado en un
compuesto de composicin definida, que sea susceptible de pesarse.
Existen cuatro mtodos gravimtricos:
1. Los que se usan reactivos qumicos para la precipitacin.
2. Los que se usan electricidad para la precipitacin (electrogravimetra).
3. Mtodos de volatilizacin.
4. Mtodos de absorcin.
Los ms frecuentes son los que se usan reactivos qumicos para la precipitacin. La
electrogravimetra es de poca utilizacin. Los de volatizacin son muy escasos, pero la
determinacin de agua es factible aunque es un mtodo no selectivo, solo sirve cuando la
nica sustancia voltil es el agua: es un mtodo muy sencillo ya que solo requiere una
pesada antes de volatilizar y otra despus. La absorcin se usa para la determinacin de
CO2 pero por lo dems es poco usada.
Dado a que dentro de la prctica, se utiliz el mtodo gravimtrico por precipitacin, se
enfatiza en su definicin, as:
GRAVIMETRIA POR PRECIPITACION
En este mtodo, el analito se convierte en un precipitado poco soluble, que se filtra, se
purifica, se convierte en un producto de composicin conocida (mediante un tratamiento
trmico), y finalmente se pesa [1].
A continuacin, se enumeran algunas caractersticas a tener en cuenta en cada uno de los
pasos mencionados, as:
La preparacin de la muestra muchas veces no requiere de tratamiento, pero cuando la
mezcla es slida hay que disolverla (por va seca o hmeda).
Adicin del reactivo precipitante
El reactivo se debe aadir lentamente y agitando con el objetivo de obtener cristales
grandes. Siempre se debe aadir un exceso del agente precipitante para disminuir la
solubilidad por la presencia del ion comn.
Filtracin
Se separa el precipitado del resto de la solucin, mediante papel filtro, tambin conocido
como papel gravimtrico.
Lavado
Se realizan varios lavados, para eliminar posibles impurezas presentes en la muestra. Esta
es la fase ms delicada de la gravimetra. El lquido o solucin con el que se hacen los
lavados, no debe ser voltil, no debe aumentar la superficie del precipitado y tampoco debe
transformar el precipitado en coloide que pueda atravesar el papel filtro. Algunas
disoluciones de lavado no voltiles son: agua, disolventes orgnicos, cidos y sales
aninicas y NH3 como nico lcali utilizable. Soluciones que no aumentan la superficie del
precipitado son: el agua y disolventes orgnicos (acetona, etanol y alcoholes de peso
molecular elevado), entre otros.
Calcinacin
Por ltimo, se calcina el analito (es el proceso de calentar una sustancia a temperatura
elevada), por debajo de su entalpa o punto de fusin, para provocar la descomposicin
trmica o de forma general, un cambio de estado en su constitucin fsica o qumica.
Los objetivos de la calcinacin suelen ser:
* Eliminar el agua, presente como humedad absorbida, agua de cristalizacin o agua
de constitucin.
* Eliminar el dixido de carbono, el dixido de azufre u otro compuesto orgnico voltil .
* Para oxidar (calcinacin oxidante) una parte o toda la sustancia (usado comnmente para
convertir menas sulfurosas a xidos en el primer paso de recuperacin de metales como el
zinc, el plomo y el cobre).
* Para reducir (calcinacin reductora) metales a partir de sus menas (fundicin) [2].
Teniendo en cuenta que la determinacin y cuantificacin de SO3 se efectu en una muestra
de yeso, es necesario precisar previamente algunas de sus caractersticas, ya que ello
contribuye al desarrollo del pertinente anlisis, as:
YESO
Es un producto preparado bsicamente a partir de una piedra natural denominada aljez,
mediante deshidratacin, al que puede aadirse en fbrica determinadas adiciones de otras
sustancias qumicas para modificar sus caractersticas de fraguado, resistencia,
adherencia, retencin de agua y densidad. Una vez amasado con agua, puede ser utilizado
directamente. Tambin, se emplea para la elaboracin de materiales prefabricados. El yeso,
como producto industrial, es sulfato de calcio hemihidrato (CaSO4H2O), tambin llamado
vulgarmente "yeso cocido". Se comercializa molido, en forma de polvo. Una variedad de
yeso, denominada alabastro, se utiliza profusamente, por su facilidad de tallado, para
elaborar pequeas vasijas, estatuillas y otros utensilios.
Estado natural
En estado natural el aljez, piedra de yeso o yeso crudo, contiene 32.6% de CaO, 46.5%
SO3 y 20,9% de agua y es considerado una roca sedimentaria, incolora o blanca en estado
puro, sin embargo, generalmente presenta impurezas que le confieren variadas
coloraciones, entre las que se encuentra la arcilla, xido de hierro, slice, caliza, etc.
En la naturaleza se encuentra la anhidrita o karstenita, sulfato clcico, CaSO4, presentando
una estructura compacta y sacaroidea, que absorbe rpidamente el agua, ocasionando un
incremento en su volumen hasta de 30% o 50%, siendo el peso especfico 2,9 y su dureza
es de 2 en la escala de Mohs.
Tambin se puede encontrar en estado natural la basanita, sulfato clcico semihidrato,
CaSO4H2O, aunque raramente, por ser ms inestable.
Usos
Es utilizado profusamente en construccin como pasta para guarnecidos, enlucidos y
revoques; como pasta de agarre y de juntas. Tambin es utilizado para obtener estucados
y en la preparacin de superficies de soporte para la pintura artstica al fresco. Prefabricado,
como paneles de yeso, para tabiques, y escayolados para techos.
Se usa como aislante trmico, pues el yeso es mal conductor de calor y electricidad, para
confeccionar moldes de dentaduras, en odontologa, para usos quirrgicos en forma de
frula para inmovilizar un hueso y facilitar la regeneracin sea en una fractura, en los
moldes utilizados para preparacin y reproduccin de esculturas, en la elaboracin de tizas
para escritura, en la fabricacin de cemento, etc.
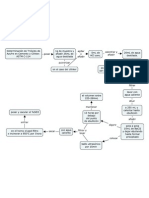
METODOLOGIA
Preparacin de la muestra
Se pes exactamente 0.540g de yeso en un vaso qumico de 400mL, se agreg 50mL de
HCl 2M y se llev a ebullicin. A continuacin, se adicion 100mL de agua caliente y se
continu calentando por 5 minutos ms. Se filtr rpidamente en papel franja negra y se
lav 5 veces con porciones de 5mL de agua caliente, recogiendo el filtrado y las aguas de
lavado en el mismo vaso.
Precipitacin
El filtrado obtenido anteriormente, se calent hasta ebullicin y se agreg lentamente sobre
este, 20mL de BaCl2 0.5M, se agito y se dej reposar por 3 horas aproximadamente.
Posteriormente, se comprob que la precipitacin haya sido completa adicionando una gota
de BaCl2 por las paredes del vaso.
Filtracin
Se filtr convencionalmente el precipitado formado en papel franja azul y se lav 15 veces
con porciones de agua fra hasta la ausencia de cloruros.
Calcinacin
Durante media hora se calcino un crisol de porcelana limpio y seco, en una mufla a 900C,
se dej enfriar y se pes. Posteriormente, sobre el crisol ya preparado, se coloc el
precipitado obtenido anteriormente junto con el papel filtro, se llev a un calentador elctrico
hasta carbonizar el papel, evitando la formacin de llama. Luego, se calcino en una mufla
a 900C durante una hora. Finalmente se dej enfriar en un desecador y se pes.
RESULTADOS Y ANALISIS
En primer lugar, para la determinacin de trixido de azufre presente en la muestra de yeso
industrial, se pes exactamente 0.540g de dicha muestra y se agreg 50mL de HCl 2M. En
este proceso se evidencio la aparicin de una efervescencia que se mantuvo durante los
10 primeros mL de HCl adicionados. Dicha efervescencia se puede explicar teniendo en
cuenta que la muestra de yeso industrial no es completamente pura ya que, en su
fabricacin pueden llevarse a cabo adiciones de otras sustancias qumicas para modificar
sus caractersticas de fraguado, resistencia, adherencia, retencin de agua y densidad, as,
es posible que dentro de su composicin se hayan encontrado carbonatos, que al
reaccionar con el HCl adicionado formaron acido carbnico, cuya descomposicin origino
agua y CO2 gaseoso correspondiente a la efervescencia. As:
CaCO3(s) + 2HCl(ac) CaCl2(ac) + CO2(g) + H2O(l)
Una vez adicionado el HCl, se llev la solucin formada a calentamiento hasta ebullicin,
se agreg 100mL de agua caliente y se continu con el calentamiento a ebullicin por 5
minutos ms. Con este proceso se busc disolver los sulfatos presentes en la muestra como
CaSO4
.
1/2H2O, que es insoluble en agua. As, el HCl cumpli con varias funciones: en
primer lugar, al ser utilizado como disolvente, produjo la disociacin de los iones del
compuesto, rompiendo la red tridimensional que estos formaban en el slido. Por otra parte,
gener el medio acido para obtener un precipitado ms adecuado (de grano grueso, fcil
de filtrar), evito la posible precipitacin de las sales de bario de aniones como CO3
-2
, PO4
-3
o CrO4
-2
, los cuales son insolubles en medio neutro o bsico, y adems evit la
coprecipitacin de Ba(OH)2.
Una vez realizado el anterior procedimiento, se filtr inmediatamente la solucin en papel
filtro franja negra y se lav cinco veces con agua caliente (recogiendo el filtrado y las aguas
de lavado en el mismo beaker), con el objetivo solubilizar totalmente los sulfatos de la
muestra, asegurando su recoleccin cuantitativa en el filtrado, adems de eliminar (o
retener en el papel filtro) las posibles impurezas presentes durante el proceso.
Posteriormente, el filtrado obtenido se calent hasta ebullicin y se agreg cuidadosamente
20mL del reactivo precipitante BaCl2 0.5M (reactivo en exceso); en este procedimiento, la
solucin se torn turbia de color blanco, con la presencia de una suspensin cristalina
temporal; que al dejarla en digestin o en contacto con las aguas madres, por ms de una
hora precipito totalmente. En la digestin el precipitado de BaSO4 pierde el agua dbilmente
adherida y como resultado se obtiene una masa ms densa y pura que se filtra con mayor
facilidad.
Adems, se encontr que la precipitacin del sulfato de bario se ve favorecida por l bajo
grado de la sobresaturacin relativa (generado por la adicin lenta del reactivo precipitante
y la agitacin), donde el proceso de crecimiento de las partculas predomino sobre el
proceso de nucleacin (donde se junta un nmero mnimo de tomos, iones o molculas
para dar una partcula solida estable) permitiendo as, su sedimentacin. Por otra parte, se
encontr que dentro de la precipitacin del analito, pudieron presentarse fenmenos
simultneos como la coprecipitacin (adsorcin en la superficie, formacin de cristales
mixtos, oclusin, atrapamiento mecnico), donde los compuestos que son normalmente
solubles, son separados de la solucin por el precipitado, lo cual puede generar errores en
la medida de la masa final, por lo tanto, para obtener resultados ms exactos y evitar
fenmenos como adsorcin en la superficie, formacin de cristales mixtos, oclusin
atrapamiento mecnico; se tuvo en cuenta aspectos como la cintica del crecimiento del
cristal en la adicin lenta del reactivo precipitante y el medio de reaccin, que al ser acido
evito la formacin de partculas slidas no deseadas.
La ecuacin qumica que representa la reaccin de precipitacin, es la siguiente:
Ca
+2
(ac) + SO4
-2
(ac) + BaCl2(ac) BaSO4(s) + CaCl2(ac)
La Kps (Kps = [Ba
+2
] [SO4
-2
]) del BaSO4 es 1.1x10
-10
lo cual ratifica su baja solubilidad en
agua, donde las fuerzas intermoleculares presentes en el BaSO4 son muy fuertes (alta
energa reticular), razn por la cual se form el precipitado insoluble susceptible de pesar.
De forma general, se puede decir que el precipitado obtenido, se form a partir de tres
etapas fundamentales: nucleacin, crecimiento y envejecimiento.
Durante la etapa de la nucleacin, se produjo la formacin de cristales pequeos, se supone
que el nmero de cristales queda definido en esta etapa. Una vez formados los ncleos, el
material en solucin se deposita en la etapa de crecimiento sobre ellos y no se forman
nuevos ncleos luego de esta etapa. En consecuencia tambin el tamao promedio de las
partculas se definira en esta etapa, grande si se formaron pocos ncleos o pequeo si los
ncleos fueron muchos.
Durante la etapa de crecimiento, el material de la solucin sobresaturada se deposit sobre
los ncleos preexistentes hasta alcanzar cristales de tamao macroscpico; idealmente, en
esta etapa no se formaron nuevos ncleos. El crecimiento de los ncleos es un proceso
complejo: los iones no se depositan al azar sobre la superficie del cristal, deben respetar
las secuencias del retculo. En primer lugar, los iones deben alcanzar la superficie del slido
por difusin desde el seno de la solucin, y luego se irn incorporando ordenadamente al
retculo.
Por ltimo, en la etapa de envejecimiento, el slido recientemente precipitado se deja por
algn tiempo en contacto con la solucin a partir de la cual se obtuvo ("aguas madres"). En
esta etapa, se forman cristales ms grandes y regulares que son ms fcilmente filtrables
y tambin ms puros. El envejecimiento, incluye cambios estructurales de diversos tipos
que sufre un precipitado luego de su formacin [4].
Una vez obtenido BaSO4 slido, se filtr en papel franja azul y se realizaron 15 lavados
hasta la ausencia de cloruros. Los lavados fueron realizados con el objetivo de eliminar las
impurezas presentes en el precipitado; en este caso, el lquido con el que se realizaron los
lavados, fue simplemente agua (la cual no es voltil), por lo que no se afect en el aumento
de la superficie del precipitado y tampoco transformo el precipitado en coloide que pudiera
atravesar el papel filtro.
Para determinar la ausencia de cloruros que pudieron haber interferido en el peso real de
la muestra, a partir del dcimo lavado, se realizaron pruebas con AgNO3, en donde si al
adicionar este reactivo al agua de lavado, se enturbecia (color blanco), se infera la
presencia de cloruros, debido al AgCl formado, Asi:
AgNO3(ac) + HCl(ac) AgCl(s) + HNO3(ac) (4)
Por lo tanto fue necesario determinar la ausencia de estos para que su presencia no
interfiriera con el peso real de la muestra, razn por la cual se continuaron haciendo lavados
hasta que tras la adicin de AgNO3, al lavado, la solucin permaneciera incolora.
Finalmente, se dobl de forma adecuada el papel filtro que contena la muestra y se
introdujo en un crisol (previamente preparado), se llev a un calentador elctrico con el
objetivo de carbonizar el papel filtro. Posteriormente, se llev a calcinacin en una mufla a
900C durante una hora, con lo cual se busc que el precipitado cristalino de BaSO4
eliminara el posible exceso de agua e impurezas presentes en el, adems de adquirir una
composicin definida.
El BaSO4, cuando est puro, se descompone a 1400 C. Puede ser reducido por el carbn
formado por ignicin incorrecta del papel de filtro, as:
BaSO4 + 4C BaS + 4CO
Una vez calcinado el BaSO4, se pes el crisol, que contena la muestra, y a partir de su
masa dada por la diferencia de pesos del crisol vaco y el crisol + muestra, se calcul el
porcentaje de SO3 presente en la muestra de yeso industrial tomada inicialmente, que se
asumi como 100% en CaSO4
.
1/2H2O, debido a que es la correspondiente a una muestra
de yeso industrial que ha sido tratada segn lo reportado en la literatura.
Usos del yeso
Es utilizado profusamente en construccin como pasta para guarnecidos, enlucidos y
revoques; como pasta de agarre y de juntas. Tambin es utilizado para obtener estucados
y en la preparacin de superficies de soporte para la pintura artstica al fresco. Prefabricado,
como paneles de yeso, para tabiques, y escayolados para techos.
Se usa como aislante trmico, pues el yeso es mal conductor de calor y electricidad, para
confeccionar moldes de dentaduras, en odontologa, para usos quirrgicos en forma de
frula para inmovilizar un hueso y facilitar la regeneracin sea en una fractura, en los
moldes utilizados para preparacin y reproduccin de esculturas, en la elaboracin de tizas
para escritura, en la fabricacin de cemento, etc.
ANLISIS CUANTITATIVO
Tabla N1: Datos experimentales
Peso papel filtro | 1.091g |
Peso crisol | 16.905g |
Peso crisol + muestra | 17.439g |
Peso precipitado calcinado | 0.534g |
La ecuacin global que representa la precipitacin del sulfato de bario es la siguiente:
CaSO4
.
2H2O + BaCl2 BaSO4 + CaCl2 + 2H2O
Determinacin de reactivo limitante
Como fue necesario agregar un exceso de BaCl2, se tiene entonces que el reactivo que
limito la reaccin es el CaSO4
.
1/2H2O. Por lo tanto:
Moles de CaSO4
.
1/2H2O que van a reaccionar
0.540g CaSO4
.
2H2O * (1mol CaSO4
.
1/2H2O / 145.2g CaSO4
.
1/2H2O)
= 3.72x10
-3
mol CaSO4
.
1/2H2O
PORCENTAJE TEORICO DE SO3 EN LA MUESTRA DE YESO INDUSTRIAL
0.540g CaSO4
.
1/2H2O * (1mol CaSO4
.
1/2H2O / 145.2g CaSO4
.
1/2H2O)*
(1molBaSO4 / 1molCaSO4
.
1/2H2O) * (233.4g BaSO4 / 1mol BaSO4)
= 0.868g BaSO4
Ahora, para determinar el porcentaje terico de SO3, se sigue la siguiente frmula:
%SO3 = P * FW * 100
En donde:
P = Peso del precipitado calcinado.
F = Factor gravimtrico del BaSO4 a SO3.
W = Peso de la muestra.
Teniendo en cuenta que el factor gravimtrico es la relacin de uno o ms pesos atmicos
(o pesos formula) de una sustancia a uno o ms pesos atmicos (o pesos formula) de otra
sustancia a travs de una sustancia que los relaciona, se tiene que:
Masa molar SO3 / Masa molar BaSO4 = 80.064 / 233.404 = 0.3430
As, el peso del SO3 en el BaSO4 es:
Peso de BaSO4 * Factor gravimetrico
Peso SO3 = 0.534g BaSO4 * 0.3430
Peso SO3 = 0.183g SO3
As:
%SO3 = 0.868g * 0.3430 / 0.540g * 100
%SO3 = 55.16%
PORCENTAJE EXPERIMENTAL DE SO3 EN LA MUESTRA DE YESO INDUSTRIAL
%SO3 = 0.534g * 0.3430 / 0.540g *100
%SO3 = 33.92%
Porcentaje de rendimiento
% de rendimiento = (0.534g BaSO4 / 0.868g BaSO4) * 100%
% de rendimiento = 61.52%
De acuerdo al porcentaje de rendimiento obtenido, se puede concluir que posiblemente, la
muestra de yeso industrial analizada no se encontraba totalmente pura, adems es
probable que se haya presentado perdida de muestra durante todo el proceso de la
obtencin de BaSO4, dando con ello un bajo porcentaje de rendimiento
DEDUCCION DE LA FORMULA PARA CALCULAR EL %SO3 EN LA MUESTRA:
0.534g BaSO4 * 1mol BaSO4 / 233.4g BaSO4 * 1mol SO3 / 1mol BaSO4
* 80.1gSO3 / 1mol SO3 = 0.1833g SO3
Como se sabe que la cantidad inicial tomada de muestra que es 0.540g corresponde al
100%, entonces el %SO3 presente en esta ser de:
0.1833g SO3 / 30.540g CaSO4
.
1/2H2O * 100= 33.92%
CONCLUSIONES
Una vez realizada la prctica se puede concluir que la aplicacin del anlisis gravimtrico,
a pesar de ser desplazado por mtodos volumtricos primero y luego por mtodos
instrumentales, conserva la ventaja de ser un mtodo absoluto, es decir que la
determinacin no necesita de patrones de comparacin. Cabe resaltar adems que el
mtodo gravimtrico ms utilizado es aquel en el cual se utiliza un reactivo precipitante por
medio del cual, precipita una sustancia muy poco soluble la cual est relacionada (directa
o indirectamente) con el compuesto a analizar (analito), en este caso SO3/BaSO4, en donde
para determinar la cantidad de SO3 en la muestra de yeso comercial, se utiliz el factor
gravimtrico entre las dos sustancias.
BIBLIOGRAFIA
[1]: SKOOG D. HOLLER J., Fundamentos de Qumica Analtica. Mc Graw-Hill. Volumen 1.
2001. Capitulo 4. Pp: 70.
[2]: GARCIA M J. COLOM M F. JARAMILLO J. Manual del Auxiliar de Laboratorio.
Temario Ebook. Editorial MAD. Segunda Edicin. 2003. Espaa. Pp: 357-358.
[3]: FLASCHKA H.A., BARNARD, Jr. A. J., STURROCK P. E. Quimica Analitica
Cuantitativa, Introduccin a los Principios. Compaa Editorial Continental, S. A. Primera
Edicin. Volumen 1. 1973. Mxico. Captulo 6. Pp: 75
[4]: MTODOS GRAVIMTRICOS. La Formacin y Propiedades de los Precipitados.
Captulo 12. Pp: 7-1,7-2, 7-3.
Das könnte Ihnen auch gefallen
- Yodometría-Determinación concentración Na2S2O3-hipoclorito sodioDokument8 SeitenYodometría-Determinación concentración Na2S2O3-hipoclorito sodioSthefanía Elizabeth TisalemaNoch keine Bewertungen
- PRÁCTICA Nro 1 Corrección Del Punto de Ebullición en Función de La TemperaturaDokument5 SeitenPRÁCTICA Nro 1 Corrección Del Punto de Ebullición en Función de La TemperaturaBelén TapiaNoch keine Bewertungen
- Sintesis Del Complejo BIS GLICINATO de COBRE (II)Dokument4 SeitenSintesis Del Complejo BIS GLICINATO de COBRE (II)Benyi No la C100% (1)
- Marco Teórico 4 To LABDokument5 SeitenMarco Teórico 4 To LABBruno GonzálezNoch keine Bewertungen
- Cinética de saponificación del acetato de etiloDokument9 SeitenCinética de saponificación del acetato de etiloLeydi Jhoana Garcia CardenasNoch keine Bewertungen
- Informe QuimicaDokument12 SeitenInforme QuimicaAstrid100% (1)
- Informe GravimetriaDokument6 SeitenInforme GravimetriaEyi ChirinosNoch keine Bewertungen
- Informe de Adsorcion 1Dokument4 SeitenInforme de Adsorcion 1vanessa lopezNoch keine Bewertungen
- 7 Infor Obtención P-Nitroacetanilida OrganicaDokument8 Seiten7 Infor Obtención P-Nitroacetanilida OrganicaNonoy ZambranoNoch keine Bewertungen
- Reducción selectiva m-dinitrobenceno m-nitroanilinaDokument2 SeitenReducción selectiva m-dinitrobenceno m-nitroanilinaAlfonso ARNoch keine Bewertungen
- Determinación Gravimétrica de Un Componente (Enviar)Dokument4 SeitenDeterminación Gravimétrica de Un Componente (Enviar)ANDERSON RUBIO CLEVESNoch keine Bewertungen
- Ácido Cinámico FINALDokument8 SeitenÁcido Cinámico FINALAndres Felipe Vargas GaviriaNoch keine Bewertungen
- Síntesis de Tris (Acetilacetonato) de Manganeso (Iii)Dokument5 SeitenSíntesis de Tris (Acetilacetonato) de Manganeso (Iii)roshifernandez0% (1)
- 7 Ir NitrogenadosDokument14 Seiten7 Ir NitrogenadosgodifasNoch keine Bewertungen
- Taller de GravimetriaDokument6 SeitenTaller de Gravimetriamaria martinezNoch keine Bewertungen
- Bromuro de ButiloDokument7 SeitenBromuro de ButiloDiana RodriguezNoch keine Bewertungen
- Informe 7 Preparación de 3-CarbetoxicumarinaDokument11 SeitenInforme 7 Preparación de 3-CarbetoxicumarinaDani SantoyoNoch keine Bewertungen
- Marcha AnalíticaDokument6 SeitenMarcha AnalíticaRodrigo Cori Córdova100% (1)
- Practica 1 Amarillo MartiusDokument7 SeitenPractica 1 Amarillo Martiusjaimeangel100% (1)
- Cinamaldehido 2Dokument6 SeitenCinamaldehido 2Yuli SanchezNoch keine Bewertungen
- Análisis de cationes mediante marchas sistemáticasDokument11 SeitenAnálisis de cationes mediante marchas sistemáticasJuan Pablo Morales TejadaNoch keine Bewertungen
- Analisis Sitematico de Cationes Del Grupo 1Dokument11 SeitenAnalisis Sitematico de Cationes Del Grupo 1Jose Medina Felix50% (2)
- Ácido O-YodobenzoicoDokument4 SeitenÁcido O-YodobenzoicoAna Méndez0% (1)
- Analisis Elemental Cualitativo ValenDokument5 SeitenAnalisis Elemental Cualitativo ValenCatalina Duque HenaoNoch keine Bewertungen
- Electroquimica AvanzDokument79 SeitenElectroquimica AvanzLEONOR100% (1)
- GravimetriaDokument10 SeitenGravimetriaJean Carlo MachucaNoch keine Bewertungen
- Determinación Del Contenido de Hipoclorito Sódico en UnDokument6 SeitenDeterminación Del Contenido de Hipoclorito Sódico en UnLuisa SandovalNoch keine Bewertungen
- Determinación de hierro con método ZimmermannDokument9 SeitenDeterminación de hierro con método ZimmermannStefhania HerranNoch keine Bewertungen
- Analisis de Cationes Del Tercer GrupoDokument7 SeitenAnalisis de Cationes Del Tercer GrupoYessenia AlejoNoch keine Bewertungen
- Experimento 4 Determinación Gravimétrica de NíquelDokument5 SeitenExperimento 4 Determinación Gravimétrica de NíquelBrandon CaballeroNoch keine Bewertungen
- Informe de Quimica Aldheidos y CetonasDokument7 SeitenInforme de Quimica Aldheidos y Cetonassanty barbaNoch keine Bewertungen
- Informe #7 Valoraciones Por Formación de ComplejosDokument5 SeitenInforme #7 Valoraciones Por Formación de ComplejosLinaRodriguez0126Noch keine Bewertungen
- Determinacion de La Curva de Solubilidad FINALDokument10 SeitenDeterminacion de La Curva de Solubilidad FINALmariaNoch keine Bewertungen
- OBTENCIÓN DE BROMURO DE n-BUTILODokument5 SeitenOBTENCIÓN DE BROMURO DE n-BUTILOPau FlurscheimNoch keine Bewertungen
- ComplejosDokument41 SeitenComplejosMartin GonzalezNoch keine Bewertungen
- Condensación AldolicaDokument3 SeitenCondensación AldolicaViridiana AyalaNoch keine Bewertungen
- Bromacion Acetanilida PDFDokument2 SeitenBromacion Acetanilida PDFKaterin LondoñoNoch keine Bewertungen
- Métodos Mohr, Volhard y Volhard ModificadoDokument11 SeitenMétodos Mohr, Volhard y Volhard ModificadoÁvila Velázquez Denisse IvetteNoch keine Bewertungen
- 73541436Dokument62 Seiten73541436alonsoNoch keine Bewertungen
- Obtención de sulfato ferroso heptahidratado: propiedades químicasDokument6 SeitenObtención de sulfato ferroso heptahidratado: propiedades químicasZabala DanielNoch keine Bewertungen
- Principales Propiedades Fisicas Del CO2Dokument6 SeitenPrincipales Propiedades Fisicas Del CO2Maycol Quezada OsorioNoch keine Bewertungen
- 1 Piridinas PDFDokument60 Seiten1 Piridinas PDFManuel Mata100% (2)
- Síntesis de amarillo de Martius a partir de 1-naftolDokument4 SeitenSíntesis de amarillo de Martius a partir de 1-naftolDaniel Maldonado0% (1)
- Sodio y ZincDokument10 SeitenSodio y ZincmartinNoch keine Bewertungen
- Determinacion de Vitamina CDokument6 SeitenDeterminacion de Vitamina CJonat ChNoch keine Bewertungen
- Síntesis pirimidina etoxicarbonil fenil metilDokument7 SeitenSíntesis pirimidina etoxicarbonil fenil metilFernando ValdezNoch keine Bewertungen
- Organometalica 1Dokument19 SeitenOrganometalica 1Kade CadeNoch keine Bewertungen
- Absorción Del Ácido Acético Sobre Carbón VegetalDokument8 SeitenAbsorción Del Ácido Acético Sobre Carbón VegetalAni VazquezNoch keine Bewertungen
- Destilación A Presión ReducidaDokument7 SeitenDestilación A Presión ReducidaAndrupezNoch keine Bewertungen
- Ejercicios ComplementariosDokument7 SeitenEjercicios ComplementariosKaren Grijalva0% (1)
- Determinacion Del Naoh y Na2co3Dokument14 SeitenDeterminacion Del Naoh y Na2co3Carla Flores DiasNoch keine Bewertungen
- Síntesis de aspirina mediante esterificación de ácido salicílico y anhídrido acéticoDokument3 SeitenSíntesis de aspirina mediante esterificación de ácido salicílico y anhídrido acéticoCastañeda Zepeda Héctor AlejandroNoch keine Bewertungen
- Práctica 6: Determinación de Ni en Una Muestra Comercial Por Gravimetría.Dokument18 SeitenPráctica 6: Determinación de Ni en Una Muestra Comercial Por Gravimetría.Enrique DelgadoNoch keine Bewertungen
- Energía libre de Gibbs: determinación experimental de la espontaneidad de la combustión de la maderaDokument5 SeitenEnergía libre de Gibbs: determinación experimental de la espontaneidad de la combustión de la maderaGraciela OrozcoNoch keine Bewertungen
- Informe 1 QIIE Proceso SolvayDokument7 SeitenInforme 1 QIIE Proceso SolvayIgnacio Peña MendezNoch keine Bewertungen
- Titulación yodométrica con almidónDokument3 SeitenTitulación yodométrica con almidónWALTEROGAMEZ - GAMPLAYS DIRECTOS Y MASNoch keine Bewertungen
- Aldehidos y Cetonas, Condensacion AldolicaDokument9 SeitenAldehidos y Cetonas, Condensacion AldolicaLiliana BuenoNoch keine Bewertungen
- Sales de DiazonioDokument4 SeitenSales de DiazonioBooth DeschanelNoch keine Bewertungen
- Determinacion Gravimetrica de So3 en Yeso PDFDokument10 SeitenDeterminacion Gravimetrica de So3 en Yeso PDFJean Pierre Gerónimo FloresNoch keine Bewertungen
- Determinación de la densidad y calidad de calizasDokument4 SeitenDeterminación de la densidad y calidad de calizasMithzy Angulo MejiaNoch keine Bewertungen
- Lock Out Tag Out Dge - Rev01Dokument23 SeitenLock Out Tag Out Dge - Rev01Carlitos GuerraNoch keine Bewertungen
- Riesgos 7561Dokument36 SeitenRiesgos 7561Celene HernándezNoch keine Bewertungen
- Laboratrio Identificación de BiomoléculasDokument8 SeitenLaboratrio Identificación de BiomoléculasCarlitos GuerraNoch keine Bewertungen
- Izaje de Cargas PDFDokument26 SeitenIzaje de Cargas PDFpipeo25Noch keine Bewertungen
- Plan Izaje FormatoDokument5 SeitenPlan Izaje FormatoGabriel100% (2)
- Guantes de Proteccion Individual PDFDokument2 SeitenGuantes de Proteccion Individual PDFArturo Salgado RamírezNoch keine Bewertungen
- Criterios Conocimeiento Desempeno TelehandlerDokument2 SeitenCriterios Conocimeiento Desempeno TelehandlerOso Grizzly0% (1)
- Matriz de RiesgoDokument1 SeiteMatriz de RiesgoCarlitos Guerra100% (1)
- Papaya FTPDokument7 SeitenPapaya FTPCarlitos GuerraNoch keine Bewertungen
- Escalas y CuestionariosDokument36 SeitenEscalas y CuestionariosAlessandro ReyesNoch keine Bewertungen
- FRM-PRJ-12-COMMIS-V1.0 - Verificacion Sistema Inventario Tanques - TemperaturaDokument3 SeitenFRM-PRJ-12-COMMIS-V1.0 - Verificacion Sistema Inventario Tanques - TemperaturaCarlitos GuerraNoch keine Bewertungen
- Metodosdeextraccionypurificaciondealcaloides 140908170606 Phpapp01Dokument9 SeitenMetodosdeextraccionypurificaciondealcaloides 140908170606 Phpapp01Dany CéspedesNoch keine Bewertungen
- Check List GeneradorDokument1 SeiteCheck List GeneradorCarlitos Guerra100% (1)
- Estrés Y Condiciones Laborales en El Trabajo Docente Stress and Work Conditions in TeachingDokument11 SeitenEstrés Y Condiciones Laborales en El Trabajo Docente Stress and Work Conditions in TeachingCarlitos Guerra100% (1)
- FotomultiplicadoresDokument47 SeitenFotomultiplicadoresCarlitos GuerraNoch keine Bewertungen
- Img 490Dokument1 SeiteImg 490Carlitos GuerraNoch keine Bewertungen
- 44 RadonDokument5 Seiten44 RadonCarlitos GuerraNoch keine Bewertungen
- ProgramacionDokument16 SeitenProgramacionCarlitos GuerraNoch keine Bewertungen
- Tema 1 - 2Dokument16 SeitenTema 1 - 2Carlitos GuerraNoch keine Bewertungen
- Robotica AplicadaDokument5 SeitenRobotica AplicadaCarlitos GuerraNoch keine Bewertungen
- Img 480Dokument1 SeiteImg 480Carlitos GuerraNoch keine Bewertungen
- 4253Dokument9 Seiten4253sia1212Noch keine Bewertungen
- ClinkerDokument17 SeitenClinkerCarlitos GuerraNoch keine Bewertungen
- Img 483Dokument1 SeiteImg 483Carlitos GuerraNoch keine Bewertungen
- Img 502Dokument1 SeiteImg 502Carlitos GuerraNoch keine Bewertungen
- SO3 Cemento y ClinkerDokument1 SeiteSO3 Cemento y ClinkerCarlitos GuerraNoch keine Bewertungen
- Objetiv OsDokument2 SeitenObjetiv OsCarlitos GuerraNoch keine Bewertungen
- Lanzador de Proyectiles Del Proyecto de Fisica Ultimo para PresentarDokument8 SeitenLanzador de Proyectiles Del Proyecto de Fisica Ultimo para PresentarCarlitos GuerraNoch keine Bewertungen
- Capas granulares estabilizadasDokument13 SeitenCapas granulares estabilizadasVíctor García García ErasoNoch keine Bewertungen
- Tema 1 - 2Dokument16 SeitenTema 1 - 2Carlitos GuerraNoch keine Bewertungen
- Diseño de Muros de Corte en Edificaciones.Dokument8 SeitenDiseño de Muros de Corte en Edificaciones.Ruben VS100% (2)
- Distribucion de FrecuenciaDokument6 SeitenDistribucion de FrecuenciaTom M NavaNoch keine Bewertungen
- Ejercicios FísicaDokument3 SeitenEjercicios FísicachicanomarceloNoch keine Bewertungen
- Medicion de Las Caracteristicas Estaticas Del Tiristor y Del TriacDokument5 SeitenMedicion de Las Caracteristicas Estaticas Del Tiristor y Del TriacAdrian DiazNoch keine Bewertungen
- Calibracion Presion (TH2)Dokument14 SeitenCalibracion Presion (TH2)Abel CanulNoch keine Bewertungen
- Curso BombasDokument193 SeitenCurso Bombasluis100% (1)
- 100 Herramientas y 5 Equipos Utilizados en El TallerDokument24 Seiten100 Herramientas y 5 Equipos Utilizados en El TallerDr Wrestling71% (14)
- Fundamentos ReologiaDokument65 SeitenFundamentos ReologiaWilliam RoaNoch keine Bewertungen
- PROCEDIMIENTO CompresionDokument6 SeitenPROCEDIMIENTO CompresionalexNoch keine Bewertungen
- Trigonometría y sus aplicaciones en agrimensura, navegación y astronomíaDokument3 SeitenTrigonometría y sus aplicaciones en agrimensura, navegación y astronomíadjemilianoNoch keine Bewertungen
- Norma NNH001Dokument14 SeitenNorma NNH001ManuelNoch keine Bewertungen
- Calculo vectorial: derivadas direccionales y gradienteDokument1 SeiteCalculo vectorial: derivadas direccionales y gradienteLuisNoch keine Bewertungen
- Capitulo 4Dokument19 SeitenCapitulo 4gervin_delgadoingNoch keine Bewertungen
- Rápidas estructuras hidráulicasDokument44 SeitenRápidas estructuras hidráulicasStefany Milagros Rios ChavezNoch keine Bewertungen
- Teoría del todo: la búsqueda de una ecuación para describir el universoDokument2 SeitenTeoría del todo: la búsqueda de una ecuación para describir el universoerramos3100% (1)
- Distribucion Muestral de La MediaDokument5 SeitenDistribucion Muestral de La MediaCarlos ContrerasNoch keine Bewertungen
- Funciones MultivariablesDokument2 SeitenFunciones MultivariablesDaiana Belén Espinoza Arroyo67% (3)
- Procedimiento Diseño GeopresionesDokument28 SeitenProcedimiento Diseño GeopresionesAle VRNoch keine Bewertungen
- Ficha Tecnica Cinchos PlasticosDokument2 SeitenFicha Tecnica Cinchos PlasticosSamuel GarciaNoch keine Bewertungen
- Guia Practica de Cilindrado y Ref Rent AdoDokument4 SeitenGuia Practica de Cilindrado y Ref Rent AdoelrafasaNoch keine Bewertungen
- GUIA 3 DE EJERCICIOS Calculo Aplicado Al Proyecto - 2017 PDFDokument1 SeiteGUIA 3 DE EJERCICIOS Calculo Aplicado Al Proyecto - 2017 PDFcristian astudilloNoch keine Bewertungen
- Química Analítica ExperimentalDokument4 SeitenQuímica Analítica ExperimentalScott Thomas WeilandNoch keine Bewertungen
- Higiene, Inspección y Control de La MielDokument9 SeitenHigiene, Inspección y Control de La MielPacherres Alcántara José E.Noch keine Bewertungen
- Definicion Del ContactorDokument8 SeitenDefinicion Del ContactorJesus Wilder Ala QuirozNoch keine Bewertungen
- Arcos de AceroDokument8 SeitenArcos de AceroAnonymous MMJ4rMCciNoch keine Bewertungen
- Final DarlingtonDokument8 SeitenFinal Darlingtonjhon valdivia vasquezNoch keine Bewertungen
- Lípidos SelectividadDokument7 SeitenLípidos SelectividadClarisa LopezNoch keine Bewertungen
- Contenidos de Unidades 5to SecDokument8 SeitenContenidos de Unidades 5to SecOscar Evangelista FloresNoch keine Bewertungen
- MC A 006 Bomas MultifasicasDokument30 SeitenMC A 006 Bomas MultifasicasMarianna A. 'DzibNoch keine Bewertungen