Beruflich Dokumente
Kultur Dokumente
Infolixipya 140714230204 Phpapp01 PDF
Hochgeladen von
Joel Santiago MelgarOriginaltitel
Copyright
Verfügbare Formate
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
Verfügbare Formate
Infolixipya 140714230204 Phpapp01 PDF
Hochgeladen von
Joel Santiago MelgarCopyright:
Verfügbare Formate
PAULA ANDREA RAMIREZ PEREZ
ANGIE GABRIELA MARTINEZ
LABORATORIO DE HIDRO Y
ELECTROMETALRGIA
28/03/2014
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
1
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
PAULA ANDREA RAMIREZ PEREZ
ANGIE GABRIELA MARTINEZ
PRESENTADO A
M.s.C. METALURGICO JHON FREDDY PALACIOS
UNIVERSIDAD INDUSTRIAL DE SANTANDER
FACULTAD DE INGENIERIAS FISICOQUIMICAS
INGENIERIA METALURGICA Y CIENCIA DE MATERIALES
LABORATORIO DE HIDRO Y ELECTROMETALRGIA
BUCARAMANGA
2014
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
2
OBJETIVOS
GENERAL
Afianzar conocimientos sobre el proceso de lixiviacin de un mineral de cobre, por
agitacin y percolacin a nivel de laboratorio.
ESPECFICOS
Interpretar los resultados experimentales para evaluar el efecto de algunas variables
sobre la eficiencia y cintica del proceso.
Medir la eficiencia mediante el clculo de la disolucin del cobre y del consumo de
cido.
Comparar los procesos de lixiviacin por percolacin y agitacin y determinar el ms
viable a nivel tanto tcnico como econmico.
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
3
MARCO TEORICO
1. LIXIVIACIN DE MINERALES
Etapa de disolucin selectiva de los metales presentes en las especies mineralogas de
cualquier naturaleza, desde los slidos que las contienen, mediante una solucin disolvente
acuosa. Para llevar a cabo un proceso de lixiviacin es necesario tener en cuenta los
siguientes pasos:
Muchos factores alteran la lixiviacin, por lo tanto se debe tener en cuenta que todos los
tipos de menas tienen su propio modo de disolucin. La influencia de la ganga sobre el
proceso de lixiviacin de minerales como por ejemplo de cobre, puede manifestarse
principalmente a travs del consumo de cido, de la cintica de disolucin y del grado de
penetracin de las partculas.
Como la lixiviacin es un proceso qumico, este se puede acelerar y optimizar mejorando el
rendimiento cintico y se logra aplicando uno de los siguientes factores:
Uso de diferentes reactivos y variacin de su composicin.
Agitacin cuando es posible.
Temperatura y presin.
1.1 ETAPAS DEL PROCESO DE LIXIVIACIN
La li xi viacin se reali za en tres (3) etapas:
Disolucin del metal.
Separacin slido lquido.
Lavado de colas.
La lixiviacin constituye el proceso extractivo fundamental de la hidrometalurgia, puesto que
por ser el primer proceso hidrometalrgico aplicado en la recuperacin de un metal desde
el slido que lo contiene, la eficiencia de este proceso repercutir en muy alto grado sobre
el porcentaje de recuperacin del metal.
Explotacin minera y transporte de mineral.
Triturado primario, secundario, normalmente siempre en seco.
Molienda hmeda y clasificacin.
Concentracin de acuerdo a principios como la concentracin gravitacional o fsico-
qumico.
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
4
De acuerdo a las caractersticas fsico-qumicas del mineral a tratar se
selecciona el agente li xi viante y con ell o la tcnica apropiada de l i xi viacin,
entre las cuales se encuentran:
- Con agitacin: Lixiviacin con agitacin en tanques y lixiviacin por presin.
- Por percolacin: Li xi viacin in situ, li xi vi aci n en botaderos, li xi vi aci n en
pil as y l i xi viacin por percolacin en tanques.
1.2 LIXIVIACIN POR AGITACIN
La lixiviacin por agitacin consiste en introducir un agente lixiviante junto con el material en
un medio de agitacin, donde los slidos se encuentran en suspensin con el agente
lixiviante. Para la aplicacin se requiere que el mineral est finamente molido, por esto se
elabora solamente a minerales frescos de leyes altas, debido a que por su contenido se
justifica una molienda hmeda, a cambio de una mayor recuperacin y menor tiempo de
proceso , o tambin a concentrados o calcinas de tostacin.
Este sistema de lixiviacin se ha aplicado para recuperar cobre, oro y cobalto. El sistema
de lixiviacin por agitacin es adecuado para la aplicacin de factores que favorezcan la
cintica de la reaccin, tales como:
-Agitacin intensa.
-Temperaturas que pueden ser cercanas a 250C y presiones superiores a la
atmosfrica.
-Presin de gases controlada.
-Uso de reactivos oxidantes y altamente agresivos.
Los equipos de lixiviacin por agitacin son: tanques agitados abiertos o en autoclaves a
presin. Los agitadores mecnicos son simplemente impulsores colocados en el interior del
tanque, mientras que los tanques agitados con aire son a menudo tanques de tipo
"Pachuca".
Agitacin mecnica. Agitacin neumtica.
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
5
Habitualmente se aplica un lavado, despus de la lixiviacin. Este lavado se realiza a
contracorriente y su fin es desimpregnar de las soluciones los slidos de las colas. Pero
algunas veces se prefiere lavar las colas en filtros al vaco, as se ahorra agua y se evita
una alta dilucin de las soluciones ricas.
1.3 LIXIVIACIN POR PERCOLACIN
La lixiviacin por percolacin es usada para describir tcnicas en la que la solucin lixiviante
se percola hacia arriba o hacia abajo a travs del mineral que se ha triturado y se ha
colocado en tanques. Los tanques se encuentran distribuidos de tal manera que un sistema
de contracorriente es empleado, adems estos equipos se encuentran provistos de un falso
fondo cubierto con un medio filtrante. Los nuevos slidos son agregados al ltimo tanque y
el agente lixiviante al primero bombendose sucesivamente de un tanque a otro hasta
alcanzar el ultimo tanque, el ciclo de lixiviacin puede variar de 2-14 das y la extraccin del
metal puede ser tan alta como 80% para minerales oxidados de cobre.
Este proceso es apropiado para minerales porosos y arenosos y es inaplicable a minerales
que tienden a compactarse en masas impermeables. El mtodo se usa tambin para lixiviar
menas de oro, plata, uranio y vanadio. Para el caso de menas aurferas las extracciones
son bajas, no ms all del 40-50%.
Para una buena percolacin se exige regularidad en el tamao de las partculas, las ms
pequeas se compactan en los huecos de las ms grandes, de tal manera que obstruyen
los canales.
En la prctica, normalmente para minerales oxidados de cobre la granulometra
recomendada es de 9mm a 18mm y si se producen muchos finos deben removerse antes
de cargarse a los tanques para prevenir prdidas serias de permeabilidad. La presencia de
finos no debe ser mayor del 20%.
Los tanques se construyen de concreto reforzados con revestimientos tales como plsticos
reforzados, a veces cubiertos con madera. Cada tanque est equipado con filtros
especiales protegidos de posibles daos causados por las cargas y descargas.
EQUIPOS Y MATERIALES UTILIZADOS (AGITACIN)
Recipientes para lixiviacin con capacidad de 3 Kg de pulpa.
Agitadores mecnicos de alta velocidad (500-1500rpm).
Balanza comn.
Filtro para pulpas de lixiviacin.
Mena de cobre oxidada.
cido sulfrico analtico.
Equipos y materiales para anlisis qumico de cobre en minerales y soluciones de
cido sulfrico.
Equipos y materiales para anlisis qumico de cido sulfrico en soluciones
acuosas.
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
6
MATERIALES Y EQUIPOS (PERCOLACIN)
Columnas de percolacin con capacidad de 1Kg de mineral.
Bombas peristlticas o de acuario
Balanza comn
Mena de cobre oxidada para lixiviar
cido sulfrico
Equipo y materiales para anlisis qumico de cobre (minerales y soluciones
sulfatadas) y de cido sulfrico en solucin.
2. PROCEDIMIENTO
2.1 LIXIVIACIN POR AGITACIN
Solucin de H2SO4 (5%
peso) sln lixiviante
Mezclar mineral y solucin
Alcuota de 40 ml
ml.
Agitacin mecnica
(ajustar las rpm de la
prueba)
Tomar muestras filtradas a los
5, 10, 20, 40 y 60 min.
Separacin mediante filtro prensa
(Separacin Solido-liquido)
Medir volumen de la
sln rica y pH.
Cuarteo y peso de
muestra (500 g)
Medicin de pH
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
7
Preparar las columnas de
percolacin para efectuar los
ensayos de lixiviacin.
Preparar 2 litros de solucin
lixiviante de H2SO4 al 5% en peso y
titularla.
Por cuarteo tomar y pesar 1 Kg de
mena para efectuar cada ensayo.
Depositar homogneamente la
muestra de mineral en el recipiente
de lixiviacin.
Agregar lentamente la solucin
lixiviante al recipiente donde est
el mineral, poniendo a funcionar el
sistema de recirculacin de la
solucin cuando sea el caso. Anotar
la hora.
Observar la coloracin del lixiviante
al ponerse en contacto con el
mineral y a medida que progresa el
proceso.
Tomar muestras de 40 ml de la
solucin lixiviante as: 2, 15, 25, 40
y 50 horas de iniciada la
experiencia.
Filtrar y guardar las muestras en
recipientes adecuados para anlisis
posterior del contenido de cido
libre y cobre disuelto.
Efectuar la separacin slido-
lquido dejando escurrir bien el
lquido y medir el volumen de
solucin rica obtenida.
Efectuar 3 lavados con agua a las
colas guardando muestras de las
soluciones de lavado para anlisis
de cobre y cido. Utilizar por cada
lavado 4 volmenes de lquido
retenido por ese mineral (28%).
Tomar una muestra de 100 gramos
de colas hmedas para determinar
por secado el volumen de solucin
retenida por esos residuos slidos.
Secar y pesar las colas sobrantes y
luego tomar una muestra para
anlisis qumico de cobre.
2.2 LIXIVIACIN POR PERCOLACIN
Someter las colas a 3 lavados,
tomar alcuotas (40ml).
Pesar 100g y secar para determinar
el volumen de solucin retenida
Colas sobrantes secarlas en estufa
y pesarlas.
Pesar y por diferencia de peso
determinar humedad retenida.
Determinar por anlisis qumico el
cobre no disuelto de una muestra
de las colas.
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
8
3. RESULTADOS
LIXIVIACIN POR AGITACIN
Mineral Cabeza:
1. Retencin de lquido: 10%
2. Cu total
Peso muestra para anlisis: 0,475 gramos
Dilucin final: 1000 ml
Lectura absorcin atmica: 15.2 ppm
3. Cu soluble
Peso muestra para anlisis: 0,462 gramos
Dilucin final: 500 ml
Lectura absorcin atmica: 13.9 ppm
Titulacin de cido libre en la solucin inicial
1. Volumen alcuota de muestra: 20 ml
2. Volumen carbonato gastado [ml] : 44.5 - 51.0 - 34.3 - 36.6 - 35.6 - 38.6 -
49.300
ENSAYO 1
500 RPM, 20% S, 25c, peso del mineral: 500 gramos, volumen de solucin
lixiviante: 2 litros
Muestra
No
Volumen
muestra
Inicial
Ml
Determinacin concentracin de Cobre Titulacin de cido libre
Volumen
alicuota
uL
Volumen
dilucin final
para anlisis
mL
Lectura
concentracin
equipo AA
ppm
Volumen
alcuota de
muestra
mL
Volumen
carbonato
gastado
mL
1 40 500 100 2.05 20
21.2 - 31.2
2 40 500 100 4.82 20
17.2 - 28.1
3 40 500 100 7.21 20
16.0 - 26.3
4 40 100 100 1.85 20
15.2 - 21.4
5 40 100 100 2.67 20
13.2 - 21.2
Lavado
1
40 1000 100 3.24 20
4.3 - 4.2
Lavado
2
40 1000 100 1.85 20
0.8 - 2.2
Lavado
3
40 1000 100 0 20
0.3 - 0.4
Tabla 1. Concentracin de cobre y Titulacin de cido libre para las diferentes muestras y lavados
realizados en el ensayo 1.
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
9
ENSAYO 2.
500 rpm, 40% S, 35C, peso mineral: 500 gramos, volumen solucin lixiviante: 0.750
litros.
Muestra
No
Volumen
muestra
inicial [ml]
Concentracin de Cobre Titulacin de cido libre
Volumen
alcuota
[l]
Volumen
dilucin
final para
anlisis [ml]
Concentra-
cin equipo
AA [ppm]
Volumen
alcuota de
muestra [ml]
Volumen
carbonato
gastado [ml]
1 40 500 100 5.85 20 22.1 - 25.1
2 40 500 100 4.82 20 18.2 - 24.4
3 40 500 100 3.29 20 15.5 - 23.6
4 40 100 100 4.85 20 10.6 - 23.1
5 40 100 100 5.67 20 8.8 - 22.8
Lavado 1 40 1000 100 7.8 20 2.8 - 4.0
Lavado 2 40 1000 100 4.9 20 0.8 - 2.0
Lavado 3 40 1000 100 0 20 0.0 - 0.7
Tabla 2. Concentracin de cobre y Titulacin de cido libre para las diferentes muestras y lavados
realizados en el ensayo 2.
ENSAYO 3.
1500 rpm, 20% S, 25C, peso mineral: 500 gramos, volumen solucin lixiviante: 2 litros.
Muestra
No
Volumen
muestra
inicial [ml]
Concentracin de Cobre Titulacin de cido libre
Volumen
alcuota
[l]
Volumen
dilucin
final para
anlisis [ml]
Concentra-
cin equipo
AA [ppm]
Volumen
alcuota de
muestra
[ml]
Volumen
carbonato
gastado [ml]
1 40 500 100 2.24 20 18.5 - 32.6
2 40 500 100 5.56 20 12.9 - 31.7
3 40 500 100 7.89 20 12.8 - 27.75
4 40 100 100 1.98 20 10.9 - 25.1
5 40 100 100 3.02 20 9.6 - 24.4
Lavado 1 40 1000 100 3.28 20 3.2 - 5.6
Lavado 2 40 1000 100 2 20 0.1 - 1.8
Lavado 3 40 1000 100 0 20 0.0 - 0.8
Tabla 3. Concentracin de cobre y Titulacin de cido libre para las diferentes muestras y lavados
realizados en el ensayo 3.
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
10
ENSAYO 4.
500 rpm, 40% S, 25C, peso mineral: 500 gramos, volumen solucin lixiviante: 0.750
litros.
Muestra
No
Volumen
muestra
inicial [ml]
Concentracin de Cobre Titulacin de cido libre
Volumen
alcuota
[l]
Volumen
dilucin
final para
anlisis [ml]
Concentra-
cin equipo
AA [ppm]
Volumen
alcuota de
muestra
[ml]
Volumen
carbonato
gastado
[ml]
1 40 500 100 4.01 20 34.2 - 22.0
2 40 500 100 2.41 20 32.6 - 17.0
3 40 500 100 1.85 20
30.5 -
16.5
4 40 100 100 2.65 20 23.2 - 17.2
5 40 100 100 3.51 20 18.5
Lavado 1 40 1000 100 3.2 20 4.5 - 2.8
Lavado 2 40 1000 100 1.82 20 0.5 - 1.0
Lavado 3 40 1000 100 0 20 0.0 - 0.0
Tabla 4. Concentracin de cobre y Titulacin de cido libre para las diferentes muestras y lavados
realizados en el ensayo 4.
ENSAYO 5.
Esttico, 20% S, peso mineral: 500 gramos, volumen solucin lixiviante: 2000 mililitros.
Muestra
No
Volumen
muestra
inicial [ml]
Concentracin de Cobre Titulacin de cido libre
Volumen
alcuota
[l]
Volumen
dilucin
final para
anlisis [ml]
Concentra-
cin equipo
AA [ppm]
Volumen
alcuota de
muestra
[ml]
Volumen
carbonato
gastado
[ml]
1 40 500 100 4.15 20
35.5 -
41.1
2 40 500 100 3.1 20
34.9 -
37.5
3 40 500 100 2.82 20 33.7 - 30.3
4 40 100 100 4.19 20
32.9 -
27.5
5 40 100 100 5.81 20
30.4 -
25.0
Lavado 1 40 1000 100 3.21 20 6.0 - 6.1
Lavado 2 40 1000 100 2.8 20 0.8 - 1.5
Lavado 3 40 1000 100 0 20 0.0 - 0.4
Tabla 5. Concentracin de cobre y Titulacin de cido libre para las diferentes muestras y lavados
realizados en el ensayo 5.
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
11
LICOR (Solucin rica) FINAL Y COLAS (Residuos) DE LIXIVIACIN
Ensayo pHi pHf
*Licor filtrado
final [ml]
% Lquido
retenido [ml]
Peso total
Colas
secas [g]
1
0.92
0.92
1.10
1.09
1700
1680
20.04
16.18
473.59
463.54
2 0.92 1.33 400 30.41 463.22
3 0.92 1.29 1650 25.65 462.35
4 0.92 1.02 401 22.46 460.2
5 0.92 0.92 1540 13.88 480.43
Tabla 6. Licor (solucin rica) final y colas (residuos) de lixiviacin. *Licor filtrado final obtenido de
separacin S/L, Volumen ml.
% =
=
COLAS DE LIXIVIACIN
Ensayo
Peso muestra
para anlisis [g]
Dilucin final
[ml]
Lectura Absorcin
Atmica [ppm]
1 0.730 1000 12.5
2 0.601 1000 7.5
3 0.635 1000 10.5
4 0.630 1000 11.5
5 0.550 1000 13.5
Tabla 7. Concentracin determinada por absorcin atmica para las muestras de cada ensayo.
Colas de lixiviacin Ensayo 1:
Peso muestra para anlisis: 0.730 gramos
Dilucin final: 1000 ml
Lectura absorcin atmica: 12.5 ppm
Colas de lixiviacin Ensayo 2:
Peso muestra para anlisis: 0.601 gramos
Dilucin final: 1000 ml
Lectura absorcin atmica: 7.5 ppm
Colas de lixiviacin Ensayo 3:
Peso muestra para anlisis: 0.635 gramos
Dilucin final: 1000 ml
Lectura absorcin atmica: 10.5 ppm
Colas de lixiviacin Ensayo 4:
Peso muestra para anlisis: 0.630 gramos
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
12
LIXIVIACIN POR PERCOLACIN
Mineral Cabeza:
1. Retencin de lquido:20%
2. Cu total
Peso muestra para anlisis: 0,561 gramos
Dilucin final: 1000 ml
Lectura absorcin atmica: 16.9 ppm
3. Cu soluble
Peso muestra para anlisis: 0,252 gramos
Dilucin final: 500 ml
Lectura absorcin atmica: 12.7 ppm
Titulacin de cido libre en la solucin inicial
Volumen alcuota de muestra ( ml)
20
Volumen carbonato gastado (ml)
48.6 - 33.05 - 33.0 - 37.8 - 37.0
ENSAYO 1
Solucin esttica; mineral triturado a -1/4
Peso mineral: 500 gramos Volumen solucin lixiviante: 1.5 litros.
Muestra
Volumen
muestra
inicial
mL
Determinacin concentracin de Cobre Titulacin de cido libre
Volume
n
alicuota
uL
Volumen
dilucin
final para
anlisis mL
Lectura
concentracin
equipo AA
ppm
Volumen
alcuota de
muestra ml
Volumen
carbonato
gastado
ml
5-6 das 40 1000 100 5,22 20
28.2 -
40.1
Lavado 1 40 40000 50 3,45 20 2.0 - 3.0
Lavado 2 40 40000 40 1,05 20 0.2 - 1.0
Lavado 3 40 40000 40 0 20 0.0 - 0.0
Tabla 8. Concentracin de cobre y Titulacin de cido libre para las diferentes muestras y lavados
realizados en el ensayo 1.
ENSAYO 2
Solucin esttica; mineral molido a -60#Tyler
Peso mineral: 500 gramos Volumen solucin lixiviante: 1.5 litros
Muestra
Volumen
muestra
inicial mL
Determinacin concentracin de Cobre Titulacin de cido libre
Volumen
alicuota
uL
Volumen
dilucin
final para
anlisis
mL
Lectura
concentraci
n equipo AA
ppm
Volumen
alcuota de
muestra ml
Volumen
carbonato
gastado ml
5-6 das 40 1000 100 8.90 20 28.6 - 26.7
Lavado 1 40 40000 50 3.45 20 5.4 - 3.05
Lavado 2 40 40000 40 1.05 20 0.8 - 2.24
Lavado 3 40 40000 40 0 20 0.0 - 1.0
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
13
Tabla 9. Concentracin de cobre y Titulacin de cido libre para las diferentes muestras y lavados
realizados en el ensayo 2.
ENSAYO 3
Solucin con circulacin ascendente; mineral triturado a -1/4
Peso mineral: 500 gramos Volumen solucin lixiviante: 1.5 litros
Muestra
Volumen
muestra
inicial mL
Determinacin concentracin de Cobre Titulacin de cido libre
Volumen
alicuota
uL
Volumen
dilucin
final para
anlisis
mL
Lectura
concentracin
equipo AA
ppm
Volumen
alcuota de
muestra ml
Volumen
carbonato
Gastado ml
5-6 das 40 100 100 8.52 20 28.3 - 31.2
Lavado 1 40 500 50 7,3 20 3.2 - 2.5
Lavado 2 40 1000 50 2 20 0.2 - 0.2
Lavado 3 40 1000 50 0 20 0.0 - 0.0
Tabla 10. Concentracin de cobre y Titulacin de cido libre para las diferentes muestras y
lavados realizados en el ensayo 3.
ENSAYO 4
Solucin con circulacin descendente; mineral triturado a -1/4
Peso mineral: 500 gramos Volumen solucin lixiviante: 1.5 litros
Muestra
Volumen
muestra
inicial mL
Determinacin concentracin de Cobre Titulacin de cido libre
Volumen
alicuota
uL
Volumen
dilucin
final para
anlisis mL
Lectura
concentracin
equipo AA
ppm
Volumen
alcuota
de
muestra
ml
Volumen
carbonato
gastado ml
5-6 das 40 100 100 6.03 20 12.3 - 12.4
Lavado 1 40 500 50 5,32 20 3.2 - 1.3
Lavado 2 40 1000 50 1,5 20 0.2 - 0.4
Lavado 3 40 1000 50 0 20 0.0 - 0.0
Tabla 11. Concentracin de cobre y Titulacin de cido libre para las diferentes muestras y
lavados realizados en el ensayo 4.
ENSAYO 5
Solucin con circulacin descendente; mineral molido a -60#Tyler
Peso mineral: 500 gramos Volumen solucin lixiviante: 1.5 litros
Muestra
Volumen
muestra
inicial mL
Determinacin concentracin de Cobre Titulacin de cido libre
Volumen
alicuota
uL
Volumen
dilucin final
para
anlisis mL
Lectura
concentraci
n equipo AA
ppm
Volumen
alcuota de
muestra ml
Volumen
carbonato
gastado ml
5-6 das 40 100 100 5.9 20 18.6 - 19.5
Lavado 1 40 40000 50 4.45 20 6.0 - 3.8
Lavado 2 40 40000 40 1.15 20 0.6 - 1.5
Lavado 3 40 40000 40 0.0 20 0.0 - 0.5
Tabla 12. Concentracin de cobre y Titulacin de cido libre para las diferentes muestras y
lavados realizados en el ensayo 5.
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
14
COLAS (RESIDUOS) DE LIXIVIACIN Y LICOR (SOLUCIN RICA) FINAL
Ensayo pHi pHf Volumen de licor
(filtrado) final total
mL
Peso de
colas totales
secas
g
Volumen de solucin
retenida/100 gramos de
colas hmedas
mL = % Lquido retenido
1 1.15 1.27 1245 443.69 2.71
2 1.15 1.31 1080 474.74 21.26
3 1.15 1.49 1330 489.97 6.43
4 1.15 1.27 1260 485.03 5.86
5 1.15 1.53 1150 478.65 29.35
Tabla 13. Licor (solucin rica) final y colas (residuos) de lixiviacin. *Licor filtrado final obtenido de
separacin S/L, Volumen ml.
Colas de lixiviacin Ensayo 1:
Peso muestra anlisis: 0,552 gramos
Dilucin final: 1000 ml
Lectura absorcin atmica: 12,9 ppm
Colas de lixiviacin Ensayo 2:
Peso muestra anlisis: 0,549 gramos
Dilucin final: 1000 ml
Lectura absorcin atmica: 13,5 ppm
Colas de lixiviacin Ensayo 3:
Peso muestra anlisis: 0,631 gramos
Dilucin final: 1000 ml
Lectura absorcin atmica: 1,5 ppm
Colas de lixiviacin Ensayo 4:
Peso muestra anlisis: 0,632 gramos
Dilucin final: 1000 ml
Lectura absorcin atmica: 15,9 ppm
Colas de lixiviacin Ensayo 5:
Peso muestra anlisis: 0,631gramos
Dilucin final: 1000 ml
Lectura absorcin atmica: 15,5 ppm
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
15
CLCULO Y ANLISIS DE RESULTADOS
LIXIVIACIN POR AGITACIN
1. Calcular el volumen de cido sulfrico (reactivo disponible en el laboratorio) necesario para
preparar 10 litros de la solucin lixiviante, al 5% en peso, y comparar este resultado con
relacin al obtenido en la titulacin de la solucin inicial.
10 litros de solucin lixiviante, 5% p/p
Pureza: 99% Densidad: 1.83 g/ml
Pureza 100% Densidad: 1.87 g/ml
P.M = 98.08 g/mol
% =
[]
+
100
4
=
5
100
(
4
+
4
= 0.05
4
+0.05
4
0.05
4
= 0.05
(1) Teniendo en cuenta que: 0.95
4
= 0.05
= 19
4
El volumen de la solucin a partir de:
donde =
(2) Es igual a
4
+
4
= 1.83 / ;
= 1/
Reemplazando (1) en (2) para un volumen de 10 litros 10000 =
4
1.83/
+
19
4
1/
4
= 511.6
4
=
511.6
1.87/
= 279.6 (Para una solucin 100% de pureza)
4
=
279.6
0.99
= 282.4 (Con una pureza 99%)
2. Con los resultados de los anlisis qumicos efectuar los clculos para elaborar las grficas
siguientes:
a. Acido libre Vs tiempo y Consumo de cido Vs tiempo (En una sola grfica)
Con los datos de volumen de Na2CO3 usado para la titulacin, la relacin de Na2CO3 y el
peso de H2SO4 por litro de solucin, se puede calcular la cantidad de cido libre y de cido
consumido.
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
16
= 2 (
2
3
)
=
Tiempo [min]
Volumen de Na2CO3 consumido (promedio)
Ensayo 1 Ensayo 2 Ensayo 3 Ensayo 4 Ensayo 5
0 41,1 41,1 41,1 41,1 41,1
5 26,2 23,1 25,6 28,1 38,3
10 22,7 21,3 22,3 24,8 36,2
20 21,2 19,6 20,3 23,5 32
40 18,3 16,9 18 20,2 30,2
60 17,2 15,8 17 18,5 27,7
Tabla 14. Volumen de Na2CO3 consumido en promedio para cada ensayo en cada tiempo.
Clculo tipo de cido libre:
Ensayo 1; t = 5 min; volumen de la solucin lixiviante = 2 litros.
= 2(26.2) 2 = 104.8
Tiempo [min]
Acido Libre [g]
Ensayo 1 Ensayo 2 Ensayo 3 Ensayo 4 Ensayo 5
inicial 164,4 6,165 164,4 6,165 6,165
5 104,8 3,465 102,4 4,215 5,745
10 90,8 3,195 89,2 3,72 5,43
20 84,8 2,94 81,2 3,525 4,8
40 73,2 2,535 72 3,03 4,53
60 68,8 2,37 68 2,775 4,155
Tabla 15. cido libre en cada ensayo para cada tiempo
Grfica 1. cido libre para cada ensayo en funcin del tiempo.
1
10
100
1000
0 10 20 30 40 50 60 70
C
I
D
O
L
I
B
R
E
TIEMPO
cido Libre Vs Tiempo
ensayo 1 ensayo 2 ensayo 3 ensayo 4 ensayo 5
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
17
Clculo tipo de cido consumido:
Ensayo 1; t = 5 min; volumen de la solucin lixiviante = 2 litros.
=
= 164.4 104.8 = 59.6
Tiempo [min]
cido Consumido [g]
Ensayo 1 Ensayo 2 Ensayo 3 Ensayo 4 Ensayo 5
5 59,6 2,7 62 1,95 0,42
10 73,6 2,97 75,2 2,445 0,735
20 79,6 3,225 83,2 2,64 1,365
40 91,2 3,63 92,4 3,135 1,635
60 95,6 3,795 96,4 3,39 2,01
Tabla 16. cido consumido en cada tiempo para cada ensayo.
Grfica 2. cido consumido para cada ensayo en cada tiempo.
Se puede observar el comportamiento que presenta el cido libre en la solucin y el cido
consumido con respecto al tiempo. En la grfica 1, la disminucin del cido libre a medida
que el tiempo transcurre, queriendo decir que se consume mayor cantidad de cido.
Definiendo al tiempo como una variable importante en el proceso de lixiviacin por
agitacin.
La temperatura tambin juega un factor importante, observndose un aumento de cido
libre en solucin en el caso del ensayo 2, al trabajarse la agitacin a los 35C. Al comparar
los ensayos en los que se utiliz agitacin y el ensayo esttico, se determin que a mayor
velocidad de agitacin se consume ms acido en el proceso.
0.1
1
10
100
0 10 20 30 40 50 60 70
C
I
D
O
C
O
N
S
U
M
I
D
O
TIEMPO
cido consumido Vs Tiempo
ensayo 1 ensayo 2 ensayo 3 ensayo 4 ensayo 5
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
18
b. Cobre disuelto (%) Vs tiempo
%
=
[ ][]
[]
100
%
=
0.0152/1
0.475
100
= . %
= %
= 500 0.032
=
%
=
[ ][]
[]
100
%
=
0.0139/0.5
0.462
100
= . %
= %
= 500 0.015
= .
Ahora, para realizar la grfica del porcentaje de cobre disuelto en funcin del tiempo, se
utilizan los resultados obtenidos de las pruebas de absorcin atmica para las alcuotas en
cada uno de los ensayos.
1
=
2
2
Dnde, V1: Volumen de la alcuota
V2: Volumen de la dilucin final
C1: Concentracin de Cu disuelto en la alcuota
C2: Lectura de concentracin por AA
Concentracin de Cu disuelto [mg/l]
1
=
[/] []
[]
Cantidad de Cu disuelto [g]
[] =
1
[
[]
Siendo: Vsln: Volumen real de la solucin en un tiempo t
Porcentaje de Cu disuelto
%
=
[]
[]
100
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
19
Clculo tipo del porcentaje de cobre disuelto
Ensayo 1, t = 5 minutos, Volumen de la solucin lixiviante= 2 litros
Volumen alcuota= 500l
Lectura AA= 2.05ppm
Volumen dilucin final=100ml
Concentracin de Cu disuelto [mg/l]
1
=
2.0510
3
100
510
4
= 410/
Cantidad de Cu disuelto [g] = 0.41 2 = 0.82
Porcentaje de Cu disuelto %
=
0.82
16
100 = 5.13%
Tiempo
[min]
% Cu disuelto
Ensayo 1 Ensayo 2 Ensayo 3 Ensayo 4 Ensayo 5
5 5.13 5.5 5.63 3.75 1.06
10 11.81 21.38 13.63 10.69 3.81
20 17.31 27.56 18.94 15.5 6.75
40 21.75 38.19 23.25 20.88 9.88
60 30.69 41.81 34.75 25.88 13.38
Tabla 17. Porcentaje de cobre disuelto en funcin del tiempo, para cada ensayo realizado.
Grfica 3. Porcentaje de cobre disuelto en funcin del tiempo, para cada ensayo realizado.
Analizando la grfica 3, se puede determinar que el ensayo 2 disuelve mayor cantidad de
cobre con un diferencia notoria de la curva con respecto a las otras de los otros ensayos,
adems si el anlisis se basa con la temperatura y velocidad de agitacin, el comportamiento
0
5
10
15
20
25
30
35
40
45
0 10 20 30 40 50 60 70
%
C
U
D
I
S
U
E
L
T
O
TIEMPO
%Cu disuelto Vs Tiempo
Ensayo 1 Ensayo 2 Ensayo 3 Ensayo 4 Ensayo 5
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
20
de disolucin de cobre aumenta con el aumento de estas variables mencionadas,
observndose en el comportamiento creciente de la curva del ensayo nmero dos.
c. Kilogramos de H2S04 consumido/kilogramo de cobre disuelto Vs tiempo.
Tiempo
[min]
H2SO4 Consumido/ Cu disuelto
Ensayo 1 Ensayo 2 Ensayo 3 Ensayo 4 Ensayo 5
5 74.196 30.358 70.490 33.275 73.182
10 39.704 8.820 35.065 14.570 34.166
20 29.257 7.435 27.901 10.833 34.853
40 26.564 6.029 25.172 9.525 28.380
60 19.723 5.742 17.561 8.301 25.627
Tabla 18. H2S04 consumido/kilogramo de cobre disuelto para cada tiempo usado en cada ensayo.
Grfica 4. H2S04 consumido/kilogramo de cobre disuelto para cada tiempo usado en cada ensayo.
En la grfica 4, se confirma el comportamiento sobresaliente del ensayo 2, presentando
una menor relacin H2SO4 consumido/Cu disuelto; esto debe directamente a la explicacin
de la grfica 3 donde se observa la mayor disolucin de cobre por parte de este ensayo,
adems de la mayor relacin acido consumido/cobre disuelto por parte del ensayo 5, el cual
se mantuvo esttico, sin agitar evitando que se diera satisfactoriamente el fenmeno que
controla el proceso de lixiviacin.
3. Analizando los resultados obtenidos en esta prctica, deducir cul es el fenmeno
(qumico difusional) que controla este proceso de lixiviacin.
En el anlisis de las curvas de los ensayos 3 y 5 en la grfica 3, se observa que existe una
mayor dilucin de cobre en presencia de agitacin, existiendo un fenmeno de difusin en
el proceso. Pero como lo que se desea evaluar es el fenmeno que controla el proceso de
sistemas agitados, se hace una comparacin entre la prueba 1 y 3, ya que permite evaluar
la disolucin a iguales condiciones variando nicamente la velocidad de agitacin.
La prueba 3 muestra resultados de disolucin de cobre muy cercanos a la disolucin
alcanzada en la prueba 1, pero ligeramente mayor. A pesar de que la diferencia en la
0
10.000
20.000
30.000
40.000
50.000
60.000
70.000
80.000
0 10 20 30 40 50 60 70
H
2
S
O
4
C
O
N
S
U
M
I
D
O
/
C
U
D
I
S
U
E
L
T
O
TIEMPO
H
2
SO
4
Consumido/Cu Disuelto Vs Tiempo
Ensayo 1 Ensayo 2 Ensayo 3 Ensayo 4 Ensayo 5
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
21
velocidad de agitacin (de 500 rpm a 1500 rpm) es notoria, las diluciones son muy
parecidas, esto lleva a decir que el fenmeno que controla el proceso de lixiviacin del
mineral de cobre experimental, es qumico.
Existe una influencia de la difusin; sin embargo prevalece el fenmeno qumico. La
influencia de la difusin pudo ser corroborada con la precedente comparacin de las
pruebas 5 y 1. Adems, si se compara la prueba 2 y 4 se llega a la misma conclusin, ya
que a pesar de operar a condiciones de agitacin iguales se obtienen porcentajes de
dilucin de disimilitud marcada.
4. Determinar la Energa de Activacin (Ea) de este proceso de lixiviacin., y con base
en su valor confirmar o negar lo deducido anteriormente, respecto al fenmeno que
controla este proceso.
La energa de activacin es la energa que necesita un sistema antes de poder iniciar un
determinado proceso. La energa de activacin suele utilizarse para denominar la energa
mnima necesaria para que se produzca una reaccin qumica dada.
La ecuacin de Arrhenius:
= /
Esta ecuacin relaciona la constante de velocidad con la temperatura para cada caso en
particular de una reaccin qumica.
Para determinar la constante de reaccin (k):
(K):
= dnde, Ca es la concentracin de Cu disuelto.
Co es la concentracin de Cu total.
0
Se tiene que a t = 0, Cao = 0, entonces:
1
= (1 )
Aplicando logaritmos:
1
= [(1 )] +
=
1
1
[(1 )] +
1
1
La concentracin de cobre disuelto [M] se determina, teniendo en cuenta el peso molecular
del cobre y el volumen real de la solucin, mediante la siguiente relacin:
[] [] =
1
63.54
1
[]
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
22
[
+2
] = 5.13
+2
1
+2
63.54
+2
1
2
= 0.04036
t Ca ln t ln Ca
5 0.04036 1.60944 -3.20992
10 0.09292 2.30259 -2.37602
20 0.1362 2.99573 -1.99363
40 0.17114 3.68888 -1.76527
60 0.24148 4.09434 -1.42097
Tabla 19. Parmetros de ecuacin cintica para el ensayo 2.
t Ca ln t ln Ca
5 0.04328 1.60944 -3.14006
10 0.16824 2.30259 -1.78236
20 0.21687 2.99573 -1.52846
40 0.30052 3.68888 -1.20224
60 0.32901 4.09434 -1.11167
Tabla 20. Parmetros de ecuacin cintica para el ensayo 4.
Grfica 5. Parmetros de ecuacin cintica para los ensayos 2 y 4.
Se determina el orden de reaccin (n) y con este la constante cintica para las pruebas 2 y
4.
Ensayo 2: = 0.6611 4.0956
1
1
= = 0.6611 = 0.5126
1
1
[(1 )] = 4.0956 =
1
1.5126
4.0956
0.6611
= .
Ensayo 4: = 0.7438 3.9384
1
1
= = 0.7438 = 0.3444
1
1
[(1 )] = 3.9384 =
1
1.3444
3.9384
0.7438
= .
-3.5
-3
-2.5
-2
-1.5
-1
-0.5
0
0 0.5 1 1.5 2 2.5 3 3.5 4 4.5
L
N
C
A
LN T
Ln Ca Vs Ln t
Ensayo 2 Ensayo 4
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
23
Representacin lineal de la ecuacin de Arrhenius ln = ln
0
Ensayo k ln k T 1/T
2 0.00135 -6.60765 298 0.00336
4 0.00373 -5.59135 308 0.00325
Tabla 21. Datos para trazar la representacin lineal de la ecuacin de Arrhenius.
Grfica 6. Ln(K) Vs 1/T, para los ensayos 2 y 4.
= 9328 +24.695
= 9328
= 9328 8.314
1
1000
= 77.55/
Teniendo en cuenta:
Control qumico para Ea > 40 kJ/mol
Control difusional para Ea entre 5 y 20 kJ/mol
Control mixto para 20 kJ/mol < Ea < 40 kJ/mol
Se determina que la energa de activacin est dentro del rango de control qumico (Ea >
40 kJ/mol), con lo cual se confirma lo deducido anteriormente, es decir, que el fenmeno
que controla el proceso de lixiviacin es el qumico.
5. Calcular el volumen de solucin evaporada
Clculo ejemplo para el ensayo 1.
100
=
18.11
100
=
468.57
= 572.19
-6.8
-6.6
-6.4
-6.2
-6
-5.8
-5.6
-5.4
0.00324 0.00326 0.00328 0.0033 0.00332 0.00334 0.00336 0.00338
L
N
K
1/T
Ln k Vs 1/T
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
24
Ahora,
100
=
572.1918.11
100
= 103.62
(
+
= 2000 (1690 +103.62) = 206.38
Ensayo
Vinicial
[ml]
Vfinal
[ml]
%Lquido
Retenido* [ml]
Wcolas secas
[g]
Wcolas
humedas [g]
Vsln retenida
[ml]
Vsln evaporada
[ml]
1 2000 1690 18.11 468.57 572.19 103.62 206.38
2 750 400 30.41 463.22 665.64 202.42 147.58
3 2000 1650 25.65 462.35 621.86 159.51 190.50
4 750 401 22.46 460.20 593.50 133.30 215.7
5 2000 1540 13.88 480.43 557.86 77.43 382.57
Tabla 22. Volumen de solucin evaporada en colas para lixiviacin por agitacin de los ensayos
realizados. *% de lquido retenido = Volumen de la solucin retenida/100g de colas hmedas.
6. De acuerdo a los resultados obtenidos disear un sistema simple de lavado de las
colas.
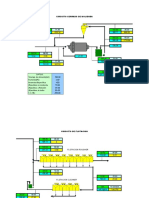
Figura 1. Diseo de lavado de colas para un sistema de lixiviacin por agitacin.
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
25
Este diseo (figura 1), consiste en el lavado de las colas del sistema de lixiviacin por
agitacin a una velocidad de 1500 rpm, representando dos etapas simples, primero el
descargue de la solucin licor con las colas (o slidos) del tanque de agitacin, seguido por
el cargue en un separador (filtro prensa), con el fin de separar los slidos del lquido
(solucin licor), esta ir posteriormente a un proceso de recuperacin del cobre disuelto; la
segunda etapa consta del lavado de las colas, necesario para la recuperacin del cobre
disuelto y el cido libre que se encuentra en el lquido retenido naturalmente por el mineral,
se realizan dos lavados con agua, de los cuales, se recupera la mayora del cobre disuelto
y el cido libre de las colas.
7. Utilizando dibujos describir los tanques industriales utilizados en este mtodo de
lixiviacin.
Figura 2. Tanque de lixiviacin agitada de minerales.
Caracterizado por el uso de aspas con agitado mecnico de la solucin lixiviante y la pulpa
mineral, colocando en constante contacto las partculas de la pulpa en suspensin y la
solucin lixiviante, favoreciendo su lixiviacin. Este proceso es aplicado a minerales con
una alta ley
Figura 3. Tanques de lixiviacin de agitacin en serie a escala industrial.
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
26
Figura 4. Autoclave
Las autoclaves son tanques agitadores que adems de la agitacin a la pulpa a partir de
bombeo de un gas, el proceso de disolucin es promovido por temperatura y presin,
reduciendo los tiempos de tratamiento. Este proceso asegura una alta disolucin del metal
en el mineral, es muy aplicado a menas con una alta ley.
Figura 5. Tanque pachuca
Tanques cilndricos cuya agitacin se realiza por bombeo neumtico, permitiendo que las
partculas se mantengan en suspensin, y entren en contacto con la solucin lixiviante.
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
27
LIXIVIACIN POR PERCOLACIN
1. Con los resultados de los anlisis qumicos efectuar los clculos para elaborar las
grficas siguientes:
a. Acido libre Vs tiempo y Consumo de cido Vs tiempo
El cido libre en la solucin a cualquier tiempo, se determina mediante la cantidad de
carbonato de sodio utilizada y el volumen de la solucin presente un tiempo determinado.
La cantidad de cido en la solucin inicial es el mismo para todos los ensayos al igual que
el cobre soluble en el mineral y se calcula sacando un promedio de los datos inciales.
El cido consumido se determina mediante la diferencia entre el cido libre en la solucin
inicialmente y el cido presente libre.
=
. +. +. +. +.
= .
Para el Ensayo 1:
6 das de lixiviacin.
Volumen de solucin lixiviante = 1,5 L
Cantidad de cido inicial= X1
2 37.89 =
X
1
g
litros de sln
X
1
= 75.78 1.5 = 113.67gH
2
SO
4
Cantidad de cido libre en solucin a los 6 das de lixiviacin: X2
2 34.15 =
X
2
g
litros de sln
X
2
= 68.3 1.5 = 102.45gH
2
SO
4
Cantidad de cido consumido a los 6 das de lixiviacin.
Acido consumido = 113.67gH
2
SO
4
102.45gH
2
SO
4
= 11.22gH
2
SO
4
Tiempo: 6 das Ensayo 1 Ensayo 2 Ensayo 3 Ensayo 4 Ensayo 5
Acido Inicial 0.11367 0.11367 0.11367 0.11367 0.11367
cido libre 0.10245 0.08295 0.08925 0.03705 0.05715
cido consumido 0.01122 0.03072 0.02442 0.07662 0.05652
Tabla 23. Acido Libre y Acido consumido
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
28
b. Cobre disuelto (%) Vs tiempo
Cu total en la muestra
% =
% =
. /
.
= . %
Cu total en mineral
= . = .
Cu soluble en muestra
% =
%
=
.
.
= . %
Cu soluble en mineral
= . = .
Entonces por medio de los resultados obtenidos a partir de pruebas de absorcin atmica
para cada alcuota en los diferentes ensayos, se puede realizar la grfica correspondiente
al porcentaje de cobre disuelto contra tiempo, mediante la siguiente relacin:
Dnde:
V1: Volumen de la alcuota
V2: Volumen de la dilucin final
C1: Concentracin de Cu disuelto en la alcuota
C2: Lectura de concentracin por AA
Concentracin de Cu disuelto [mg/l]
=
[/] []
[]
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
29
Cantidad de Cu disuelto [g]
[] =
[]
Donde:
Vsln: Volumen real de la solucin en un tiempo t
Porcentaje de Cu disuelto
%
=
[]
[]
Para el Ensayo 1:
6 das de lixiviacin
C
1
=
5.22(100)(0.001)
1000(0.000001)
= 522mg/l
Cu
disuelto
= 522
1
1000
(1.5) = 0.783g%Cu
disuelto
=
0.783
15.05
100 = 5.2%
Tiempo: 6 das Ensayo 1 Ensayo 2 Ensayo 3 Ensayo 4 Ensayo 5
%Cu disuelto 5.2 8.87 84.92 60.1 58.8
Tabla 24 .Porcentaje de Cu disuelto
c. Los kilogramos de H2SO4 consumidos/kilogramo de cobre disuelto a los 6 das de
lixiviacin.
Para el Ensayo 1:
0.01122KgH
2
SO
4
consumido
0.000783Kg de Cu disuelto
= 14.3295
Tiempo: 6 das Ensayo 1 Ensayo 2 Ensayo 3 Ensayo 4 Ensayo 5
Acido consumido 14.3295 23.0112 1.9108 8.4709 6.3864
Tabla 25. H2SO4 consumido/ Cu disuelto
2. Calcular el volumen de solucin evaporada.
Para el Ensayo 1:
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
30
=
.
= .
Luego
=
..
= .
(
+
= ( +. ) = .
Ensayo
Vinicial
[ml]
Vfinal
[ml]
%Lquido
Retenido [ml]
Wcolas
secas [g]
Wcolashumedas
[g]
Vsln retenida
[ml]
Vsln evaporada
[ml]
1 1500 1245 2.71 443.69 456.05 12.36 242.64
2 1500 1080 21.26 474.74 602.92 128.18 291.82
3 1500 1330 6.43 489.97 523.64 33.67 136.33
4 1500 1260 5.86 485.03 515.22 30.19 209.81
5 1500 1150 29.32 478.65 677.21 198.56 151.44
Tabla 26. Datos volumen solucin evaporada en colas para lixiviacin por percolacin.
(% lquido retenido (Volumen de la solucin retenida/100 gramos de colas hmedas)
3. De acuerdo a los resultados obtenidos disear un sistema de lavado de las colas.
Figura 6. Diseo de lavado de colas, sistema de lixiviacin por percolacin.
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
31
En la figura se muestra la propuesta de un sistema simple de lavado de colas para un
proceso de lixiviacin por percolacin. Se utiliza un esperador para sustituir el filtro de
prensa utilizado normalmente en el proceso de lixiviacin por agitacin, para lixiviar mineral
de granulometra gruesa. Despus de que las colas que vienen del tanque de lixiviacin
pasan por el espesador, se extrae el cobre disuelto que queda retenido en ellas (solucin
licor) y se aumenta la recuperacin del metal en los lavados. Gracias a estos sistemas de
lavado de colas es posible recuperar cobre aun sin extraer y el cido presente en el mineral.
De acuerdo con los resultados obtenidos, son necesario dos lavados, ya que por encima
de este nmero los lavados que se realicen son innecesarios debido a que ha sido
recuperado prcticamente todo el metal de inters y el cido presente.
4. Utilizando dibujos describir los tanques industriales utilizados en este
mtodo de lixiviacin.
La siguiente figura muestra una serie de tanques de lixiviacin que presentan un aspecto
largo y fino, cilindro recto en la tapa y en la parte inferior, puede producir buena diferencia
de la concentracin para hacer la dispersin que se realizar suavemente y naturalmente.
As, el efecto de lixiviacin es mejor que el del mtodo de inmersin, y la extraccin ser
comparativamente completa. Estos tanques son ampliamente utilizados en la industria
farmacutica.
Figura 7. Sistema de percolacin.
En la industria metalrgica, esta tcnica consiste en contactar un lecho de mineral con una
solucin acuosa que percola e inunda la batea o estanque.
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
32
Los minerales a tratar por este mtodo deben presentar contenidos metlicos altos o muy
altos, debiendo ser posible lixiviar el mineral en un perodo razonable (3 a 14 das) y en
trozos de tamao medio, con tonelajes suficientes de mineral percolable en el yacimiento
que permitan amortizar la mayor inversin inicial que requiere este tipo de proceso.
5. Comparar los resultados obtenidos al final de las pruebas de los dos
mtodos de lixiviacin (agitacin y percolacin)
El contenido de cido libre y el consumo de acido
Teniendo en cuenta parmetros como el tiempo, se observ que a pesar que los dos
mtodos requirieron intervalos diferentes la cantidad de cido libre y consumido fue similar.
Para tiempos iguales de operacin, dado que las cinticas son diferentes, ambos mtodos
no proporcionarn resultados iguales. Por lo anterior, se comprueba que la cintica es
mucho menor en el mtodo de percolacin.
Tambin hay que tener en cuenta que los consumos de cido y contenido de cido libre,
son similares, pero no iguales, esto se debe a factores como la diferencia en granulometra,
la cual afecta considerablemente el proceso, esto en cuanto a las velocidades de reaccin.
El cobre disuelto (%)
Enambos procesos de lixiviacin hubo un comportamiento destacado en uno de los
ensayos (agitacin: ensayo 2 y percolacin: ensayo 3), influenciados por factores como la
temperatura y la direccin de circulacin de la solucin, para lixiviacin por agitacin y
percolacin respectivamente, sin embargo la mayor disolucin se present en la segunda.
La mayor disolucin por parte de la percolacin est relacionada directamente con el tiempo
prolongado del proceso, no obstante se debe determinar cul de los dos mtodos es
adecuado basndose en los costos para ser implementado en la industria.
Los kilogramos de H2SO4 consumidos/kilogramo de cobre disuelto
Los mejores resultados relacionando las variables consumo de cido y cobre disuelto se
reflejan en el mtodo de agitacin, pues el consumo fue menor.
6. Con base en la caracterizacin de la mena y los resultados experimentales,
discutir cul sera el mtodo ms apropiado, de los dos ensayos en
laboratorio, para extraer de estas menas el cobre por lixiviacin, teniendo en
cuenta tanto factores tcnicos como econmicos.
El mtodo ms apropiado para extraer el cobre por lixiviacin depende del anlisis
costo/beneficio, pero teniendo en cuenta los resultados experimentales obtenidos para los
dos ensayos de los sistemas de lixiviacin, se puede decir que el mtodo ms apropiado
es el mtodo de lixiviacin por percolacin con circulacin ascendente ya que utilizando
este mtodo se obtuvo porcentajes de cobre disuelto muy alto con un menor consumo de
cido a comparacin del mtodo de lixiviacin por agitacin por ese motivo el mtodo de
lixiviacin por percolacin genera disminucin en los costos de operacin, generando un
aumento en el tiempo de obtencin del metal de inters.
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
33
La lixiviacin por percolacin ha sido un proceso muy antiguo utilizado para explotar
grandes depsitos de mineral, usualmente de baja ley, de un tiempo para ac se ha
comprobado que tiene excelente aplicacin en depsitos pequeos, de baja o alta ley, ya
que los costos que dicho proceso conlleva son relativamente bajos permitiendo as que la
extraccin sea rentable para la empresa.
La lixiviacin por percolacin tiene un sistema operativo muy flexible, donde el ingeniero
puede planificar a su beneficio el procedimiento que desea aplicar, pues es l quien tiene
la capacidad de controlar las variables del proceso. Este tipo de lixiviacin por ejemplo,
permite implementar tratamientos que duren semanas, meses, todo dependiendo del
mineral con que se trabaje. Es por esto que se hace importante conocer inicialmente, la
caracterizacin de la mena pues estos resultados permitirn establecer las mejores
condiciones para una extraccin eficiente del mineral.
Mediante el anlisis de caracterizacin de la mena se obtiene factores importantes como la
permeabilidad del mineral de manera que el lquido lixiviante pase a travs de todo el
material y que el contacto entre el agente lixiviante y el mineral sea el ptimo este factor de
gran importancia para el mtodo de lixiviacin por percolacin.
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
34
CONCLUCIONES
La velocidad de agitacin durante el proceso de lixiviacin es un factor importante a
tener en cuenta, ya que est relacionada directamente con la cantidad de cobre que
se va a disolver en la solucin, ocasionando disminucin o aumento en el porcentaje
de recuperacin.
La granulometra utilizada en el proceso de lixiviacin por percolacin, es un aspecto
que se debe tener en cuenta, ya que se observ que al tener finos se consume una
cantidad menor de cido, sin embargo no es recomendable el uso de estos, ya que
se pueden presentar perdidas por deslizamiento del mineral en las corrientes de
solucin lixiviante.
A medida que aumenta el tiempo de las pruebas, se alcanzan resultados
satisfactorios en cuando a la obtencin del cobre disuelto, ya que se consigue una
relacin directamente proporcional con el aumento del tiempo.
Para el proceso de lixiviacin por percolacin esttico, se observ un menor
consumo de cido, sin embargo el porcentaje de cobre present una disminucin
por lo que la eficiencia se atribuy baja.
La temperatura es relevante en el proceso de lixiviacin por agitacin, vindose
influenciado al aumento de la misma, disminuyendo el cido consumido durante el
ensayo, y aumenta el porcentaje de cobre disuelto,
El consumo de cido que se presenta por percolacin es parecido al conseguido por
agitacin, pero cabe resaltar que este procedimiento requiere un tiempo muy
extenso para obtener los resultados deseados, presentando as una velocidad de
reaccin menor y a su vez demostrando que su cintica es ms lenta comparada
con el proceso de agitacin.
El proceso de lixiviacin por percolacin genera una disminucin en los costos de
operacin, pero generando un aumento en el tiempo utilizado en la obtencin del
metal de inters.
OBSERVACIONES
Algunos parmetros a tener en cuenta en el momento de seleccionar un proceso de
lixiviacin que se adapte a las mejores condiciones para la recuperacin de un
material son el tamao de partcula, as como la altura del lecho de mineral, el ciclo
de lixiviacin, el consumo de cido, la ley del mineral y el consumo de agua.
UNIVERSIDAD INDUSTRIAL DE SANTANDER
LIXIVIACIN DE MINERALES POR AGITACIN Y PERCOLACIN
35
BIBLIOGRAFIA
DOMIC E; Hidrometalurgia. Fundamentos, Procesos y Aplicaciones;
Santiago de Chile, 2001
PEDRAZA, Julio Elas. Apuntes de clase de Metalrgia Extractiva II,
capitulo 5, lixiviacin de materiales.
http://es.scribd.com/doc/39872456/41/Lixiviacion-por-Agitacion
http://es.scribd.com/doc/39872456/40/Lixiviacion-por-percolacion
Das könnte Ihnen auch gefallen
- Informe Lixiviación Por Percolación, Agitación y Titulación. Universidad Industrial de Santander (Uis)Dokument41 SeitenInforme Lixiviación Por Percolación, Agitación y Titulación. Universidad Industrial de Santander (Uis)Heyler Sainn Ruiz100% (1)
- 08 Lixiviacion Por Agitacion PDFDokument24 Seiten08 Lixiviacion Por Agitacion PDFizars21Noch keine Bewertungen
- Reporte de Practica Lixiviacion Dinamica de Oro y PlataDokument8 SeitenReporte de Practica Lixiviacion Dinamica de Oro y Plataespirilo1659Noch keine Bewertungen
- Concentracion GravimetricaDokument42 SeitenConcentracion GravimetricaGera DiazNoch keine Bewertungen
- Los Minerales y Los Procesos de Concentracion Por FlotacionDokument30 SeitenLos Minerales y Los Procesos de Concentracion Por FlotacionEdwin Barboza DuranNoch keine Bewertungen
- Capitulo IIIDokument39 SeitenCapitulo IIINataniel LinaresNoch keine Bewertungen
- Hidrometalurgia Materia Segunda Prueba 2022Dokument66 SeitenHidrometalurgia Materia Segunda Prueba 2022Pauly IsidoraNoch keine Bewertungen
- Presentacion Lixiviacion en Pilas CuDokument21 SeitenPresentacion Lixiviacion en Pilas CumamutmutNoch keine Bewertungen
- 5 Cinetica y Variables Del Proceso de CianuracionDokument18 Seiten5 Cinetica y Variables Del Proceso de CianuracionYanella Smith Arevalo GonzalesNoch keine Bewertungen
- Flotacion de Oxidos y SilicatosDokument2 SeitenFlotacion de Oxidos y SilicatosFrancisco Tadeo Rodriguez Sanez100% (1)
- Articulo Termodinamica Lixiviacion Oro - En.esDokument15 SeitenArticulo Termodinamica Lixiviacion Oro - En.esJose MorenoNoch keine Bewertungen
- Cinetica de La Molienda y Analisis GranulometricoDokument9 SeitenCinetica de La Molienda y Analisis GranulometricoJHONNoch keine Bewertungen
- Plantas Concentradoras de Minerales PolimetalicosDokument4 SeitenPlantas Concentradoras de Minerales PolimetalicosDavid Rodriguez Remigio100% (2)
- Flotacion OxidosDokument6 SeitenFlotacion OxidosJessica ShepardNoch keine Bewertungen
- Análisis QuímicoDokument12 SeitenAnálisis QuímicoJackeline Jazmin Verastegui AlegriaNoch keine Bewertungen
- Inf de Hidro Lixiviacion de CobreDokument35 SeitenInf de Hidro Lixiviacion de CobreFiorelaRosarioJimenezLopezNoch keine Bewertungen
- Minerales de CobreDokument263 SeitenMinerales de Cobre72211537florNoch keine Bewertungen
- Investigacion CELDAS COMERCIALES DE FLOTACIÓNDokument9 SeitenInvestigacion CELDAS COMERCIALES DE FLOTACIÓNGabriela Leonor Avecillas AbadNoch keine Bewertungen
- Introducción y Lixiviación de Metales PreciososDokument44 SeitenIntroducción y Lixiviación de Metales PreciososRonald Alarcon RomaniNoch keine Bewertungen
- Cianicidas-Hidro 2Dokument19 SeitenCianicidas-Hidro 2Juan Diego Falcon ChuraNoch keine Bewertungen
- Preparacion Del Mineral y Pulpa para La FlotaciónDokument1 SeitePreparacion Del Mineral y Pulpa para La FlotaciónJonna HerreraNoch keine Bewertungen
- Balance ConcentraciónDokument18 SeitenBalance ConcentraciónJuanDi Moreno CalderónNoch keine Bewertungen
- Flotacion de OxidosDokument10 SeitenFlotacion de OxidosJhoelvis Choque100% (2)
- PB. Flotación de MineralesDokument43 SeitenPB. Flotación de MineralesDavid Velázquez100% (1)
- Beneficio de MineralesDokument40 SeitenBeneficio de MineralesMelissaNoch keine Bewertungen
- 16 Páginas PreliminaresDokument9 Seiten16 Páginas PreliminaresBrian100% (1)
- Determinación de Concentración de Iones Nitrato Por Espectrofotometría MolecularDokument8 SeitenDeterminación de Concentración de Iones Nitrato Por Espectrofotometría MolecularEymi Gianella Layza EscobarNoch keine Bewertungen
- Moliendabilidad - Cinetica de FlotacionDokument29 SeitenMoliendabilidad - Cinetica de FlotacionJose Pacheco100% (2)
- Tratamiento Metalurgico de MineralesDokument22 SeitenTratamiento Metalurgico de MineralesLILIANITACB100% (2)
- Informe Pruebas de Flotacion Bach - Reactivos STD Vs CYTECDokument6 SeitenInforme Pruebas de Flotacion Bach - Reactivos STD Vs CYTECJose Paolo Farfan DiazNoch keine Bewertungen
- Tratamiento MetalúrgicoDokument42 SeitenTratamiento MetalúrgicoChristian Joseph Encinas Yanarico0% (1)
- Capítulo 10 Separación Por Flotación Electroquímica de Minerales SulfuradosDokument25 SeitenCapítulo 10 Separación Por Flotación Electroquímica de Minerales SulfuradosBraulio ala andiaNoch keine Bewertungen
- Metalurgia ExtractivaDokument9 SeitenMetalurgia ExtractivaCesar AljuNoch keine Bewertungen
- Flotación Del Oro 1ER TrabajoDokument6 SeitenFlotación Del Oro 1ER TrabajoJoelMine100% (2)
- Fiq-Gpl-Pea-01 - Guía de Laboratorio Metalurgia IDokument87 SeitenFiq-Gpl-Pea-01 - Guía de Laboratorio Metalurgia IGabriela Acosta DeledesmaNoch keine Bewertungen
- 05 Uso de Colectores Cytec en Plantas de Flotación de Polimetálicos en La Minería de Bolivia - Luis Cuevas PetroquimDokument14 Seiten05 Uso de Colectores Cytec en Plantas de Flotación de Polimetálicos en La Minería de Bolivia - Luis Cuevas PetroquimdikoNoch keine Bewertungen
- Evaluación de Reactivos de FlotaciónDokument10 SeitenEvaluación de Reactivos de Flotaciónoskar0706Noch keine Bewertungen
- Lixiviacion en MineriaDokument21 SeitenLixiviacion en MineriaDeiby Michael Villalta Galvez100% (1)
- El Beneficio de Los Minerales de Oro en Ontario PDFDokument15 SeitenEl Beneficio de Los Minerales de Oro en Ontario PDFTimothy SmithNoch keine Bewertungen
- Cinetica de La CianuracionDokument6 SeitenCinetica de La CianuracionJulia Marina Constantino SaavedraNoch keine Bewertungen
- Cinetica MetalurgicaDokument16 SeitenCinetica MetalurgicaAlcajer Miguel Alarcon EspinozaNoch keine Bewertungen
- Caracterización de MineralesDokument87 SeitenCaracterización de MineralesJimenez AtencioNoch keine Bewertungen
- Tesis de Molienda de Minerales PDFDokument189 SeitenTesis de Molienda de Minerales PDFChristy Estrada100% (2)
- Informe Lixiviacion AgitadaDokument27 SeitenInforme Lixiviacion AgitadaRaúl Alejandro Pérez MoralesNoch keine Bewertungen
- Descripcion General Del Proceso MetalurgicoDokument10 SeitenDescripcion General Del Proceso MetalurgicoRicardoMoranNoch keine Bewertungen
- Practica de Concentracion de Minerales IDokument48 SeitenPractica de Concentracion de Minerales IFlor Elizabeth Fernandez Ramos100% (1)
- Minería Del OroDokument14 SeitenMinería Del OroDanessi RomeroNoch keine Bewertungen
- Diagrama de Flujo Planta Marta - DIGESA 2Dokument10 SeitenDiagrama de Flujo Planta Marta - DIGESA 2carlos753100% (1)
- Preparacion de ReactivosDokument5 SeitenPreparacion de ReactivosFranz PalaciosNoch keine Bewertungen
- Analisis de Minerales 2017Dokument64 SeitenAnalisis de Minerales 2017Ludwin Salazar ValdiviaNoch keine Bewertungen
- Las Pilas de LixiviaciónDokument15 SeitenLas Pilas de LixiviaciónElisabeth Barraza0% (1)
- Lixiviacion Por AgitacionDokument36 SeitenLixiviacion Por AgitacionFelipeDeejayValenzuelaNoch keine Bewertungen
- N 04lixiviación de Minerales de Oxido de Cobre YeisonDokument18 SeitenN 04lixiviación de Minerales de Oxido de Cobre YeisonAlex Joel Paredes LeyvaNoch keine Bewertungen
- AGITACIÓNDokument26 SeitenAGITACIÓNsantos28Noch keine Bewertungen
- Experimento 4 - Lixiviacion AgitacionDokument5 SeitenExperimento 4 - Lixiviacion AgitacionNandeiro1591Noch keine Bewertungen
- Practica 1 - Procesos Extractivos ESIQIEDokument7 SeitenPractica 1 - Procesos Extractivos ESIQIEVictor Ambriz100% (2)
- Taller MetalúrgicoDokument10 SeitenTaller MetalúrgicoCarla Jazmin Ventura GagoNoch keine Bewertungen
- 6to Informe de Mineria y Medio AmbienteDokument12 Seiten6to Informe de Mineria y Medio Ambienteelvis santivañezNoch keine Bewertungen
- LixiviacionDokument6 SeitenLixiviacionKevin SimentalNoch keine Bewertungen
- Practica 5Dokument10 SeitenPractica 5MARIA DEL PILAR VILCHEZ MOLINANoch keine Bewertungen
- Tecnicas Recuperacion Suelos DosDokument109 SeitenTecnicas Recuperacion Suelos DosYCaroline86Noch keine Bewertungen
- Guia para Evaluar EIAs de Proyectos MinerosDokument132 SeitenGuia para Evaluar EIAs de Proyectos MinerosGino RománNoch keine Bewertungen
- 6th Central Pay Commission Salary CalculatorDokument15 Seiten6th Central Pay Commission Salary Calculatorrakhonde100% (436)
- Recuperación de Oro Desde Soluciones Cianuradas Tecnología Del Carbón ActivadoDokument6 SeitenRecuperación de Oro Desde Soluciones Cianuradas Tecnología Del Carbón ActivadoashbyNoch keine Bewertungen
- Manual Gestion AmbientalDokument0 SeitenManual Gestion Ambientaljoko.lomejorNoch keine Bewertungen
- Guia Tec Operacion Dep RelavesDokument42 SeitenGuia Tec Operacion Dep Relavessnarf273Noch keine Bewertungen
- 7mo Trabajo Medio AmbienteDokument11 Seiten7mo Trabajo Medio AmbienteAventur2014Noch keine Bewertungen
- Cierre AbandonoDokument37 SeitenCierre AbandonoBajoneando A Las PersonasNoch keine Bewertungen
- Tema2 Restauracion de Espacios Degradados Por Las Actividades ExtractivasDokument51 SeitenTema2 Restauracion de Espacios Degradados Por Las Actividades ExtractivasashbyNoch keine Bewertungen
- 1734GPGBiodiversity SpanishDokument172 Seiten1734GPGBiodiversity SpanishIvan MoralesNoch keine Bewertungen
- Guia Minero AmbientalDokument109 SeitenGuia Minero AmbientalEdwin Negrette HernandezNoch keine Bewertungen
- Capitulo4 Mineria de Lixiviacion en Vertederos (Dump Leaching)Dokument8 SeitenCapitulo4 Mineria de Lixiviacion en Vertederos (Dump Leaching)ashbyNoch keine Bewertungen
- Tecnologias Limpias en Industrias ExtractivasDokument338 SeitenTecnologias Limpias en Industrias Extractivasmenino13Noch keine Bewertungen
- Empresa y Medio AmbienteDokument40 SeitenEmpresa y Medio AmbienteashbyNoch keine Bewertungen
- Capitulo 9Dokument0 SeitenCapitulo 9Mauricio CruzNoch keine Bewertungen
- 5to Trabajo Medio Ambiente Mineria en El PerúDokument4 Seiten5to Trabajo Medio Ambiente Mineria en El PerúashbyNoch keine Bewertungen
- 3er Trabajo Medio Ambiente Mineria en El PerúDokument7 Seiten3er Trabajo Medio Ambiente Mineria en El PerúashbyNoch keine Bewertungen
- Hidrometalurgia I O. BenaventeDokument105 SeitenHidrometalurgia I O. Benaventejamie04100% (10)
- Metalurgia Ciencia de Hoy, Arte Del PasadoDokument7 SeitenMetalurgia Ciencia de Hoy, Arte Del PasadoashbyNoch keine Bewertungen
- 1er Trabajo Medio Ambiente Mineria PeruDokument4 Seiten1er Trabajo Medio Ambiente Mineria PeruashbyNoch keine Bewertungen
- Capitulo 8Dokument9 SeitenCapitulo 8MTR0644Noch keine Bewertungen
- Procesos Hidrometalúrgicos en La Mineria Del Oro, Plata, Cobre y Uranio - Lixiviación de Minerales de Oro y Plata, Cap7 23pDokument23 SeitenProcesos Hidrometalúrgicos en La Mineria Del Oro, Plata, Cobre y Uranio - Lixiviación de Minerales de Oro y Plata, Cap7 23pIvanCruzNoch keine Bewertungen
- Procesos Hidrometalúrgicos en La Mineria Del Oro, Plata, Cobre y Uranio - Minería de Lixiviación en Eras o Pilas, Cap5 10pDokument10 SeitenProcesos Hidrometalúrgicos en La Mineria Del Oro, Plata, Cobre y Uranio - Minería de Lixiviación en Eras o Pilas, Cap5 10pIvanCruzNoch keine Bewertungen
- 2do Trabajo Medio Ambiente Mineria PeruDokument4 Seiten2do Trabajo Medio Ambiente Mineria PeruashbyNoch keine Bewertungen
- Capitulo10 Lixiviacion de Minerales de UranioDokument21 SeitenCapitulo10 Lixiviacion de Minerales de UranioashbyNoch keine Bewertungen
- Capitulo2 Sistemas de Mineria Por LixiviacionDokument3 SeitenCapitulo2 Sistemas de Mineria Por LixiviacionashbyNoch keine Bewertungen
- Capitulo 3Dokument2 SeitenCapitulo 3MTR0644Noch keine Bewertungen
- Como Produce CuDokument6 SeitenComo Produce CujuanfrienNoch keine Bewertungen
- Capitulo1 Procesos Hidrometalurgicos en La Mineria de Oro, Plata, Cobre y UranioDokument13 SeitenCapitulo1 Procesos Hidrometalurgicos en La Mineria de Oro, Plata, Cobre y Uranioashby100% (4)
- HIDROMETALURGIA Fundamentos Procesos y AplicacionesDokument15 SeitenHIDROMETALURGIA Fundamentos Procesos y AplicacionesAlice94% (16)