Beruflich Dokumente
Kultur Dokumente
Ejercicios Gases
Hochgeladen von
Rosario QF0 Bewertungen0% fanden dieses Dokument nützlich (0 Abstimmungen)
91 Ansichten1 SeiteGases
Originaltitel
Ejercicios gases
Copyright
© © All Rights Reserved
Verfügbare Formate
DOCX, PDF, TXT oder online auf Scribd lesen
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenGases
Copyright:
© All Rights Reserved
Verfügbare Formate
Als DOCX, PDF, TXT herunterladen oder online auf Scribd lesen
0 Bewertungen0% fanden dieses Dokument nützlich (0 Abstimmungen)
91 Ansichten1 SeiteEjercicios Gases
Hochgeladen von
Rosario QFGases
Copyright:
© All Rights Reserved
Verfügbare Formate
Als DOCX, PDF, TXT herunterladen oder online auf Scribd lesen
Sie sind auf Seite 1von 1
1.
2.
3.
4.
5.
6.
Una muestra de 100ml de gas seco medido a 20C y a 750mmHg ocupa un
volumen de 104ml cuando se recogi sobre agua a 25C y 750mmHg. Calcular:
a) La presin de vapor de agua a 25C
b) La humedad relativa del gas.
La presin de vapor del agua a 25C es 23,75mmHg
Aire a 20C y 1 atm con una humedad relativa del 80%, se comprime dentro de
un tanque de 1000lotros de capacidad a una presin de 6atm la temperatura se
eleva a 25C. La presin de vapor de agua a 20C es 17,5mmHg y a 25C es
23,8mmHg. Aplicando la ley de los gases perfectos y despreciando el volumen
de agua que se condensa dentro del tanque, calcule la masa de la misma.
Suponiendo que el aire seco contiene 77% de nitrgeno y 21% de oxgeno en
volumen calcular la densidad del aire hmedo a 25C y a 1atm, cuando la
=60%. El vapor de agua tiene una presin de 23,76mmHga dicha temperatura.
Suponiendo que el aire seco contiene 75% de N2 y el resto de O2 (en peso).
Calcular la densidad del aire hmedo a 25C, Patm=300mmHg; Pv*=25mmHg;
h=200mmHg
Se tiene aire a 20C y 1atm, con una humedad relativa del 60%, se comprime
dentro de un tanque de 1000litros de capacidad a una presin de 6atm; la
temperatura se eleva a 25C, la presin de vapor del agua a 20C y 25C
respectivamente es 17,5mmHg y 23,8mmHg. Aplicando la ley de los gases
ideales y despreciando el volumen del agua que se condensa dentro del tanque,
calcular el peso de la misma.
100 litros de aire a 20C y presin de 1013,25 milibares, se hacen burbujear
lentamente a travs de ter etlico. El aire saturado de vapor de ter sa le a 20C
y a la misma presin, calcular:
a) Los gramos de ter que se evaporan
b) el volumen final de mezcla
c) si la mezclas e comprime isotrmicamente a 10132,5 milibares, la cantidad de
ter que se recupera de nuevo al estado lquido. La presin de vapor de ter a
20C es 422 mmHg. Suponer despreciable el volumen de ter lquido formado
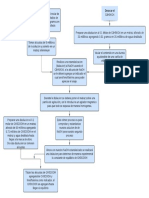
7. En el laboratorio de Quimica de la Facultad de Ingenieria de la UMSA se
recoge 2,7mg de H2 sobre agua. Luego el sistema se estabiliza a 25C de
acuerdo con la figura, en la cual h es 30cm. Si el volumen ocupado por el gas es
de 50cm3, calcular:
a) La fraccin molar del hidrogeno
b) la densidad del gas hmedo
c) La humedad relativa del sistema
d) La humedad absoluta La presin de vapor a 25C es de 23,76mmHg
1.
2.
3.
4.
5.
6.
Una muestra de 100ml de gas seco medido a 20C y a 750mmHg ocupa un
volumen de 104ml cuando se recogi sobre agua a 25C y 750mmHg. Calcular:
a) La presin de vapor de agua a 25C
b) La humedad relativa del gas.
La presin de vapor del agua a 25C es 23,75mmHg
Aire a 20C y 1 atm con una humedad relativa del 80%, se comprime dentro de
un tanque de 1000lotros de capacidad a una presin de 6atm la temperatura se
eleva a 25C. La presin de vapor de agua a 20C es 17,5mmHg y a 25C es
23,8mmHg. Aplicando la ley de los gases perfectos y despreciando el volumen
de agua que se condensa dentro del tanque, calcule la masa de la misma.
Suponiendo que el aire seco contiene 77% de nitrgeno y 21% de oxgeno en
volumen calcular la densidad del aire hmedo a 25C y a 1atm, cuando la
=60%. El vapor de agua tiene una presin de 23,76mmHga dicha temperatura.
Suponiendo que el aire seco contiene 75% de N2 y el resto de O2 (en peso).
Calcular la densidad del aire hmedo a 25C, Patm=300mmHg; Pv*=25mmHg;
h=200mmHg
Se tiene aire a 20C y 1atm, con una humedad relativa del 60%, se comprime
dentro de un tanque de 1000litros de capacidad a una presin de 6atm; la
temperatura se eleva a 25C, la presin de vapor del agua a 20C y 25C
respectivamente es 17,5mmHg y 23,8mmHg. Aplicando la ley de los gases
ideales y despreciando el volumen del agua que se condensa dentro del tanque,
calcular el peso de la misma.
100 litros de aire a 20C y presin de 1013,25 milibares, se hacen burbujear
lentamente a travs de ter etlico. El aire saturado de vapor de ter sa le a 20C
y a la misma presin, calcular:
a) Los gramos de ter que se evaporan
b) el volumen final de mezcla
c) si la mezclas e comprime isotrmicamente a 10132,5 milibares, la cantidad de
ter que se recupera de nuevo al estado lquido. La presin de vapor de ter a
20C es 422 mmHg. Suponer despreciable el volumen de ter lquido formado
7. En el laboratorio de Quimica de la Facultad de Ingenieria de la UMSA se
recoge 2,7mg de H2 sobre agua. Luego el sistema se estabiliza a 25C de
acuerdo con la figura, en la cual h es 30cm. Si el volumen ocupado por el gas es
de 50cm3, calcular:
a) La fraccin molar del hidrogeno
b) la densidad del gas hmedo
c) La humedad relativa del sistema
d) La humedad absoluta La presin de vapor a 25C es de 23,76mmHg
Das könnte Ihnen auch gefallen
- Cuestionario P-4 GasesDokument3 SeitenCuestionario P-4 Gasesdraggus0% (2)
- Practica de EstequiometriaDokument2 SeitenPractica de EstequiometriaCarlos Delafuente100% (1)
- Tubo de RubensDokument11 SeitenTubo de RubensJesurun BlablaNoch keine Bewertungen
- Práctica 4. Presión de Vapor ReidDokument5 SeitenPráctica 4. Presión de Vapor Reidlidia gómezNoch keine Bewertungen
- Estequiometria Problemas 02Dokument1 SeiteEstequiometria Problemas 02andres_old_condeNoch keine Bewertungen
- EX PARCIAL QU114 2005 2aDokument1 SeiteEX PARCIAL QU114 2005 2aLuis Fernando Chalco RamosNoch keine Bewertungen
- Taller Nomenclatura.Dokument2 SeitenTaller Nomenclatura.Jose Manuel Casadiegos Rojas100% (1)
- NomenclaturaDokument24 SeitenNomenclaturaSuzel Iveth Ábrego100% (1)
- Practico4 2015Dokument2 SeitenPractico4 2015Carlos A. Diaz100% (1)
- Otros ExamnesDokument9 SeitenOtros ExamnesEliseo FloresNoch keine Bewertungen
- Practica 2do Parcial-1Dokument5 SeitenPractica 2do Parcial-1CristhianAlvarez100% (1)
- Guia GasesDokument7 SeitenGuia GasessonybrunNoch keine Bewertungen
- Secme 29297Dokument37 SeitenSecme 29297Darlyz Gonzalez Rosas100% (1)
- Laboratorio de HidrocarburosDokument24 SeitenLaboratorio de HidrocarburosCristian Joel Saco CardenasNoch keine Bewertungen
- Ejercicios Tema 5. Química GeneralDokument5 SeitenEjercicios Tema 5. Química GeneralPablo Molero MartínNoch keine Bewertungen
- Determinación Experimental de La Constante de Equilibrio Del Ácido Acético.Dokument1 SeiteDeterminación Experimental de La Constante de Equilibrio Del Ácido Acético.ckireNoch keine Bewertungen
- Guia de Ejercicios GasesDokument2 SeitenGuia de Ejercicios GasesVeronica Yoko MoralesNoch keine Bewertungen
- EJERCICIOS DE FORMULACIÓN INORGÁNICA para EntregarDokument15 SeitenEJERCICIOS DE FORMULACIÓN INORGÁNICA para EntregarDamian Yarahel Contreras Martinez100% (1)
- Ejercicios Nomenclatura InorganicaDokument9 SeitenEjercicios Nomenclatura InorganicaInes HuamaníNoch keine Bewertungen
- Problema GasesDokument2 SeitenProblema GasesRCNoch keine Bewertungen
- Soluc SchaumDokument81 SeitenSoluc SchaumDuvan GutierrezNoch keine Bewertungen
- Informe Porcentaje de Oxígeno en El Bromato de PotasioDokument13 SeitenInforme Porcentaje de Oxígeno en El Bromato de Potasioleidy alvarez100% (1)
- 2do Parcial Examen de Petroquimica II PDFDokument2 Seiten2do Parcial Examen de Petroquimica II PDFDaniel fernando VillalobosNoch keine Bewertungen
- Guia - de - Ejercicios Cientifico - El - Estado - Gaseoso - IiDokument9 SeitenGuia - de - Ejercicios Cientifico - El - Estado - Gaseoso - IiJoselo MamaniNoch keine Bewertungen
- Informe Tubo de RubensDokument6 SeitenInforme Tubo de RubensDanisNoch keine Bewertungen
- Taller Área y Volumen de Solido 2Dokument1 SeiteTaller Área y Volumen de Solido 2moises mosquera quinteroNoch keine Bewertungen
- Tarea Preparatoria FinalDokument7 SeitenTarea Preparatoria FinalAdrian EstebanNoch keine Bewertungen
- Practica de Quimica FinalDokument7 SeitenPractica de Quimica FinalReynaldo Suarez LimaNoch keine Bewertungen
- Taller - 11 - Reacciones QuimicasDokument3 SeitenTaller - 11 - Reacciones QuimicasAndrea BaqueroNoch keine Bewertungen
- QMC 100 Cuestionario 2020 1 para 1er Parcial-2Dokument9 SeitenQMC 100 Cuestionario 2020 1 para 1er Parcial-2Jhonatan Erwin Nina ValenciaNoch keine Bewertungen
- Práctica Celda de DaniellDokument8 SeitenPráctica Celda de DanielllasisolNoch keine Bewertungen
- Gases Ideales y Gases Húmedos Ejercicios Grupo AlfaDokument3 SeitenGases Ideales y Gases Húmedos Ejercicios Grupo AlfaAlejandro VasquezNoch keine Bewertungen
- Reacciones de AlquenosDokument6 SeitenReacciones de AlquenosAguila PaulNoch keine Bewertungen
- Examen Parcial de Fisicoquímica 1 (Teoría) UNMSM - IQDokument2 SeitenExamen Parcial de Fisicoquímica 1 (Teoría) UNMSM - IQAyudaFIQ-SMNoch keine Bewertungen
- Taller de Gases IdealesDokument3 SeitenTaller de Gases IdealesL. TNoch keine Bewertungen
- Ejercicios de Equilibrio QuimicoDokument37 SeitenEjercicios de Equilibrio QuimicoAngel BaronNoch keine Bewertungen
- Densidad de Gases090309Dokument5 SeitenDensidad de Gases090309Alfonso RiveraNoch keine Bewertungen
- Calor y Dilatacic3b3n TermicaDokument17 SeitenCalor y Dilatacic3b3n Termicasergio menco arizaNoch keine Bewertungen
- Ejercicios Sobre Densidad Temperatura y PresionDokument6 SeitenEjercicios Sobre Densidad Temperatura y PresionRuth BanegasNoch keine Bewertungen
- Ejercicios Ley General Del Estado GaseosoDokument5 SeitenEjercicios Ley General Del Estado GaseosoMARIO ANDRES REYES GONZALEZNoch keine Bewertungen
- Taller EstequiometriaDokument2 SeitenTaller EstequiometriaAlexander OliverosNoch keine Bewertungen
- Informe Cationes II GrupoDokument16 SeitenInforme Cationes II GrupoMax Bryan Rodriguez GarciaNoch keine Bewertungen
- Acetona ProcesoDokument2 SeitenAcetona ProcesoJesus Manuel Yallerco VenegasNoch keine Bewertungen
- Materia Auxiliar:: Ii (Teoría) Univ. Miguel Angel Laime TancaraDokument2 SeitenMateria Auxiliar:: Ii (Teoría) Univ. Miguel Angel Laime TancaraMARITZA QUISPE VILLARREALNoch keine Bewertungen
- Banco de Preguntas 2do Parcial Lab de Quimica Ing QuimicaDokument11 SeitenBanco de Preguntas 2do Parcial Lab de Quimica Ing QuimicaAntonio TorresNoch keine Bewertungen
- Quimica Inorganica Complejos 1ra ParteDokument90 SeitenQuimica Inorganica Complejos 1ra Partedaniela estefiNoch keine Bewertungen
- Plan Global Umss Refinacion Del PetroleoDokument12 SeitenPlan Global Umss Refinacion Del PetroleobetomltvNoch keine Bewertungen
- Sem10 - Ses 20 - Mezcla de GasesDokument21 SeitenSem10 - Ses 20 - Mezcla de GasesEdson Edu Ramirez DiazNoch keine Bewertungen
- Capitulo 24-Tarea de API 62 EjerciciosDokument24 SeitenCapitulo 24-Tarea de API 62 EjerciciosJeyson Dueñas Porras100% (2)
- Identificacion de Compuestos OrganicosDokument20 SeitenIdentificacion de Compuestos OrganicosKenia ManzanoNoch keine Bewertungen
- Problemas de Gases Ideales PREGUNTASDokument11 SeitenProblemas de Gases Ideales PREGUNTASIng Ronald PortalesNoch keine Bewertungen
- VII GasesDokument1 SeiteVII GasesMaria Laura Villarroel MurilloNoch keine Bewertungen
- 6 INFORME - Calor de Combustión...Dokument17 Seiten6 INFORME - Calor de Combustión...Anderson Alejandro Benites ZelayaNoch keine Bewertungen
- PRACTICA N.1docx PDFDokument3 SeitenPRACTICA N.1docx PDFBeymar ContrerasNoch keine Bewertungen
- CineticaDokument4 SeitenCineticaLupita Alavez100% (1)
- Determinacion de NitratosDokument8 SeitenDeterminacion de NitratosHVVa100% (1)
- Estado GaseosoDokument176 SeitenEstado GaseosoJesusAlejandroNoch keine Bewertungen
- Gases HumedosDokument1 SeiteGases Humedoscesar marcaNoch keine Bewertungen
- Guia 3 QuimicaDokument5 SeitenGuia 3 Quimicaflores.11060408Noch keine Bewertungen
- Guia de XRD: Botón Frontal de Encendido de Fuente de Rayos-XDokument2 SeitenGuia de XRD: Botón Frontal de Encendido de Fuente de Rayos-XRosario QFNoch keine Bewertungen
- T 05 OcwDokument72 SeitenT 05 OcwRosario QFNoch keine Bewertungen
- Ciclos MaquinasDokument16 SeitenCiclos MaquinasRosario QFNoch keine Bewertungen
- ElectronicaDokument9 SeitenElectronicaRosario QFNoch keine Bewertungen
- Aproximaciones Lineales de Sistemas FisicosDokument4 SeitenAproximaciones Lineales de Sistemas FisicosRosario QFNoch keine Bewertungen
- Cartilla Ultimo 2021Dokument21 SeitenCartilla Ultimo 2021Rosario QFNoch keine Bewertungen
- DensidadesDokument2 SeitenDensidadesRosario QFNoch keine Bewertungen
- Precipitación PHDokument5 SeitenPrecipitación PHantonioNoch keine Bewertungen
- Taller Carbohidratos BQ 2022Dokument4 SeitenTaller Carbohidratos BQ 2022Stephani Valencia florezNoch keine Bewertungen
- Cap1-Procesos de Produccion y Manejo de HidrocarburosDokument44 SeitenCap1-Procesos de Produccion y Manejo de HidrocarburosJulio César Sastré de DiosNoch keine Bewertungen
- 1er Avanse-ARTICULO REV. DE LIT - de Escoria de Hornos de Fundicio de AfirmadosDokument13 Seiten1er Avanse-ARTICULO REV. DE LIT - de Escoria de Hornos de Fundicio de Afirmadosjeankarlos charcapeNoch keine Bewertungen
- BiodigestorDokument8 SeitenBiodigestorAbad AriadnaNoch keine Bewertungen
- Peracet 101Dokument12 SeitenPeracet 101didi2805Noch keine Bewertungen
- Catalogo Institucional 2019Dokument15 SeitenCatalogo Institucional 2019Ernesto Alonso Carballo BenavidesNoch keine Bewertungen
- Previo 4 M-NitroanilinaDokument5 SeitenPrevio 4 M-NitroanilinaAlan100% (3)
- Evaporador FlashDokument16 SeitenEvaporador FlashVictorNoch keine Bewertungen
- Exposición LADBE Omar Landeta DomínguezDokument7 SeitenExposición LADBE Omar Landeta DomínguezLaloNoch keine Bewertungen
- Estabilización de Suelo Unidad IIDokument28 SeitenEstabilización de Suelo Unidad IIVictor Alfonso LaraNoch keine Bewertungen
- F2 - S14 - PPT - Trasferencia de CalorDokument23 SeitenF2 - S14 - PPT - Trasferencia de CalorLuis Tamay LópezNoch keine Bewertungen
- Experimentos CaserosDokument7 SeitenExperimentos CaserosJose CutipaNoch keine Bewertungen
- Biofiltro para GasesDokument4 SeitenBiofiltro para GasesAngel AlmanzaNoch keine Bewertungen
- FICHA AMPLIACION T 2 Detective de Las SustanciasDokument2 SeitenFICHA AMPLIACION T 2 Detective de Las Sustanciasmelirod79Noch keine Bewertungen
- Trabajo Practico Modelos AtómicosDokument1 SeiteTrabajo Practico Modelos AtómicosMiguel FerreiraNoch keine Bewertungen
- Campos de Estudio de La BiologíaDokument5 SeitenCampos de Estudio de La BiologíaXiomara Ortega BetancoNoch keine Bewertungen
- El FraguadoDokument10 SeitenEl FraguadoEJoelMozoLNoch keine Bewertungen
- El Estado InestableDokument26 SeitenEl Estado Inestablecarmelita_star0% (1)
- Clorodifluorometano: Nombre QuímicoDokument26 SeitenClorodifluorometano: Nombre Químicodnl gattoNoch keine Bewertungen
- Estudios Sobre Suelos Dpto de Lavalle, Mendoza, ArgentinaDokument38 SeitenEstudios Sobre Suelos Dpto de Lavalle, Mendoza, ArgentinajorgeNoch keine Bewertungen
- Respiración QuímicaDokument10 SeitenRespiración QuímicaSara SaviNoch keine Bewertungen
- Presentación Viaker AEROPUERTOSDokument27 SeitenPresentación Viaker AEROPUERTOSGERARDO100% (1)
- Catalizador Macropoxy 646 Coaltar 388Dokument4 SeitenCatalizador Macropoxy 646 Coaltar 388Closet de MayteNoch keine Bewertungen
- Ejrcicios 7.11 y 7.13Dokument7 SeitenEjrcicios 7.11 y 7.13YANIDED MILAGROS GENESIS VALLADOLID GIRONNoch keine Bewertungen
- Calculo Termico y Balance Energetico Del MotorDokument43 SeitenCalculo Termico y Balance Energetico Del MotorZhalom Chiclayo CuzcoNoch keine Bewertungen
- Examen Inricaba 2018Dokument2 SeitenExamen Inricaba 2018Diego Fierro100% (3)
- ASTM A450 Tubes PDFDokument10 SeitenASTM A450 Tubes PDFhdierkeNoch keine Bewertungen
- Fichas de SeguridadDokument31 SeitenFichas de SeguridadSussan VillamizarNoch keine Bewertungen
- Proyecto Final de Medio AmbienteDokument10 SeitenProyecto Final de Medio AmbienteKarlita Macarena Farías GuerraNoch keine Bewertungen