Beruflich Dokumente
Kultur Dokumente
RMN 2014
Hochgeladen von
Leydi Jhoana Garcia CardenasCopyright
Verfügbare Formate
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
Verfügbare Formate
RMN 2014
Hochgeladen von
Leydi Jhoana Garcia CardenasCopyright:
Verfügbare Formate
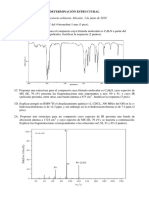
Qumica Orgnica II
Gua de estudio Tema 1: RMN - EM
Tema 1: INTRODUCCIN AL EMPLEO DE TCNICAS ESPECTROSCPICAS
PARA LA DILUCIDACIN DE ESTRUCTURAS ORGNICAS.
1. Usando los datos de la siguiente tabla que ilustra el efecto de la electronegatividad del
heterotomo sustituyente sobre el desplazamiento qumico de protones indique:
1
2
3
4
5
6
7
8
9
* Por definicin
CH3F
CH3Cl
CH3Br
CH3I
CH2Cl2
CHCl3
CH3CCl3
(CH3)4C
(CH3)4Si
4,26 ppm
3,05 ppm
2,68 ppm
2,16 ppm
5,30 ppm
7,27 ppm
2,70 ppm
0,86 ppm
0,00 ppm*
a) Cmo vara el desplazamiento qumico de los protones, en los compuestos 1 a 4,
con la electronegatividad del halgeno?
b) Cmo vara el desplazamiento qumico con el nmero de halgenos vecinos, en
los compuestos 2, 5 y 6?
c) Comparando los compuestos 6 y 7, establecer cmo se modifica el corrimiento
qumico de un protn con la distancia de un tomo electronegativo.
d) Explique por qu (CH3)4Si absorbe a campos ms altos (desplazamiento qumico
ms bajo) que cualquier otra molcula de la Tabla. Podra imaginar una molcula
cuyos protones tengan un desplazamiento qumico a campos ms altos que el TMS,
es decir un valor negativo de ?
2. Cuntas seales de absorcin RMN 1H se observaran en el espectro de los siguientes
compuestos?
a) Bromuro de t-butilo
b) (CH3)3C-CCl(CH3)2
c) 2-cloro-2-metoxipropano
3. Dadas las siguientes frmulas moleculares determinar el grado de instauraciones (n de
instauraciones y/o anillos):
N= [ i ni (vi-2) ] + 2
2
Donde, ni es la cantidad de cada tomo
vi es el nmero de valencia de cada tomo
a. C6H12O; b. C6H10O; c. C6H8O2; d. C4H8O2; e. C2H3N; f. C7H8O y g. C6H5NO2
Qumica Orgnica II
Gua de estudio Tema 1: RMN - EM
4. Un compuesto desconocido de frmula molecular C5H11Br tiene un espectro 1H RMN
consistente en dos lneas, una a 1,01 ppm (integral relativa 4,5) y la otra a
3,17 ppm (integral relativa 1). Proponga la estructura de ese compuesto.
5. Proponer la estructura de los compuestos que responde a los siguientes datos:
a) Un compuesto C7H15Cl tiene dos seales RMN 1H a 1,08 y 1,59 con integracin
relativa 3:2.
b) Un compuesto C5H9Cl3 tiene tres seales RMN 1H a 1,99; 4,31 y 6,55 con
integracin relativa 6:2:1.
6. Prediga el espectro 1H RMN de CH3CHCl2, analizando el modelo de multiplicidad para
una serie equivalente de protones a en presencia de tres protones equivalentes adjuntos b.
Incluya un anlisis de la intensidad relativa de cada lnea del modelo de particin. Asuma
que las constantes de acoplamiento son aproximadamente las mismas que las encontradas
en el bromuro de etilo.
7. Predecir el espectro 1H RMN de los siguientes compuestos:
a) (CH3)2 CH-I
b) Cl2CH-CH2-Cl
c) Cl-CH2-C(CH3)2Cl
d) CH3-O-CH2-CH2-CH2-O-CH3
8. Proponer la estructura de un compuesto C4H8Cl2 con el siguiente espectro
1
H RMN: 1,60 (3H, d, J= 7,5 Hz); 2,15 (2H, c, J=7,5 Hz); 3,72 ( 2H, t, J=7,5 Hz); 4,27
(1H, sexteto, J=7,5 Hz).
9.
Proponer la estructura para los siguientes compuestos:
a) C3H7Br, 1H RMN: 1,03 (3H, t, J=7 Hz); 1,88 (2H, sexteto, J=7 Hz); 3,40 (2H, t,
J=7 Hz).
b) C2H3Cl3, 1H RMN: 3,98 (2H, d, J=7 Hz); 5,87 (1H, t, J=7 Hz).
c) C5H8Br4, 1H RMN: 3,36 (s, la nica lnea del espectro).
Qumica Orgnica II
Gua de estudio Tema 1: RMN - EM
10. El siguiente diagrama corresponde a la simulacin de un espectro de 1H RMN de un
compuesto de frmula molecular C10H12O2
a) Ignorando la seal del TMS a = 0, cuntos grupos de seales hay en el espectro?
b) Cul es la multiplicidad (s, d, t, c, q) de la seal ms apantallada del espectro?
c) Qu unidad estructural corresponde al singulete a = 3.8 ppm?
A) CH3C=O B) CH2 C) OH D) OCH3 E) CCH3 F) C=CH
d) A partir de la separacin de las lneas (J), qu seal est acoplada con el cuarteto a = 2.9
ppm? A) = 1.2 ppm B) = 3.8 ppm C) = 6.9 ppm D) = 7.9 ppm
e) Utilizando el trazo de integracin y la frmula molecular, asigne un nmero entero de
protones a cada una de las seales que se indican a continuacin:
7.9 ppm; 6.9 ppm; 3.8 ppm; 2.9 ppm; 1.2 ppm
g) Proponer una estructura para el compuesto.
11. Cuando 3-bromo-1-propeno se deja reaccionar con HBr, en presencia de perxidos, se
forma un compuesto A, que tiene el siguiente espectro RMN 1H: 3,60 (4H, t, J=6 Hz);
1,38 (2H, quinteto, J=6 Hz). Teniendo en cuenta la reaccin:
a) Qu estructura esperaras para el producto A? Utiliza el espectro 1H RMN para
confirmar o refutar tu hiptesis.
Qumica Orgnica II
Gua de estudio Tema 1: RMN - EM
12. Imagina que en tu mesada de laboratorio existen dos frascos rotulados como ismeros
C4H9Br que contienen una sustancia lquida incolora. El espectro de 1H RMN del
compuesto A se presenta como un singulete a 1,63, y el espectro 1H RMN del
compuesto B se diagrama a continuacin. Qu estructura esperara para los productos A y
B?
13. Un hidrocarburo insaturado de frmula molecular C8H14 presenta el siguiente espectro
de 1H RMN. Proponer una estructura para l. La molcula presenta un plano de
simetra.
14. Dos ismeros de un compuesto de frmula molecular C3H5OCl, presentan en sus
espectros de 1H RMN tres seales: un singulete que integra para tres hidrgenos entre 3,5
y 4 ppm y sendos dobletes que integran cada uno para un hidrgeno entre 5 y 6,5 ppm. Al
amplificar esta zona se pudo observar que para ismero A la constante de acoplamiento
era de 7,0 Hz, mientras que para el ismero B era de 13,1 Hz. Proponer la estructura de
ambos compuestos.
Qumica Orgnica II
Gua de estudio Tema 1: RMN - EM
15. Un compuesto de frmula molecular C5H10O presenta el siguiente espectro de 1H RMN
Mientras que otro de formula molecular C7H14O con propiedades fsico-qumicas muy
similares responde al espectro
Proponer la estructura de ambos compuestos carbonlicos y dar una explicacin de
porqu en el segundo caso las seales a 1,3 y 1,58 se observan tan distorsionadas.
16. Proponer la estructura de una molcula oxigenada que posee cuatro tomos de carbono,
que presenta en su espectro IR una notable banda de estiramiento -OH (3339 cm-1) y
responde al siguiente espectro de 1H RMN.
Qumica Orgnica II
Gua de estudio Tema 1: RMN - EM
17. En qu solucin el protn del grupo hidroxilo de etanol se presenta como un triplete? A)
Etanol absoluto; B) Etanol 0,2M en Cl4C. Fundamenta tu respuesta.
18. Los siguientes espectros de 1H RMN corresponden a un par compuestos saponificables
que como caracterstica ms notable de sus espectros IR presentan una banda en la zona de
1740 cm-1 atribuible a sendos estiramientos C=O. Proponer la estructura de ambos compuestos
sabiendo que sus frmula moleculares son C4H8O2 y C5H10O2.
19. Inequvocamente los siguientes espectros de 1H RMN corresponden a dos aldehdos como
lo indica la presencia de los singuletes que se observan en zonas de campos bajos (alrededor
de 10 ppm). Esto se confirma puesto que en los dos espectros IR se detectan bandas en la
zona de 2700-2750 cm-1(estiramiento C-H de grupo H-C=O) y los tpicos estiramientos C=O
en la zona de 1700 cm-1. Adems uno de ellos posee anillo aromtico con un caracterstico
patrn de sustitucin en posicin para, mientras que el otro es un compuesto aliftico.
Proponer la estructura para cada uno de los aldehdos y asignar las seales presentes en cada
uno de los espectros.
Qumica Orgnica II
Gua de estudio Tema 1: RMN - EM
20. A diferencia de la seal de los aldehdos los hidrgenos cidos no presentan picos
agudos si no que, si se observan, se ven ensanchados y an ms desprotegidos (ms de 11
ppm). Proponer las estructuras de los dos cidos carboxlicos que se corresponden con los
siguientes espectros de 1H RMN sabiendo que sus PM son 74 y 178 respectivamente.
Qumica Orgnica II
Gua de estudio Tema 1: RMN - EM
21. Las seales marcadas con las letras C en el espectro 1 y D en el espectro 2
corresponden a hidrgenos de aminas primarias. Observa las similitudes y diferencias con
respecto a la seal de los protones de cidos carboxlicos del ejercicio anterior en relacin a
la forma de la seal y al corrimiento qumico. Proponer las estructuras para ambas aminas
sabiendo que la aromtica tiene un PM de 107 y la aliftica de 87. La seal que se observa
a campos ms altos en el espectro de la amina aliftica corresponde a la superposicin de
dos grupos metilos no equivalentes.
Qumica Orgnica II
Gua de estudio Tema 1: RMN - EM
22. Asignar la estructura de un compuesto con propiedades cidas cuya frmula molecular es
C10H14O (PM 150) y su espectro de 1H RMN se grafica a continuacin. El compuesto en
cuestin presenta una ancha banda en la regin del espectro IR comprendida entre los 35003200cm-1.
23. Un compuesto carbonlico (banda a 1720 cm-1 en el espectro IR correspondiente a
estiramiento C=O, probablemente de cetona), de frmula molecular C8H14O (PM 126)
presenta el siguiente espectro de 1H RMN. Proponer una estructura que justifique la
aparicin de cada una de sus seales.
24. El siguiente es el espectro de un derivado hidroxilado en el anillo aromtico del cido
cinmico realizado en un espectrmetro Bruker operando a 400 MHz, utilizando CDCl3
como disolvente y una gota de D2O. Determina la posicin de hidroxilacin en base a la
asignacin de las seales de los hidrgenos aromticos.
COOH
HO
Qumica Orgnica II
Gua de estudio Tema 1: RMN - EM
25. Tienes tres viales sin etiqueta, cada uno de ellos contiene un ismero del
triclorobenceno (1,2,3-triclorobenceno; 1,2,4-triclorobenceno y 1,3,5-triclorobenceno). Con
el fin de identificar correctamente cada compuesto y poner la etiqueta correcta a cada vial,
has registrado sus espectros de 13C RMN. Qu espectro corresponde a cada compuesto si
el espectro A presenta dos seales entre 125 y 140 ppm, el B seis seales entre 125 y 140
ppm y el C cuatro seales entre 125 y 140 ppm?
26. Tienes cuatro viales sin etiqueta, cada uno de ellos contiene un ismero del
dicloropropano (1,1-dicloropropano; 2,2-dicloropropano; 1,2-dicloropropano
y
1,3dicloropropano). Con el fin de identificar correctamente cada compuesto y poner la etiqueta
correcta a cada vial, has registrado sus espectros de 13C y 1H RMN. Qu espectro
corresponde a cada compuesto si:
a) El espectro de 13C RMN A presenta tres seales entre 0 y 60 ppm y el de 1H
RMN A tres seales entre 0 y 5 ppm, siendo la seal ms desapantallada es un
sexteto.
b) El espectro de 13C RMN B presenta dos seales entre 0 y 70 ppm y el de 1H
RMN B Una seal singulete a 1.2 ppm.
c) El espectro de 13C RMN C presenta dos seales entre 0 y 70 ppm y el de 1H
RMN C dos seales entre 0 y 10 ppm, siendo la seal ms desapantallada es un
triplete.
d) El espectro de 13C RMN D presenta tres seales entre 0 y 70 ppm y el de 1H
RMN D tres seales entre 0 y 10 ppm, siendo la seal ms desapantallada es un
triplete.
27. Podras indicar cul de los espectros de 13C RMN que se muestran a continuacin
corresponde al aminocido leucina y cual a isoleucina? Justifica tu respuesta.
10
Qumica Orgnica II
Gua de estudio Tema 1: RMN - EM
28. En la representacin del espectro de 13C RMN y DEPT 135 (Distortionless Enhancement
by Polarisation Transfer) del monoterpeno limoneno indica cuales seales corresponden a
carbonos cuaternarios, CH, CH2 y cules a CH3
29. El siguiente es el espectro de 13C RMN, el DEPT 90 y el DEPT 135 de 2metilciclopentanona. Asigna cada uno de los picos.
11
Qumica Orgnica II
Gua de estudio Tema 1: RMN - EM
30. Haciendo uso de los espectros bidimensionales COSY (Correlated spectroscopy) y
HETCOR (Heteronuclear Correlated spectroscopy) asigna todas las seales de 1H y 13CRMN
del 2-butenoato de etilo.
COSY
12
Qumica Orgnica II
Gua de estudio Tema 1: RMN - EM
HETCOR
13
Qumica Orgnica II
Gua de estudio Tema 1: RMN - EM
31. Los modernos espectrmetros de masas de alta resolucin son capaces de distinguir
iones que difieren tan solo en unas pocas milsimas de unidades de masa. Por lo tanto, se
puede determinar la masa exacta de cualquier in molecular o fragmento inico. Esto es as
tanto que las principales editoriales estn aceptando las mediciones de HRMS
(espectrometra de masa de alta resolucin) para reemplazar los datos que se obtienen del
anlisis elemental.
Compuestos con las siguientes frmulas moleculares: C7H14, C6H10O, C5H6O2 y
C5H10N2 poseen la misma masa nominal, es decir, el mismo nmero entero redondeado, y
por lo tanto los cuatro deberan presentar un ion molecular a m/z 98. Sin embargo si
calculamos las masas atmicas de los elementos a partir de las masas exactas de sus
istopos naturales es factible distinguirlos y aproximarse a los valores experimentales que
se obtienen por HRMS. Calcular el PM de los diferentes compuestos haciendo uso de los
valores de masa tabulados.
1H :
1,00783
12,00000
14N : 14,0031
12C :
16O:
15,9949
31,9721
35Cl : 34,9689
32S :
37Cl :
36,9659
78,9183
81Br: 80,9163
79Br:
32. Aplicando las reglas de fragmentacin formula los cuatro cationes radicales que debieran
dar origen a los picos de mayor abundancia en el EM de la 5-metil-1-fenilhexan-2-ona.
O
m/z 91
m/z 133
m/z 98
m/z 146
14
Qumica Orgnica II
Gua de estudio Tema 1: RMN - EM
33. Cul de las siguientes molculas dio origen espectro de masas que se ilustra a
continuacin? Asignar al menos tres picos proponiendo las rutas de fragmentacin adecuadas.
34. Cul de los siguientes espectros corresponde a 1-pentanol y cul a acetato de etilo?
Asignar al menos dos picos proponiendo las rutas de fragmentacin adecuadas para cada uno
de ellos.
15
Qumica Orgnica II
Gua de estudio Tema 1: RMN - EM
35. El in molecular mostrado en la figura siguiente al fragmentarse rinde un pico muy intenso
de m/z 70. Plantear el mecanismo de fragmentacin por medio del cual se justifica su
aparicin.
O
36. Las levaduras son microorganismos eucariticos que pueden metabolizar sustratos
xenobiticos. Entre otras enzimas poseen diferentes tipos de reductasas. Al suministrar 2ciclohexenona a un medio de cultivo donde se desarroll la cepa de levaduras AX22 se obtuvo
un producto de reduccin. En base al anlisis de sus espectros de RMN seala si se redujo el
carbonilo, el doble enlace o ambos.
1
H RMN: =3,17 ppm (q, J=7Hz, 1H); 2,00 ppm (s ancho, 1H); 1,60 ppm (m, 4H); 1,47 ppm
(m, 6H).
13
C RMN: = 72,7 ppm (CH); 36,5 ppm (2xCH2); 28,3 ppm (CH2); 21,8 ppm (2xCH2).
37. Un qumico de productos naturales ha aislado un monoterpeno oxigenado a partir de la
especie vegetal Salvia officinalis. En base al anlisis de sus datos espectroscpicos definir de
cul de los siguientes monoterpenos se trata. Justifique adecuadamente su respuesta.
OH
OH
OH
Terpineol
Camphor
Borneol
16
Thymol
Pulegona
Qumica Orgnica II
Gua de estudio Tema 1: RMN - EM
DEPT
17
Qumica Orgnica II
Gua de estudio Tema 1: RMN - EM
18
Qumica Orgnica II
Gua de estudio Tema 1: RMN - EM
COSY
HETCOR
19
Das könnte Ihnen auch gefallen
- GED1 - Espectrometrías 2020Dokument11 SeitenGED1 - Espectrometrías 2020guadakyuhyunNoch keine Bewertungen
- 1 - RMN 2014Dokument19 Seiten1 - RMN 2014leydi jhoana garciaNoch keine Bewertungen
- RMN de compuesto orgánicoDokument19 SeitenRMN de compuesto orgánicoGABRIELANoch keine Bewertungen
- SOLUCIONARIO-GUÍA-6 (Espectroscopia)Dokument12 SeitenSOLUCIONARIO-GUÍA-6 (Espectroscopia)clauNoch keine Bewertungen
- Espectroscopía IR y RMN Módulo 2 ProblemasDokument14 SeitenEspectroscopía IR y RMN Módulo 2 ProblemasMayoNoch keine Bewertungen
- Guia Ejercicios RMNDokument33 SeitenGuia Ejercicios RMNLuis Arturo GarcíaNoch keine Bewertungen
- Usos de La Espectroscopia de RMNDokument4 SeitenUsos de La Espectroscopia de RMNManuel ChumpitazNoch keine Bewertungen
- Ejercicios de Espectros RMN de Protón para Resolver 12072020.LMEB PDFDokument15 SeitenEjercicios de Espectros RMN de Protón para Resolver 12072020.LMEB PDFluis manuel espinozaNoch keine Bewertungen
- Análisis orgánico RMNDokument4 SeitenAnálisis orgánico RMNDaniel Camilo BermudezNoch keine Bewertungen
- Tema 4. Guía de Ejercicios Cátedra QOIIDokument22 SeitenTema 4. Guía de Ejercicios Cátedra QOIIDaniela BordonesNoch keine Bewertungen
- Espectroscopía EjemplosDokument14 SeitenEspectroscopía EjemplosSule Granados DNoch keine Bewertungen
- RMN 2 DDokument7 SeitenRMN 2 DLeandro SasiambarrenaNoch keine Bewertungen
- Detjun 2010Dokument5 SeitenDetjun 2010Sarah Jayne BurlinghamNoch keine Bewertungen
- Tutorial para La Interpretacion de RMN 1HDokument40 SeitenTutorial para La Interpretacion de RMN 1HDianita Ruano ContrerasNoch keine Bewertungen
- Examen Resuelto 1Dokument8 SeitenExamen Resuelto 1Latika CzNoch keine Bewertungen
- Ejercicios de FitrDokument7 SeitenEjercicios de Fitrrafael velozNoch keine Bewertungen
- Seminario EspectrosDokument6 SeitenSeminario EspectrosInaa MartinezNoch keine Bewertungen
- Lab Quimica OrganicaDokument2 SeitenLab Quimica OrganicaMaría del Carmen Fernández-Tejeda MarinoNoch keine Bewertungen
- Taller de EjerciciosDokument3 SeitenTaller de EjerciciosJimmy JavierNoch keine Bewertungen
- Taller de espectroscopia en Química Orgánica: Elucidación estructural mediante IR, RMN 1H y EEMDokument5 SeitenTaller de espectroscopia en Química Orgánica: Elucidación estructural mediante IR, RMN 1H y EEMCamilo Zapata100% (1)
- Serie 4 IrDokument14 SeitenSerie 4 IrmaximilianodemasiNoch keine Bewertungen
- Ejercicios de RMN de Protones ALCOHOLES Con RespuestasDokument13 SeitenEjercicios de RMN de Protones ALCOHOLES Con RespuestasMaca GonzalezNoch keine Bewertungen
- Ing - Met - Plan de Estudios 2011Dokument6 SeitenIng - Met - Plan de Estudios 2011Estefanny MendiolaNoch keine Bewertungen
- Espectroscopia RMN Del Carbono 13Dokument10 SeitenEspectroscopia RMN Del Carbono 13Marlenne Bojorquez OrozcoNoch keine Bewertungen
- Ejercicios para El Parcial 1Dokument6 SeitenEjercicios para El Parcial 1Melissa Massih MonteroNoch keine Bewertungen
- Seminario AromaticosDokument3 SeitenSeminario AromaticosInaa MartinezNoch keine Bewertungen
- Informe de RMNDokument6 SeitenInforme de RMNLeidy Paola Acevedo AgudeloNoch keine Bewertungen
- Taller de Resonancia Magnética Nuclear de ProtonesDokument8 SeitenTaller de Resonancia Magnética Nuclear de Protonesgerson vargasNoch keine Bewertungen
- AlquinosDokument13 SeitenAlquinosKarla TenorioNoch keine Bewertungen
- Parcial de ElucidacionesDokument12 SeitenParcial de ElucidacionesSkade JötunheimNoch keine Bewertungen
- Seminarios Tai 2Dokument16 SeitenSeminarios Tai 2Antonio LopezNoch keine Bewertungen
- Documento Sin TítuloDokument19 SeitenDocumento Sin TítuloJuan Pablo Rubio LassoNoch keine Bewertungen
- RMN PDFDokument11 SeitenRMN PDFAicrag JehisbellNoch keine Bewertungen
- Problemasdeespectroscopia 20042005Dokument31 SeitenProblemasdeespectroscopia 20042005Edinson Diaz RojasNoch keine Bewertungen
- Elucidacion Estructuras QuimicasDokument5 SeitenElucidacion Estructuras QuimicasJuanDaa Gllo ZptaNoch keine Bewertungen
- Interpretar espectros RMNDokument4 SeitenInterpretar espectros RMNVICTOR RAUL MACEDO QUISPENoch keine Bewertungen
- 2 ParcialDokument5 Seiten2 ParcialLaura MilanoNoch keine Bewertungen
- Seminario AromaticosDokument4 SeitenSeminario AromaticosfederNoch keine Bewertungen
- EnunprobDokument8 SeitenEnunprobBlueAbeNoch keine Bewertungen
- Taller EspectroscópicoDokument6 SeitenTaller EspectroscópicoacidicbasicNoch keine Bewertungen
- Ejercicios UV-Visibles Química OrgánicaDokument6 SeitenEjercicios UV-Visibles Química OrgánicaSesilu Susej Prada33% (6)
- EJERCICIOS Qº 2 BACH (Isomer, Prop Atom, Nº Cuant, Enlace)Dokument4 SeitenEJERCICIOS Qº 2 BACH (Isomer, Prop Atom, Nº Cuant, Enlace)Marta Ferreira TorrenteNoch keine Bewertungen
- Pec-2 - 2021 - 2022 2Dokument13 SeitenPec-2 - 2021 - 2022 2Bea SNoch keine Bewertungen
- EeuvDokument6 SeitenEeuvellechim2020Noch keine Bewertungen
- Problemas de benceno y aromaticidadDokument17 SeitenProblemas de benceno y aromaticidadElvis Camarena89% (9)
- Boceto Informe 3 InstrumentalDokument8 SeitenBoceto Informe 3 InstrumentalBRAYAN ALEXIS DE SOUSA LORANoch keine Bewertungen
- Elucidacion EstructuralDokument13 SeitenElucidacion EstructuralAlbertoCaceresMuñozNoch keine Bewertungen
- Examen QOII Septiembre 2012Dokument5 SeitenExamen QOII Septiembre 2012Alba María Soto de JesúsNoch keine Bewertungen
- Taller Isomeria-AgroindusrialDokument7 SeitenTaller Isomeria-AgroindusrialLuis casilloNoch keine Bewertungen
- EXAMEN DE ANALITICA E INSTRUMENTAL: Espectroscopia IR, Cromatografía de gases y líquidosDokument2 SeitenEXAMEN DE ANALITICA E INSTRUMENTAL: Espectroscopia IR, Cromatografía de gases y líquidosLuisa Fernanda Zapata OchoaNoch keine Bewertungen
- Tema 4-INFRARROJODokument22 SeitenTema 4-INFRARROJORoger ChavezNoch keine Bewertungen
- Ejercicios Ron InórgánicaDokument1 SeiteEjercicios Ron InórgánicaLaura OrtegaNoch keine Bewertungen
- Cuestionario sobre el análisis espectroscópico del feniltiotetrazol y su tautómeroDokument2 SeitenCuestionario sobre el análisis espectroscópico del feniltiotetrazol y su tautómeroLuiz TurnerNoch keine Bewertungen
- Quimica OrganicaDokument25 SeitenQuimica OrganicaAnghii Patricio100% (1)
- Análisis Espectral de Un Compuesto Orgánico Desconocido C4h8o2Dokument4 SeitenAnálisis Espectral de Un Compuesto Orgánico Desconocido C4h8o2Rubén darío Romo ChamorroNoch keine Bewertungen
- Átomos de carbono en compuestos orgánicosDokument4 SeitenÁtomos de carbono en compuestos orgánicosLaura SanabriaNoch keine Bewertungen
- Caracterización química, morfológica y estructural de materialesVon EverandCaracterización química, morfológica y estructural de materialesNoch keine Bewertungen
- Informe Proyecto Aula EntregarDokument7 SeitenInforme Proyecto Aula EntregarLeydi Jhoana Garcia CardenasNoch keine Bewertungen
- CalcioDokument3 SeitenCalcioDanny EliBerNoch keine Bewertungen
- Cinética de Saponificación (Autoguardado)Dokument12 SeitenCinética de Saponificación (Autoguardado)Leydi Jhoana Garcia CardenasNoch keine Bewertungen
- Ejercicios de nomenclatura de aldehidos y cetonasDokument3 SeitenEjercicios de nomenclatura de aldehidos y cetonasKelly Gabriela Misse Colmenares54% (13)
- Experimentacion en Ingenieria Quimica I DEFDokument9 SeitenExperimentacion en Ingenieria Quimica I DEFLeydi Jhoana Garcia CardenasNoch keine Bewertungen
- Problemario Balance de MateriaDokument23 SeitenProblemario Balance de MateriaYang Hayabusa89% (9)
- Ejercicios de nomenclatura de aldehidos y cetonasDokument3 SeitenEjercicios de nomenclatura de aldehidos y cetonasKelly Gabriela Misse Colmenares54% (13)
- Procesos Termicos Modulo 2014Dokument81 SeitenProcesos Termicos Modulo 2014Leydi Jhoana Garcia CardenasNoch keine Bewertungen
- Aminoacidos TerminadoDokument15 SeitenAminoacidos TerminadoLeydi Jhoana Garcia CardenasNoch keine Bewertungen
- Fenomenos de TransporteDokument6 SeitenFenomenos de TransporteLeydi Jhoana Garcia CardenasNoch keine Bewertungen
- Cinética de saponificación del acetato de etiloDokument9 SeitenCinética de saponificación del acetato de etiloLeydi Jhoana Garcia CardenasNoch keine Bewertungen
- Aminoácidos y proteínas: reacciones colorimétricas para su detecciónDokument3 SeitenAminoácidos y proteínas: reacciones colorimétricas para su detecciónLeydi Jhoana Garcia CardenasNoch keine Bewertungen
- Taller02-Parte2 31309147Dokument10 SeitenTaller02-Parte2 31309147Leydi Jhoana Garcia CardenasNoch keine Bewertungen
- Act9 Snsa AdmDokument10 SeitenAct9 Snsa AdmShecidd AlmendarizNoch keine Bewertungen
- Hoja de Seguridad Cloro en Pastillas TCCA MAGNACHLORDokument7 SeitenHoja de Seguridad Cloro en Pastillas TCCA MAGNACHLORElizabeth BarzolaNoch keine Bewertungen
- Proyecto CONFIODokument15 SeitenProyecto CONFIONery IxcotNoch keine Bewertungen
- CONTRATIEMPO: ASESINATO EN UN HOTELDokument4 SeitenCONTRATIEMPO: ASESINATO EN UN HOTELKaren AlexandraNoch keine Bewertungen
- Banco Doctor Vilca Unidad 2Dokument14 SeitenBanco Doctor Vilca Unidad 2JesusNoch keine Bewertungen
- Modelo de LaudoDokument9 SeitenModelo de LaudoManuel Edevaldo Lopes VieiraNoch keine Bewertungen
- Sistema RenalDokument90 SeitenSistema RenalTtalgi Fst100% (1)
- Determinacion de Bacterias ColiformesDokument4 SeitenDeterminacion de Bacterias ColiformesRaul GomezNoch keine Bewertungen
- ICSDDokument7 SeitenICSDCamilo ArizaNoch keine Bewertungen
- Que Es El HG y Cual Es Su Principal Función OrtopédicaDokument2 SeitenQue Es El HG y Cual Es Su Principal Función OrtopédicaLadii AguilarNoch keine Bewertungen
- Ingresos consolidados del municipio de Puerto Bravo en 2012Dokument4 SeitenIngresos consolidados del municipio de Puerto Bravo en 2012Yulisa CaguaNoch keine Bewertungen
- Diversidad de Serpientes de RisaraldaDokument23 SeitenDiversidad de Serpientes de RisaraldaCEFSA Centro de Formación de Seguridad y Alturas SAS100% (3)
- Protocolo de Intervención Policial para La AtenciónDokument3 SeitenProtocolo de Intervención Policial para La AtenciónambiwoNoch keine Bewertungen
- Clasificación de Los Elementos Químicos Por Su ReactividadDokument4 SeitenClasificación de Los Elementos Químicos Por Su ReactividadJose Guadalupe Treviño PeralesNoch keine Bewertungen
- Educar sin estrés en 7 díasDokument4 SeitenEducar sin estrés en 7 díasadrianaNoch keine Bewertungen
- Estudio de delimitación de faja marginal en ríos de ApurímacDokument97 SeitenEstudio de delimitación de faja marginal en ríos de ApurímacBoris Buhezo0% (1)
- Eett B Licitacion - 07.11.2022Dokument14 SeitenEett B Licitacion - 07.11.2022Eduardo SalazarNoch keine Bewertungen
- Mapa MetabolitosDokument1 SeiteMapa MetabolitosDaniel TorresNoch keine Bewertungen
- Green Heart Documento Actual Prfesor A SubirDokument34 SeitenGreen Heart Documento Actual Prfesor A SubirDigna Haro AlbarránNoch keine Bewertungen
- Carimbo Procesos IIDokument12 SeitenCarimbo Procesos IIFabiola Azcuña CastroNoch keine Bewertungen
- Metodología HPLC - FlavonoidesDokument2 SeitenMetodología HPLC - FlavonoidesMario Sergio Espinoza AguilarNoch keine Bewertungen
- Ale ErgonomíaDokument51 SeitenAle Ergonomíapaucarcielo071Noch keine Bewertungen
- Tension SuperficialDokument9 SeitenTension SuperficialJBCristopherNoch keine Bewertungen
- Tratamiento de Crudo PDFDokument128 SeitenTratamiento de Crudo PDFJON LOPEZNoch keine Bewertungen
- La Importancia de Las PalabrasDokument2 SeitenLa Importancia de Las PalabrasMaria Recuenco LainNoch keine Bewertungen
- Crucigrama Equilibrio QuimicoDokument1 SeiteCrucigrama Equilibrio QuimicoLizeth Rojas67% (3)
- Hoja de Seguridad AmbientadorDokument4 SeitenHoja de Seguridad AmbientadorADRIANA MARTINEZNoch keine Bewertungen
- Síntesis de isómeros cis y trans de cloruro de diclorobis(etilendiamina) cobalto(IIIDokument11 SeitenSíntesis de isómeros cis y trans de cloruro de diclorobis(etilendiamina) cobalto(IIIWENDY NATHALIA ROJAS ARCENoch keine Bewertungen
- Curso Jabón Batido Cremoso o Whipped SoapDokument35 SeitenCurso Jabón Batido Cremoso o Whipped SoapDIANA LORENA OROZCO GALLEGO100% (2)
- Torre de EnfriamientoDokument5 SeitenTorre de EnfriamientoCamila Utrera SilvaNoch keine Bewertungen