Beruflich Dokumente
Kultur Dokumente
Informe Entalpía de Mezclas de Fluidos Binarios
Hochgeladen von
DalíAsesoríasCopyright
Verfügbare Formate
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
Verfügbare Formate
Informe Entalpía de Mezclas de Fluidos Binarios
Hochgeladen von
DalíAsesoríasCopyright:
Verfügbare Formate
DETERMINACIN DE LA ENTALPA DE MEZCLA DE
BINARIOS
FLUDOS
Marisol Montao Guevara - Edicson Mesa Palomino
Grupo H1 - Subgrupo 5
Universidad Industrial de Santander.
Facultad de Ciencias. Escuela de Qumica.
Bucaramanga, Julio de 2013
1. RESULTADOS EXPERIMENTALES
Tabla 1. Datos de los deltas de temperatura
para las diferentes muestras
T(T
Mezcla
TOa(K) TOb(K) Tab(K) T Mezcla (K) MezclaN
TOb)(K)
1
2
7
6
5
4
3
25,52
35,04
24,26
04
25,93
26,19
29,94
32,78
24,52
35,04
24,26
25,93
26,19
29,94
32,78
0
0
0
0
0
0
0
30,27
36,17
22,29
25,93
28,12
31,62
34,82
5,75
1.13
1,97
0,58
1,93
1,68
2,04
A partir de los datos dela Tabla 1, se registraron los
valores Temperatura Vs Tiempo para cada uno de
las mezclas (ver Tabla 2).
Grfica 1. Temperatura Vs Tiempo durante 3
minutos para la mezcla 1
Tabla 2. Datos de Temperatura Vs
Tiempo para la Mezlca 1 (532,2943 g
H2O).
VOLTAJE (V)
CORRIENTE (A)
TEMPERATURA
(C)
30,23
30,68
31,17
31,61
32,09
32,57
33,01
33,50
34,00
34,56
34,87
35,39
35,81
35,15
36,04
36,03
36,02
35,97
35,96
35,90
35,88
35,85
35,84
35,79
35,77
35,77
35,67
10,73
4,43
TIEMPO (S)
0
30
60
90
120
150
180
210
240
270
300
330
360
390
420
450
480
510
540
570
600
630
640
670
700
730
760
Determinacin de la Entalpa de Mezclas de Fluidos Binarios - Laboratorio de Fisicoqumica II
26,30
26,27
MEZCLA
ENERGA
VOLTAJE (V)
CORRIENTE (A)
TEMPERATURA (C)
27,59
27,81
28,19
28,61
29,15
29,24
29,43
29,50
29,71
29,83
29,98
30,10
20,29
30,30
30,28
30,25
30,23
30,22
30,17
MEZCLA
ENERGA
VOLTAJE (V)
CORRIENTE (A)
TEMPERATURA (C)
31,43
31,40
31,50
31,64
31,84
31,98
32,03
32,25
32,37
32,49
32,55
32,73
32,93
33,47
33,49
33,48
33,45
33,50
33,32
MEZCLA
ENERGA
VOLTAJE (V)
CORRIENTE (A)
Temperatura (C)
Temperatura Vs. Tiempo (Mezcla 1) al
desconectarse de la fuente V=4,954
36
y = -0,0011x + 36,548
R = 0,9634
35,8
35,6
0
200
400
600
800
Tiempo (S)
Grfica 2. Temperatura Vs Tiempo
durante
3
minutos
despus
de
desconectarse de la fuente con un voltaje =
4,954 W/h para la mezcla
Tabla 3. Datos de Temperatura Vs
Tiempo para las mezclas 7, 6, 5, 4, 3.
MEZCLA
ENERGA
VOLTAJE (V)
CORRIENTE (A)
TEMPERATURA (C)
22,32
22,62
23,06
23,53
23,93
24,40
24,31
24,09
24,29
25,92
25,89
25,93
25,88
25,90
25,85
25,95
25,94
MEZCLA
ENERGA
VOLTAJE (V)
CORRIENTE (A)
TEMPERATURA (C)
25,33
25,36
25,65
26,15
26,24
26,26
26,28
26,22
26,25
7
10,79
4,45
TIEMPO (S)
0
30
60
90
120
150
180
210
240
270
300
330
360
390
420
450
480
6
0,958 W/ h
10,86
4,48
TIEMPO (S)
0
30
60
90
120
150
180
210
240
2
270
300
5
2,228W/h
10,68
4,52
TIEMPO (S)
0
30
60
90
120
150
180
210
240
270
300
330
360
390
420
450
480
510
540
4
3,458W/h
10,95
4,52
TIEMPO (S)
0
30
60
90
120
150
180
210
240
270
300
330
360
390
420
450
480
510
510
3
4,907W/h
10,68
4,52
Determinacin de la Entalpa de Mezclas de Fluidos Binarios - Laboratorio de Fisicoqumica II
Tabla 4. Moles de A y B
34,62
34,63
34,70
34,84
35,01
35,08
35,25
35,41
35,59
35,75
35,83
36,01
36,37
36,47
36,64
36,88
36,90
36,86
36,58
0
30
60
90
120
150
180
210
240
270
300
330
360
390
420
450
480
510
540
Mezcla
1
2
3
4
5
Tabla
5.
Fracciones
correspondientes para A y B
Mezcla
1
2
3
4
5
Determinacin de la fraccin molar:
Para la Mezcla 1.
Moles de Acetona =
Fraccin Molar de A= X A
XA
X A Xb
Fraccin Molar de A
1mol
(155,133g )
2, 6746molesacetona
58 g
XA
Moles A
24 moles
26,7 moles
8 moles
8,9 moles
10,0309 moles
24moles
0,8997
24moles 2, 6746moles
Determinacin de la entalpa integral de mezcla
Fraccin
Molar A
0,8997
0,8886
0,8974
0,8889
0,7468
Moles B
2,7moles
3,3 moles
0,9 moles
1,1 moles
3,4 moles
molares
Fraccin
Molar B
0,1003
0,1114
0,1026
0,110
0,1231
Determinacin de la Entalpa de Mezclas de Fluidos Binarios - Laboratorio de Fisicoqumica II
Se observa
el calor integral de esta
solucin est relacionado con el nmero de
moles de disolventes en los que se ha
disuelto el soluto. Esta grafica nos muestra
el efecto trmico que tiene al mezclar
acetona con agua por ello se denomina
calor integral de solucin al cambio de
entalpia. Esta grafica nos muestra la
cantidad de calor absorbida o desprendida
por mol de sustancia en el proceso
completo, es decir, cuando se disuelve toda
la sustancia en la cantidad de disolvente.
Podemos concluir de esta grafica que la
entalpia integral depende de T, P, XA, XB.
CONCLUSIONES
La entropa molar de las mezcla es la
sumatoria de las propiedades extensivas de
cada uno de los componentes a la
temperatura de la muestra.
BIBLIOGRAFIA
1. Atkins, Jones 2006. Principios de Qumica.
Los cambios de descubrimiento. Editorial
Media Panamericana, BuEnos aires. Argentina.
Pginas 221.
2. Robert Busch Brete. Revista phywe
chemistry. (2008). Laboratory Experiments.
Pginas 2
Determinacin de la Entalpa de Mezclas de Fluidos Binarios - Laboratorio de Fisicoqumica II
Anexos
Determinacin de la Entalpa de Mezclas de Fluidos Binarios - Laboratorio de Fisicoqumica II
Determinacin de la Entalpa de Mezclas de Fluidos Binarios - Laboratorio de Fisicoqumica II
Das könnte Ihnen auch gefallen
- Curso Práctico de Química GeneralVon EverandCurso Práctico de Química GeneralBewertung: 4 von 5 Sternen4/5 (4)
- Casos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSVon EverandCasos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSBewertung: 4.5 von 5 Sternen4.5/5 (7)
- Propiedades ColigativasDokument13 SeitenPropiedades Coligativasbrendads89100% (6)
- Ingeniería química. Soluciones a los problemas del tomo IVon EverandIngeniería química. Soluciones a los problemas del tomo INoch keine Bewertungen
- Bus - Especificaciones k410 6x2 Low Driver - tcm80-257452Dokument2 SeitenBus - Especificaciones k410 6x2 Low Driver - tcm80-257452Juan Diego Chinchay Rojas100% (2)
- Solucion Exa Qg1 II Parcial 2012 II TDokument7 SeitenSolucion Exa Qg1 II Parcial 2012 II TLuis Vaca100% (1)
- Momentos de Inercia problemas resueltosDokument164 SeitenMomentos de Inercia problemas resueltosJhonyNoch keine Bewertungen
- Grafeno Vs SilicioDokument19 SeitenGrafeno Vs Siliciocarp1aNoch keine Bewertungen
- Diagrama de Fases-Sistema BinarioDokument11 SeitenDiagrama de Fases-Sistema Binariopmori92Noch keine Bewertungen
- Practica 2 RecristalizaciónDokument2 SeitenPractica 2 RecristalizaciónDayra HuertasNoch keine Bewertungen
- Equilibrio químico y destilación de mezclas binarias y ternariasDokument37 SeitenEquilibrio químico y destilación de mezclas binarias y ternariasCARMENZANoch keine Bewertungen
- Calor de neutralización: Entalpía reacciones ácidos-basesDokument8 SeitenCalor de neutralización: Entalpía reacciones ácidos-basesLuis Manuel GuerreroNoch keine Bewertungen
- Solucion Ex QG1 2 Parcial 2012Dokument9 SeitenSolucion Ex QG1 2 Parcial 2012Luis Vaca100% (1)
- Informe 3 Lab de Fiqui - Variación de La Solubilidad Con La TemperaturaDokument6 SeitenInforme 3 Lab de Fiqui - Variación de La Solubilidad Con La TemperaturaPIERO MATIAS HERRERA SUAREZNoch keine Bewertungen
- Informe 3 Calor IntegralDokument12 SeitenInforme 3 Calor IntegralJose LuisNoch keine Bewertungen
- Calor Específico de SólidosDokument5 SeitenCalor Específico de SólidosDavid QuinteroNoch keine Bewertungen
- Calor de NeutralizaciónDokument30 SeitenCalor de NeutralizaciónRomer SavaNoch keine Bewertungen
- Determinacion Calor de SolucionDokument15 SeitenDeterminacion Calor de Solucionsimon j ochoa aNoch keine Bewertungen
- Como Hacer Un InformeDokument6 SeitenComo Hacer Un InformeMarimar MoralesNoch keine Bewertungen
- Informe 12, Nota-19Dokument13 SeitenInforme 12, Nota-19Claudia AngelesNoch keine Bewertungen
- 1er Informe, Calores de ReacciónDokument2 Seiten1er Informe, Calores de ReacciónEsteban De Jesús CamargoNoch keine Bewertungen
- Informe #3 Calor 2Dokument9 SeitenInforme #3 Calor 2LeiraleNoch keine Bewertungen
- Laboratorio 1 Calor Integral y Calor Diferencial de SolucionDokument3 SeitenLaboratorio 1 Calor Integral y Calor Diferencial de SolucionDANNA VALENTINA CARDENAS CALDERONNoch keine Bewertungen
- Diagrama de fases fenol-aguaDokument10 SeitenDiagrama de fases fenol-aguaSteffaniaNoch keine Bewertungen
- Informe Fisicoquímica Ambiental UnadDokument53 SeitenInforme Fisicoquímica Ambiental Unadc1e2s3100% (2)
- Volumen Parcial Molar 1 PDFDokument5 SeitenVolumen Parcial Molar 1 PDFLïgïa Herrera MoralesNoch keine Bewertungen
- Informe Lab FisicoquimicaDokument40 SeitenInforme Lab FisicoquimicaCARMENZA100% (1)
- Entalpia de Formacion de Una SalDokument7 SeitenEntalpia de Formacion de Una SalOscar PortilloNoch keine Bewertungen
- Indice de RefraccionDokument15 SeitenIndice de RefraccionSusana Zárate RuizNoch keine Bewertungen
- Cinetica de La Reaccion de Solvolisis Del Cloruro de TerbutiloDokument14 SeitenCinetica de La Reaccion de Solvolisis Del Cloruro de Terbutiloconah1234Noch keine Bewertungen
- Calor integral de solución del etanolDokument7 SeitenCalor integral de solución del etanolOscar PortilloNoch keine Bewertungen
- Solucion Examen de Qg1 2p (Autoguardado)Dokument10 SeitenSolucion Examen de Qg1 2p (Autoguardado)Luis VacaNoch keine Bewertungen
- Constante de Equilibrio Disolucion Del KNO3Dokument10 SeitenConstante de Equilibrio Disolucion Del KNO3Miguel Angel M. GNoch keine Bewertungen
- Diagrama de FasesDokument15 SeitenDiagrama de FasesEl DOn100% (1)
- P8LQ14 Hernandez Hernandez Deissy JovitaDokument10 SeitenP8LQ14 Hernandez Hernandez Deissy JovitaDey HzNoch keine Bewertungen
- Coeficinete de Expansión Gillary RevLRDokument6 SeitenCoeficinete de Expansión Gillary RevLRluisNoch keine Bewertungen
- Como Varía El Volumen Del Aire Al CalentarloDokument8 SeitenComo Varía El Volumen Del Aire Al Calentarlojudith100% (1)
- Termodinámica básica ENES-IPNDokument8 SeitenTermodinámica básica ENES-IPNEmmanuel Villa MendozaNoch keine Bewertungen
- Practica1Lab EyC2017Dokument8 SeitenPractica1Lab EyC2017Miguel AngelNoch keine Bewertungen
- Informe Metodo de JobDokument5 SeitenInforme Metodo de JobJenny C. Rodriguez100% (3)
- Regla de fases UNMSM diagrama binaria naftaleno diclorobencenoDokument7 SeitenRegla de fases UNMSM diagrama binaria naftaleno diclorobencenoDiego AllccaNoch keine Bewertungen
- Regla de Fases DiagramaDokument16 SeitenRegla de Fases DiagramaJoselyn Matias BrañezNoch keine Bewertungen
- Practica de Laboratorio de Fisicoquímica Ii #2Dokument32 SeitenPractica de Laboratorio de Fisicoquímica Ii #2Luis Angel GomezNoch keine Bewertungen
- Termoquímica: Calor de reaccionesDokument6 SeitenTermoquímica: Calor de reaccioneswiininaNoch keine Bewertungen
- Reporte Entalpias de ReacciónDokument8 SeitenReporte Entalpias de Reacciónalejitoceron2013Noch keine Bewertungen
- Calor Integral InformeDokument3 SeitenCalor Integral Informedmitryvx100% (1)
- Laboratorio de Ebulloscopia 2Dokument6 SeitenLaboratorio de Ebulloscopia 2Diego CerqueraNoch keine Bewertungen
- Informe 8 Termoquimica y Termodinamica PDFDokument5 SeitenInforme 8 Termoquimica y Termodinamica PDFJuan Arias100% (1)
- Supongamos Que Pretendemos Llevar A Cabo A Temperatura Elevada Una Reacción Que Es Suavemenete Exotérmica A 298Dokument5 SeitenSupongamos Que Pretendemos Llevar A Cabo A Temperatura Elevada Una Reacción Que Es Suavemenete Exotérmica A 298Estuardo ChaconNoch keine Bewertungen
- Sistema Binario Sólido-Liquido Laboratorio-FisicoquimicaDokument5 SeitenSistema Binario Sólido-Liquido Laboratorio-Fisicoquimicamarcelina60% (1)
- Informe 6 FisicoquímicaDokument16 SeitenInforme 6 FisicoquímicaAngela Abanto BelloNoch keine Bewertungen
- Laboratorio QMC 206 Practica Nº5Dokument6 SeitenLaboratorio QMC 206 Practica Nº5Lucia Maturano PeñarandaNoch keine Bewertungen
- Ejercicios A DesarrollarDokument2 SeitenEjercicios A DesarrollarMaria Del RosarioNoch keine Bewertungen
- Trabajo Practico n3.Dokument7 SeitenTrabajo Practico n3.Sebastian RomeroNoch keine Bewertungen
- Practica 2 Fisico 11Dokument3 SeitenPractica 2 Fisico 11SebastianNoch keine Bewertungen
- Reporte de Laboratorio N°3-2022-1Dokument17 SeitenReporte de Laboratorio N°3-2022-1Angel MarellaNoch keine Bewertungen
- PNT de MuestraDokument10 SeitenPNT de MuestraIria RieloNoch keine Bewertungen
- 7 Guía de Problemas N°7Dokument4 Seiten7 Guía de Problemas N°7Lucas SolisNoch keine Bewertungen
- Practica EyCDokument5 SeitenPractica EyCViridiana Guadalupe Alvarez SantinNoch keine Bewertungen
- 1453-Texto Del Artículo (PDF y MP3) - 6209-1-10-20220808Dokument26 Seiten1453-Texto Del Artículo (PDF y MP3) - 6209-1-10-20220808DalíAsesoríasNoch keine Bewertungen
- ArdilaNovoaDanielEduardo2019 PDFDokument31 SeitenArdilaNovoaDanielEduardo2019 PDFDalíAsesoríasNoch keine Bewertungen
- Preinforme 3. Técnicas CromatográficasDokument7 SeitenPreinforme 3. Técnicas CromatográficasDalíAsesoríasNoch keine Bewertungen
- Egipto FinalDokument35 SeitenEgipto FinalDalíAsesoríasNoch keine Bewertungen
- 4 +Novarua+24+Artículo+4Dokument20 Seiten4 +Novarua+24+Artículo+4DalíAsesoríasNoch keine Bewertungen
- LF - Taller4 - Grupo 1Dokument2 SeitenLF - Taller4 - Grupo 1DalíAsesoríasNoch keine Bewertungen
- Kelly Ortíz - Marisol MontañoDokument14 SeitenKelly Ortíz - Marisol MontañoDalíAsesoríasNoch keine Bewertungen
- Resolución No 000112 Del 3 de Junio de 2014 OEADokument6 SeitenResolución No 000112 Del 3 de Junio de 2014 OEAJEAN PAUL RAMIREZ TOVARNoch keine Bewertungen
- Lopez Palacio Juan Guillermo 2014Dokument48 SeitenLopez Palacio Juan Guillermo 2014DalíAsesoríasNoch keine Bewertungen
- INFORME DE LABORATORIO CASCARA SAGRADA (Rhamnus Purshiana) 2021 GRUPO 4Dokument4 SeitenINFORME DE LABORATORIO CASCARA SAGRADA (Rhamnus Purshiana) 2021 GRUPO 4DalíAsesoríasNoch keine Bewertungen
- Expo EgiptoDokument6 SeitenExpo EgiptoDalíAsesoríasNoch keine Bewertungen
- Técnicas Cromatográficas Extracto Aceite EsencialDokument9 SeitenTécnicas Cromatográficas Extracto Aceite EsencialDalíAsesoríasNoch keine Bewertungen
- Formato GradoDokument1 SeiteFormato GradoDalíAsesoríasNoch keine Bewertungen
- Propuesta Individual EmprendimientoDokument23 SeitenPropuesta Individual EmprendimientoSebastiana MontañoNoch keine Bewertungen
- Formato Producto Difusion Cartel Cientifico PosterDokument3 SeitenFormato Producto Difusion Cartel Cientifico PosterDalíAsesoríasNoch keine Bewertungen
- Plantilla Maestría UnabDokument24 SeitenPlantilla Maestría UnabDalíAsesoríasNoch keine Bewertungen
- Boletin Dinamica Empresarial 75Dokument4 SeitenBoletin Dinamica Empresarial 75DalíAsesoríasNoch keine Bewertungen
- Certificado de Asistencia TytDokument1 SeiteCertificado de Asistencia TytDalíAsesoríasNoch keine Bewertungen
- Colombia - Informe Del Sector Agroquímico - Julio 2021Dokument18 SeitenColombia - Informe Del Sector Agroquímico - Julio 2021DalíAsesoríasNoch keine Bewertungen
- Evaluación Ergonómica y Psicosocial de Puesto Administrativo y Su Contraste Al Actual Teletrabajo Por PandemiaDokument41 SeitenEvaluación Ergonómica y Psicosocial de Puesto Administrativo y Su Contraste Al Actual Teletrabajo Por PandemiaDalíAsesoríasNoch keine Bewertungen
- Tabla de Atributos - Usos Del Suelo - Calculo de AreasDokument4 SeitenTabla de Atributos - Usos Del Suelo - Calculo de AreasDalíAsesoríasNoch keine Bewertungen
- Dialnet LaGlobalizacionYSuInfluenciaEnLaAgricultura 6332793 PDFDokument22 SeitenDialnet LaGlobalizacionYSuInfluenciaEnLaAgricultura 6332793 PDFSantiago MedinaNoch keine Bewertungen
- Exposición 1. Esteroquímica FenoterolDokument8 SeitenExposición 1. Esteroquímica FenoterolDalíAsesoríasNoch keine Bewertungen
- Montaño - DETECTOR DE PRECIPITADOSDokument8 SeitenMontaño - DETECTOR DE PRECIPITADOSDalíAsesoríasNoch keine Bewertungen
- Inglés Básico IIDokument1 SeiteInglés Básico IIDalíAsesoríasNoch keine Bewertungen
- RecristalizaciónDokument4 SeitenRecristalizaciónDalíAsesoríasNoch keine Bewertungen
- Taller4 Reacciones de AdiciónDokument1 SeiteTaller4 Reacciones de AdiciónDalíAsesoríasNoch keine Bewertungen
- Presentación de Estructura Del Plan de NegociosDokument10 SeitenPresentación de Estructura Del Plan de NegociosDalíAsesoríasNoch keine Bewertungen
- Ensayo Administrador de EmpresasDokument5 SeitenEnsayo Administrador de EmpresasDalíAsesoríasNoch keine Bewertungen
- Actividades 7 Origen Del Sistema Solar-MartitaDokument2 SeitenActividades 7 Origen Del Sistema Solar-MartitaPaula Alondra López AjúNoch keine Bewertungen
- PDF Modificacion Del Estudio de Impacto Ambiental Del Proyecto de Expansion A 3300 TMD Unidad Minera Pachapaqui CompressDokument160 SeitenPDF Modificacion Del Estudio de Impacto Ambiental Del Proyecto de Expansion A 3300 TMD Unidad Minera Pachapaqui CompressKEN INGNoch keine Bewertungen
- Aislamiento - Prueba 794ACDokument9 SeitenAislamiento - Prueba 794ACnicolasNoch keine Bewertungen
- Curiosidades Del Mes de DiciembreDokument2 SeitenCuriosidades Del Mes de Diciembremelissa100% (1)
- Visita A La Cadena SER.Dokument23 SeitenVisita A La Cadena SER.Mara González GómezNoch keine Bewertungen
- TRICOTILOMANIADokument7 SeitenTRICOTILOMANIAkandy24100% (1)
- Transito HidrogramasDokument10 SeitenTransito HidrogramasLuis Cueva PeralesNoch keine Bewertungen
- NootrópicosDokument13 SeitenNootrópicosOsukaru Kuro Neko100% (1)
- SEGI02 TareaDokument6 SeitenSEGI02 TareaKiko AcabNoch keine Bewertungen
- Toxicidad metales guion informativoDokument3 SeitenToxicidad metales guion informativoEybar Villamizar MoraNoch keine Bewertungen
- Galvanómetro MedicionesDokument8 SeitenGalvanómetro MedicionesnacolNoch keine Bewertungen
- Sin Título 1Dokument40 SeitenSin Título 1David BanerNoch keine Bewertungen
- Plan de Atencion de Enfermeria AlzahimerDokument11 SeitenPlan de Atencion de Enfermeria AlzahimerJesica carolina Duran VargasNoch keine Bewertungen
- Amar Sin ApegosDokument1 SeiteAmar Sin ApegosDaDashaNoch keine Bewertungen
- Gammapatías monoclonales y Mieloma MúltipleDokument37 SeitenGammapatías monoclonales y Mieloma MúltipleOscar ValerNoch keine Bewertungen
- Cito EsqueletoDokument10 SeitenCito EsqueletoRocío PonceNoch keine Bewertungen
- Radiactividad en El Proceso de Reciclado de ChatarraDokument10 SeitenRadiactividad en El Proceso de Reciclado de ChatarraSbaz22Noch keine Bewertungen
- Prelab 3 - Cinetica de Decoloracion FenolftaleinaDokument12 SeitenPrelab 3 - Cinetica de Decoloracion FenolftaleinaBenjamin Quena CastroNoch keine Bewertungen
- B ESCALA DE ASIADokument12 SeitenB ESCALA DE ASIAoriana vizzarroNoch keine Bewertungen
- SHANCAYANDokument39 SeitenSHANCAYANZōe CaminoNoch keine Bewertungen
- Estructura, Clasificacion, Propiedades Proteinas y AaDokument43 SeitenEstructura, Clasificacion, Propiedades Proteinas y Aajonathan samuel chafla cuencaNoch keine Bewertungen
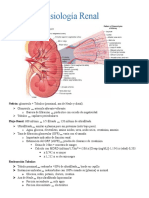
- Fisiología renal: nefrón, flujo renal, ultrafiltrado, reabsorción tubular y regulación hormonalDokument5 SeitenFisiología renal: nefrón, flujo renal, ultrafiltrado, reabsorción tubular y regulación hormonalJean Claudio Miranda ParraNoch keine Bewertungen
- Londres 4 Días 2 Pax 350 Eur/PaxDokument3 SeitenLondres 4 Días 2 Pax 350 Eur/PaxAinhoa Bonilla GomezNoch keine Bewertungen
- Guia Tercer Parcial Mate Ii Prim 2017Dokument5 SeitenGuia Tercer Parcial Mate Ii Prim 2017Victor MendozaNoch keine Bewertungen
- UNAM Química de Coordinación Tarea Previa 3Dokument2 SeitenUNAM Química de Coordinación Tarea Previa 3Judas IscarioteNoch keine Bewertungen
- UP6 MaintenanceDokument32 SeitenUP6 MaintenanceEmilio AlNoch keine Bewertungen
- Algebra Lineal UCE Seguimiento SílaboDokument2 SeitenAlgebra Lineal UCE Seguimiento SílaboEsteban RivadeneiraNoch keine Bewertungen