Beruflich Dokumente
Kultur Dokumente
Normas Laboratoriais
Hochgeladen von
Antonio PortelaOriginaltitel
Copyright
Verfügbare Formate
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
Verfügbare Formate
Normas Laboratoriais
Hochgeladen von
Antonio PortelaCopyright:
Verfügbare Formate
UNIVERSIDADE FEDERAL DO MARANHO UFMA
CENTRO DE CINCIAS EXATAS E TECNOLGICAS - CCET
Antnio Jos Portela de Jesus Santos
Qumica Geral: Termoqumica
So Lus, 2016
Antonio Jos Portela de Jesus Santos
Qumica Geral: Termoqumica
Trabalho apresentado como requisito parcial para
obteno de nota na disciplina Qumica Geral, no
Curso de Engenharia Eltrica, na Universidade
Federal do Maranho.
Prof. MSc. Adriana Murad Fernandes
So Lus, 2016
RESUMO
Esta atividade tem como finalidade abordar sobre a termoqumica, ramo da
qumica que estuda o calor (a energia) envolvido nas reaes qumicas e nas
mudanas de estado fsico, baseando-se nos princpios da termodinmica.
Quando numa reao ou mudana de estado ocorre liberao de calor,
dizemos que um processo exotrmico. Por outro lado, se h absoro de calor,
trata-se de um processo endotrmico.
A termoqumica importante para a sociedade pois utilizando-a podemos
prever o quanto de calor libera ou absorve uma reao. Isso pode ser utilizado para
se obter benefcios nas reas de combustveis, de alimentos, da sade, entre outros.
Palavras-chave: Absoro. Benefcios. Calor. Termoqumica. Endotrmico. Energia.
Exotrmico. Liberao. Prever. Sociedade. Termoqumica.
SUMRIO
INTRODUO.............................................................................................. 4
DESENVOLVIMENTO.................................................................................. 5
2.1 Termoqumica: Conceitos gerais...................................................................5
2.1.1
Termos tcnicos utilizados................................................................5
2.1.2
Entalpia.............................................................................................6
2.1.3
Energia interna..................................................................................6
2.1.4
Diagrama de energia.........................................................................7
2.1.5
Fatores que influenciam na entalpia.................................................8
2.1.6
Entalpia de combusto ou calor de combusto................................9
2.1.7
Entalpia de dissoluo ou calor de dissoluo.................................10
2.1.8
Entalpia de neutralizao.................................................................11
2.1.9
Entalpia de ligao...........................................................................11
2.1.10 Aplicaes da termoqumica............................................................12
REFERNCIAS............................................................................................13
1 INTRODUO
A Termoqumica o ramo que estuda as trocas de energia, na forma de
calor, envolvidas nas reaes qumicas e nas mudanas de estado fsico.
Quando uma reao ou mudana de estado libera calor, dizemos que
um processo exotrmico. Por outro lado, se h absoro de calor, trata-se de um
processo endotrmico.
Esses processos esto continuamente em nosso cotidiano, tais como na
fotossntese das plantas, na queima de combustveis, na poluio do meio ambiente,
nas mudanas de estado fsico da gua, nas reaes que ocorrem em nosso
organismo e assim por diante.
2 DESENVOLVIMENTO
2.1 Termoqumica: Conceitos gerais
A termoqumica explica as perdas ou ganhos de calor (energia) que
acontecem durante uma reao qumica. Com isso podemos predizer a quantidade
de calor (energia) que ser liberado ou absorvido durante uma reao qumica.
So alguns exemplos de reaes que liberam energia (liberam calor) a
queima do carvo, a queima do gs de cozinha (gs butano) e a queima de
combustveis (gasolina, diesel, etanol), dentre outras reaes. Entretanto, existem
reaes que absorvem energia (absorvem calor) como o cozimento de alimentos, a
fotossntese das plantas e a evaporao de lquidos.
Simplificando, no processo exotrmico o sistema libera ou produz calor
(sensao de resfriamento) enquanto no processo endotrmico o sistema absorve o
calor (sensao de aquecimento).
2.1.1 Termos tcnicos
Alguns dos termos que so utilizados na termoqumica e seus significados:
- Reao endotrmica: So as reaes que absorvem calor;
- Reao exotrmica: So as reaes que liberam ou produzem calor;
- Calorimetria: estudo e medio das quantidades de calor (energia) liberados ou
absorvidos durante as reaes qumicas e processos qumicos;
- Caloria: quantidade de calor necessria para elevar de 14,5 C para 15,5 C a
temperatura de 1 g de gua. Bastante expressa na forma de 1kcal=1000cal;
- Variao de entalpia: a medida da quantidade de calor liberada ou absorvida pela
reao, a presso constante. geralmente expressa por H;
- Equao termoqumica: a equao qumica qual acrescentamos a entalpia da
reao e na qual mencionamos todos os fatores que possam influir no valor dessa
entalpia;
2.1.2 Entalpia
Entalpia (H) o nome dado funo termoqumica igual soma da energia
interna com o produto da presso pelo volume do sistema.
Matematicamente, temos:
E + PV = H = Entalpia
E2 + PV2 = H2 = Entalpia no estado final
E1 + PV1 = H1 = Entalpia no estado inicial
(E + PV) = H = Variao de entalpia
Desta forma pode-se obter a frmula da variao de energia num sistema,
que dada por: E = H P. V
A entalpia sempre se refere energia liberada ou absorvida pela reao em
sistemas abertos, como o caso das reaes feitas em contato com o ar
atmosfrico.
A variao de entalpia a medida da quantidade de calor absorvido ou
liberado de uma reao qumica, a presso constante.
2.1.3 Energia interna
Energia interna nada mais do que a capacidade de um sistema de realizar
um trabalho.
Podemos considerar um sistema gasoso fechado que possui um mbolo que
se desloca sem atrito. Aps o aquecimento do sistema o mbolo se deslocou, o que
significa que o sistema realizou trabalho contra o meio exterior. Se esse trabalho for
positivo, o gs perde energia, sob a forma de trabalho, com o meio exterior e alm
disso, recebe calor (processo endotrmico). Se for negativo, o gs est recebendo
energia, na forma de trabalho, do meio exterior e alm disso perde calor (processo
exotrmico).
Com isso, chegamos ao Primeiro princpio da termodinmica: a variao de
energia interna de um sistema igual diferena entre o calor trocado com o meio
exterior e o trabalho realizado pelo (ou sobre) o sistema. Matematicamente, temos:
E = E1 E2 = Q T.
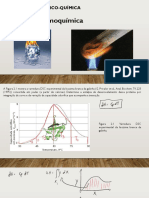
2.1.4 Diagrama de energia
Pela Lei de Hess, temos que a variao de entalpia s depende do estado
inicial e final do processo no dependendo das etapas intermedirias.
Independente do caminho percorrido pelos dois estados, a variao de
entalpia ser a mesma.
Seja um sistema no qual o estado inicial ser representado por A, e o estado
final por D. Considere que existam dois caminhos, pelos quais podemos obter o
estado final a partir do estado inicial.
Fonte: ColgioWeb
Veja abaixo a representao das entalpias dos vrios estados por linhas
horizontais:
Fonte: ColegioWeb
Logo, conforme a Lei de Hess, devemos ter:
HD HA = H1 = H2 + H3 + H4
por esta razo que a Lei de Hess tambm conhecida como a lei da
Atividade das Entalpias.
Dessa forma, possvel representar as variaes de entalpia no formato de
diagrama.
2.1.5 - Fatores que influenciam na entalpia
A variao de entalpia depende de vrios fatores: Quantidade de reagentes
e produtos, forma alotrpica das substncias simples, estado fsico de reagentes e
de produtos, temperatura, presso, existncia ou no de soluo.
Quantidade de substancias:
A 25C e 1atm
0,5H2(g) + 0,5I2(g) -> 1HI
H = +25,9kJ
H2(g) + I2(g) -> 2HI
H = +51,8kJ
Com isso observamos: se dobrarmos as quantidades de reagentes e
produtos, dobraremos a entalpia e tambm a variao de entalpia.
Temperatura:
A 25C e 1atm
Fe2O3(s) + 3H2(g) -> 2Fe(s) + 3H2O(l)
H = -8,39kcal
A 85C e 1atm
Fe2O3(s) + 3H2(g) -> 2Fe(s) + 3H2O(l)
H = -7,1kcal
Tal diferena tem explicao: a quantidade de calor necessria para aquecer
os reagentes de 25C a 85C (2,70 kcal) diferente da quantidade de calor
necessria para aquecer os produtos de 25C para 85C (3,39kcal).
Presso:
Existem substancias que necessitam de presso mnima para a ocorrncia
de variao de entalpia. Alguns gases precisam de at 1000atm. Nos clculos,
utilizada a presso de 1atm, considerada presso padro, vlida para todas as
presses com que se trabalha. Embora no interfira na entalpia, ela pode interferir
indiretamente, afetando o estado fsico de reagentes e produtos.
Estado fsico:
2H2(g) + O2(g) -> 2H2O(g)
H = -115,6kcal
2H2(g) + O2(g) -> 2H2O(l)
H = -136,6kcal
Na transformao de H2O(g) em H2O(l) h liberao de 583 cal/g (calor
latente de liquefao a 25C e 1atm) ou 18 . 583 = 10,5kcal/mol. Como na reao h
formao de 2 mol de gua, a diferena de 2 . 10,5 = 21kcal
Forma alotrpica:
Influem tambm na entalpia ou calor de uma reao as diferentes formas
alotrpicas apresentadas pelos elementos qumicos, como por exemplo:
carbono, como grafite ou diamante;
enxofre, monoclnico ou rmbico;
fsforo, branco ou vermelho;
oxignio, como gs oxignio (O2) ou oznio (O3).
Por exemplo:
C (grafite) + O2 (g) -> CO2 (g)
H1 = 393,1 kJ/mol
C (diamante) + O2 (g) -> CO2 (g)
H2 = 395,0 kJ/mol
Como regra geral, podemos dizer que a forma alotrpica de entalpia maior
a mais reativa; e a de entalpia menor a mais estvel (e portanto mais abundante
quando ocorre na natureza). No ltimo exemplo, a grafite , sem dvida, mais
estvel (e mais abundante na natureza) do que o diamante.
2.1.6 - Entalpia de combusto ou calor de combusto
A Entalpia de combusto, tambm chamada de calor de combusto, a
variao da energia liberada sob a forma de calor atravs da queima de 1 mol de
qualquer substncia, estando todos os reagentes no estado padro (temperatura de
25C, presso de 1 atm. Em nmeros, a variao de entalpia ser sempre negativa,
uma vez que, as reaes de combusto so sempre exotrmicas (H positivo:
10
reao endotrmica, H negativo: reao exotrmica). Nesse tipo de reao, a
energia dos reagentes sempre maior do que a dos produtos. A variao de entalpia
(H) de uma reao obtida a partir da diferena da entalpia dos produtos pela
entalpia dos reagentes. Frmula geral: H = Hp Hr
Diz-se que h combusto quando uma substncia, o combustvel, reage com
oxignio, comburente, gerando a queima. A combusto pode ser classificada
segundo a proporo entre combustvel e gs oxignio
2.1.7 - Entalpia de dissoluo ou calor de dissoluo
a variao de entalpia envolvida na dissoluo de 1mol de determinada
substncia numa quantidade de gua suficiente para que a soluo obtida seja
diluda.
Um tpico processo onde a entalpia de dissoluo pode ser facilmente
evidenciada refere-se dissoluo em gua do vulgo "percloreto de ferro" corretamente cloreto frrico - frequentemente realizada por profissionais ou amantes
de eletrnica a fim de se obter uma soluo adequadamente diluda de forma a
poder ser utilizada no processo de corroso de placas de circuito impresso - placas
de material isolante com uma fina camada de cobre em sua superfcie -, placas
estas sobre as quais primeiro desenham-se e posteriormente corroso montam-se
os circuitos eletrnicos projetados. A dissoluo deve ser feita vagarosamente
tamanho o aquecimento que a mesma provoca, sempre se jogando o percloreto na
gua, e nunca o contrrio. A entalpia de dissoluo para tal produto
consideravelmente alta em mdulo - contudo negativa em valor, visto que a
dissoluo exotrmica.
11
2.1.8 - Entalpia de neutralizao
Entalpia (ou calor) de neutralizao a variao de entalpia (quantidade de
calor liberada) verificada na neutralizao de 1 mol de H + do cido por 1 mol de OH da base, supondo-se todas as substncias em diluio total ou infinita, a 25 C e 1
atm.
Ex:
1 H+(aq) + 1 OH-(aq) H2O()
Esse tipo de reao denominada de neutralizao porque o pH do meio
neutralizado; o pH da gua 7,0 (neutro).
Visto que libera calor, corresponde a reaes exotrmicas, em que a entalpia
(energia global do sistema) sempre ser negativa, menor que zero.
2.1.9 - Entalpia de ligao
Para formar as mais diversas substncias que nos cercam, ligaes
qumicas so quebradas e outras so estabelecidas por meio das reaes.
quantidade de energia envolvida no rompimento de 1 mol de ligaes qumicas entre
tomos numa temperatura de 25C e presso de 1 atmosfera damos o nome de
entalpia de ligao ou energia de ligao.
A quebra das ligaes dos reagentes sempre um processo endotrmico,
ou seja, necessita de calor para que acontea. J o rearranjo dos tomos para
formar novas molculas um processo exotrmico, libera energia. Portanto, o
clculo da variao de entalpia (H) dado pela diferena de energia liberada na
formao das ligaes dos produtos pela energia absorvida no rompimento das
ligaes dos reagentes.
12
2.1.10 Aplicaes da termoqumica
A termoqumica utilizada basicamente para se prever o quanto de energia
uma reao qumica libera ou absorve para ocorrer. Isso pode ser utilizado para
vrias aplicaes, como avaliar a qualidade de combustveis, o controle da
alimentao j que se consumirmos muitos alimentos que fornecem muita energia o
nosso corpo provavelmente armazenar o excesso de energia em forma de gordura.
Tambm so utilizadas as reaes da termoqumica nas usinas termoeltricas (na
qual ocorre uma reao que libera energia em forma de vapor que move um gerador
que converte essa energia em energia eltrica)
13
REFERNCIAS
CORVE, Geraldo Jos. Qumica Covre: O homem e a natureza Vol.2. 1a edio.
FTD, 2000.
FELTRE, Ricardo. Qumica Volume 2. Moderna, 2004.
S QUMICA. TERMOQUMICA. Disponvel em: <
http://www.soq.com.br/conteudos/em/termoquimica/>. Acesso em: 12/06/2016
18h20min
ATKINS, P.W.; JONES, Loretta. Princpios de qumica: questionando a vida
moderna e o meio ambiente. 3.ed. Porto Alegre: Bookman, 2006.
COLGIO WEB. TERMOQUMICA. Disponvel em: <
http://www.colegioweb.com.br/termoquimica-i/>. Acesso em 12/06/2016 18h15min
Das könnte Ihnen auch gefallen
- Enem 2018 - Ciências Da Natureza E Suas TecnologiasVon EverandEnem 2018 - Ciências Da Natureza E Suas TecnologiasNoch keine Bewertungen
- SOLUCAODokument18 SeitenSOLUCAOSilvio MattosNoch keine Bewertungen
- Arantes, Elaine - Etica e Cidadania - redeEtecBrasil - 2013Dokument120 SeitenArantes, Elaine - Etica e Cidadania - redeEtecBrasil - 2013Leila Aoyama100% (4)
- Termoquímica IntroduçãoDokument28 SeitenTermoquímica IntroduçãoleaorsNoch keine Bewertungen
- Capitulo 4 Segunda ProvaDokument47 SeitenCapitulo 4 Segunda ProvaJoão AzevedoNoch keine Bewertungen
- Química OrgânicaDokument16 SeitenQuímica OrgânicaJoão PauloNoch keine Bewertungen
- 1 - Transistor Bipolar PDFDokument53 Seiten1 - Transistor Bipolar PDFAntonio PortelaNoch keine Bewertungen
- Aula TermoquimicaDokument5 SeitenAula TermoquimicaLucas GabrielNoch keine Bewertungen
- Termoquímica 2 ContinuaçãoDokument11 SeitenTermoquímica 2 ContinuaçãoLouNoch keine Bewertungen
- Aula Biofisica TermodinâmicaDokument42 SeitenAula Biofisica TermodinâmicaDavid Cesar Rocha100% (1)
- Introdução À TermoquímicaDokument6 SeitenIntrodução À TermoquímicaJoanna de Paoli100% (1)
- Relatório Fisico QuimicaDokument20 SeitenRelatório Fisico Quimicatigresa69Noch keine Bewertungen
- Relatório 7 F.QDokument12 SeitenRelatório 7 F.QNanda MouraNoch keine Bewertungen
- Questions 1683920145872-TermoquimicaDokument39 SeitenQuestions 1683920145872-TermoquimicaTortruguitaah CascudaNoch keine Bewertungen
- QUIMICADokument9 SeitenQUIMICAJODACOSNoch keine Bewertungen
- TermodinâmicaDokument12 SeitenTermodinâmicaWaldiney SantosNoch keine Bewertungen
- Apostila de Química III 63.107Dokument45 SeitenApostila de Química III 63.107cesarNoch keine Bewertungen
- Relatório de Química Geral - Calor de NeutralizaçãoDokument8 SeitenRelatório de Química Geral - Calor de NeutralizaçãoAntônia Vitória CavalcanteNoch keine Bewertungen
- Aula 3 Entalpia EntropiaDokument14 SeitenAula 3 Entalpia EntropiaJoao Paulo RochaNoch keine Bewertungen
- Apostila de Química III 63.1072Dokument45 SeitenApostila de Química III 63.1072Richard De Medeiros Castro100% (1)
- Aula 5Dokument36 SeitenAula 5Thauan GomesNoch keine Bewertungen
- (Lerio) Quimica FisicaDokument19 Seiten(Lerio) Quimica FisicaOrlando ManuelNoch keine Bewertungen
- Termoquà MicaDokument42 SeitenTermoquà MicaLuiz Fillipe VargasNoch keine Bewertungen
- Biofísica Aula 2 Termodinamica 2016 BetaniaDokument53 SeitenBiofísica Aula 2 Termodinamica 2016 BetaniaBetânia Glória Campos100% (1)
- Aula 2 Calorimetria e TermoquimicaDokument43 SeitenAula 2 Calorimetria e TermoquimicaMartinõ MarcellNoch keine Bewertungen
- EntalpiaDokument8 SeitenEntalpiaThuyline DyandraNoch keine Bewertungen
- Quím 2 AnoDokument9 SeitenQuím 2 AnoFabio FerreiraNoch keine Bewertungen
- TERMODINAMICADokument13 SeitenTERMODINAMICAPedro Tembo BandeNoch keine Bewertungen
- A Lei de Hess Consiste em Calcular As Entalpias de Reações QGDokument7 SeitenA Lei de Hess Consiste em Calcular As Entalpias de Reações QGMércio Emanuel AfonsoNoch keine Bewertungen
- Estudo Dirigido - TermoquimicaDokument4 SeitenEstudo Dirigido - TermoquimicaThiago HenriquesNoch keine Bewertungen
- Relatório Termodinâmica (Calor de Combustão Padrão)Dokument9 SeitenRelatório Termodinâmica (Calor de Combustão Padrão)Priscila SerpaNoch keine Bewertungen
- Termodinamica Parte IVDokument26 SeitenTermodinamica Parte IVGilda SilvaNoch keine Bewertungen
- Gás NaturalDokument52 SeitenGás NaturalAdalton FernandoNoch keine Bewertungen
- Relatorio 1 TermoquimicaDokument12 SeitenRelatorio 1 TermoquimicaLucas CNoch keine Bewertungen
- TermoquímicaDokument6 SeitenTermoquímicaANA PAULA SILVA DOS ANJOSNoch keine Bewertungen
- Termoquimica Mais AvançadaDokument9 SeitenTermoquimica Mais Avançadajupter2005100% (1)
- Termodinamica em Bioquimica Profa FernandaDokument22 SeitenTermodinamica em Bioquimica Profa FernandaEduardo BlackNoch keine Bewertungen
- Aula 01.curso de QuímicaDokument7 SeitenAula 01.curso de Químicaribamar_01100% (1)
- QuímicaDokument2 SeitenQuímicaakatiavitoriaNoch keine Bewertungen
- A Termoquímica-WPS OfficeDokument6 SeitenA Termoquímica-WPS OfficeWayne RegyNoch keine Bewertungen
- Bioenergetica QuestionárioDokument7 SeitenBioenergetica QuestionárioElifas OliveiraNoch keine Bewertungen
- Variacao Da EntalpiaDokument14 SeitenVariacao Da EntalpiaAlfredo Zacarias Feduca AzcNoch keine Bewertungen
- Aula 4 - TermoquímicaDokument38 SeitenAula 4 - TermoquímicaPEDIGOTO ffNoch keine Bewertungen
- Termoquímica e CinéticaDokument23 SeitenTermoquímica e CinéticaronneiafonsoNoch keine Bewertungen
- TermoquímicaDokument7 SeitenTermoquímicaArly maluleque MalulequeNoch keine Bewertungen
- Pré Relatório - Gabriella 6Dokument4 SeitenPré Relatório - Gabriella 6Gabriella FrotamendesNoch keine Bewertungen
- Aquecimento Química Termoquímica 23 11 2021Dokument17 SeitenAquecimento Química Termoquímica 23 11 2021Vinicius de OliveiraNoch keine Bewertungen
- Pratica 5: Dterminação Do Calor de ReaçãoDokument4 SeitenPratica 5: Dterminação Do Calor de ReaçãopatriciaNoch keine Bewertungen
- Quimica - 002 TermoquimicaDokument6 SeitenQuimica - 002 Termoquimicacon_seguirNoch keine Bewertungen
- TermoquimicaDokument18 SeitenTermoquimicaJoelma Dias100% (1)
- PedroDokument9 SeitenPedroAnastacio Augusto Mucupela Augusto MucupelaNoch keine Bewertungen
- VOD-Termoquímica - Equações Gráficos e Entalpia de Formação-2019Dokument15 SeitenVOD-Termoquímica - Equações Gráficos e Entalpia de Formação-2019Natel AmaralNoch keine Bewertungen
- Entalpia Das Transformações QuímicasDokument2 SeitenEntalpia Das Transformações Químicasjulia_goncalves1994Noch keine Bewertungen
- Atividade Quimica 5Dokument3 SeitenAtividade Quimica 5Edson BernusseNoch keine Bewertungen
- Capitulo 8 Termoquimica PDFDokument13 SeitenCapitulo 8 Termoquimica PDFDenis AlmNoch keine Bewertungen
- 5 Bioenergética e FosforilaçãoDokument15 Seiten5 Bioenergética e FosforilaçãoAna SilvaNoch keine Bewertungen
- Aula 8 - FQ - TermoquímicaDokument18 SeitenAula 8 - FQ - TermoquímicaJ. Messias BrittoNoch keine Bewertungen
- Termo Química ExemplificaDokument11 SeitenTermo Química ExemplificaDANTY TanckNoch keine Bewertungen
- Biofísica para ciências biomédicas – 4ª ediçãoVon EverandBiofísica para ciências biomédicas – 4ª ediçãoNoch keine Bewertungen
- 190 PDFDokument63 Seiten190 PDFBruno CaarlosNoch keine Bewertungen
- Regulamento Promoção Equatorial MaranhãoDokument11 SeitenRegulamento Promoção Equatorial MaranhãoAntonio PortelaNoch keine Bewertungen
- Segunda ParteDokument9 SeitenSegunda ParteAntonio PortelaNoch keine Bewertungen
- Cont I Lista 04 2015 1 GDokument2 SeitenCont I Lista 04 2015 1 GAntonio PortelaNoch keine Bewertungen
- Resumo Controle 1Dokument2 SeitenResumo Controle 1Antonio PortelaNoch keine Bewertungen
- ConclusãoDokument1 SeiteConclusãoAntonio PortelaNoch keine Bewertungen
- Ficticia de TrafoDokument131 SeitenFicticia de TrafoGersica CristineNoch keine Bewertungen
- Abntex2cite AlfDokument22 SeitenAbntex2cite AlfWillber NascimentoNoch keine Bewertungen
- Cont Lista 07B 2015 1 G PDFDokument2 SeitenCont Lista 07B 2015 1 G PDFAntonio PortelaNoch keine Bewertungen
- LT Carta Smith PDFDokument21 SeitenLT Carta Smith PDFluherbackNoch keine Bewertungen
- Produtos Notaveis - PDF 5 PDFDokument2 SeitenProdutos Notaveis - PDF 5 PDFAntonio PortelaNoch keine Bewertungen
- Consultório de Avaliação Física: Elaborado Por: Antonio José Portela de Jesus SantosDokument26 SeitenConsultório de Avaliação Física: Elaborado Por: Antonio José Portela de Jesus SantosAntonio PortelaNoch keine Bewertungen
- Cont I Lista 06 2015 1 G PDFDokument2 SeitenCont I Lista 06 2015 1 G PDFAntonio PortelaNoch keine Bewertungen
- Proj Tanq JV 2019 GDokument6 SeitenProj Tanq JV 2019 GAntonio PortelaNoch keine Bewertungen
- Certidao 1534862292741 PDFDokument1 SeiteCertidao 1534862292741 PDFAntonio PortelaNoch keine Bewertungen
- Mate Matic A Comput Ac IonalDokument170 SeitenMate Matic A Comput Ac IonalfrechesNoch keine Bewertungen
- Aula08 Transformadores Parte02Dokument28 SeitenAula08 Transformadores Parte02Cézar NobreNoch keine Bewertungen
- ET74C Aula17 Modelos TBJ R01Dokument39 SeitenET74C Aula17 Modelos TBJ R01Antonio PortelaNoch keine Bewertungen
- SEP 1 - Cap 1 Circuitos TrifasicosDokument48 SeitenSEP 1 - Cap 1 Circuitos TrifasicosLucas MarinhoNoch keine Bewertungen
- CA SispoliDokument36 SeitenCA Sispoli323130Noch keine Bewertungen
- Edital Prpg44-18selecao PpgeeDokument5 SeitenEdital Prpg44-18selecao PpgeeAntonio PortelaNoch keine Bewertungen
- Python para IniciantesDokument15 SeitenPython para IniciantesAntonio PortelaNoch keine Bewertungen
- Calendario Academico VigenteDokument8 SeitenCalendario Academico VigenteMisael AraujoNoch keine Bewertungen
- Plano de NegociosDokument24 SeitenPlano de NegociosAntonio PortelaNoch keine Bewertungen
- Controle de Um Inversor de Frequência Via CLPDokument40 SeitenControle de Um Inversor de Frequência Via CLPEduardo BittencourtNoch keine Bewertungen
- Equipe 1 Planejmento EstratégicoDokument4 SeitenEquipe 1 Planejmento EstratégicoAntonio PortelaNoch keine Bewertungen
- Texto Principios Da Natureza Buraco Negro Luiz Augusto de C G Rodrigues - Docx 3 Aq2eJDOx3rcM4kV7Dokument25 SeitenTexto Principios Da Natureza Buraco Negro Luiz Augusto de C G Rodrigues - Docx 3 Aq2eJDOx3rcM4kV7Mr.AmArELuNoch keine Bewertungen
- Lista de Exercícios - Capítulo 6 PDFDokument1 SeiteLista de Exercícios - Capítulo 6 PDFIsabela De Souza InocenteNoch keine Bewertungen
- Apostila Capacitor2Dokument26 SeitenApostila Capacitor2Leandro NadalNoch keine Bewertungen
- Relatório Análise Granulométrica e SedimentaçãoDokument19 SeitenRelatório Análise Granulométrica e SedimentaçãoTorben UlissesNoch keine Bewertungen
- Atividade Laboratorial - FermentaçãoDokument6 SeitenAtividade Laboratorial - FermentaçãoDaniela Passos 52618 - CMNoch keine Bewertungen
- Exercicios GlucidosDokument6 SeitenExercicios GlucidospscacaoNoch keine Bewertungen
- Exercicios de Manometria CorrDokument3 SeitenExercicios de Manometria CorrRodrigo PérisséNoch keine Bewertungen
- Geração de Energia EletricaDokument23 SeitenGeração de Energia EletricaPedro Jhonathan Martins SanchesNoch keine Bewertungen
- Trab QTDokument26 SeitenTrab QTDelfa SualeheNoch keine Bewertungen
- Aula01 Remoto ExercíciosDokument3 SeitenAula01 Remoto ExercíciosEmerson MatheusNoch keine Bewertungen
- Radiacao e CombinadosDokument6 SeitenRadiacao e CombinadosEvandro LimaNoch keine Bewertungen
- NBR 5356 - 2007 - Transformadores de Potência - Parte 2 - Aq PDFDokument27 SeitenNBR 5356 - 2007 - Transformadores de Potência - Parte 2 - Aq PDFfabianohyaNoch keine Bewertungen
- PMD em FibrasDokument8 SeitenPMD em FibrasRicardi Martinelli MartinsNoch keine Bewertungen
- Física I - AP2 - 2024Dokument2 SeitenFísica I - AP2 - 2024Ibraimo Rui Esmael EsmaelNoch keine Bewertungen
- Relatório de Grade: Ceitep - Centro de Educação E Inovação Técnico ProfissionalDokument2 SeitenRelatório de Grade: Ceitep - Centro de Educação E Inovação Técnico ProfissionalShen PadeiroNoch keine Bewertungen
- Relatorio 10 - Equilibrio Ácido - BaseDokument11 SeitenRelatorio 10 - Equilibrio Ácido - BaseGustavo Rossoni RuyNoch keine Bewertungen
- Reações Acido BaseDokument2 SeitenReações Acido BaseLucilia PereiraNoch keine Bewertungen
- Lista de Exercicios Aula 5Dokument12 SeitenLista de Exercicios Aula 5Azt RibNoch keine Bewertungen
- GlassecViracon E Book Vidros Temperados e TermoendurecidosDokument20 SeitenGlassecViracon E Book Vidros Temperados e TermoendurecidosMaison propre FrancaNoch keine Bewertungen
- Geografia - 6 Ano - 1BDokument31 SeitenGeografia - 6 Ano - 1BGentil Eronides da SvaNoch keine Bewertungen
- Descritores FÍSICArer3reDokument2 SeitenDescritores FÍSICArer3rebritomtaNoch keine Bewertungen
- MHSDokument13 SeitenMHSMarcella ZonNoch keine Bewertungen
- Sulamérica Faculdades: AtençãoDokument2 SeitenSulamérica Faculdades: Atençãolivia sampaioNoch keine Bewertungen
- 01 - Manual de Operaã Ã EsDokument61 Seiten01 - Manual de Operaã Ã EsHebert FirmoNoch keine Bewertungen
- Fluxograma PelotizaçãoDokument1 SeiteFluxograma PelotizaçãoJu CottaNoch keine Bewertungen
- Trabalho de Química: Maria Clara Delfino N°27 1°L Professora RachelDokument8 SeitenTrabalho de Química: Maria Clara Delfino N°27 1°L Professora RachelMaria ClaraNoch keine Bewertungen
- ESCÂNDIODokument2 SeitenESCÂNDIOCamila OliveiraNoch keine Bewertungen
- Glossário de SoldaDokument25 SeitenGlossário de SoldaRogerio ContiNoch keine Bewertungen