Beruflich Dokumente
Kultur Dokumente
Evaluación y Primera Actividad
Hochgeladen von
Santiago Giraldo0 Bewertungen0% fanden dieses Dokument nützlich (0 Abstimmungen)
10 Ansichten3 SeitenOriginaltitel
Evaluación y primera actividad.docx
Copyright
© © All Rights Reserved
Verfügbare Formate
DOCX, PDF, TXT oder online auf Scribd lesen
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
© All Rights Reserved
Verfügbare Formate
Als DOCX, PDF, TXT herunterladen oder online auf Scribd lesen
0 Bewertungen0% fanden dieses Dokument nützlich (0 Abstimmungen)
10 Ansichten3 SeitenEvaluación y Primera Actividad
Hochgeladen von
Santiago GiraldoCopyright:
© All Rights Reserved
Verfügbare Formate
Als DOCX, PDF, TXT herunterladen oder online auf Scribd lesen
Sie sind auf Seite 1von 3
TERMODINMICA - EVALUACIN CONCERTADA
1. (20%) Primer examen parcial (individual): Primera ley de la termodinmica en
sistemas abiertos.
2. (20%) Segundo examen parcial: Ciclo de Rankine (real) simple y Ciclo (real) de
refrigeracin por compresin de vapor.
3. (20%) Trabajo Termodinmica (Formato de Entrega: Impreso/manuscrito En grupos
de mximo 4 personas) (Plazo: Octubre 1)
a. Consultar y describir brevemente los pasos para el diseo de un cuarto de
refrigeracin.
b. Consultar sobre la cintica de los procesos de congelacin de los alimentos (tiempo
de congelacin) y las propiedades de los alimentos congelados. Referenciar cinco
artculos (en ingls) relacionados y presentar un resumen de cada uno de ellos.
c. Consultar en qu consiste el mtodo de la diferencia de temperatura media
logartmica (LMTD) utilizado en el anlisis de los intercambiadores de calor.
Referenciar cinco artculos (en ingls) relacionados y presentar un resumen de cada
uno de ellos.
d. Consultar sobre la aplicacin de los Fluidos Supercrticos en el campo de los
alimentos. Referenciar cinco artculos (en ingls) relacionados y presentar un
resumen de cada uno de ellos.
e. Consultar y definir brevemente el concepto de exerga y mostrar su importancia en
el campo de los alimentos.
f. Consultar qu es el diagrama de Molliere, listar las variables que maneja y explicar
cmo es su lectura.
El diagrama entalpa-entropa, tambin conocido como diagrama de Mollier,
tiene diversas aplicaciones tcnicas. Es muy usado para estimar la entalpa
de sustancias puras, y de las mezclas de sustancias que se encuentran con
mayor frecuencia en Ingeniera.
Se pueden definir cinco zonas en el diagrama. A la izquierda est la zona que
describe el estado slido, separada de la zona de coexistencia de fases
slidolquido por una curva en lnea cortada que pasa por el punto B. A su
derecha la zona de lquido y la curva en lnea cortada que pasa por el punto D
separa la zona de lquido de la zona de coexistencia de fases lquido-vapor.
Esta se encuentra separada de la zona de vapor por la curva en lnea cortada
que pasa por el punto E. Por lo general figuran en este diagrama las curvas que
corresponden a las evoluciones a presin constante (isobaras), las de
sobrecalentamiento constante, y las de ttulo constante. Las curvas de
sobrecalentamiento constante representan el lugar comn de todos los estados
del sistema en los que la temperatura excede de la de saturacin en un valor
fijo. Las curvas de ttulo constante representan el lugar comn de todos los
estados del sistema para los que el contenido de vapor es el mismo. Adems,
en ciertos diagramas tambin se incluyen curvas de volumen constante.
Supongamos que se tiene hielo cuyo estado se representa por el punto A en la
zona del slido. Si se calienta a presin constante se alcanza la curva de fusin
en el punto B y si se sigue calentando se alcanza la curva de puntos de burbuja
en el punto D. Si continuamos calentando se alcanza la curva de puntos de
roco en el punto E. A partir de ese punto y hasta el F el proceso produce vapor
recalentado. Normalmente la zona de slido no tiene aplicacin, de manera
que el diagrama usado para clculos tcnicos tiene el origen de coordenadas
aproximadamente en donde est el punto D. Los diagramas usados en la
prctica tienen un aspecto parecido al que se observa a la derecha. La zona
rayada diagonal es lo que realmente se representa en la prctica. En l
podemos ver las curvas de ttulo constante en el interior de la zona de
coexistencia de fases, en lnea cortada y las curvas isobaras y de
recalentamiento constante en la zona de vapor recalentado. En estos
diagramas interesa fundamentalmente estimar valores de entalpa lo mas
exactamente que sea posible en la zona de vapor recalentado, situada por
encima y a la derecha de la curva de puntos de roco. Por eso es la zona mas
ampliada del diagrama de Mollier en la forma usada para clculos de
ingeniera.
El diagrama entalpa-entropa, tambin conocido como diagrama de Mollier, tiene diversas
aplicaciones tcnicas. Es muy usado para estimar la entalpa de sustancias puras, y de las mezclas
de
sustancias
que
se
encuentran
con
mayor
frecuencia
en
Ingeniera.
La carta de Mollier sirve para simplificar clculos de la entalpia, de la entropa, de la presin, de la
temperatura, del volumen especfico y de la calidad del vapor y del agua. El diagrama de Mollier es
la representacin de las propiedades del agua y vapor de agua. Se usa un sistema principal de
coordenadas
H-S
(Entalpa-Entropa).
Se pueden definir cinco zonas en el diagrama. A la izquierda est la zona que describe el estado
slido,
separada
de
la
zona
de
coexistencia
de fases slidolquido por una curva en lnea cortada que pasa por el punto B. A su derecha la zona
de lquido y la curva en lnea cortada que pasa por el punto D separa la zona de lquido de la zona
de coexistencia de fases lquido-vapor.Esta se encuentra separada de la zona de vapor por la
curva en lnea cortada que pasa por el punto E.
4. (20%) Presentacin acerca de un problema termodinmico (En grupos de mximo 4
personas) (Noviembre)
a. Proponer un problema termodinmico relacionado con el campo de los alimentos.
b. Realizar una revisin bibliogrfica con el objetivo de indagar acerca de la
problemtica propuesta y los conceptos termodinmicos involucrados mediante una
consulta -en profundidad- de diversas fuentes: libros, artculos cientficos, tesis,
conferencias, normativas tcnicas, entre otras, de tal forma que se posibilite abrir
una discusin acerca del problema.
c. Con base en la revisin bibliogrfica, realizar una presentacin con diapositivas (en
ppt) bajo las siguientes condiciones: uno, deben participar todos los integrantes del
grupo; dos, debe planearse para presentarse en un tiempo mximo de 20 minutos;
tres, deben entregarse memorias de la presentacin; cuatro, debe hacerse alusin a
las propiedades termodinmicas y a los modelos matemticos relacionados con la
temtica; y por ltimo, las explicaciones de los conceptos debe representarse y
privilegiar el uso de imgenes, grficos o dibujos.
5. (20%) Seguimiento (Quices, Consultas, Talleres, entre otros.) En esta evaluacin se
ponderarn las mejores cinco notas de cada estudiante.
ACTIVIDAD PARA LA PRXIMA CLASE: CONSTITUYENDO UN SENTIDO
HACIA LA TERMODINMICA EN LA INGENIERA DE ALIMENTOS
1. Leer el captulo 1 del libro Qu es la entropa? de Vittorio Silvestrini. El enlace
para la descarga del libro est disponible en http://lolabits.es/Nomada/QUE-ES-LAENTROPIA-Vittorio-Silvestrini,8943578.pdf
2. Ver (desde el minuto 55) el video: La humanidad desde el espacio disponible en:
https://www.youtube.com/watch?v=IzcU6sGm_Pw
3. Ver el video Las leyes de la termodinmica en 5 minutos disponible en:
https://www.youtube.com/watch?v=Bvfn6eUhUAc
Das könnte Ihnen auch gefallen
- BlockchainDokument5 SeitenBlockchainSantiago GiraldoNoch keine Bewertungen
- CambiosDokument4 SeitenCambiosSantiago GiraldoNoch keine Bewertungen
- Qué Cambios Ha Marcado La Era DigitalDokument1 SeiteQué Cambios Ha Marcado La Era DigitalSantiago GiraldoNoch keine Bewertungen
- Problemas de DiluciónDokument1 SeiteProblemas de DiluciónSantiago GiraldoNoch keine Bewertungen
- TenacidadDokument2 SeitenTenacidadSantiago GiraldoNoch keine Bewertungen
- Informe de ManometriaDokument1 SeiteInforme de ManometriaSantiago GiraldoNoch keine Bewertungen
- Cibergrafia Higiene y Manipulacion AlimentosDokument3 SeitenCibergrafia Higiene y Manipulacion AlimentosSantiago GiraldoNoch keine Bewertungen
- F3.PR5.PE2 Lista de Verificación Unidades de Servicio v2Dokument4 SeitenF3.PR5.PE2 Lista de Verificación Unidades de Servicio v2Santiago GiraldoNoch keine Bewertungen
- Manual de Responsabilidad Social para PYMESDokument100 SeitenManual de Responsabilidad Social para PYMESyosolinoNoch keine Bewertungen
- Casi Nunca Por C. DominguezDokument14 SeitenCasi Nunca Por C. DominguezJuan ÁlvarezNoch keine Bewertungen
- Diseñando La Propuesta de Valor Mega 0Dokument2 SeitenDiseñando La Propuesta de Valor Mega 0DamianNoch keine Bewertungen
- Sesión 1Dokument5 SeitenSesión 1MARIO DANIEL AGUIRRE NEYRANoch keine Bewertungen
- Rendición de Caja Chica ModeloDokument6 SeitenRendición de Caja Chica ModeloPool Pinelo GomezNoch keine Bewertungen
- Trastorno Del ApegoDokument36 SeitenTrastorno Del ApegoLeticia MoralesNoch keine Bewertungen
- Evolucion Del Sistema Productivo Agropecuario ArgentinoDokument6 SeitenEvolucion Del Sistema Productivo Agropecuario ArgentinoMartin CarugattiNoch keine Bewertungen
- Incado de PilotesDokument9 SeitenIncado de PilotesDIEGONoch keine Bewertungen
- Mat I BDokument178 SeitenMat I BEduardo RubioNoch keine Bewertungen
- TRABAJO DE CIVIL - Luis NarvaezDokument12 SeitenTRABAJO DE CIVIL - Luis NarvaezJunior OchoaNoch keine Bewertungen
- Iso Iec 27003-2017Dokument52 SeitenIso Iec 27003-2017Jorge Cabal Prieto75% (4)
- S07Virtual - El Informe de Recomendación - PC1 - Formato BorradorDokument5 SeitenS07Virtual - El Informe de Recomendación - PC1 - Formato BorradorEduardo ZavaletaNoch keine Bewertungen
- SEGUNDA CONDICIÓN DE EQUILIBRIO - MiluzkaDokument11 SeitenSEGUNDA CONDICIÓN DE EQUILIBRIO - MiluzkaMiletLeeSan-ConNoch keine Bewertungen
- Tarea Semana 6Dokument6 SeitenTarea Semana 6Joyas Mar PauNoch keine Bewertungen
- Mpls PreguntasDokument7 SeitenMpls PreguntasluisNoch keine Bewertungen
- DECRETO 3112 DE 1997 - Habilitación y Prestación de Servicio Transporte FluvialDokument17 SeitenDECRETO 3112 DE 1997 - Habilitación y Prestación de Servicio Transporte FluvialMelissa ScottNoch keine Bewertungen
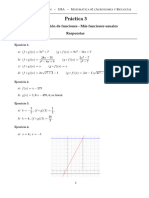
- Matemática 61 (CBC) - Práctica 3 - ResoluciónDokument7 SeitenMatemática 61 (CBC) - Práctica 3 - ResoluciónPedro MayolNoch keine Bewertungen
- Formato para Ejercicio TRDDokument2 SeitenFormato para Ejercicio TRDEsteban CorrealesNoch keine Bewertungen
- Informe Del Laboratorio de Física 1 Presion HidrostaticaDokument5 SeitenInforme Del Laboratorio de Física 1 Presion HidrostaticaJucelso López Contreras100% (1)
- Curriculum Vitae Juan Jaime Pardo RodriguezDokument7 SeitenCurriculum Vitae Juan Jaime Pardo RodriguezPaola Meza MaldonadoNoch keine Bewertungen
- El Ocio y El Tiempo Libre en La Sociedad Actual-José Luis Muñoz Corvalán-MurciaDokument8 SeitenEl Ocio y El Tiempo Libre en La Sociedad Actual-José Luis Muñoz Corvalán-MurciaAndrea GarmendiaNoch keine Bewertungen
- Serv Cap 108 01riesgoelectrico 151215164114Dokument12 SeitenServ Cap 108 01riesgoelectrico 151215164114JOHAN CONTRERASNoch keine Bewertungen
- Tema 5Dokument51 SeitenTema 5Melissa Torres VergaraNoch keine Bewertungen
- Carta de Una Persona MigranteDokument5 SeitenCarta de Una Persona MigranteIgnacioSDRNoch keine Bewertungen
- Igc20-Lem-240-10 Sucs - C10-M11Dokument3 SeitenIgc20-Lem-240-10 Sucs - C10-M11Carlos DiazNoch keine Bewertungen
- Modulador RFDokument2 SeitenModulador RFJuan Camilo Cortes CanchimboNoch keine Bewertungen
- Fiona Davenport - 1. Bought For MarriageDokument99 SeitenFiona Davenport - 1. Bought For MarriageSilvana Ciao100% (4)
- La IatrogeniaDokument29 SeitenLa IatrogeniaShessly GM0% (1)
- MEM. CALCULO ESCALERA MET. No. 1Dokument12 SeitenMEM. CALCULO ESCALERA MET. No. 1Industrial FurnitureNoch keine Bewertungen
- 4-Sintesis de Infancia y PoderDokument4 Seiten4-Sintesis de Infancia y Poderrosi86troncoso100% (5)