Beruflich Dokumente
Kultur Dokumente
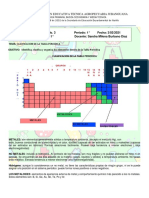
Grupos de La Tabla Periodica
Hochgeladen von
Juan Carlos Silva Gonzalez100%(1)100% fanden dieses Dokument nützlich (1 Abstimmung)
69 Ansichten4 SeitenLa tabla periódica está organizada en 18 grupos verticales. Los elementos dentro de cada grupo comparten propiedades químicas similares como su configuración electrónica y valencia. Algunos grupos tienen nombres como los metales alcalinos en el grupo 1 y los gases nobles en el grupo 18. Aunque los grupos del 3 al 10 no tienen nombres comunes, los elementos dentro de cada grupo tienden a mostrar patrones en sus propiedades físicas como el radio atómico y la energía de ionización.
Originalbeschreibung:
Originaltitel
GRUPOS DE LA TABLA PERIODICA.docx
Copyright
© © All Rights Reserved
Verfügbare Formate
DOCX, PDF, TXT oder online auf Scribd lesen
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenLa tabla periódica está organizada en 18 grupos verticales. Los elementos dentro de cada grupo comparten propiedades químicas similares como su configuración electrónica y valencia. Algunos grupos tienen nombres como los metales alcalinos en el grupo 1 y los gases nobles en el grupo 18. Aunque los grupos del 3 al 10 no tienen nombres comunes, los elementos dentro de cada grupo tienden a mostrar patrones en sus propiedades físicas como el radio atómico y la energía de ionización.
Copyright:
© All Rights Reserved
Verfügbare Formate
Als DOCX, PDF, TXT herunterladen oder online auf Scribd lesen
100%(1)100% fanden dieses Dokument nützlich (1 Abstimmung)
69 Ansichten4 SeitenGrupos de La Tabla Periodica
Hochgeladen von
Juan Carlos Silva GonzalezLa tabla periódica está organizada en 18 grupos verticales. Los elementos dentro de cada grupo comparten propiedades químicas similares como su configuración electrónica y valencia. Algunos grupos tienen nombres como los metales alcalinos en el grupo 1 y los gases nobles en el grupo 18. Aunque los grupos del 3 al 10 no tienen nombres comunes, los elementos dentro de cada grupo tienden a mostrar patrones en sus propiedades físicas como el radio atómico y la energía de ionización.
Copyright:
© All Rights Reserved
Verfügbare Formate
Als DOCX, PDF, TXT herunterladen oder online auf Scribd lesen
Sie sind auf Seite 1von 4
-GRUPOS DE LA TABLA
PERIODICA-
A las columnas verticales de la tabla peridica se las conoce como grupos o
familias. Hay 18 grupos en la tabla peridica estndar. En virtud de un convenio
internacional de denominacin, los grupos estn numerados de 1 a 18 desde la
columna ms a la izquierda los metales alcalinos hasta la columna ms a la
derecha los gases nobles.53 Anteriormente se utilizaban nmeros romanos
segn la ltima cifra del convenio de denominacin de hoy en da por ejemplo,
los elementos del grupo 4 estaban en el IVB y los del grupo 14 en el IVA. En
Estados Unidos, los nmeros romanos fueron seguidos por una letra A si el
grupo estaba en el bloque s o p, o una B si perteneca al d. En Europa, se
utilizaban letras en forma similar, excepto que A se usaba si era un grupo
precedente al 10, y B para el 10 o posteriores. Adems, sola tratarse a los
grupos 8, 9 y 10 como un nico grupo triple, conocido colectivamente en ambas
notaciones como grupo VIII. En 1988 se puso en uso el nuevo sistema de
nomenclatura IUPAC se pone en uso, y se desecharon los nombres de grupo
previos.54
Algunos de estos grupos tienen nombres triviales no sistemticos, como se ve
en la tabla de abajo, aunque no siempre se utilizan. Los grupos del 3 al 10 no
tienen nombres comunes y se denominan simplemente mediante sus nmeros de
grupo o por el nombre de su primer miembro por ejemplo, el grupo de
escandio para el 3, ya que presentan un menor nmero de similitudes y/o
tendencias verticales.53
Grupo 1 (I A): metales alcalinos
Grupo 2 (II A): metales alcalinotrreos
Grupo 3 (III B): familia del Escandio (tierras raras y actinidos)
Grupo 4 (IV B): familia del Titanio
Grupo 5 (V B): familia del Vanadio
Grupo 6 (VI B): familia del Cromo
Grupo 7 (VII B): familia del Manganeso
Grupo 8 (VIII B): familia del Hierro
Grupo 9 (VIII B): familia del Cobalto
Grupo 10 (VIII B): familia del Nquel
Grupo 11 (I B): familia del Cobre
Grupo 12 (II B): familia del Zinc
Grupo 13 (III A): trreos
Grupo 14 (IV A): carbonoideos
Grupo 15 (V A): nitrogenoideos
Grupo 16 (VI A): calcgenos o anfgenos
Grupo 17 (VII A): halgenos
Grupo 18 (VIII A): gases nobles
La explicacin moderna del ordenamiento en la tabla peridica es que los
elementos de un grupo poseen configuraciones electrnicas similares y la misma
valencia, entendida como el nmero de electrones en la ltima capa. Dado que las
propiedades qumicas dependen profundamente de las interacciones de los
electrones que estn ubicados en los niveles ms externos, los elementos de un
mismo grupo tienen propiedades qumicas similares y muestran una tendencia
clara en sus propiedades al aumentar el nmero atmico.55
Por ejemplo, los elementos en el grupo 1 tienen una configuracin electrnica ns1
y una valencia de 1 un electrn externo y todos tienden a perder ese electrn
al enlazarse como iones positivos de +1. Los elementos en el ltimo grupo de la
derecha son los gases nobles, los cuales tienen lleno su ltimo nivel de energa
regla del octeto y, por ello, son excepcionalmente no reactivos y son tambin
llamados gases inertes.
Los elementos de un mismo grupo tienden a mostrar patrones en el radio atmico,
energa de ionizacin y electronegatividad. De arriba a abajo en un grupo,
aumentan los radios atmicos de los elementos. Puesto que hay niveles de
energa ms llenos, los electrones de valencia se encuentran ms alejados del
ncleo. Desde la parte superior, cada elemento sucesivo tiene una energa de
ionizacin ms baja, ya que es ms fcil quitar un electrn en los tomos que
estn menos fuertemente unidos. Del mismo modo, un grupo tiene una
disminucin de electronegatividad desde la parte superior a la inferior debido a
una distancia cada vez mayor entre los electrones de valencia y el ncleo.56
Hay excepciones a estas tendencias, como por ejemplo lo que ocurre en el grupo
11, donde la electronegatividad aumenta ms abajo en el grupo.57 Adems, en
algunas partes de la tabla peridica como los bloques d y f, las similitudes
horizontales pueden ser tan o ms pronunciadas que las verticales.58 59 60.
GRUPO DE LA TABLA PERIODICA
VERONICA SILVA GARCIA
LICENCIADA:
IBIS DONADO
ITISOL
BIOLOGIA
9-A
SOLEDAD-ATLANTICO
2016
Das könnte Ihnen auch gefallen
- Estructura de La Tabla PeriódicaDokument3 SeitenEstructura de La Tabla Periódicaesni10Noch keine Bewertungen
- De la estructura atómica a la quiralidad.: Algunos conceptos de la químicaVon EverandDe la estructura atómica a la quiralidad.: Algunos conceptos de la químicaBewertung: 5 von 5 Sternen5/5 (1)
- Practica 4 Tabla PeriodicaDokument11 SeitenPractica 4 Tabla PeriodicaDiego Celis0% (2)
- Estructura y Organización de La Tabla PeriódicaDokument13 SeitenEstructura y Organización de La Tabla PeriódicaAriNoch keine Bewertungen
- QUIMICA, Elementos Tabla PeriodicaDokument16 SeitenQUIMICA, Elementos Tabla Periodicajeanetteaponte7353Noch keine Bewertungen
- Estructura y Organizacion de La Tabla PeriodicaDokument14 SeitenEstructura y Organizacion de La Tabla PeriodicaBetty PierreNoch keine Bewertungen
- Tabla PeriódicaDokument10 SeitenTabla PeriódicaNoel GalaNoch keine Bewertungen
- Tabla Periodica RamsesDokument10 SeitenTabla Periodica RamsesRamsésNoch keine Bewertungen
- Grupos de La Tabla PeriodicaDokument1 SeiteGrupos de La Tabla PeriodicaDeilyn ParedesNoch keine Bewertungen
- Repaso Quimica SeptimoDokument4 SeitenRepaso Quimica SeptimoluciaNoch keine Bewertungen
- Trabajo de Quimica 2Dokument6 SeitenTrabajo de Quimica 2erlin4rafael4palmeroNoch keine Bewertungen
- Configuracion Electronica y El Espectro de Los ElementosDokument17 SeitenConfiguracion Electronica y El Espectro de Los ElementosWagnerRonaldCcalloTurpoNoch keine Bewertungen
- Características de PersonalidadDokument8 SeitenCaracterísticas de PersonalidadVictorNoch keine Bewertungen
- Historia de La Tabla PeriódicaDokument12 SeitenHistoria de La Tabla PeriódicaWicho AlonzoNoch keine Bewertungen
- Propiedades Tabla PeriodicaDokument5 SeitenPropiedades Tabla PeriodicaPAPELERIA PEKESNoch keine Bewertungen
- Propiedades Físicas y Químicas de La Tabla PeriodicaDokument3 SeitenPropiedades Físicas y Químicas de La Tabla PeriodicaJoan Stiven Astudillo V50% (2)
- Familias de La Tabla PeriódicaDokument8 SeitenFamilias de La Tabla Periódicaines martinezNoch keine Bewertungen
- Estructura de La Tabla PeriodicaDokument5 SeitenEstructura de La Tabla PeriodicaS H O C K O U TNoch keine Bewertungen
- La Tabla PeriodicaDokument4 SeitenLa Tabla PeriodicaIvan Esmit MayhuaNoch keine Bewertungen
- Estructura y Organización de La Tabla PeriodicaDokument2 SeitenEstructura y Organización de La Tabla PeriodicaSosa Limpias Anahi100% (1)
- Grupos de La Tabla PeriódicaDokument5 SeitenGrupos de La Tabla PeriódicaMolly TresanNoch keine Bewertungen
- Ficha de Estudio Julio Tercer GradoDokument17 SeitenFicha de Estudio Julio Tercer GradoElvis RamirezNoch keine Bewertungen
- Trabajo #3 de QuimicaDokument11 SeitenTrabajo #3 de QuimicaAdrian Humberto FloresNoch keine Bewertungen
- Tabla Periã DicaDokument7 SeitenTabla Periã DicaJF CesarNoch keine Bewertungen
- Clasificación de Los Elementos y Su Presencia % en El Cuerpo HumanoDokument4 SeitenClasificación de Los Elementos y Su Presencia % en El Cuerpo HumanoMemo AguilarNoch keine Bewertungen
- Grupos Aequipo3Dokument36 SeitenGrupos Aequipo3Edgar Derek PeraltaNoch keine Bewertungen
- Tabla PeriodicaDokument10 SeitenTabla PeriodicaChon Hdez100% (1)
- Tabla Periodica Tema 3 UltmoDokument29 SeitenTabla Periodica Tema 3 UltmoCristhian ChavezNoch keine Bewertungen
- 4 2siiDokument10 Seiten4 2siiCHRISTOPHER ENMANUEL POCASANGRE PAZNoch keine Bewertungen
- Grupos de La Tabla PeriodicaDokument3 SeitenGrupos de La Tabla PeriodicaJoselee Ramos TitoNoch keine Bewertungen
- Tabla Periodica de LosDokument1 SeiteTabla Periodica de LosLes JimenezNoch keine Bewertungen
- Familias de La Tabla Periodica IDokument5 SeitenFamilias de La Tabla Periodica IAnita Tenemaza100% (2)
- Partes de La Tabla PeriódicaDokument4 SeitenPartes de La Tabla Periódicasandro portillaNoch keine Bewertungen
- Cómo Aumenta El RADIO ATÓMICO en La Tabla PeriódicaDokument5 SeitenCómo Aumenta El RADIO ATÓMICO en La Tabla PeriódicaAngel MuñozNoch keine Bewertungen
- Tabla PeriodicaDokument16 SeitenTabla PeriodicaGermanNoch keine Bewertungen
- Propiedades de La Tabla PeriódicaDokument16 SeitenPropiedades de La Tabla PeriódicamanuellleNoch keine Bewertungen
- Clasificación de Los Grupos de La TablaDokument7 SeitenClasificación de Los Grupos de La TablaInesita Ortega SilvaNoch keine Bewertungen
- Cuadro Sinoptico de Las Propiedades Periodicas de La TablaDokument8 SeitenCuadro Sinoptico de Las Propiedades Periodicas de La TablaKarla Navarro67% (3)
- Practica #1 - Estudio de La Tabla PeriodicaDokument13 SeitenPractica #1 - Estudio de La Tabla PeriodicaAlvaro Barrientos CarvajalNoch keine Bewertungen
- Características de La TablaDokument6 SeitenCaracterísticas de La TablaLuisao Aldas OlallaNoch keine Bewertungen
- CARPETA RECUPERATIVA 1ero de SECUNDARIADokument26 SeitenCARPETA RECUPERATIVA 1ero de SECUNDARIAEsther Alberti PinzasNoch keine Bewertungen
- Clasificacion de Los ElementosDokument4 SeitenClasificacion de Los ElementosYesica Núñez RiosNoch keine Bewertungen
- Tabla Periodica de Los Elementos QuimicosDokument4 SeitenTabla Periodica de Los Elementos QuimicosDz AlexisNoch keine Bewertungen
- La Tabla Periódica ActualDokument18 SeitenLa Tabla Periódica ActualPepe TeranNoch keine Bewertungen
- Taller de QuimicaDokument7 SeitenTaller de Quimicacristina arrietaNoch keine Bewertungen
- Investigacion Tabla PeriodicaDokument9 SeitenInvestigacion Tabla PeriodicaMisael IxcotNoch keine Bewertungen
- Qué Es La Tabla PeriódicaDokument5 SeitenQué Es La Tabla PeriódicaElero JoseNoch keine Bewertungen
- TP QuimicaDokument4 SeitenTP QuimicaHiNoch keine Bewertungen
- Presentacion Tecnologico.Dokument6 SeitenPresentacion Tecnologico.Isael Perez JacomeNoch keine Bewertungen
- FQ TeoriaDokument6 SeitenFQ TeoriacharlyNoch keine Bewertungen
- Unidad - II (1) Tabla Periodica SafaDokument10 SeitenUnidad - II (1) Tabla Periodica SafaMaria Laura PaglialongaNoch keine Bewertungen
- Tema #3. La Tabla PeriódicaDokument6 SeitenTema #3. La Tabla PeriódicaandreaNoch keine Bewertungen
- Descripcion de La Tabla PeriodicaDokument5 SeitenDescripcion de La Tabla PeriodicaAngel tNoch keine Bewertungen
- División de La Tabla PeriódicaDokument7 SeitenDivisión de La Tabla Periódicaabigail Dominic George PerezNoch keine Bewertungen
- SergioDokument13 SeitenSergioGraciela Ticona LuqueNoch keine Bewertungen
- Material de Química 2Dokument10 SeitenMaterial de Química 2KIMBERLY NICOLLE GONZALEZ HERNANDEZNoch keine Bewertungen
- Tabla PeriodicaDokument19 SeitenTabla PeriodicaJoaquin AraujoNoch keine Bewertungen
- Definicion Del AtomoDokument10 SeitenDefinicion Del AtomoYelytsa RendónNoch keine Bewertungen
- Triadas de DöbereinerDokument7 SeitenTriadas de DöbereinerGaby Cruz100% (1)
- Tarea 1 Unidad 1Dokument2 SeitenTarea 1 Unidad 1Juan Carlos Silva GonzalezNoch keine Bewertungen
- La Guerra y La DiplomaciaDokument2 SeitenLa Guerra y La DiplomaciaJuan Carlos Silva GonzalezNoch keine Bewertungen
- Playa MendozaDokument1 SeitePlaya MendozaJuan Carlos Silva GonzalezNoch keine Bewertungen
- Estructura Organizativa de Un Operador PortuarioDokument10 SeitenEstructura Organizativa de Un Operador PortuarioJuan Carlos Silva GonzalezNoch keine Bewertungen
- A Partir de La Lectura de La Documentación Del MóduloDokument9 SeitenA Partir de La Lectura de La Documentación Del MóduloJuan Carlos Silva GonzalezNoch keine Bewertungen
- Mejorar La Seguridad en La Utilización de MedicamentosDokument9 SeitenMejorar La Seguridad en La Utilización de MedicamentosJuan Carlos Silva GonzalezNoch keine Bewertungen
- El Boom de Las Commodities y El Crecimiento Economico en America LatinaDokument4 SeitenEl Boom de Las Commodities y El Crecimiento Economico en America LatinaJuan Carlos Silva GonzalezNoch keine Bewertungen
- RESEÑA Violencia de GéneroDokument6 SeitenRESEÑA Violencia de GéneroJuan Carlos Silva GonzalezNoch keine Bewertungen
- Influencia de La Cultura YanquiDokument2 SeitenInfluencia de La Cultura YanquiJuan Carlos Silva Gonzalez100% (2)
- Primera Relación Hernan CortezDokument1 SeitePrimera Relación Hernan CortezJuan Carlos Silva GonzalezNoch keine Bewertungen
- Adopcion Entre Parejas GaysDokument33 SeitenAdopcion Entre Parejas GaysJuan Carlos Silva GonzalezNoch keine Bewertungen
- Guía Trabajo Amor DemoniosDokument4 SeitenGuía Trabajo Amor DemoniosJuan Carlos Silva GonzalezNoch keine Bewertungen
- Guía Trabajo Amor DemoniosDokument4 SeitenGuía Trabajo Amor DemoniosJuan Carlos Silva GonzalezNoch keine Bewertungen
- Ejercicios Resueltos Circuitos PDFDokument4 SeitenEjercicios Resueltos Circuitos PDFJavis PerezNoch keine Bewertungen
- Manual Monitoreo Rio Rocha CDokument62 SeitenManual Monitoreo Rio Rocha CerickNoch keine Bewertungen
- Planilla de Formulas Lacteas y Cuadros Comparativos. Abarca, Castillo, Rodríguez, TriviñoDokument3 SeitenPlanilla de Formulas Lacteas y Cuadros Comparativos. Abarca, Castillo, Rodríguez, TriviñoEvelyn Gabriela Zamora GormazNoch keine Bewertungen
- Guia No 3 Quimica Grado 11Dokument4 SeitenGuia No 3 Quimica Grado 11sandra burbanoNoch keine Bewertungen
- Ficha Oxidos AcidosDokument2 SeitenFicha Oxidos AcidosYamila GandolfoNoch keine Bewertungen
- Infografía QuímicaDokument5 SeitenInfografía QuímicaJose Angel Cortes Baillet100% (2)
- Laboratorio 1Dokument21 SeitenLaboratorio 1Daniel Jose Vilcarano Castellanos100% (1)
- Problemas Propiedades MecanicasDokument2 SeitenProblemas Propiedades MecanicasPaul Alvarado0% (1)
- Obtencion de AluminaDokument12 SeitenObtencion de Aluminasussi0% (1)
- Info 8 AnaliticaDokument3 SeitenInfo 8 AnaliticaAndres QuinteroNoch keine Bewertungen
- P ComplejosDokument2 SeitenP ComplejosLuis VillonNoch keine Bewertungen
- ARO SoldadorDokument2 SeitenARO SoldadorFrancisco MancoNoch keine Bewertungen
- Discos de Corte TyrolitDokument5 SeitenDiscos de Corte TyrolitJacinto LopezNoch keine Bewertungen
- Taller Evaluativo de Refuerzo - Quimica - II Periodo - OnceDokument2 SeitenTaller Evaluativo de Refuerzo - Quimica - II Periodo - OnceMichelle :DNoch keine Bewertungen
- Balanceo Por El Método Del Número de OxidaciónDokument14 SeitenBalanceo Por El Método Del Número de OxidaciónIrvin JosueNoch keine Bewertungen
- 3390 Ingecons PLDokument1 Seite3390 Ingecons PLVivi RodriguezNoch keine Bewertungen
- Ciclo Del AzufreDokument2 SeitenCiclo Del AzufreLucy Lara Aguilar100% (1)
- Taller Tabla Periòdica - Ing Industrial - LEON-ROSERO-RENDONDokument4 SeitenTaller Tabla Periòdica - Ing Industrial - LEON-ROSERO-RENDONЯaulNoch keine Bewertungen
- Ava Nat - Sistema de Elementos QuimicosDokument6 SeitenAva Nat - Sistema de Elementos QuimicosR MarolvNoch keine Bewertungen
- Reacciones de Los MetalpirrolesDokument10 SeitenReacciones de Los MetalpirrolesJosé Álvarez RoblesNoch keine Bewertungen
- Nomenclatura CorregidaDokument8 SeitenNomenclatura CorregidaMaca GuerreroNoch keine Bewertungen
- Apunte Soldadura - Winschu PDFDokument92 SeitenApunte Soldadura - Winschu PDFJuanQüínNoch keine Bewertungen
- NH-FT-PT-086 FULL KIDS SACHET X 15gDokument1 SeiteNH-FT-PT-086 FULL KIDS SACHET X 15gNatural Health E.U. CalidadNoch keine Bewertungen
- Redox. Ejercicios EvAUDokument8 SeitenRedox. Ejercicios EvAUmartaNoch keine Bewertungen
- Iones Poliatomicos (Parte 1)Dokument15 SeitenIones Poliatomicos (Parte 1)Laura Nicole83% (6)
- Trabajo Evaluativo - 4º Año - Dic - 2020Dokument4 SeitenTrabajo Evaluativo - 4º Año - Dic - 2020Miqueas MamaniNoch keine Bewertungen
- Celdas ElectroquimicasDokument5 SeitenCeldas ElectroquimicasWalther JesusNoch keine Bewertungen
- Electrólisis de La SalmueraDokument9 SeitenElectrólisis de La SalmueraNenisKaroNoch keine Bewertungen
- Determinación de Cloruros en Aguas Corrientes y Aguas Minerales Naturales Por El Procedimiento de MohrDokument23 SeitenDeterminación de Cloruros en Aguas Corrientes y Aguas Minerales Naturales Por El Procedimiento de MohrsilviaNoch keine Bewertungen
- Taller Introdutorio John Steven EspañaDokument12 SeitenTaller Introdutorio John Steven EspañaStiven EspañaNoch keine Bewertungen