Beruflich Dokumente
Kultur Dokumente
Tema 1 - Introduccion
Hochgeladen von
Jose Maria Redondo GomezOriginaltitel
Copyright
Verfügbare Formate
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
Verfügbare Formate
Tema 1 - Introduccion
Hochgeladen von
Jose Maria Redondo GomezCopyright:
Verfügbare Formate
QUMICA DE SUPERFICIES - TEMA 1.- INTRODUCCIN.
TEMA 1.- INTRODUCCIN
SUPERFICIES.
1 de 9
LA
QUMICA
DE
1. Definiciones.
Esta materia trata de los procesos de degradacin qumica de las superficies de los
diversos materiales. Generalmente se le aplica el trmino corrosin, que en el sentido
ms amplio, es un fenmeno natural, por medio del cual los sistemas qumicos expresan
su tendencia hacia un estado de equilibrio estable y puede definirse de varias maneras:
a) destruccin o deterioracin de un material a causa de su reaccin con el medio
ambiente;
b) destruccin de los materiales por medios cualesquiera, excepto mecnicos;
c) proceso inverso de la metalurgia extractiva, en virtud del cual los materiales
metlicos tienden a volver al estado combinado, en el que se encuentran en la
naturaleza, etc., etc.
La definicin ms apropiada depende del alcance que se le quiera dar; la ltima slo es
aplicable a metales y aleaciones, las primeras a todo slido, metlico o no.
En los ltimos temas de esta asignatura, se estudiarn los procesos de degradacin
qumica de los materiales no metlicos, centrndonos por tanto en primer lugar en los
procesos de corrosin aplicados a los metales.
En este mbito metlico, la corrosin puede definirse como la reaccin qumica o
electroqumica de un metal o aleacin con su medio circundante con el consiguiente
deterioro de sus propiedades.
La Federacin Europea de Corrosin establece una precisin adicional y distingue entre
corrosin con oxidacin del metal y formacin de cationes metlicos y la disolucin de
un metal en otros metales o sales fundidas. De acuerdo con esta definicin bsica
problemas mecnicos como ruptura por sobrecarga de una pieza metlica, desgaste,
erosin, cavitacin o la hinchazn de un plstico por transformaciones internas del
polmero que lo constituye no caen dentro de la corrosin propiamente dicha. Cambios
de fase como por ejemplo la transformacin de estao blanco en su variedad alotrpica
gris (peste del estao) tampoco pueden clasificarse como corrosin porque no interviene
un medio agresivo circundante.
Sin embargo, s se dan formas de corrosin en las cuales se sobreponen dos efectos, uno
qumico o electroqumico que constituye el de corrosin propiamente dicho y otro
mecnico, por ejemplo, en el proceso de corrosin-erosin, o de corrosin bajo tensin.
Respecto a los materiales no metlicos como polmeros o cermicos los mecanismos de
deterioro difieren del de los metales; y en estos casos se habla en general de
degradacin.
QUMICA DE SUPERFICIES - TEMA 1.- INTRODUCCIN.
2 de 9
La reaccin bsica de corrosin es por tanto:
De acuerdo con ello tambin es posible definir la corrosin desde un punto de vista ms
qumico como el trnsito de un metal de su forma elemental a su forma inica o
combinada con cesin de electrones a un no metal como el oxgeno o el azufre, por
ejemplo. Es decir, el metal, a travs de la corrosin, retorna a la forma combinada
formando xidos, sulfuros, hidrxidos, etc., que es como los metales se encuentran
habitualmente en la naturaleza por tratarse de formas termodinmicamente ms estables.
Desde el primer momento de su extraccin, para lo cual es necesario cambiar las
condiciones termodinmicas utilizando reductores, altas temperaturas, etc., el metal
muestra una tendencia inherente a reaccionar con el medio ambiente (atmsfera, agua,
suelo, etc.) retornando a la forma combinada. El proceso de corrosin es natural y
espontneo, y cuanto mayor es la energa gastada en la obtencin del metal a partir del
mineral, tanto ms fcilmente el metal revierte al estado combinado, es decir, tanto ms
favorecida termodinmicamente est la reaccin de corrosin.
Metalurgia extractiva y corrosin son, por tanto, procesos de accin opuesta. Se ha
dicho que el beneficio de los minerales y produccin de los metales constituye media
batalla: la otra mitad es mantener estos metales en buen estado durante su vida en
servicio. La corrosin ha sido descrita como una enorme industria al revs: todo son
prdidas sin jams un beneficio.
2. Importancia de la corrosin. Prdidas econmicas originadas por la corrosin
Las prdidas econmicas derivadas de la corrosin pueden clasificarse en directas e
indirectas.
Las prdidas directas se relacionan con los costes necesarios para la reposicin de
estructuras equipo, maquinaria o componentes que pueden quedar inservibles por efecto
de la corrosin, gastos de mantenimiento (pinturas, etc.) y utilizacin de aleaciones
resistentes a la corrosin en aplicaciones en las que mecnicamente sera suficiente un
material menos costoso.
Respecto a las prdidas indirectas, ms difciles de establecer, pero sin duda mucho
mayores que las directas, se pueden establecer a modo de ejemplo las siguientes:
a) Prdidas por interrupciones de la produccin: parada de una central trmica por
problemas de corrosin en la caldera o en un intercambiador de calor, por
ejemplo.
b) Prdidas de producto: prdidas de petrleo o gas con riesgo de accidente a travs
de oleoductos o tuberas corrodas.
c) Prdidas por contaminacin de productos: contaminacin de alimentos por
cationes metlicos procedentes de envases metlicos.
QUMICA DE SUPERFICIES - TEMA 1.- INTRODUCCIN.
3 de 9
d) Prdidas de rendimiento: formacin de productos de corrosin en el interior de
tuberas, lo que reduce los coeficientes de transmisin de calor cuando forman
parte de un intercambiador o producen obstrucciones parciales que obligan a
aumentar la capacidad de bombeo.
e) Prdidas por sobredimensionado: teniendo en cuenta el espesor de pared que se
prev se va a perder por corrosin a lo largo de la vida de un equipo es habitual
sobredimensionar reactores qumicos, calderas, tubos de condensadores, tuberas
enterradas, estructuras en contacto con el agua de mar, etc.
f) Prdidas por accidentes derivados de la corrosin: las lesiones o la muerte de
personas por la explosin de una tubera de gas como consecuencia de
problemas de corrosin.
Se estima que la relacin entre gastos directos e indirectos se sita entre 1:6 y 1:10.
En marzo de 1969 se constituy en Inglaterra una comisin a peticin del entonces
Ministro de Tecnologa, cuya tarea deba ser elaborar un estudio sobre la importancia
econmica del problema de la corrosin y de las posibilidades de su prevencin.
La comisin fue presidida por el Dr. T. P. Hoar de la Universidad de Cambridge y, en
total, participaron 21 especialistas de distintas ramas de la ciencia, la tecnologa y la
economa. Al iniciarse el ao 1971 se public el informe que se refiere slo a metales
(prescinde de los daos en los sectores de hormign armado o plsticos, por ejemplo).
El informe HOAR se ha convertido en un clsico a la hora de evaluar las prdidas por
corrosin por ser el primero elaborado con rigor. Los resultados aportados por este
informe son muy llamativos; as, por ejemplo, se estima que: a) Los costes directos
generados al ao por la corrosin alcanzan alrededor de un 3,5% del producto interior
bruto (PIB) de un pas.
b) Si se sacara mayor provecho de la tecnologa ya existente para el control de la
corrosin se podra ahorrar entre el 20 y el 25% de estos costos.
La distribucin de costes por sectores y de ahorro potencial sugerido por el informe se
describe en la Tabla 1.
Es preciso destacar que se trata de una estimacin sobre costes directos, de manera que
la inclusin de los indirectos, difciles de evaluar como ya se ha comentado, elevara
considerablemente la cifra. Por otra parte, no se incluyen prdidas relativas a la
degradacin de materiales no metlicos, de los cuales no existen actualmente datos
precisos y fiables.
Se estima que entre el 10 y el 12% de la produccin mundial de acero se pierde
completamente cada ao a causa de la corrosin.
Por otra parte, cuanto mayor es el nivel de desarrollo de un pas, y, por tanto, mayor es
el nmero y ms sofisticadas son sus instalaciones y procesos tecnolgicos, mayores
son las prdidas previstas. Aunque mejoren con el tiempo los medios y tcnicas de
QUMICA DE SUPERFICIES - TEMA 1.- INTRODUCCIN.
4 de 9
proteccin, las prdidas no disminuyen, porque, simultneamente, aumenta la
agresividad de las atmsferas y los progresos tecnolgicos imponen condiciones cada
vez ms severas.
Tabla 1. Distribucin de costes de la corrosin por industrias o sectores y estimacin de
ahorros potenciales si se aplicaran adecuadamente los conocimientos y tecnologas
conocidas para la proteccin contra la corrosin.
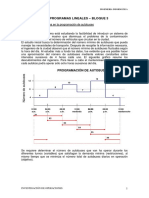
La tendencia en el desarrollo de la ingeniera es
hacia el desarrollo de procesos en condiciones
ms crticas, con la aplicacin de cargas
mecnicas, presiones y temperaturas cada vez
ms elevadas, y la utilizacin de medios
progresivamente ms agresivos, fluyendo a
mayor velocidad. La introduccin de materiales
de alta resistencia mecnica permite al
ingeniero reducir el peso, empleando secciones
transversales ms delgadas; pero, a menos que
la resistencia qumica de los nuevos materiales
sea superior a la de los materiales que
reemplazan, los riesgos de fallo por corrosin
aumentan. La Figura 1 muestra una de las
tendencias generales de incremento de la
corrosin al aumentar la agresividad de las
condiciones de proceso, en este caso la
temperatura.
QUMICA DE SUPERFICIES - TEMA 1.- INTRODUCCIN.
5 de 9
3. Clasificacin de los procesos de corrosin.
Para facilitar su valoracin y estudio se pueden clasificar los procesos de corrosin
segn criterios muy variados: por el mecanismo de ataque, segn el medio corrosivo, en
funcin de la morfologa, de acuerdo con los factores mecnicos que inciden en el
proceso, etc. En la tabla 2 se intenta ofrecer un muestrario de clasificaciones, pero sin
pretensiones de agotar el tema.
Tabla 2. Clasificaciones de los procesos de corrosin, segn diferentes criterios.
4. Mecanismos de los procesos de corrosin.
La clasificacin segn el mecanismo es, sin duda, la ms importante desde el punto de
vista cientfico.
Cualquier proceso de corrosin transcurre a travs de uno u otro de los dos mecanismos
que se analizan a continuacin: Corrosin directa y corrosin electroqumica.
4.1. Corrosin directa Se da fundamentalmente cuando el material metlico opera a
alta temperatura y por tanto no existe la posibilidad de que aparezca una pelcula de
humedad sobre la superficie metlica. Este mecanismo es caracterstico de materiales
metlicos expuestos a gases y vapores calientes.
El mecanismo consiste en la reaccin qumica heterognea directa entre la superficie
metlica y un gas agresivo que generalmente es el O2 con formacin de pelculas de
xido, a travs de reacciones del tipo:
2M + O2 <=> 2MO (para un metal divalente)
QUMICA DE SUPERFICIES - TEMA 1.- INTRODUCCIN.
6 de 9
La reaccin tiene las mismas posibilidades de producirse sobre cualquier punto de la
superficie, por lo que el fenmeno, desde el punto de vista morfolgico, suele ser
homogneo o generalizado.
Los productos de corrosin estn formados generalmente por xidos que se originan "in
situ" sobre la superficie metlica, de manera que si stos no funden o volatilizan a la
temperatura de operacin del material, introducen un efecto barrera entre el metal y el
gas agresivo dificultando en mayor o menor medida, pero siempre ms que un
mecanismo electroqumico, el contacto entre ambos y la correspondiente reaccin de
corrosin.
Esto es as hasta el punto de que la seleccin de materiales metlicos resistentes a la
corrosin a alta temperatura se basa fundamentalmente en la eleccin de la aleacin
capaz de generar, en el medio y a la temperatura a los que va a operar, capas de
productos de corrosin que impidan lo ms posible el contacto entre el metal y el medio
de ataque (capas de productos oxidados protectoras).
El mecanismo de la corrosin directa se ajusta al esquema de la Figura 2, de manera que
una vez formada la primera capa de xido, el proceso consta de varias etapas, que se
estudiarn en el tema 2.
Figura 2. Esquema mostrando el mecanismo de corrosin seca, para el caso del hierro.
En la oxidacin directa o corrosin seca, que sucede a temperaturas elevadas, la
formacin de iones metlicos tiene lugar en toda la superficie, en la intercara
metal/productos de corrosin y difunden, al igual que los electrones liberados, en
direccin a la intercara externa productos de corrosin/atmsfera, donde se generan los
aniones agresivos, O= en unos casos, S= o Cl- en otros, etc., que difunden en sentido
contrario. La reaccin se produce en el lugar de encuentro, normalmente en la intercara
externa, pues, debido al volumen relativamente menor de los cationes, stos difunden a
mayor velocidad que los aniones.
QUMICA DE SUPERFICIES - TEMA 1.- INTRODUCCIN.
7 de 9
Analizando someramente el mecanismo descrito se pueden establecer las caractersticas
bsicas de un proceso de corrosin seca o directa de forma diferencial con las
correspondientes a un fenmeno de corrosin electroqumica:
Se da en ausencia de electrolito.
Se trata de procesos de corrosin generalizados
Se da fundamentalmente a temperaturas altas.
La circulacin de electrones tiene lugar a travs de la pelcula de xido.
La circulacin de iones se produce tambin a travs de la pelcula de xido.
Los productos de corrosin ms habituales son xidos que se forman "in situ" sobre
la superficie metlica dificultando, generalmente de forma importante, la posterior
reaccin de corrosin.
4.2. Corrosin electroqumica. La corrosin se debe a la actuacin de pilas
electroqumicas, en las que el metal sufre disolucin en las regiones andicas. El
proceso por tanto no afecta por igual a toda la superficie metlica, pues en las regiones
catdicas no hay ataque.
Est plenamente demostrado que los fenmenos electroqumicos contribuyen, en
conjunto, en mucho mayor grado al fallo de los metales que la corrosin directa (el otro
mecanismo que se describir a continuacin). Pero no debe interpretarse este hecho en
el sentido de que en determinados casos la corrosin directa no pueda alcanzar una
importancia decisiva y llegue a ser la verdadera responsable del deterioro del metal.
La corrosin electroqumica se da cuando los materiales metlicos se hallan en contacto
con medios de conductividad electroltica, en particular con el agua, soluciones salinas,
o la simple humedad de la atmsfera y de los suelos. De acuerdo con esto, la presencia
de molculas de agua sobre la superficie es la condicin necesaria para que ocurra
corrosin electroqumica.
La unin elctrica entre dos metales distintos, por ejemplo el cinc y el cobre sumergidos
en una solucin conductora, genera una corriente elctrica debido a la diferencia entre
los potenciales electroqumicos de ambos metales. El paso de carga a travs del lquido
(electrolito) consiste en el movimiento de aniones y cationes que la transportan hacia el
nodo y el ctodo, respectivamente.
La superficie del metal con mayor tendencia a la disolucin (zona andica) es corroda
en un proceso en que los tomos metlicos dejan sus electrones en el seno del metal
pasando a la solucin como ion positivo. Por otro lado, la superficie del metal con
menor tendencia termodinmica a la disolucin (catdica) permanece inmune al ataque.
Ella recibe, a travs de la masa metlica, los electrones liberados en el nodo, que son
suministrados a un captador (oxidante) presente en el electrolito en los procesos de
reduccin catdica.
QUMICA DE SUPERFICIES - TEMA 1.- INTRODUCCIN.
8 de 9
Puede actuar como captador de electrones cualquier oxidante, pero en la mayora de los
casos acta como tal el O2 disuelto, en el electrolito en medios neutros y alcalinos, o el
H+ en medio cido.
En estos casos, las reacciones en el ctodo son:
o bien
Aunque tambin podra darse la reaccin inversa de la andica, pudiendo establecerse
en algn caso condiciones de equilibrio, sin balance efectivo de corrosin.
El conjunto del proceso queda representado en la Figura 3.
Figura 3. Representacin esquemtica del proceso de corrosin electroqumica para un
metal divalente.
En realidad, la circulacin de la corriente tiene lugar porque los metales estn dotados
de electrones de valencia movibles y con un relativamente elevado grado de libertad, lo
que favorece su transferencia a otras sustancias que llegan a la superficie metlica con
capacidad para fijarlos. El gradiente de energa necesario para separar un electrn, en la
ionizacin de un tomo metlico, determina la mayor o menor afinidad del metal por el
electrn y cambia de un metal a otro. Sern activos los metales de baja energa de
ionizacin y nobles los que la posean alta. Cambia tambin esta energa al pasar de una
a otra de las regiones, macro o microscpicamente diferenciadas, que integran cualquier
superficie metlica, por lo que no es necesaria la presencia de dos metales distintos para
que funcionen las pilas de corrosin.
QUMICA DE SUPERFICIES - TEMA 1.- INTRODUCCIN.
9 de 9
En el contacto entre metales o regiones metlicas de actividad diversa, las reas ms
activas tienden a ser los nodos de las pilas de corrosin. Sobre ellas se localiza, por
tanto, el ataque electroqumico, que necesariamente ha de estar acompaado por un
proceso de reduccin en el ctodo. As, las reacciones electroqumicas bsicas son:
La Figura 4 muestra esquemticamente la superficie de un material metlico indicando
zonas con diferente potencial electroqumico. Las que presenten potencial de reduccin
mayor (ms nobles) tendrn comportamiento catdico. Las de potencial de reduccin
menor (activas) sern nodos y sobre ellas se localizar la corrosin.
Figura 4. Representacin esquemtica de la superficie de un material metlico mostrando
zonas con distinto potencial electroqumico (pilas de corrosin).
A la vista de lo anterior se pueden establecer las caractersticas bsicas de un proceso de
corrosin electroqumica:
Se da en presencia de electrolito.
Se suele dar a temperaturas moderadas (inferiores a 100-150 C aproximadamente).
Se localiza sobre las regiones de comportamiento andico.
La circulacin de electrones tiene lugar desde el nodo hasta el ctodo a travs del
propio metal.
El circuito se cierra a travs del electrolito mediante el transporte de carga por parte
de los iones.
Los productos primarios de corrosin ms habituales (cuando la reaccin catdica es
la aceptacin de electrones por el O2) son hidrxidos que se forman en el seno del
electrolito aunque pueden, posteriormente, fijarse sobre la superficie metlica
introduciendo un cierto efecto de barrera slida entre el metal y el medio agresivo
dificultando ligeramente la posterior reaccin heterognea metal-lquido (corrosin)
en la interfase. Estos hidrxidos suelen posteriormente pasar a xidos en presencia
de ms oxgeno.
Das könnte Ihnen auch gefallen
- Química: BQ. Mauricio Galaz MDokument25 SeitenQuímica: BQ. Mauricio Galaz MMauricio GalazNoch keine Bewertungen
- Aral Actividad2y3Dokument2 SeitenAral Actividad2y3Iolanda Na ArañeiraNoch keine Bewertungen
- Informe Trabajo Final Cristalografia. Grupo de La Domeykita.Dokument22 SeitenInforme Trabajo Final Cristalografia. Grupo de La Domeykita.Francisco FigueroaNoch keine Bewertungen
- Elementos de Proteccion Personal-JcDokument37 SeitenElementos de Proteccion Personal-JcAna Milena RojasNoch keine Bewertungen
- Estimación de Precios de Cuenta para ColombiaDokument15 SeitenEstimación de Precios de Cuenta para ColombialeocabezasNoch keine Bewertungen
- Objetivos Fundamentales de TostaciónDokument12 SeitenObjetivos Fundamentales de TostaciónLucia Melania Yañez Rivas100% (1)
- Guia # 8 Grado SeptimoDokument10 SeitenGuia # 8 Grado SeptimoAngie Joel Cortes Bermudez CortesNoch keine Bewertungen
- Drude PDFDokument11 SeitenDrude PDFluchatosNoch keine Bewertungen
- Todas Las PreguntasDokument2 SeitenTodas Las PreguntasHomero JuaresNoch keine Bewertungen
- Problemas de PL - Bloque 3Dokument10 SeitenProblemas de PL - Bloque 3Ana PerezNoch keine Bewertungen
- Polarización Inducida BDokument55 SeitenPolarización Inducida BLuis Fernando Flores AristaNoch keine Bewertungen
- Modelos y NucleosDokument2 SeitenModelos y NucleosSusana BorbonNoch keine Bewertungen
- Capitulo VI - Metalurgia Extractiva Del AluminioDokument20 SeitenCapitulo VI - Metalurgia Extractiva Del AluminioFrancisco Javier Alarcón GarridoNoch keine Bewertungen
- Orfebreria Momposina PDFDokument6 SeitenOrfebreria Momposina PDFGanesha DE DiosNoch keine Bewertungen
- Tarea 2 Procesos de Manufactura Kevin RugamaDokument7 SeitenTarea 2 Procesos de Manufactura Kevin RugamaKEVIN JOSE RUGAMA DAVILA100% (1)
- 17 EpitermalesDokument47 Seiten17 EpitermalesValentinaNoch keine Bewertungen
- Soldadura - Oxiacetilenico (Oaw) PDFDokument19 SeitenSoldadura - Oxiacetilenico (Oaw) PDFsaulNoch keine Bewertungen
- Trabajo en CalienteDokument10 SeitenTrabajo en CalienteEmmanuel HernandezNoch keine Bewertungen
- Tratamiento de Aguas Residuales Mediante Tecnologia ElectroquimicaDokument6 SeitenTratamiento de Aguas Residuales Mediante Tecnologia ElectroquimicaivonlunitaNoch keine Bewertungen
- Porcelana DentalDokument5 SeitenPorcelana DentalbeluNoch keine Bewertungen
- Practica 2 Liquidos PenetrantesDokument5 SeitenPractica 2 Liquidos PenetrantesMarlen AlbertoNoch keine Bewertungen
- Minerales 1ESODokument29 SeitenMinerales 1ESOAlfredo Varela SuárezNoch keine Bewertungen
- Trabajo Final Enseñanza de Las Cs. Naturales Jablonski, RodriguezDokument10 SeitenTrabajo Final Enseñanza de Las Cs. Naturales Jablonski, RodriguezAgustina RodriguezNoch keine Bewertungen
- Laboratorio SoldaduraDokument19 SeitenLaboratorio SoldaduraValentinaNoch keine Bewertungen
- Teorias Relativas A La Estabilidad de Coloides LiofobicosDokument18 SeitenTeorias Relativas A La Estabilidad de Coloides LiofobicosjhonathanNoch keine Bewertungen
- Stihl FS 400 - 450Dokument92 SeitenStihl FS 400 - 450Andres Libardo Botero BoteroNoch keine Bewertungen
- Autoevaluación N°1 - Revisión de IntentosDokument3 SeitenAutoevaluación N°1 - Revisión de IntentosOctavio Fernando Picon MedinaNoch keine Bewertungen
- Consideraciones para La Interpretación de Los Análisis de Aceite Publicado Por Cepsa Lubricantes SDokument5 SeitenConsideraciones para La Interpretación de Los Análisis de Aceite Publicado Por Cepsa Lubricantes Snestor mospanNoch keine Bewertungen
- I NFORMEDokument7 SeitenI NFORMEIsaías Avemañay100% (1)
- FDS Hidróxido de Sodio Anhidro REV06Dokument42 SeitenFDS Hidróxido de Sodio Anhidro REV06DaríoNoch keine Bewertungen