Beruflich Dokumente
Kultur Dokumente
Teorías Atómicas
Hochgeladen von
liyumonvi0 Bewertungen0% fanden dieses Dokument nützlich (0 Abstimmungen)
44 Ansichten3 SeitenEl documento describe las teorías atómicas de Dalton, Thomson, Rutherford y Bohr. La teoría de Dalton estableció que la materia está compuesta de átomos indivisibles de diferentes elementos. El modelo de Thomson propuso que el átomo consiste en una esfera positiva con electrones incrustados. Rutherford sugirió que el átomo tiene un núcleo central con electrones que orbitan alrededor. Finalmente, Bohr describió el átomo como un núcleo central con electrones que giran en órbitas definidas alrededor del núcle
Originalbeschreibung:
quimica
Originaltitel
TEORÍAS ATÓMICAS
Copyright
© © All Rights Reserved
Verfügbare Formate
DOCX, PDF, TXT oder online auf Scribd lesen
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenEl documento describe las teorías atómicas de Dalton, Thomson, Rutherford y Bohr. La teoría de Dalton estableció que la materia está compuesta de átomos indivisibles de diferentes elementos. El modelo de Thomson propuso que el átomo consiste en una esfera positiva con electrones incrustados. Rutherford sugirió que el átomo tiene un núcleo central con electrones que orbitan alrededor. Finalmente, Bohr describió el átomo como un núcleo central con electrones que giran en órbitas definidas alrededor del núcle
Copyright:
© All Rights Reserved
Verfügbare Formate
Als DOCX, PDF, TXT herunterladen oder online auf Scribd lesen
0 Bewertungen0% fanden dieses Dokument nützlich (0 Abstimmungen)
44 Ansichten3 SeitenTeorías Atómicas
Hochgeladen von
liyumonviEl documento describe las teorías atómicas de Dalton, Thomson, Rutherford y Bohr. La teoría de Dalton estableció que la materia está compuesta de átomos indivisibles de diferentes elementos. El modelo de Thomson propuso que el átomo consiste en una esfera positiva con electrones incrustados. Rutherford sugirió que el átomo tiene un núcleo central con electrones que orbitan alrededor. Finalmente, Bohr describió el átomo como un núcleo central con electrones que giran en órbitas definidas alrededor del núcle
Copyright:
© All Rights Reserved
Verfügbare Formate
Als DOCX, PDF, TXT herunterladen oder online auf Scribd lesen
Sie sind auf Seite 1von 3
TEORAS ATMICAS
En 1803, Dalton (1766-1844) formula su teora atmica, con la que trataba
de explicar las leyes qumicas conocidas hasta esta fecha. Dicha teora fue
admitida por los hombres de ciencia hasta principios del siglo XX, en que,
como consecuencia de nuevos descubrimientos, surgi la necesidad de
desarrollar nuevas teoras.
Teora atmica de Dalton
La teora atmica de Dalton se resume en los siguientes puntos:
La materia es discontinua. Est formada por
partculas materiales independientes
llamadas tomos, los cuales son
indivisibles.
Los tomos de un mismo elemento son
iguales entre s tanto en masa como en
propiedades fsicas y qumicas.
Los tomos de elementos diferentes son distintos en cuanto a masa y
dems propiedades.
Los compuestos se forman por la unin de tomos de los
elementos correspondientes, en una relacin numrica sencilla.
Modelo atmico de Thomson
El modelo atmico de Thomson (1856-1940) postula que
el tomo se compone de una esfera cargada
positivamente en la que reside la mayor parte de la
masa del tomo y sobre la cual se incrustan los
electrones.
Modelo atmico de Rutherford
Segn el modelo atmico de Rutherford (1831-1937), el
tomo est formado por una esfera en la que se
concentra casi toda la masa del sistema (protones y
neutrones) y en torno a la cual giran unas partculas
(electrones) de la misma manera que lo hacen los
planetas en torno al Sol.
Los protones del ncleo se encuentran cargados
positivamente y los electrones negativamente.
Modelo atmico de Bohr
Para Bohr (1885-1962), el tomo est constituido de la siguiente forma:
En el centro del mismo se ubica el
ncleo, pequea regin del tomo
donde residen la casi totalidad de su
masa y la carga positiva. El nmero de
cargas positivas del ncleo (protones)
coincide con el nmero atmico del
elemento.
En torno al ncleo giran los electrones
(en nmero igual al de protones y al
nmero atmico), portadores de la carga negativa, describiendo
rbitas circulares.
Los electrones mientras giran en su rbita no emiten radiaciones.
Cuando saltan a una rbita ms cercana al ncleo emiten radiacin
energtica, y cuando pasan a una rbita superior la absorben.
LAS MODERNAS TEORAS ATMICAS
Hacia 1920, como consecuencia del estudio de los espectros de elementos
con gran nmero de electrones, se dud de la bondad de la teora de Bohr.
Sommerfeld (1868-1951) descubri que la teora de Bohr era incompleta,
pues las rbitas electrnicas tambin podan ser elpticas. Modific los
postulados de ste, afirmando que las rbitas descritas por los electrones
dentro de un nivel energtico definido podan ser circulares o elpticas, lo
que supone diferencias en los estados energticos de los electrones
(subniveles energticos).
Posteriormente se dedujo que el movimiento de los electrones no se
desarrolla en rbitas bien definidas, sino que describe un movimiento
complejo.
El movimiento del electrn describe rbitas complejas, con lo cual existe la
probabilidad de encontrarlo en una posicin determinada. Las zonas donde
probablemente se encuentra el electrn reciben el nombre de orbitales.
Das könnte Ihnen auch gefallen
- Teorías AtómicasDokument4 SeitenTeorías AtómicasJohanna MuñozNoch keine Bewertungen
- Teorias AtomicasDokument2 SeitenTeorias AtomicasJC ArlosNoch keine Bewertungen
- Informe de LaboratorioDokument3 SeitenInforme de Laboratorioandrea caitaNoch keine Bewertungen
- Ficha de Resumen ÁtomoDokument2 SeitenFicha de Resumen ÁtomoHerlis Esmith Mija TacureNoch keine Bewertungen
- Teorias AtomicasDokument1 SeiteTeorias AtomicascyberNoch keine Bewertungen
- Teorías AtómicasDokument7 SeitenTeorías AtómicasMariano BiondiNoch keine Bewertungen
- Hoja de EstudioDokument4 SeitenHoja de EstudioAzucena TriviñoNoch keine Bewertungen
- Teorias AtomicasDokument2 SeitenTeorias AtomicasEl RISASNoch keine Bewertungen
- Hoja de EstudioDokument4 SeitenHoja de EstudioAzucena TriviñoNoch keine Bewertungen
- Modelos AtomicosDokument6 SeitenModelos AtomicosDanielNoch keine Bewertungen
- ATOMOSDokument10 SeitenATOMOSPamela PalominoNoch keine Bewertungen
- QG1 - C5 - Teoría AtómicaDokument39 SeitenQG1 - C5 - Teoría AtómicaJULIÁN HERNÁNDEZ COLORADONoch keine Bewertungen
- Modelos AtomicosDokument10 SeitenModelos AtomicosJuan martin CastroNoch keine Bewertungen
- Teorias Del AtomoDokument5 SeitenTeorias Del AtomoArturo CuevaNoch keine Bewertungen
- Estructura Atómica 2Dokument29 SeitenEstructura Atómica 2u20231212683Noch keine Bewertungen
- Evolucion Del AtomoDokument8 SeitenEvolucion Del AtomoAlex BolañoNoch keine Bewertungen
- Los AtomosDokument4 SeitenLos AtomosEmmanuel Benitez RiosNoch keine Bewertungen
- El ÁtomoDokument3 SeitenEl ÁtomoYetzabeth LandaetaNoch keine Bewertungen
- El Átomo A Través Del TiempoDokument2 SeitenEl Átomo A Través Del TiempoCristian Javier Herazo BertelNoch keine Bewertungen
- El Átomo A Través Del TiempoDokument4 SeitenEl Átomo A Través Del TiempoDaniela Acevedo Castro100% (1)
- Teria AtomicaDokument4 SeitenTeria AtomicaLuis BororNoch keine Bewertungen
- El Modelo Atómico de SchrödingerDokument9 SeitenEl Modelo Atómico de SchrödingerAlex Villacis HidalgoNoch keine Bewertungen
- Mapa de Las Teorias AtomicasDokument1 SeiteMapa de Las Teorias AtomicasLuis Enrique Galicia MarquezNoch keine Bewertungen
- Historia de La Teoria AtomicaDokument6 SeitenHistoria de La Teoria AtomicaFreddy ManalNoch keine Bewertungen
- La Materia y Los ÁtomosDokument3 SeitenLa Materia y Los ÁtomosAMBAR SUÁREZNoch keine Bewertungen
- Teorías de La MateriaDokument4 SeitenTeorías de La Materiaビラロエル ケルビンNoch keine Bewertungen
- RazonesDokument2 SeitenRazonesCecil MorenoNoch keine Bewertungen
- Modelos Atómicos (Dalton, Thomson, Rutherford y Bohr)Dokument3 SeitenModelos Atómicos (Dalton, Thomson, Rutherford y Bohr)Angello GAMERNoch keine Bewertungen
- 2 AtomosDokument69 Seiten2 AtomosErick MegoNoch keine Bewertungen
- Modelos Atómicos y Las Partículas Subatómicas, 5to B LuisaDokument18 SeitenModelos Atómicos y Las Partículas Subatómicas, 5to B LuisaLuisa GarciaNoch keine Bewertungen
- Teorias Atomicas QuimicaDokument4 SeitenTeorias Atomicas QuimicaJORDI CHICAIZANoch keine Bewertungen
- Historia Del ÁtomoDokument10 SeitenHistoria Del ÁtomoCRISTHIAN FRANCISCO YOSA PEREZNoch keine Bewertungen
- Comparacion de Modelos AtomicosDokument5 SeitenComparacion de Modelos AtomicosJulian CuadradoNoch keine Bewertungen
- Que Es Un Átomo y Sus PartesDokument4 SeitenQue Es Un Átomo y Sus PartesAlejandra VargasNoch keine Bewertungen
- Teoría AtómicaDokument4 SeitenTeoría AtómicaJhonfer MedinaNoch keine Bewertungen
- Block Modelo AtomicoDokument8 SeitenBlock Modelo AtomicoLuis Felipe Menor RojasNoch keine Bewertungen
- La Teoria Del Thomson y Los Otros ManesDokument2 SeitenLa Teoria Del Thomson y Los Otros ManesDANIEL ALEJANDRO SANTACRUZ GUERRERONoch keine Bewertungen
- Vega Ramirez Brayan Giovanni-InvestigacionDokument8 SeitenVega Ramirez Brayan Giovanni-InvestigacionBrayan VegaNoch keine Bewertungen
- Teoria AtomicaDokument4 SeitenTeoria AtomicaWendy Johana Tellez OrtizNoch keine Bewertungen
- Modelos AtomicosDokument2 SeitenModelos Atomicosgaming zoneNoch keine Bewertungen
- Teoría AtómicaDokument28 SeitenTeoría AtómicaJhan Carlos Garcia Rendon (Jhanca)Noch keine Bewertungen
- Modelo AtómicoDokument12 SeitenModelo AtómicoGarcía López Raúl GeovaniNoch keine Bewertungen
- AtomoDokument22 SeitenAtomoAdelis MarquezNoch keine Bewertungen
- IntroduccionDokument2 SeitenIntroduccionEduardo Jmm O̲̲̅̅f̲̲̅̅ı̲̲̅̅c̲̲̅̅ı̲̲̅̅a̲̲̅̅l̲̲̅̅'̲̲̅̅F̲̲̅̅bNoch keine Bewertungen
- Eiao La Materia y Sus TransformacionesDokument5 SeitenEiao La Materia y Sus TransformacionesElizabeth VerneNoch keine Bewertungen
- El ÁtomoDokument6 SeitenEl ÁtomoKary HdezNoch keine Bewertungen
- El Átomo EsDokument3 SeitenEl Átomo EsJose PinedaNoch keine Bewertungen
- Modelo Atómico de DaltonDokument6 SeitenModelo Atómico de DaltonYahaira Discua RamirezNoch keine Bewertungen
- Clase ESTRUCTURA DE LA MATERIA Y SUS PROPIEDADESDokument24 SeitenClase ESTRUCTURA DE LA MATERIA Y SUS PROPIEDADESBerny DiazNoch keine Bewertungen
- Modelos AtomicosDokument10 SeitenModelos AtomicosAyelen Domínguez GómezNoch keine Bewertungen
- Terias AtomicasDokument6 SeitenTerias AtomicasKatrina GraterolNoch keine Bewertungen
- El Átomo y Los EnlacesDokument24 SeitenEl Átomo y Los EnlacesDdaniialejanddrooNoch keine Bewertungen
- Método Atómico de DaltonDokument2 SeitenMétodo Atómico de DaltongdefreitesNoch keine Bewertungen
- Consultar Los Postulados de Las Teorías AtómicasDokument16 SeitenConsultar Los Postulados de Las Teorías AtómicasLuis HernandezNoch keine Bewertungen
- Que Es El Modelo AtómicoDokument3 SeitenQue Es El Modelo AtómicoVictoria Conejo LucioNoch keine Bewertungen
- Modelos AtómicosssDokument6 SeitenModelos Atómicosssedhit82coriaNoch keine Bewertungen
- MateriaDokument5 SeitenMateriaRichard Alexander ABNoch keine Bewertungen
- Teoria Atomica ModernaDokument4 SeitenTeoria Atomica ModernaCristian OviedoNoch keine Bewertungen
- De la estructura atómica a la quiralidad.: Algunos conceptos de la químicaVon EverandDe la estructura atómica a la quiralidad.: Algunos conceptos de la químicaBewertung: 5 von 5 Sternen5/5 (1)
- El Ministerio Público y La Policía NacionalDokument25 SeitenEl Ministerio Público y La Policía NacionalliyumonviNoch keine Bewertungen
- Preguntas ReformismoDokument2 SeitenPreguntas ReformismoliyumonviNoch keine Bewertungen
- Fechas Civicas de MayoDokument4 SeitenFechas Civicas de MayoliyumonviNoch keine Bewertungen
- Los Rios Profundos ... AnalisisDokument6 SeitenLos Rios Profundos ... AnalisisliyumonviNoch keine Bewertungen
- Los PLANETAS ENANOSDokument3 SeitenLos PLANETAS ENANOSliyumonviNoch keine Bewertungen
- Alan WalkerDokument3 SeitenAlan WalkerliyumonviNoch keine Bewertungen
- DiabetesDokument1 SeiteDiabetesliyumonviNoch keine Bewertungen
- HOMINIZACIÓNDokument4 SeitenHOMINIZACIÓNliyumonviNoch keine Bewertungen
- Normas de Convivencia EscolarDokument1 SeiteNormas de Convivencia EscolarliyumonviNoch keine Bewertungen
- Congreso de Tacna 1837Dokument2 SeitenCongreso de Tacna 1837liyumonvi100% (3)
- Etapas EmbrionariasDokument6 SeitenEtapas EmbrionariasliyumonviNoch keine Bewertungen
- Hepatitis BDokument3 SeitenHepatitis BliyumonviNoch keine Bewertungen
- Partes de La Celul1Dokument3 SeitenPartes de La Celul1liyumonviNoch keine Bewertungen
- Visión y Misión Del Área de Formación Ciudadana y CívicaDokument1 SeiteVisión y Misión Del Área de Formación Ciudadana y Cívicaliyumonvi100% (1)
- PreguntasDokument2 SeitenPreguntasliyumonviNoch keine Bewertungen
- Sustantivos ContablesDokument2 SeitenSustantivos ContablesliyumonviNoch keine Bewertungen
- La ZamacuecaDokument11 SeitenLa ZamacuecaliyumonviNoch keine Bewertungen
- Historia de La QuímicaDokument1 SeiteHistoria de La QuímicaliyumonviNoch keine Bewertungen
- Cuento Los Niños en La FincaDokument1 SeiteCuento Los Niños en La Fincaliyumonvi67% (3)
- Informe 1Dokument6 SeitenInforme 1fabriziod16Noch keine Bewertungen
- Fisica de ParticulasDokument2 SeitenFisica de Particulasjalexito1Noch keine Bewertungen
- Laboratorio 2Dokument7 SeitenLaboratorio 2Luis Fernando ZG0% (1)
- Estadística de Bose-Einstein - Wikipedia, La Enciclopedia LibreDokument3 SeitenEstadística de Bose-Einstein - Wikipedia, La Enciclopedia LibreMiguel AngelNoch keine Bewertungen
- Depósito de Capa Atómica (Hailin)Dokument28 SeitenDepósito de Capa Atómica (Hailin)Brnardo RanNoch keine Bewertungen
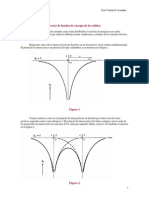
- Teoria de Bandas PDFDokument12 SeitenTeoria de Bandas PDFFelipe AndresNoch keine Bewertungen
- Capitulo 7 Raymond ChangDokument19 SeitenCapitulo 7 Raymond ChangSantiagoAlcantaraNoch keine Bewertungen
- Comparacion de Los Modelos AtomicosDokument5 SeitenComparacion de Los Modelos AtomicosAna Maria Manzano GuetteNoch keine Bewertungen
- La Mecánica Cuántica - El Acoplamiento LSDokument31 SeitenLa Mecánica Cuántica - El Acoplamiento LSLarry Theran Suarez0% (1)
- La Regla de Hund para El Llenado de ElectronesDokument2 SeitenLa Regla de Hund para El Llenado de ElectronesCarrasco RicardoNoch keine Bewertungen
- Atomos y Sistema PeriodicoDokument30 SeitenAtomos y Sistema PeriodicoAnonymous pykOLRFNoch keine Bewertungen
- TERNIUM Fundamentos Diodos PDFDokument19 SeitenTERNIUM Fundamentos Diodos PDFmanuel bolivarNoch keine Bewertungen
- Cadete Tema 3Dokument5 SeitenCadete Tema 3GianmarcoSugarAventureroNoch keine Bewertungen
- Configuración Electrónica Recorte Del Diagrama de MoellerDokument3 SeitenConfiguración Electrónica Recorte Del Diagrama de MoellerKelian Mauro González ColmanNoch keine Bewertungen
- Regla Del OctetoDokument4 SeitenRegla Del OctetoAxel Mata ArellanoNoch keine Bewertungen
- Pozo de Potencial InfinitoDokument9 SeitenPozo de Potencial InfinitoDaniel Parra OspinaNoch keine Bewertungen
- DiodosDokument28 SeitenDiodosjoseNoch keine Bewertungen
- Ficha de Configuracion ElectronicaDokument3 SeitenFicha de Configuracion ElectronicaLUCIA MORAN CRUCES100% (1)
- Evaluación Configuración ElectrónicaDokument2 SeitenEvaluación Configuración Electrónicasiliana pallaresNoch keine Bewertungen
- Series Espectrales Del HidrógenoDokument3 SeitenSeries Espectrales Del Hidrógenocaceresccp100% (1)
- Teorema de Bloch. Masa Efectiva. Densidad de Estados. Método LCAO. Método K P.Dokument26 SeitenTeorema de Bloch. Masa Efectiva. Densidad de Estados. Método LCAO. Método K P.Isabel100% (3)
- Esqueleto de La Tabla PeriodicaDokument2 SeitenEsqueleto de La Tabla PeriodicaEduardo CamperoNoch keine Bewertungen
- Taller 2Dokument2 SeitenTaller 2Julia SabogalNoch keine Bewertungen
- Re Programacion FS 277 II 2019Dokument7 SeitenRe Programacion FS 277 II 2019Tesla NoralesNoch keine Bewertungen
- P1 Electrónica Analógica. R08-PC01Dokument22 SeitenP1 Electrónica Analógica. R08-PC01alejandro LópezNoch keine Bewertungen
- Repaso Prueba (Raynier Riffo) (Quimica)Dokument28 SeitenRepaso Prueba (Raynier Riffo) (Quimica)Sebastian SolisNoch keine Bewertungen
- Química Pre AvanzadoDokument45 SeitenQuímica Pre AvanzadoJenny Maria Caycho AvilaNoch keine Bewertungen
- Neutrino SSDokument7 SeitenNeutrino SSKaren VillaNoch keine Bewertungen
- Configuración ElectróDokument4 SeitenConfiguración ElectróErin Phillips100% (1)
- BohrDokument4 SeitenBohrAna Paula HernandezNoch keine Bewertungen