Beruflich Dokumente
Kultur Dokumente
Disoluciones Amortiguadoras de PH PDF
Hochgeladen von
Adrizz FrancoOriginaltitel
Copyright
Verfügbare Formate
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
Verfügbare Formate
Disoluciones Amortiguadoras de PH PDF
Hochgeladen von
Adrizz FrancoCopyright:
Verfügbare Formate
Laboratorio de qumica general II.
Departamento de qumica
inorgnica y nuclear. Clave 1211.
Profesor: M. en I. Fernando Morales Morales.
Grupo: 25.
Elaborado por: Adrian Ruz Martnez.
Clculos relacionados con las disoluciones amortiguadoras de pH.
Qu masa de cido benzoico y de benzoato de sodio se requieren pesar para preparar 500
mL de un buffer de benzoatosi con un pH de 3.5 y una concentracin 0.2M, el par acido base
acido benzoico/Benzoato tiene un pKa igual a 4.2?
- Iniciamos planteando la expresin que nos representa la concentracin total de la disolucin. Ya
que la disolucin debe tener una concentracin TOTAL de 0.2 M esto nos dice que la concentracin
de cido benzoico y la concentracin de benzoatos sumadas debe ser la concentracin total (el cido
benzoico se representar como HBenz y el ion benzoato se representar como Benz-):
|HBenz| + |Benz | = 0.2M (1)
- Ahora sabemos que para calcular el pH de una disolucin amortiguadora se usa la ecuacin de
Henderson-Hasselbach que para este equilibrio la expresin quedar como:
|Base| |Benz |
pH = pKa + log ( ) => pH = pKa + log ( ) (2)
|cido| |HBenz|
- Para obtener la masa del cido y de la base del par primero necesitamos conocer la concentracin
de estas especies para lo cual seguimos la siguiente metodologa:
o Despejando |Benz-| de (1) tenemos que:
|Benz | = 0.2M |HBenz| (3)
o Sustituyendo (3) en (2)
|Benz | 0.2M |HBenz|
pH = pKa + log ( ) = pKa + log ( )
|HBenz| |HBenz|
o Realizando simplificaciones tenemos que:
0.2M |HBenz| 0.2M |HBenz| 0.2M
pH = pKa + log ( ) = pKa + log ( ) = pKa + log ( 1)
|HBenz| |HBenz| |HBenz| |HBenz|
0.2M 0.2M
pH = pKa + log ( 1) => pH pKa = log ( 1)
|HBenz| |HBenz|
o Por propiedades de los logaritmos y sustituyendo los valores numricos que
conocemos, pH= 3.5 y pKa= 4.2, obtenemos:
Clculos asociados a disoluciones amortiguadoras de pH. Pgina 1
Laboratorio de qumica general II. Departamento de qumica
inorgnica y nuclear. Clave 1211.
0.2M 0.2M
10pHpKa = 1 => 103.54.2 = 100.7 = 1
|HBenz| |HBenz|
o De esta ltima expresin despejamos |HBenz| obteniendo:
0.2M 0.2M
100.7 = 1 => |HBenz| = 0.7 = 0.1667 M
|HBenz| 10 +1
o Ya que tenemos |HBenz| obtenemos |Benz-| con (3)
|Benz | = 0.2M |HBenz| = 0.2 M 0.1667 M = 0.0333 M
o Para comprobar que los datos obtenidos son los correctos los sustituimos en (2):
|Benz | 0.0333 M
pH = pKa + log ( ) = 4.2 + log ( ) = 3.50
|HBenz| 0.1667 M
o Y en efecto 3.50 es el pH que debemos tener la disolucin.
- Ya que hemos realizado la metodologa necesaria para encontrar las concentraciones de HBenz y
Benz- obtenemos los moles de cada especie teniendo en cuenta que se preparan 500 mL y con sus
respectivas masas moleculares, 122g/mol y 144 g/mol (el ion benzoato proviene del benzoato de
sodio):
o Masa de cido benzoico:
0.1667 mol HBenz 1L 122 g
( ) (500 mL) ( ) = 0.0834 mol HBenz ( ) = 10.1748 g HBenz
1L 1000 mL 1 mol
o Masa de benzoato de sodio:
0.0333 mol NaBenz 1L 144 g
( ) (500 mL) ( ) = 0.0167 mol NaBenz ( ) = 2.4048 g NaBenz
1L 1000 mL 1 mol
- As que para preparar 500 mL de una disolucin amortiguadora de pH, con un valor de este
igual a 3.5, y una molaridad 0.2M debemos pesar 10.1748 g cido benzoico y 2.4048 gramos
de benzoato de sodio.
Se requiere prepara un litro de una disolucin amortiguadora con una concentracin igual a
0.5 M y con un pH igual a 3.3.
o Cul par cido-base ser el apropiado para esta disolucin amortiguadora?
o Qu masa de la sal de sodio que libera la base conjugada se debe pesar?
o Qu volumen del cido que se encuentra al 48% m/m con una densidad de 1.16
g/mL se debe usar?
Clculos asociados a disoluciones amortiguadoras de pH. Pgina 2
Laboratorio de qumica general II. Departamento de qumica
inorgnica y nuclear. Clave 1211.
- Para responder al primer punto primero debemos hacernos la pregunta Cmo se elige un
par cido-base para preparar una disolucin Buffer? Para esto primero debemos ver el pH
el cual debe tener la disolucin siendo este 3.3. Sabiendo esto y como REGLA GENERAL
se debe escoger un par cido-base que tenga un pKa cercano al pH que se debe tener la
disolucin. Esto se debe a que el buffer mantiene una fuerza amortiguante o amortiguadora
cuando la relacin entre la concentracin entre la base y el cido (o viceversa) sea 1:10 lo
cual solo funciona si el pKa es cercano al pH buscado. (Existen otras propiedades para
considerar el uso de un par cido-base tales como que no existan reacciones colaterales de
coplejacin o redox entre algunos de las especies del par y el sustrato para el que se realiza
la disolucin buffer pero para el nivel de Qumica general II no las analizaremos).
- Teniendo en cuenta lo anterior escogemos un par que tenga un pKa cercano a 3.3 y este
puede ser el par cido fluorhdrico/ fluoruro (HF/F-) cuyo pKa es de 3.2.
- Ahora para obtener la masa de fluoruro de sodio (NaF) y volumen de cido fluorhdrico (HF)
a usar para preparar el buffer seguimos la metodologa del problema anterior.
o Planteamos la expresin que nos representa la concentracin total del buffer:
|HF| + |F | = 0.5 M
o Planteando la expresin de la ecuacin de Henderson-Hasselbach que para este
equilibrio tenemos que:
|Base| |F |
pH = pKa + log ( ) => pH = pKa + log ( )
|cido| |HF|
o Repetimos los pasos del problema anterior
|F | = 0.5 M |HF|
0.5 M |HF| 0.5M |HF| 0.5M
pH = pKa + log ( ) = pKa + log ( ) = pKa + log ( 1)
|HF| |HF| |HF| |HF|
0.5M 0.5M
pH pKa = log ( 1) => 10pHpKa = 1
|HF| |HF|
0.5M 0.5M
|HF| = = = 0.2213 M
10pHpKa +1 103.3.3.2 +1
|F | = 0.5 M |HF| = 0.5M 0.2213 M = 0.2782 M
o Comprobando, con la ecuacin de Henderson-Hasselbach, que los datos obtenidos
sean los correctos tenemos:
|F | 0.2782 M
pH = pKa + log ( ) = 3.2 + log ( ) = 3.30
|HF| 0.2213 M
o Ya que tenemos |HF| y |F-| y, sabiendo que se requiere preparar un litro de
disolucin, calculamos la masa de NaF y el volumen de HF que se necesitan para
obtener la disolucin buffer:
Clculos asociados a disoluciones amortiguadoras de pH. Pgina 3
Laboratorio de qumica general II. Departamento de qumica
inorgnica y nuclear. Clave 1211.
- Obteniendo la masa de NaF (MMNaF= 42 g/mol):
0.2782 mol NaF 42 g
x 1L = 0.2782 mol NaF x ( ) = 11.6844 g NaF
L mol
- Obteniendo el volumen de HF 48% m/m; = 1.16 g/mL; MMHF= 20 g/mol
Calculando la molaridad inicial de HF:
Obteniendo el volumen de disolucin:
48 g HF m m 100g
= / v= = = 86.2069 mL = 0.0862 L
100 g Dis v 1.16 g/mL
Obteniendo los moles de HF:
m 48 g
n= = = 2.4 mol HF
MM 20 g/mol
Obteniendo la molaridad de la disolucin al 48%:
n 2.4 mol HF
M= = = 27.8 M
v [L] 0.0862 Ldis
Calculando el volumen necesario, usando la frmula de dilucin tenemos que:
MI= 27.8M MF= 0.2213 M
VI= ? VF= 1L 1000 mL
MF VF (0.2213M)(1000mL)
MI VI = MF VF => VI = = = 7.98 mL 8mL
MI 27.8 M
- As que para obtener un buffer de florurosi de pH igual a 3.3 y concentracin 0.5 molar se
deben usar NaF y HF siendo la masa del primero 11.6844g y el volumen del que se debe tomar
de una disolucin 48 %m/m, del segundo, debe ser de aproximadamente 8 mL.
Se requieren preparar 250 mL de un buffer de amoniaco con un pH igual a 10 y una
concentracin de 6 M. Para esto se cuenta con NH3 28 % m/v y HCl 36% m/m con una
densidad de 1.16 g/mL Qu volumen de NH3 y de HCl se necesitan para preparar el buffer?
- Existen ocasiones, como en ste caso, en las que para preparar el buffer solo se cuenta con
el cido o con la base del par y para obtener la concentracin de la otra especie del par es
necesario hacer reaccionar a la especie del para que tenemos, con un cido o con una base
(segn sea el caso), para generar a la otra especie del par.
- Para resolver este problema primero realizamos la metodologa ya descrita para las
disoluciones buffer:
|NH3 | + |NH4+ | = 6M
|NH3 | = 6M |NH4+ |
Clculos asociados a disoluciones amortiguadoras de pH. Pgina 4
Laboratorio de qumica general II. Departamento de qumica
inorgnica y nuclear. Clave 1211.
|Base| |NH3 |
pH = pKa + log ( ) => pH = pKa + log ( )
|cido| |NH4+ |
|6M |NH4+ || 6M
pH = pKa + log ( ) = pKa + log ( 1)
|NH4+ | |NH4+ |
6M 6M 6M
pH pKa = + 1 => |NH4+ | = pHpKa = 0.75 = 0.9059M
|NH4 | 10 + 1 10 +1
|NH3 | = 6M |NH4+ | = 6M 0.9059M = 5.0941M
Comprobando los datos obtenidos:
|NH3 | 5.0941
pH = pKa + log ( + ) = 9.25 + log ( ) = 9.9999 10
|NH4 | 0.9059
- Ahora ya sabemos las concentraciones de |NH3| y |NH4+| AL EQUILIBRIO (recordemos que
un buffer se da con concentraciones al equilibrio) planteamos la tabla de variacin de
especies para conocer la cantidad de H+ necesarios:
NH3 H+ NH4+
Inicio Co=6M - -
Reacciona Co-x x x
Al equilibrio Co-x - x
- Con esto se ve que la concentracin de NH4+ al equilibrio debe ser la misma que la
concentracin de H+ (provenientes del HCl) que se agreguen por lo que necesitamos una
concentracin de HCl de 0.9059 M.
- Sabiendo esto calculamos el volumen de NH3 (MM=17g/mol) 28%m/v y de HCl (MM=36
g/mol) 36% m/m con una densidad de 1.19 g/mL necesarios para tener al final las
concentraciones de NH3 y NH4+ (5.0941M y 0.9059M, respectivamente):
- Obteniendo el volumen de NH3 28% m/v para tener como concentracin inicial, Co, 6M:
28 g NH3 280 g NH3
28% m/v = =
100 mL dis 1000 mL dis
280 g NH3 1 mol 16.5 mol NH3
x = = 16.5M
1 L dis 17 g 1L
MI= 16.6 M MF= 6M
VI= ? VF= 250 Ml
MF VF (6 M)(250 mL)
MI VI = MF VF => VI = = = 90.9 mL
MI 16.5 M
Clculos asociados a disoluciones amortiguadoras de pH. Pgina 5
Laboratorio de qumica general II. Departamento de qumica
inorgnica y nuclear. Clave 1211.
- Obteniendo el volumen de HCl 36% m/m; = 1.19 g/mL para tener una concentracin de 0.9059
mL que ser la que nos dar la concentracin, de mismo valor numrico, de NH4+.
Obteniendo la molaridad inicial del HCl.
Obteniendo el volumen de disolucin:
36 g HF m m 100g
= / v= = = 84.0336 mL = 0.0840L
100 g Dis v 1.19 g
mL
Obteniendo los moles de HCl:
m 36 g
n= = = 1 mol HCl
MM 36 g/mol
Obteniendo la molaridad de la disolucin al 36%:
n 1 mol HCl
M= = = 11.9 M
v [L] 0.0840 Ldis
Calculando el volumen necesario, usando la frmula de dilucin tenemos que:
MI= 11.9M MF= 0.9059 M
VI= ? VF= 250 mL
MF VF (0.9059M)(250mL)
MI VI = MF VF => VI = = = 19.0 mL
MI 11.9 M
- As obtenemos que se necesitan 90.9 mL de NH 3 28% m/v a los cuales se les adicionaran
19.0 mL de HCl 36 % m/m para tener al final un buffer de amoniaco con una concentracin de
6 M y con un pH igual a 10.
i
El nombre del buffer se da por medio de la base conjugada del par; as una disolucin buffer generada por el
par HBenz/Benz- se llamar buffer de benzoatos, una disolucin generada por el par HF/F- se llamar buffer
de fluoruros y una disolucin buffer del par NH4+/NH3 se llamar buffer de amoniaco.
Clculos asociados a disoluciones amortiguadoras de pH. Pgina 6
Das könnte Ihnen auch gefallen
- Soluciones BaufferDokument52 SeitenSoluciones BaufferFeña Ibarra FuentesNoch keine Bewertungen
- EJercicios Resueltos Sobre PH y POHDokument16 SeitenEJercicios Resueltos Sobre PH y POHWilliam A Lopez QuejNoch keine Bewertungen
- A1-Acido y BaseDokument17 SeitenA1-Acido y BaseKOBRINJANoch keine Bewertungen
- 4) Soluciones Reguladoras 2021 CorregidoDokument37 Seiten4) Soluciones Reguladoras 2021 CorregidorichmindNoch keine Bewertungen
- Repaso Ejs PHDokument4 SeitenRepaso Ejs PHVicto VetNoch keine Bewertungen
- Ejercicios de Laboratorio 3Dokument5 SeitenEjercicios de Laboratorio 3Rembert MorenoNoch keine Bewertungen
- Informe Biofarmacia 3Dokument8 SeitenInforme Biofarmacia 3Valeery CruzNoch keine Bewertungen
- PRACTICA SEMANA 1 - Preparación de Soluciones BufferDokument25 SeitenPRACTICA SEMANA 1 - Preparación de Soluciones BufferVIVIANA ZULEMA AZA�ERO MAGAN100% (1)
- Clase 7 QUIM 020 BUFFERS (31-3-2023)Dokument28 SeitenClase 7 QUIM 020 BUFFERS (31-3-2023)Polette Palominos OssesNoch keine Bewertungen
- Soluciones Amortiguadoras PDFDokument15 SeitenSoluciones Amortiguadoras PDFAnonymous YztNwEiK6Noch keine Bewertungen
- Clases de Acido-Base II22012Dokument49 SeitenClases de Acido-Base II22012antonioNoch keine Bewertungen
- 8 Soluciones BufferDokument18 Seiten8 Soluciones BufferNicolas Patricio SitjaNoch keine Bewertungen
- PROBLEMA de Hidrolisis y NeutralizacionDokument9 SeitenPROBLEMA de Hidrolisis y NeutralizacionDAVY MARK ANCHIRAICO SOTONoch keine Bewertungen
- Taller 9Dokument10 SeitenTaller 9yenNoch keine Bewertungen
- TP NRO.5 EQUILIBRIO ÁCIDO-BASE Y PHDokument4 SeitenTP NRO.5 EQUILIBRIO ÁCIDO-BASE Y PHColores FalangeNoch keine Bewertungen
- Solucionario Ejercicios Resueltos Semana 1Dokument27 SeitenSolucionario Ejercicios Resueltos Semana 1harold reyes cardozaNoch keine Bewertungen
- Bioquimica Practica (N° 3) Veterinaria 2021 - IDokument12 SeitenBioquimica Practica (N° 3) Veterinaria 2021 - IAlyssa Li SalazarNoch keine Bewertungen
- Taller Acido Base 22-07-23Dokument12 SeitenTaller Acido Base 22-07-23Edgar Gerardo Huaraya FernandezNoch keine Bewertungen
- Serie. A y B. DebilesDokument9 SeitenSerie. A y B. DebilesEmilio SecruNoch keine Bewertungen
- Clase 4 - BufferDokument40 SeitenClase 4 - Buffertomibosch98Noch keine Bewertungen
- Problemas de Equilibrio Iónico Ácidos y Bases - PPTX SeminarioDokument13 SeitenProblemas de Equilibrio Iónico Ácidos y Bases - PPTX SeminariojojlllNoch keine Bewertungen
- Buffer Clase de ProblemasDokument10 SeitenBuffer Clase de ProblemasHeliNoch keine Bewertungen
- Ejercicios de PHDokument16 SeitenEjercicios de PHIsmael Espinoza0% (1)
- (Ac) (Ac) (Ac) Proviene de Una Base Fuerte No Se Hidroliza I) 0,1M - F) - 0,1M 0,1MDokument9 Seiten(Ac) (Ac) (Ac) Proviene de Una Base Fuerte No Se Hidroliza I) 0,1M - F) - 0,1M 0,1MAgustina Paez carattiNoch keine Bewertungen
- Ejercicios de ácido-Base ResueltosDokument4 SeitenEjercicios de ácido-Base ResueltosClaudia Montoya SalazarNoch keine Bewertungen
- Ejemplos de Cálculo Del PH 06Dokument5 SeitenEjemplos de Cálculo Del PH 06Paul Sandoval Olaya100% (1)
- Práctica Bioquímica 1Dokument8 SeitenPráctica Bioquímica 1Fabricio Melgarejo AlvaradoNoch keine Bewertungen
- PH y BUFFERS 2019-IDokument34 SeitenPH y BUFFERS 2019-Ikeisy jcNoch keine Bewertungen
- Litro Mol HNO G HNO Mol X Disolución G HNO G X Disolución Litro Disolución GDokument37 SeitenLitro Mol HNO G HNO Mol X Disolución G HNO G X Disolución Litro Disolución GNasrine HelaliNoch keine Bewertungen
- Disoluciones Amortiguadoras PDFDokument18 SeitenDisoluciones Amortiguadoras PDFJordan Elías Bravo GarcíaNoch keine Bewertungen
- PH 2018-IDokument34 SeitenPH 2018-IAngela Boza CajjaNoch keine Bewertungen
- Ejercicios Acido BaseDokument15 SeitenEjercicios Acido BaseStefany Mariela Pineda AyalaNoch keine Bewertungen
- Soluciones BaufferDokument52 SeitenSoluciones BaufferJustin Murray90% (60)
- Equilibrio Ionico EJERCICIOS RESUELTOSDokument21 SeitenEquilibrio Ionico EJERCICIOS RESUELTOSVictoria Villavicencio Martinez25% (4)
- DISOLUCIONESDokument32 SeitenDISOLUCIONESClaudia Patricia Ballen Garzon0% (1)
- La Constante de Basicidad KBDokument3 SeitenLa Constante de Basicidad KBCarlosuarez99Noch keine Bewertungen
- Copia de EQUILIBRIO IONICODokument20 SeitenCopia de EQUILIBRIO IONICODayane CarolineNoch keine Bewertungen
- PH y BUFFERS 2019-IDokument34 SeitenPH y BUFFERS 2019-Ikeisy jcNoch keine Bewertungen
- Diapositivas Acido BaseDokument37 SeitenDiapositivas Acido BaseNicoll AndreaNoch keine Bewertungen
- Clase 3 - Soluciones BufferDokument20 SeitenClase 3 - Soluciones Bufferantosimoni13Noch keine Bewertungen
- Sesion 1 - Problemas ResueltosDokument29 SeitenSesion 1 - Problemas ResueltosEli Conejo Dada60% (5)
- Quimica Analitica Acido BaseDokument137 SeitenQuimica Analitica Acido BaseGardner1983Noch keine Bewertungen
- AGUA y PHDokument59 SeitenAGUA y PHCAMILO ANDRES TONCIO CACERESNoch keine Bewertungen
- Problem Ill As 2Dokument54 SeitenProblem Ill As 2Ronald Caceres CandiaNoch keine Bewertungen
- Problemas Se Equilibrio IonicoDokument8 SeitenProblemas Se Equilibrio IonicoElvis ÁlvarezNoch keine Bewertungen
- Ka, KB e Hidrolisis de SalesDokument20 SeitenKa, KB e Hidrolisis de SalesLourdes Marién Avila LópezNoch keine Bewertungen
- Acidos y Bases 2012Dokument2 SeitenAcidos y Bases 2012Carmen MartínezNoch keine Bewertungen
- Bloque 1discucion 4 GGDokument4 SeitenBloque 1discucion 4 GGJavier Alexander Funes OrellanaNoch keine Bewertungen
- Clases de Acido-BaseDokument47 SeitenClases de Acido-BaseG MarceloNoch keine Bewertungen
- Clase Intensiva 3Dokument3 SeitenClase Intensiva 3Jesús Yair Ramirez VillalobosNoch keine Bewertungen
- Ut 3 Volumetrías de NeutralizaciónDokument10 SeitenUt 3 Volumetrías de Neutralizaciónmario tiradoNoch keine Bewertungen
- INFORME PRACTICA #2 - Equlibrio Ácido - BaseDokument11 SeitenINFORME PRACTICA #2 - Equlibrio Ácido - BaseKEVIN ADRIAN HERNANDEZ BOCANEGRANoch keine Bewertungen
- PH TeoriaDokument7 SeitenPH Teoriaklissman Alvarado garciaNoch keine Bewertungen
- Equilibrios Acido Base Selectividad 2 ParteDokument11 SeitenEquilibrios Acido Base Selectividad 2 ParteAMYNNXXXXNoch keine Bewertungen
- BuffersDokument45 SeitenBuffersSofia Leiva JaraNoch keine Bewertungen
- Ácidos y Bases FormularioDokument6 SeitenÁcidos y Bases FormulariojuanaNoch keine Bewertungen
- Manejo de Material Volumetrico de VidrioDokument8 SeitenManejo de Material Volumetrico de VidrioAdrizz FrancoNoch keine Bewertungen
- Examen de Preparación de DisolucionesDokument1 SeiteExamen de Preparación de DisolucionesAdrizz FrancoNoch keine Bewertungen
- Examen NomenclaturaDokument1 SeiteExamen NomenclaturaAdrizz FrancoNoch keine Bewertungen
- Examen de Titulaciones Ácido-BaseDokument1 SeiteExamen de Titulaciones Ácido-BaseAdrizz FrancoNoch keine Bewertungen
- Síntesis de Ácido Adipico A Partir de CiclohexanolDokument3 SeitenSíntesis de Ácido Adipico A Partir de CiclohexanolAdrizz Franco50% (6)
- Síntesis de Ácido Benzoico. Reacción Del Haloformo.Dokument5 SeitenSíntesis de Ácido Benzoico. Reacción Del Haloformo.Adrizz Franco50% (2)
- Sintesis de NitrobencenoDokument5 SeitenSintesis de NitrobencenoAdrizz FrancoNoch keine Bewertungen
- Practica 9 Acidos y Bases FuertesDokument8 SeitenPractica 9 Acidos y Bases FuertesAdrizz Franco100% (1)
- Acidos y Bases TeoriaDokument73 SeitenAcidos y Bases TeoriaAlejandra QuinteroNoch keine Bewertungen
- VolumetríaDokument9 SeitenVolumetríaSEBASTIAN DIAZNoch keine Bewertungen
- Quimiometría NaiDokument13 SeitenQuimiometría NaiNaiara WagnerNoch keine Bewertungen
- Manual de PracticasDokument72 SeitenManual de PracticasYATZIRI ALEJANDRA REYES TEMPLOSNoch keine Bewertungen
- Informe Analitica LL ColoranteDokument12 SeitenInforme Analitica LL ColoranteCamila CausilNoch keine Bewertungen
- 5 Labo de AnalisisDokument15 Seiten5 Labo de AnalisisEduardo Sanchez TrujilloNoch keine Bewertungen
- Practica 5 Orgánica Destilación Simple y FraccionadaDokument6 SeitenPractica 5 Orgánica Destilación Simple y FraccionadaLaura Cedillo100% (3)
- Informe de Bioquimica (SOLUCIONES AMORTIGUADORAS Y CAPACIDAD AMORTIGUADORA )Dokument2 SeitenInforme de Bioquimica (SOLUCIONES AMORTIGUADORAS Y CAPACIDAD AMORTIGUADORA )Kazuma IzumiNoch keine Bewertungen
- ProyectoDokument5 SeitenProyectoLu CerinoNoch keine Bewertungen
- CapI 2019100425Dokument13 SeitenCapI 2019100425JEANINE LETICIA VARGAS GALARZANoch keine Bewertungen
- Preguntas Acido Base, Usando TeclerasDokument3 SeitenPreguntas Acido Base, Usando TeclerasAdriana Toro RosalesNoch keine Bewertungen
- Producto de SolubilidadDokument33 SeitenProducto de SolubilidadEsthefany Aguilar Gomez100% (1)
- Eco Microb Ejercicios 2018Dokument20 SeitenEco Microb Ejercicios 2018Joel MartinezNoch keine Bewertungen
- 2 Segunda Evaluacuón de Analisis Quimico e Instrumental-1Dokument3 Seiten2 Segunda Evaluacuón de Analisis Quimico e Instrumental-1davidalvarezsegNoch keine Bewertungen
- Taller 3. VOL ACIDO-BASEDokument5 SeitenTaller 3. VOL ACIDO-BASEjuan paNoch keine Bewertungen
- Determinanacion de La Concentracion Del Aceite Esencial de La MuñaDokument2 SeitenDeterminanacion de La Concentracion Del Aceite Esencial de La MuñaYanet TaccaNoch keine Bewertungen
- PH, DiapositivasDokument37 SeitenPH, Diapositivasyoliemi33% (3)
- Titulaciones Conductimétricas.Dokument10 SeitenTitulaciones Conductimétricas.Maylin CNNoch keine Bewertungen
- PRÁCTICA 07 AnaliticaDokument10 SeitenPRÁCTICA 07 AnaliticaJoel Hernan HUARACA MAURICIONoch keine Bewertungen
- Guia Ejercicios Qui-180 202020 PDFDokument185 SeitenGuia Ejercicios Qui-180 202020 PDFFelipe Aguirre KatzNoch keine Bewertungen
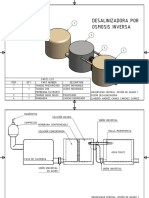
- Planos DesalinizadoraDokument6 SeitenPlanos DesalinizadoraDavidFernandoSantamaríaMaldonadoNoch keine Bewertungen
- Prueba Metalurgica Mineral MRDokument9 SeitenPrueba Metalurgica Mineral MRoswaldo sanchezNoch keine Bewertungen
- Importancia de La PermanganometriaDokument4 SeitenImportancia de La PermanganometriaRonald fuentes ttupaNoch keine Bewertungen
- Practica 12. Principio de Le ChâtelierDokument7 SeitenPractica 12. Principio de Le ChâtelierAldo CastroNoch keine Bewertungen
- LABORATORIO DE FISICOQUIMICA PRACTICA N5 Principios de Le ChateliarDokument7 SeitenLABORATORIO DE FISICOQUIMICA PRACTICA N5 Principios de Le ChateliarDANIEL FELIPE LOZANO PALOMINONoch keine Bewertungen
- Guía 8 - Equilibrioqco2022Dokument11 SeitenGuía 8 - Equilibrioqco2022raquelNoch keine Bewertungen
- Alcalinidad PDFDokument17 SeitenAlcalinidad PDFVladimir OvmfNoch keine Bewertungen
- 1.PREVIO Cinética de Acetato de Etilo Con Hidróxido de SodioDokument5 Seiten1.PREVIO Cinética de Acetato de Etilo Con Hidróxido de SodioAlberto Salgado Carmona100% (1)
- Informe - Lab Quimica G2 Juan Camilo Cardona - Juan Felipe Ramirez Garcia #6Dokument9 SeitenInforme - Lab Quimica G2 Juan Camilo Cardona - Juan Felipe Ramirez Garcia #6Felipe RamirezNoch keine Bewertungen
- 1.4 Fase de Vía HúmedaDokument22 Seiten1.4 Fase de Vía Húmedathefox13579Noch keine Bewertungen