Beruflich Dokumente
Kultur Dokumente
Qui Mica
Hochgeladen von
Idaliana Martínez0 Bewertungen0% fanden dieses Dokument nützlich (0 Abstimmungen)
7 Ansichten3 Seitencuestionario de quimica 20-40
Copyright
© © All Rights Reserved
Verfügbare Formate
DOCX, PDF, TXT oder online auf Scribd lesen
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldencuestionario de quimica 20-40
Copyright:
© All Rights Reserved
Verfügbare Formate
Als DOCX, PDF, TXT herunterladen oder online auf Scribd lesen
0 Bewertungen0% fanden dieses Dokument nützlich (0 Abstimmungen)
7 Ansichten3 SeitenQui Mica
Hochgeladen von
Idaliana Martínezcuestionario de quimica 20-40
Copyright:
© All Rights Reserved
Verfügbare Formate
Als DOCX, PDF, TXT herunterladen oder online auf Scribd lesen
Sie sind auf Seite 1von 3
20.
En que consiste el proceso de covalencia
El proceso de covalencia es un enlace donde los tomos se comparten un par de
electrones, no los dan ni reciben, LO COMPARTEN.
21. Que significa electronegatividad ?.
En mi opinin es la energa negativa que tienen las molculas
Es la medida de la capacidad de un tomo para atraer a los electrones
22. Presente diagrama de elementos electronegativos
23. Cul es el nombre del cientfico que invento la escala numrica de
electronegatividad
Fue Linus Pauling
24. Que tiene que ver la electronegatividad con el nmero atmico
En un periodo, la electronegatividad aumenta con el nmero atmico. Dentro de un
grupo, disminuye a medida que el nmero atmico aumenta
25. En que consiste los enlaces covalentes polares
Estos comparten de modo desigual electrones entre tomos de elementos diferentes
26. que entiendes por enlace metlico
Es la unin de los tomos en los cristales metlicos solidos
27. defina conductividad y solubilidad
Conductividad: propiedad natural de los cuerpos que permite el paso a travs de si el
calor o la electricidad
Solubilidad: capacidad de una sustancia o un cuerpo para disolverse al mezclarse con
un liquido
28. Como trabaja un compuesto inico y una molcula frente a la conduccin de
electrones
29. Cul es la diferencia entre lquido polar y no polar
Se denomina liquido polar a aquellas que logran formar puentes de hidrogeno entre si o
con otras sustancias y no polar como los aceites, las molculas se unen entre si por
enlaces distintos al enlace de hidrogeno
30. cuadro
Caracterstica S. Inica Covalente Metales
Estructura Iones positivos y molculas tomos
negativos
Estado de Solido Slido, liquido, Todos son slidos
agregacin gaseoso execto Hg
Punto de Fusin Alto de 300 a 1000 Bajo, muy variable Muy variable: <28C
G execto el Hg
Solubilidad Soluble en Soluble en No solubles en
disolventes polarescomponentes disolventes, todos
polares y no en acido
polares
Conductividad Buena (Fundido, en No Si (Como slido,
agua) fundido)
2 Ejemplos NaCi, CaCi2 CH4, CO2 Mg, AI, Fe
31. Que se entiende por estructura de resonancia
Se utiliza para representar molculas, iones y radicales para los cuales resulta
inadecuado una sola estructura de Lewis
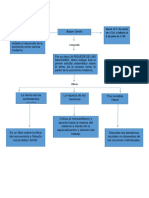
32. En que consiste la repulsin de pares de electrones de la capa de valencia
(RPECV)
En este modelo, las nubes de electrones con carga negativa que rodean el tomo
central de una molcula se repelen mutuamente tanto como es posible, es decir, los
pares de electrones que rodean el tomo central se mantienen tan alejados unos de
otros como es posible
33. Que electrones se visualizan en una distribucin (RPECV)
Se visualizan los pares de electrones no compartidos, tambin llamados pares
solitarios, as como los pares de electrones, distribuidos alrededor del tomo central tan
lejos uno de otros como es posible
34. Que es una distribucin lineal
2 globos atados uno al otro tienden a apuntar en sentido opuesto, de modo que los 2
globos y el nudo que los une forman un ngulo de 180
BeF2 BeCl2
35. Que es una distribucin plana
Cuando se atan juntos 3 globos, el nudo del centro y los 3 globos tienden a yacer en un
mismo plano y adoptar posiciones tales que los ngulos entre ellos sea de 120
BF3 NH3
36. Que es una distribucin tetradrica
Las molculas con 4 tomos unidos a un tomo central forman estructura cuya forma
se asemeja a 4 globos atados a un centro comn, los cuales se distribuyen lo ms
alejado posible formando ngulos de 109.5
CH4 SIO4
37. Que es una molcula no linear o angular
El paso de una corriente elctrica a travs del agua descompone las molculas y libera
2 volmenes de hidrogeno gaseoso por cada volumen de oxigeno gaseoso
38. Que es una molcula piramidal trigonal
la geometra molecular piramidal trigonal es un tipo de geometra molecular con un
tomo en el vrtice superior y tres tomos en las esquinas de un tringulo, en un plano
inferior. Cuando los tres tomos en las esquinas son iguales, la molcula pertenece al
grupo puntual
39. Que es una figura octadrica
Se llama a la forma de los compuestos en los que seis ligados se disponen alrededor
de un tomo o ion, central, definiendo los vrtices de un octaedro
SF6
40. En que consiste los puentes de hidrogeno
Estos intervienen las fuerzas de atraccin entre ciertas molculas polares que
contienen tomos de hidrogeno, a la formacin de puentes de hidrogeno en la molcula
de agua se debe a los puntos de ebullicin y de fusin anormalmente altos
Das könnte Ihnen auch gefallen
- Laboratorio Fisica 2 Practica 7Dokument12 SeitenLaboratorio Fisica 2 Practica 7CacaNoch keine Bewertungen
- Manual de Operaciones Planta Concentradora Flotación - TECSUPDokument34 SeitenManual de Operaciones Planta Concentradora Flotación - TECSUPAntonio HUAYHUA ROJAS100% (2)
- Un Motor de Inducción Trifasico de 10 HPDokument1 SeiteUn Motor de Inducción Trifasico de 10 HPIdaliana MartínezNoch keine Bewertungen
- Cuestionario de QuimicaDokument2 SeitenCuestionario de QuimicaIdaliana MartínezNoch keine Bewertungen
- Experiencia NDokument6 SeitenExperiencia NIdaliana MartínezNoch keine Bewertungen
- Cuestionario de QuimicaDokument2 SeitenCuestionario de QuimicaIdaliana MartínezNoch keine Bewertungen
- Análisis Del Alcohol C2 H5OHDokument1 SeiteAnálisis Del Alcohol C2 H5OHIdaliana MartínezNoch keine Bewertungen
- Informe de Lab Fisica MRUDokument4 SeitenInforme de Lab Fisica MRUIdaliana MartínezNoch keine Bewertungen
- Trabajo de EconomiaDokument1 SeiteTrabajo de EconomiaIdaliana MartínezNoch keine Bewertungen
- Ingenieria SanitariaDokument80 SeitenIngenieria SanitariagargolyNoch keine Bewertungen
- Column A de PlatosDokument100 SeitenColumn A de PlatosManuel Augusto Alvarado Huanca100% (1)
- Energia Termica - Central de Ciclo Combinado Ventajas e InconvenientesDokument2 SeitenEnergia Termica - Central de Ciclo Combinado Ventajas e InconvenientesCristopher Trejo RodriguezNoch keine Bewertungen
- Taller 4 - NewtonDokument3 SeitenTaller 4 - Newtondaniel vegaNoch keine Bewertungen
- Instrumentacion para La Espectroscopia EN EL VISIBLE Y EL UVDokument14 SeitenInstrumentacion para La Espectroscopia EN EL VISIBLE Y EL UVAndoni Godinez CamargoNoch keine Bewertungen
- Ensayo Corte Directo Suelos CohesivosDokument17 SeitenEnsayo Corte Directo Suelos CohesivosLuis JavierNoch keine Bewertungen
- Muelles MecanicosDokument33 SeitenMuelles MecanicosHaa SuperNoch keine Bewertungen
- 5° FICHA CyT (10) .Docx Efecto IveraderoDokument4 Seiten5° FICHA CyT (10) .Docx Efecto IveraderoNorma Viviana Barbaran MedinaNoch keine Bewertungen
- N5 - Diagrama de Fuerzas Cortantes y Momentos Flectores PDFDokument32 SeitenN5 - Diagrama de Fuerzas Cortantes y Momentos Flectores PDFRUBINoch keine Bewertungen
- Mapa Conceptual de Absorcion de GasesDokument1 SeiteMapa Conceptual de Absorcion de GasesCarmen Roxana Quispe CastilloNoch keine Bewertungen
- Diseño de Vigas Doblemente ReforzadasDokument4 SeitenDiseño de Vigas Doblemente ReforzadasernestoNoch keine Bewertungen
- Golpe de ArieteDokument5 SeitenGolpe de ArieteAmilcarNoch keine Bewertungen
- Introducción A La Medición Mediante Bandas ExtensométricasDokument272 SeitenIntroducción A La Medición Mediante Bandas Extensométricasxevi00Noch keine Bewertungen
- Examen AerodinamicaDokument5 SeitenExamen AerodinamicaArturo ZugarazoNoch keine Bewertungen
- Ensayo Traccion TerminadoDokument12 SeitenEnsayo Traccion TerminadoAngieRojasNoch keine Bewertungen
- C10 Remaches SoldaduraDokument26 SeitenC10 Remaches SoldaduracarlosNoch keine Bewertungen
- Producto de SolubilidadDokument5 SeitenProducto de SolubilidadMARIA PAULA NAVARRO GONZALEZNoch keine Bewertungen
- DOCUMENTO DE ESTUDIO No. 8. FRACCION DISOCIADA DE SISTEMAS ACIDO-BASE MONO Y POLIPROTICOS LOGO UADokument20 SeitenDOCUMENTO DE ESTUDIO No. 8. FRACCION DISOCIADA DE SISTEMAS ACIDO-BASE MONO Y POLIPROTICOS LOGO UAKevinVivarezNoch keine Bewertungen
- Informe de Altimetría y NivelaciónDokument22 SeitenInforme de Altimetría y NivelaciónJosé Víctor Becerra Cotrina100% (6)
- Lubricación de Equipos Pesados y LivianosDokument14 SeitenLubricación de Equipos Pesados y LivianosFRANKLIN RAMIREZ HERNANDEZNoch keine Bewertungen
- Mecánica de FluidosDokument57 SeitenMecánica de FluidosMargarita Julcamoro InfanteNoch keine Bewertungen
- Cálculos EmbragueDokument38 SeitenCálculos EmbragueRodríguez AndrésNoch keine Bewertungen
- Produccion Carburos de VanadioDokument4 SeitenProduccion Carburos de VanadioDiego LandazábalNoch keine Bewertungen
- Enlace 1Dokument2 SeitenEnlace 1Edson Luis Egusquiza CordovaNoch keine Bewertungen
- RMS 4 PDFDokument28 SeitenRMS 4 PDFMelitza Villanueva CuvasNoch keine Bewertungen
- Hidrodesalquilación Del Tolueno (Hda)Dokument14 SeitenHidrodesalquilación Del Tolueno (Hda)Alicia PastranaNoch keine Bewertungen
- DIAPOSDokument25 SeitenDIAPOSjorge luisNoch keine Bewertungen
- Laboratorio Ventilacion en Minas N 4 FINAL PDFDokument17 SeitenLaboratorio Ventilacion en Minas N 4 FINAL PDFYvan RamirezNoch keine Bewertungen