Beruflich Dokumente
Kultur Dokumente
Estequiometria de Reacciones Redox Titulación Yodimétrica de Vitamina C
Hochgeladen von
Leonardo ReyesCopyright
Verfügbare Formate
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
Verfügbare Formate
Estequiometria de Reacciones Redox Titulación Yodimétrica de Vitamina C
Hochgeladen von
Leonardo ReyesCopyright:
Verfügbare Formate
Universidad de Pamplona
Pamplona, Norte de Santander. Colombia
Laboratorio Química Básica 2
ESTEQUIOMETRIA DE REACCIONES REDOX:
TITULACIÓN YODIMÉTRICA DE VITAMINA C
PORRAS ARIZA, Mishel Yelitza; REYES FERNANDEZ, Leonardo Steyman; SERRANO
OCHOA, Camilo Andrés.
Universidad de Pamplona, Facultad de Ingenierías y Arquitectura, Departamento de Ingeniería Ambiental,
Civil y Química, Programa de Ingeniería Química.
Pamplona, Norte de Santander
02 de octubre de 2017
RESUMEN
En el presente informe de laboratorio se determinó puntos de congelación el peso molecular
de un anticongelante comercial y el factor “i” (siguiendo los pasos de la determinación del
peso molecular que consiste en añadir 1ml de etilenglicol en 10 ml de agua y e introduciendo
todo en un baño de hielo y el agitador y midiendo el tiempo cada 30 segundos y haciendo 10
lecturas hasta que se congele) Vant’ Hoff en soluciones de 0,6 gr NaCl como soluto y 3,4gr
sacarosa cómo soluto en 10 ml de agua.
PALABRAS CLAVE: Punto de congelación, anticongelante, baño de hielo, peso
molecular, etilenglicol.
ABSTRACT
In the present laboratory freezing points were determined on the molecular weight of an
antifreeze and the factor "i" (following the molecular weight determination step of adding 1
ml of ethylene glycol in 10 ml of water and introducing all into an ice bath and stirrer and
measuring the time every 30 seconds and making 10 freeze-thaw) Vant 'Hoff in solutions of
0.6 g NaCl as solute and 3.4 g saccharide as a solute in 10 ml of water.
KEYWORDS: Freezing point, antifreeze, ice bath, molecular weight, ethylene glycol.
adición de un reactivo estándar que
INTRODUCCIÓN reacciona con ella en proporción definida
y conocida.
La titulación es el método por el cual se
determina una cantidad desconocida de La adición de un reactivo estándar (un
una sustancia particular, mediante la reactivo de concentración conocida y
LABORATORIO QUÍMICA BÁSICA 2 1
Universidad de Pamplona
Pamplona, Norte de Santander. Colombia
Laboratorio Química Básica 2
frecuentemente denominado como es, en las reacciones de oxireducción). Los
reactivo titulado) se regula y se mide de agentes oxidantes o reductores presentan
alguna forma, requiriéndose un método de diferencies actividades químicas.
indicación para saber cuándo la cantidad Oxidantes fuertes tienen pronunciada
de reactivo normal juntado y precisamente tendencia a ganar electrones, que son
la suficiente para reaccionar capaces de remover un gran número de
cuantitativamente con la sustancia que se reductores. Lo mismo sucede en la pérdida
determina. de electrones en relación a los reductores.
Siendo la intensidad de la acción oxidante
Como consecuencia, conociendo la
o reductora de un sistema determinada por
proporción en que reaccionan las
su potencial de oxidación. (2)
sustancias y teniendo determinada la
cantidad de una sustancia (el reactivo Por otra parte, los métodos volumétricos
titulado) necesaria para reaccionar en esta que utilizan reacciones de oxidación y
proporción, se puede calcular fácilmente la reducción dependen de los potenciales de
cantidad desconocida de sustancia las semireacciones relacionadas, pero,
presente en el frasco de reacción. además de los potenciales favorables, los
agentes oxidantes y reductores deben ser
En una titulación, el punto en que la
estables en solución y la sustancia a ser
cantidad de reactivo titulado adicionado es
determinada debe ser colocada bajo
exactamente suficiente para que se
determinado estado de oxidación, definido
combine en una proporción
y estable, antes de iniciar la titulación. (3)
estequiométrica, o empíricamente
reproducible con la sustancia que se La yodometría se utiliza comúnmente para
determina, se llama punto de equivalencia. analizar la concentración de agentes
oxidantes en muestras de agua, tales como
El punto final de una titulación debe
la saturación de oxígeno en los estudios
coincidir con el punto de equivalencia o
ecológicos o de cloro activo en el análisis
estar muy próximo de él. La diferencia
del agua de la piscina. Para un volumen
entre los puntos de equivalencia y final se
conocido de la muestra, se añade una
llama intervalo del indicador.
cantidad en exceso de yoduro, pero
Las titulaciones se realizan casi siempre conocido, que los agentes oxidantes
con soluciones o disoluciones, sin oxidan el yoduro a yodo. El yodo se
embargo, también es fácil realizarlas con disuelve en la solución que contiene
sustancias en los estados gaseosos, sólido yoduro para dar iones triyoduro, que tienen
y de fusión, si se dispone de equipo un color marrón oscuro; y será titulado con
adecuado. (1) una solución estandarizada de tiosulfato de
sodio. (4)
Entre los tipos de titulación se encuentra el
de oxidación-reducción o más conocido En los métodos analíticos en que
como redox; y se basan en los procesos en interviene yodo no son necesarios los
que existe transferencia de electrones (esto indicadores redox normales, porque se
LABORATORIO QUÍMICA BÁSICA 2 2
Universidad de Pamplona
Pamplona, Norte de Santander. Colombia
Laboratorio Química Básica 2
dispone de almidón, un indicador interno Posteriormente, se preparó el tiosulfato,
sensible que experimenta una interacción para ello se disolvió aproximadamente
enormemente específica con yodo. El 8,7 g de tiosulfato de sodio en 500 mL de
yodo libre forma un color azul muy intenso agua recién hervida que contenía 0,5 g de
con almidón disperso coloidalmente y esta carbonato de sodio y se almacenó en un
coloración sirve de indicación de la recipiente.
presencia de yodo. (5)
Después, se preparó 500 mL de una
solución yodato potásico.
Seguidamente se estandarizó el
PARTE EXPERIMENTAL
tiosulfato; de modo que se añadió 25 mL
Materiales y métodos de yoduro de potasio a un erlenmeyer de
125 mL con una probeta,
Para esta práctica se dispuso de dos aproximadamente 1g de yoduro de
montajes, uno para preparación y potasio y 5 mL de ácido sulfúrico; y se
estandarización de la solución de tituló de inmediato tiosulfato hasta que la
tiosulfatol y el otro; para la determinación solución perdió su color quedando
y estandarización de la vitamina c, una amarillo muy claro; luego se adicionó
balanza analítica electrónica (Adventure aproximadamente 1 mL de engrudo
Oasus), una tableta de vitamina c; y almidón como indicador y con ello se
reactivos como yodato potásico (J.T. terminó la titulación.
Baker), tiosulfato de sodio (Carlo Erba),
Por último, se reiteró el procedimiento
yoduro de potasio (Carlo Erba), carbonato
desde que se estandarizó el tiosulfato
de sodio (Analiticals), almidón soluble
hasta que terminó la titulación dos veces
(Merck), además de agua destilada, ácido
más.
sulfúrico al 98%, y yoduro de mercurio II;
que de los cuales no se tenía ninguna Determinación de vitamina c.
información.
Primeramente, con ayuda de la balanza
Procedimiento analítica, se pesó una tableta de
vitamina c; se añadió en un vaso de
Preparación y estandarización precipitado con 150 mL de ácido
de la solución de tiosulfato. sulfúrico y con una varilla de vidrio se
pulverizó hasta que el sólido quedó
Inicialmente se elaboró el indicador de disuelto.
almidón, de tal manera que se preparó un
engrudo con 5g de almidón soluble y Luego, se pasó la muestra a un balón
5mg de yoduro de mercurio en 50mL de aforado de 250 mL y se aforó con agua
agua; luego el engrudo se añadió en un destilada.
vaso de precipitado con 500 mL de agua
Se colocó 25 mL de muestra en tres
hirviendo y se dejó en ebullición hasta
erlenmeyer de 250 mL. Y a cada uno se
que se volvió transparente.
LABORATORIO QUÍMICA BÁSICA 2 3
Universidad de Pamplona
Pamplona, Norte de Santander. Colombia
Laboratorio Química Básica 2
le añadió aproximadamente 1 g de ANÁLISIS DE RESULTADOS
yoduro de potasio y 25 mL de yodato
𝑉. 𝑇𝑒𝑜𝑟𝑖𝑐𝑜 − 𝑉. 𝐸𝑥𝑝𝑒𝑟𝑖𝑚𝑒𝑛𝑡𝑎𝑙
potásico y se tituló de inmediato; y %𝐸𝑟𝑟𝑜𝑟 = ∗ 100
𝑉. 𝑇𝑒𝑜𝑟𝑖𝑐𝑜
luego se añadió aproximadamente 1 mL
del indicador de almidón justo antes de Fórmula 1. Formula usada para hallar el
que se terminó el punto final de la porcentaje de error.
titulación.
Repita la experiencia y tome nota de los
volúmenes requeridos en la tabla 2.
CONCLUSIONES (Consultado el 26 de septiembre
del 2017)
En la presente practica de congelación el
peso molecular de un anticongelante 2. https://quimica.laguia2000.com/co
comercial y el factor “i” de Vant’ Hoff en nceptos-basicos/tipos-de-
titulacion (Consultado el 26 de
soluciones de NaCl y sacarosa, lo cual se
septiembre del 2017)
realizó y efectivamente el procedimiento
se realizó con normalidad, el cambio de 3. http://chemkeys.com/es/2009/07/0
cantidades de soluto y solventes en el 6/determinaciones-yodometricas/
procedimiento prácticamente a la 1/10 (Consultado el 26 de septiembre
parte lo cual no afecto mucho el del 2017)
procedimiento, lo que sí puedo afectar
significativamente son unas cantidades 4. http://www.monografias.com/trab
casi deficientes de solutos que se ajos105/yodometria-quimica-
agregaron de más, pero el efectivamente se analitica/yodometria-quimica-
pudo comprobar que en las lecturas había analitica.shtml
una constante (crioscópica) que se iba (Consultado el 2 de septiembre
manteniendo, y el baño de hielo que ayudo del 2017)
que se mantuvieran el rango de la
temperatura, gracias a que la sal 5. http://www.monografias.com/trab
mantuviera la temperatura del hielo, en fin ajos105/yodometria-quimica-
la práctica se completó como se tenía analitica/yodometria-quimica-
esperado. analitica.shtml
(Consultado el 2 de septiembre
del 2017)
BIBLIOGRAFÍA
1. https://quimica.laguia2000.com/co
nceptos-basicos/titulacion
LABORATORIO QUÍMICA BÁSICA 2 4
Universidad de Pamplona
Pamplona, Norte de Santander. Colombia
Laboratorio Química Básica 2
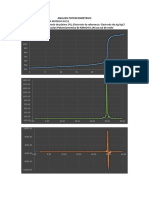
ANEXOS
Obtenga una gráfica temperatura en función del tiempo para cada uno de los sistemas
estudiados.
Reporte la temperatura de fusión del agua, solución de sacarosa, solución de cloruro
de sodio y solución anticongelante.
Reportar el “i” promedio para las soluciones de cloruro de sodio y de sacarosa.
Reportar el peso molecular promedio del anticongelante.
Comparar los resultados obtenidos con los reportados por la literatura.
LABORATORIO QUÍMICA BÁSICA 2 5
Das könnte Ihnen auch gefallen
- AminasDokument9 SeitenAminassussel badayNoch keine Bewertungen
- Presentacion Final Fundamentos DinamoDokument36 SeitenPresentacion Final Fundamentos DinamoAdriánPechCerveraNoch keine Bewertungen
- Variables Aleatorias Discretas PDFDokument3 SeitenVariables Aleatorias Discretas PDFCarlos CoxNoch keine Bewertungen
- Examen Preliminar P - CLOROANILINADokument4 SeitenExamen Preliminar P - CLOROANILINAAlejandra ZeaNoch keine Bewertungen
- Destilacion Sencilla y Fraccionada (Lab. Quimica Organica)Dokument9 SeitenDestilacion Sencilla y Fraccionada (Lab. Quimica Organica)Luis HenriqueNoch keine Bewertungen
- Determinación Volumétrica de Haluros Por Formación de PrecipitadosDokument6 SeitenDeterminación Volumétrica de Haluros Por Formación de PrecipitadosJorly Torres100% (1)
- Informe Sistema TernarioDokument6 SeitenInforme Sistema TernarioYesenia HolguinNoch keine Bewertungen
- Demanda de CloroDokument14 SeitenDemanda de CloroVeronica JjvvNoch keine Bewertungen
- Informe Practica 3Dokument24 SeitenInforme Practica 3Juan pabloNoch keine Bewertungen
- Conclusiones y Recomendaciones de Fiqui 02 de NoviembreDokument6 SeitenConclusiones y Recomendaciones de Fiqui 02 de NoviembreJvr Enriwell100% (1)
- Determinacion Potenciometrica de Cloruros 1Dokument10 SeitenDeterminacion Potenciometrica de Cloruros 1Amarië FelagundNoch keine Bewertungen
- Informe 9-Síntesis de La 1,4-Dihidroquinoxalina-2,3-DionaDokument8 SeitenInforme 9-Síntesis de La 1,4-Dihidroquinoxalina-2,3-DionaKelly GuerreroNoch keine Bewertungen
- Determinacion Cloruros Calcio y MagnesioDokument6 SeitenDeterminacion Cloruros Calcio y MagnesioJosé ChamorroNoch keine Bewertungen
- Informe Inorgánica Quimica Del Grupo 13 Aluminio y Boro 14 de MayoDokument4 SeitenInforme Inorgánica Quimica Del Grupo 13 Aluminio y Boro 14 de MayoPablo AndrésNoch keine Bewertungen
- Obtencion de Acetileno y Propiedades deDokument5 SeitenObtencion de Acetileno y Propiedades deCamilo OliverosNoch keine Bewertungen
- Informe 3Dokument5 SeitenInforme 3Santiago Ospina AreizaNoch keine Bewertungen
- Trabajo de Investigacion de FisicoquimicaDokument13 SeitenTrabajo de Investigacion de FisicoquimicaliNoch keine Bewertungen
- Informe GasesDokument10 SeitenInforme GasesDavid Fernandez0% (1)
- CUESTIONARIODokument3 SeitenCUESTIONARIOJuan Miguel VelezNoch keine Bewertungen
- Determinacion de Una Constante de Equilibrio Por Analisis QuimicoDokument3 SeitenDeterminacion de Una Constante de Equilibrio Por Analisis QuimicoveronicaNoch keine Bewertungen
- Evaluacion de Datos Analiticos - 2018Dokument15 SeitenEvaluacion de Datos Analiticos - 2018keila suarezNoch keine Bewertungen
- Informe 4. Titulaciones de Precipitación FINALxDokument5 SeitenInforme 4. Titulaciones de Precipitación FINALxCamiloNoch keine Bewertungen
- Cuestionario OrganicaDokument2 SeitenCuestionario OrganicaLuis ArroyoNoch keine Bewertungen
- Determinacion de BicarbonatosDokument3 SeitenDeterminacion de BicarbonatosCgamez 123Noch keine Bewertungen
- SaponificaciónDokument3 SeitenSaponificacióndaniel de graciaNoch keine Bewertungen
- Determinacion Del Peso Molecular de Un Liquido Facilmente Vaporizable PDFDokument4 SeitenDeterminacion Del Peso Molecular de Un Liquido Facilmente Vaporizable PDFpepitoNoch keine Bewertungen
- Preparacion de Cloruros Por El Metodo de MORHDokument15 SeitenPreparacion de Cloruros Por El Metodo de MORHJEAN CAMILO PORRAS RICO100% (1)
- Experimento 3. "Determinación de Mezclas Que Contienen Ácido Fosfórico, Fosfatos, Ácido Clorhídrico e Hidróxido"Dokument15 SeitenExperimento 3. "Determinación de Mezclas Que Contienen Ácido Fosfórico, Fosfatos, Ácido Clorhídrico e Hidróxido"Lili OliverosNoch keine Bewertungen
- Informe Organica Johan Gabriela Luis KarolainDokument11 SeitenInforme Organica Johan Gabriela Luis KarolainJohan CárdenasNoch keine Bewertungen
- Conductividad ElectricaDokument9 SeitenConductividad ElectricavkeisyNoch keine Bewertungen
- Preparación de Soluciones AmortiguadorasDokument4 SeitenPreparación de Soluciones AmortiguadorasAngelly LópezNoch keine Bewertungen
- Informe de Laboratorio 6 - Raquejo & VallejoDokument5 SeitenInforme de Laboratorio 6 - Raquejo & VallejoTomas AinstonNoch keine Bewertungen
- Taller 6 EquilibrioDokument3 SeitenTaller 6 Equilibrioliz100% (1)
- Informe de Agua Bioquimica PDFDokument3 SeitenInforme de Agua Bioquimica PDFGabriel Cerra100% (1)
- Ejercicios Clase 8Dokument60 SeitenEjercicios Clase 8marcosNoch keine Bewertungen
- Informe 5 - Síntesis de Ácido CinámicoDokument12 SeitenInforme 5 - Síntesis de Ácido CinámicoJAIME ANDRES BARRETO MONTESNoch keine Bewertungen
- Determinación de La Constante de EquilibrioDokument2 SeitenDeterminación de La Constante de EquilibrioChiran Alexis0% (1)
- Estandarizacion D Kmno4Dokument3 SeitenEstandarizacion D Kmno4Willy MelgarejoRmroNoch keine Bewertungen
- Calor de Neutralización (Fisicoquimica 1)Dokument4 SeitenCalor de Neutralización (Fisicoquimica 1)gerson velezNoch keine Bewertungen
- Informe ObtencionesDokument5 SeitenInforme ObtencionesDarioNoch keine Bewertungen
- Criterios de EspontaneidadDokument3 SeitenCriterios de EspontaneidadjosuediazNoch keine Bewertungen
- Conclusiones y ObservacionesDokument1 SeiteConclusiones y ObservacionesShamir BerrioNoch keine Bewertungen
- Titulación de Ácidos PolipróticosDokument14 SeitenTitulación de Ácidos PolipróticosRIVERA LOZANO ENRIQUE ULISESNoch keine Bewertungen
- Informe 5, Propiedades de Los Aldehidos y CetonasDokument8 SeitenInforme 5, Propiedades de Los Aldehidos y CetonasDani SantoyoNoch keine Bewertungen
- El HCL Concentrado Tiene Las Siguientes CaracterísticasDokument1 SeiteEl HCL Concentrado Tiene Las Siguientes CaracterísticasOriana Salas100% (1)
- Informe 1 - 4° SemestreDokument7 SeitenInforme 1 - 4° SemestreJohan Lf CalderonNoch keine Bewertungen
- Informe Inorganica II Prectica Complejos Octaedricos CorregidoDokument9 SeitenInforme Inorganica II Prectica Complejos Octaedricos Corregidozaira aguirre100% (1)
- Practica 1 CromoDokument3 SeitenPractica 1 CromoFercho Rojas RamosNoch keine Bewertungen
- Informe de Alquinos PDFDokument7 SeitenInforme de Alquinos PDFJunnior Alejandro AcostaNoch keine Bewertungen
- TP5 QO1 2019 - Obtención de Cloruro de Ter-ButiloDokument3 SeitenTP5 QO1 2019 - Obtención de Cloruro de Ter-ButiloMaia IacobucciNoch keine Bewertungen
- Practica 3 Fermentacion EtanolicaDokument6 SeitenPractica 3 Fermentacion EtanolicaVanessa RomeroNoch keine Bewertungen
- Alcoholes y FenolesDokument8 SeitenAlcoholes y FenolesJHONIER ANDRES TORRES URREANoch keine Bewertungen
- Obtencion de Etileno PDFDokument18 SeitenObtencion de Etileno PDFLuis Navarro100% (1)
- Practica 6 Preparacion Del Ciclohexeno Laboratorio de Quimica de Los HidrocarburosDokument5 SeitenPractica 6 Preparacion Del Ciclohexeno Laboratorio de Quimica de Los HidrocarburosJAVIER GutierrezNoch keine Bewertungen
- Informe Practica 1 Química AnalíticaDokument9 SeitenInforme Practica 1 Química AnalíticaAdolfo VillaquiránNoch keine Bewertungen
- Sal de AlumbreDokument5 SeitenSal de AlumbreLAURA ALEJANDRA LOPEZ ERAZONoch keine Bewertungen
- Determinacion de Cloruros en Aguas de PozosDokument12 SeitenDeterminacion de Cloruros en Aguas de PozosAlexander García GarcíaNoch keine Bewertungen
- AlcoholesDokument8 SeitenAlcoholesNathaly GarciaNoch keine Bewertungen
- Valoraciones Ácido-BaseDokument4 SeitenValoraciones Ácido-BaseMICHELLE ALEJANDRA RAMIREZ SUAREZNoch keine Bewertungen
- PRÁCTICA N°1 Obtencion Del HidrogenoDokument3 SeitenPRÁCTICA N°1 Obtencion Del HidrogenoRodrigo MamaniNoch keine Bewertungen
- Valoracion RedoxDokument9 SeitenValoracion RedoxAlejandra MinganNoch keine Bewertungen
- VALORACION-REDOX Del Cloro ActivoDokument9 SeitenVALORACION-REDOX Del Cloro ActivoRamon LopezNoch keine Bewertungen
- 0 TercbutiloDokument3 Seiten0 TercbutiloLeonardo ReyesNoch keine Bewertungen
- Metano YacetilenoDokument4 SeitenMetano YacetilenoLeonardo ReyesNoch keine Bewertungen
- Fpi12 MovilidadDokument1 SeiteFpi12 MovilidadLeonardo ReyesNoch keine Bewertungen
- Trabajo de ÈticaDokument1 SeiteTrabajo de ÈticaLeonardo ReyesNoch keine Bewertungen
- Reglamento UPADokument41 SeitenReglamento UPAEdilberto Estevez TroncosoNoch keine Bewertungen
- QmetriaDokument8 SeitenQmetriaLeonardo ReyesNoch keine Bewertungen
- Taller Metodologia Superficie de RespuestaDokument4 SeitenTaller Metodologia Superficie de RespuestaLeonardo ReyesNoch keine Bewertungen
- Estadistica DescriptivaDokument13 SeitenEstadistica DescriptivaLeonardo ReyesNoch keine Bewertungen
- Entregable 1Dokument3 SeitenEntregable 1Leonardo ReyesNoch keine Bewertungen
- Diseño de ProcesosDokument43 SeitenDiseño de ProcesosLeonardo ReyesNoch keine Bewertungen
- Exposición 3Dokument7 SeitenExposición 3Leonardo ReyesNoch keine Bewertungen
- Clase No. 1Dokument26 SeitenClase No. 1Leonardo ReyesNoch keine Bewertungen
- Ejercicios Inorgánica IDokument4 SeitenEjercicios Inorgánica ILeonardo ReyesNoch keine Bewertungen
- Diagrama de FlujoDokument1 SeiteDiagrama de FlujoLeonardo ReyesNoch keine Bewertungen
- Diagrama de FlujoDokument1 SeiteDiagrama de FlujoLeonardo ReyesNoch keine Bewertungen
- Ensayo 1Dokument2 SeitenEnsayo 1Leonardo ReyesNoch keine Bewertungen
- Espina de PescadoDokument1 SeiteEspina de PescadoLeonardo ReyesNoch keine Bewertungen
- Entregable 3, GuíaDokument4 SeitenEntregable 3, GuíaLeonardo ReyesNoch keine Bewertungen
- Digrama de ParetoDokument3 SeitenDigrama de ParetoLeonardo ReyesNoch keine Bewertungen
- 2CT2Dokument3 Seiten2CT2Leonardo ReyesNoch keine Bewertungen
- Entregable 2Dokument2 SeitenEntregable 2Leonardo ReyesNoch keine Bewertungen
- Exposición Inorgánica II FinalDokument16 SeitenExposición Inorgánica II FinalLeonardo ReyesNoch keine Bewertungen
- 2 Parcial 2020-02 Leonardo Steyman Reyes FernándezDokument3 Seiten2 Parcial 2020-02 Leonardo Steyman Reyes FernándezLeonardo ReyesNoch keine Bewertungen
- Trabajo - Estandarización de Soluciones y Titulación Solución BufferDokument3 SeitenTrabajo - Estandarización de Soluciones y Titulación Solución BufferLeonardo ReyesNoch keine Bewertungen
- Segundo Taller Del Primer CorteDokument2 SeitenSegundo Taller Del Primer CorteLeonardo ReyesNoch keine Bewertungen
- 2CT1Dokument7 Seiten2CT1Leonardo ReyesNoch keine Bewertungen
- Punto 5 DEC 2cDokument6 SeitenPunto 5 DEC 2cLeonardo ReyesNoch keine Bewertungen
- Nombre: - CodDokument1 SeiteNombre: - CodLeonardo ReyesNoch keine Bewertungen
- Ensayo BIOLOGIADokument7 SeitenEnsayo BIOLOGIALeonardo ReyesNoch keine Bewertungen
- Poster WYLDokument1 SeitePoster WYLLeonardo ReyesNoch keine Bewertungen
- Trabajo Final de Psicologia Del AprendizajeDokument12 SeitenTrabajo Final de Psicologia Del AprendizajeFanny Ramirez RodriguezNoch keine Bewertungen
- Taller 2. Método Algebraico, Simplex, Dos Fases y Gran M - COMPLETO PDFDokument9 SeitenTaller 2. Método Algebraico, Simplex, Dos Fases y Gran M - COMPLETO PDFJavier VilladaNoch keine Bewertungen
- Chapter 7 - Enzymatic Quorum Quenching in Biofilms - 2019 - Quorum SensingDokument21 SeitenChapter 7 - Enzymatic Quorum Quenching in Biofilms - 2019 - Quorum SensingFrancelia Quiñonez RuvalcabaNoch keine Bewertungen
- Metrado Tuberia Desague PVCDokument4 SeitenMetrado Tuberia Desague PVCJHonHuberthCalderonAguilarNoch keine Bewertungen
- Modelo Plan de Mejora de Los Aprendizajes 2021Dokument6 SeitenModelo Plan de Mejora de Los Aprendizajes 2021Freddy MezaNoch keine Bewertungen
- El Exceso en Las Causas de JustificacionDokument108 SeitenEl Exceso en Las Causas de JustificacionErik Manuel Vasquez LlerenaNoch keine Bewertungen
- Da Proceso 16-1-159290 124002002 21317235 PDFDokument7 SeitenDa Proceso 16-1-159290 124002002 21317235 PDFCarolina Torres HerreraNoch keine Bewertungen
- Flac 3DDokument20 SeitenFlac 3DBrandon LaricoNoch keine Bewertungen
- Matriz de AbastecimientosDokument5 SeitenMatriz de AbastecimientosRoberto Perez MartinezNoch keine Bewertungen
- Leccion Libro Sin Palabras Color DoradoDokument6 SeitenLeccion Libro Sin Palabras Color DoradoAlejandro Manuel Gajardo FuentesNoch keine Bewertungen
- Lillie - Lylia - WikiDex, La Enciclopedia PokémonDokument79 SeitenLillie - Lylia - WikiDex, La Enciclopedia PokémonSidajiNoch keine Bewertungen
- EWAN PTAct 7 2 8-InstructorDokument4 SeitenEWAN PTAct 7 2 8-InstructorlinkeanNoch keine Bewertungen
- D1 A1 SESION COM. Escribimos RimasDokument7 SeitenD1 A1 SESION COM. Escribimos Rimaszoila sanchez anayhuamanNoch keine Bewertungen
- Un Caso AisladoDokument41 SeitenUn Caso AisladoInmobiliaria Pilares Sociedad AnónimaNoch keine Bewertungen
- Informe Especies MayoresDokument24 SeitenInforme Especies MayoresAlvaro ATNoch keine Bewertungen
- 2006-El Ciudadano Televisivo. Estudio Sobre La Construcción Discursiva de La Ciudadanía en Noticieros Televisivos Nacionales de Argentina y ChileDokument114 Seiten2006-El Ciudadano Televisivo. Estudio Sobre La Construcción Discursiva de La Ciudadanía en Noticieros Televisivos Nacionales de Argentina y ChileUNRComNoch keine Bewertungen
- Tailandia Ficha PaisDokument10 SeitenTailandia Ficha PaisrichradlealNoch keine Bewertungen
- Integrales de MohrDokument20 SeitenIntegrales de MohrBryanReyesMogollonNoch keine Bewertungen
- Las Formas de La Escritura en Chito de Mello y Fabián SeveroDokument23 SeitenLas Formas de La Escritura en Chito de Mello y Fabián SeveroAlejandra Rivero100% (1)
- Cien Mejor Que UnoJames ZurowieckyDokument175 SeitenCien Mejor Que UnoJames ZurowieckyCaio JeandetNoch keine Bewertungen
- Eje 3 Actividad EvaluativaDokument6 SeitenEje 3 Actividad EvaluativaDiego mayorgaNoch keine Bewertungen
- Colapso de La URSS y El Sistema SocialistaDokument7 SeitenColapso de La URSS y El Sistema SocialistaJonathan BenavidesNoch keine Bewertungen
- Proyecto Mi Granja 2007 PDFDokument52 SeitenProyecto Mi Granja 2007 PDFDavid UlcoNoch keine Bewertungen
- Ecuaciones inDokument6 SeitenEcuaciones inyeny espinoza100% (1)
- Tema 3. Comportamiento Estratégico Con Información ImperfectaDokument29 SeitenTema 3. Comportamiento Estratégico Con Información ImperfectaPalm PreNoch keine Bewertungen
- Reserva Natural Las PalmeraDokument2 SeitenReserva Natural Las PalmeraLuis Eduardo Higuera100% (1)
- BiologiaDokument21 SeitenBiologiaBadr AbdounNoch keine Bewertungen
- Contrato Arrendamiento Adicional Ghetto (V. May. 18 J 2021) REV IVAN 24 MAY 2021Dokument13 SeitenContrato Arrendamiento Adicional Ghetto (V. May. 18 J 2021) REV IVAN 24 MAY 2021hectorNoch keine Bewertungen