Beruflich Dokumente
Kultur Dokumente
A - 0760 - Reglamento Sustitutivo Del Reglamento de BPM para Laboratorios Farmacéuticos
Hochgeladen von
LeonardoOriginaltitel
Copyright
Verfügbare Formate
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
Verfügbare Formate
A - 0760 - Reglamento Sustitutivo Del Reglamento de BPM para Laboratorios Farmacéuticos
Hochgeladen von
LeonardoCopyright:
Verfügbare Formate
REGLAMENTO DE BUENAS PRACTICAS PARA
LABORATORIOS FARMACEUTICOS
Acuerdo Ministerial 760
Registro Oficial 359 de 10-ene-2011
Ultima modificación: 08-feb-2013
Estado: Vigente
NOTA GENERAL:
En todo el contenido del Reglamento, sustituir las siguientes frases: "Dirección General de Salud a
través de la Dirección de Control y Mejoramiento en Vigilancia Sanitaria"; "Dirección de Control y
Mejoramiento en Vigilancia Sanitaria"; "Instituto Nacional de Higiene y Medicina Tropical "Dr.
Leopoldo Izquieta Pérez", por la frase: "Agencia Nacional de Regulación, Control y Vigilancia
Sanitaria - ARCSA, o quien ejerza sus competencias".
Dado por Acuerdo Ministerial No. 2881, publicado en Registro Oficial 889 de 8 de Febrero del 2013 .
EL MINISTRO DE SALUD PUBLICA
Considerando:
Que, la Constitución de la República del Ecuador ordena: "Art.- 361. El Estado ejercerá la rectoría del
sistema a través de la autoridad sanitaria nacional, será responsable de formular la política nacional
de salud, y normará, regulará y controlará todas las actividades relacionadas con la salud, así como
el funcionamiento de las entidades del sector";
Que, la Ley Orgánica de Salud manda: "Art. 131. El cumplimiento de las normas de buenas prácticas
de manufactura, almacenamiento, distribución, dispensación y farmacia, será controlado y certificado
por la autoridad sanitaria nacional.";
Que, el Reglamento Sustitutivo de Registro Sanitario para Medicamentos en General expedido
mediante Acuerdo Ministerial No. 00000586 de 27 de octubre del 2010, en el Art. 6 literal c)
establece como requisito para obtener el registro sanitario, el Certificado de Buenas Prácticas de
Manufactura;
Que, mediante Acuerdo Ministerial 4640, publicado en el Registro Oficial No. 486 de 19 de julio de
1994 se expidió la "Norma de Buenas Prácticas de Manufactura", mismo que requiere actualizarse
conforme a los avances de la tecnología farmacéutica;
Que, el Comité de Expertos en Especificaciones para las preparaciones Farmacéuticas de la
Organización Mundial de la Salud, mediante Informe Técnico No. 32 (WHO Serie Informes Técnicos
No. 823), Anexo 1, establece que las Buenas Prácticas de Manufactura constituyen el marco de
referencia internacionalmente adoptado por los países que conforman la Red Panamericana para la
Armonización de la Regulación Farmacéutica (RED PARF) de la cual Ecuador forma parte;
Que, la RED PARF ha establecido la Guía de Verificación de Buenas Prácticas de Manufactura para
la industria farmacéutica, la cual responde a las exigencias del Informe Técnico No. 32 (WHO Serie
de Informes Técnicos de la OMS No. 823), Anexo 1, Buenas Prácticas de Manufactura para la
fabricación de productos farmacéuticos; y,
En ejercicio de las atribuciones legales concedidas por los artículos 151 y 154, numeral 1 de la
Constitución de la República del Ecuador en concordancia con el artículo 17 del Estatuto de
Régimen Jurídico y Administrativo de la Función Ejecutiva.
REGLAMENTO DE BUENAS PRACTICAS PARA LABORATORIOS FARMACEUTICOS - Página 1
eSilec Profesional - www.lexis.com.ec
Acuerda:
Expedir el Reglamento Sustitutivo del Reglamento de Buenas Prácticas de Manufactura (BPM) para
laboratorios farmacéuticos.
CAPITULO I
Ambito de aplicación y adopción del Anexo 1 del informe 32
de la OMS y de la Guía de Verificación de Buenas Prácticas
de Manufactura de la RED PARF
Art. 1.- El presente reglamento es de obligatorio cumplimiento para los laboratorios farmacéuticos
instalados en la República del Ecuador que fabriquen, almacenen y maquilen medicamentos, como
producto terminado, semielaborado o acondicionado, en empaque primario o secundario.
Art. 2.- Se adopta oficialmente las normas de Buenas Prácticas de Manufactura de productos
farmacéuticos, informe 32 de la Organización Mundial de la Salud OMS, documento WHO serie
informes técnicos No. 823, Anexo 1, que forma parte indisoluble del presente Reglamento, el cual
será de obligatorio cumplimiento por parte de los laboratorios farmacéuticos.
Art. 3.- Para el procedimiento de inspección de BPM, como documento referencial de trabajo, se
adopta oficialmente la Guía de Verificación de Buenas Prácticas de Manufactura de la Red
Panamericana de Armonización de la Regulación Farmacéutica, (RED PARF) que establece criterios
comunes y contiene los principios importantes a considerar en la inspección de un laboratorio
farmacéutico.
CAPITULO II
De la Organización de los Laboratorios Farmacéuticos
Art. 4.- Todo laboratorio farmacéutico deberá tener un representante legal en la persona del Gerente
o Presidente y contar con organización propia que se refleje en organigramas actualizados y
firmado(s) por la(s) persona(s) responsable(s).
Art. 5.- Técnicamente los laboratorios farmacéuticos, deben organizarse de conformidad con la
capacidad física instalada y de acuerdo con las formas farmacéuticas a elaborarse, y debe contar
con un Director Técnico, de profesión químico farmacéutico o bioquímico farmacéutico, quien será
responsable de la coordinación de todas las actividades técnico industriales y de control, así como
de la aplicación de las disposiciones y normas vigentes emitidas por la autoridad sanitaria nacional.
El Director Técnico podrá además ostentar el cargo de Jefe de Producción.
Art. 6.- Además los laboratorios farmacéuticos deberán contar con un Jefe de Producción y un Jefe
de Control de Calidad, cargos que lo ejercerán profesionales Químico Farmacéuticos o Bioquímico
Farmacéuticos.
CAPITULO III
De las Inspecciones y Procedimiento para la Obtención del
Certificado de Buenas Prácticas de Manufactura (BPM)
Art. 7.- La Coordinación del Programa de Buenas Prácticas de Manufactura (BPM) a los
Laboratorios Farmacéuticos, está bajo la responsabilidad de la Dirección General de Salud a través
de la Dirección de Control y Mejoramiento en Vigilancia Sanitaria.
Las inspecciones de BPM serán realizadas por personal técnico idóneo, de profesión Químico
Farmacéutico o Bioquímico Farmacéutico con experiencia en inspecciones de Buenas Prácticas de
Manufactura, pertenecientes a la Agencia Nacional de Regulación, Control y Vigilancia Sanitaria -
ARCSA, o quien ejerza sus competencias; y, eventualmente, cuando el caso lo amerite, podrán
REGLAMENTO DE BUENAS PRACTICAS PARA LABORATORIOS FARMACEUTICOS - Página 2
eSilec Profesional - www.lexis.com.ec
participar como asesores con voz y no con voto, profesionales especializados en áreas afines como:
microbiología, biotecnología, biológicos, oncológicos/citostáticos, gestión ambiental, sistemas de
aire, ingeniería nuclear, entre otros.
Nota: Inciso segundo sustituido por Acuerdo Ministerial No. 2881, publicado en Registro Oficial 889
de 8 de Febrero del 2013 .
Art. 8.- La Dirección de Control y Mejoramiento en Vigilancia Sanitaria establecerá el procedimiento
de inspección, instrumentos y formatos a utilizarse para Certificación de Buenas Prácticas de
Manufactura, debiendo el mismo contemplar la declaración de confidencialidad, imparcialidad de los
inspectores y ausencia de conflicto de intereses.
Art. 9.- Las inspecciones de B.P.M. se realizarán con fines de:
a) Obtener el Certificado de B.P.M. por primera vez;
b) Renovar el Certificado de B.P.M.;
c) Inspecciones de seguimiento o reinspección;
d) Ampliación de áreas específicas; y,
e) Por denuncias.
Art. 10.- Para el permiso de funcionamiento, los laboratorios farmacéuticos nuevos deberán, con
carácter previo, someterse a inspección de BPM al igual que instalaciones nuevas o ampliación de
áreas, antes de iniciar la producción.
Art. 11.- La visita de reinspección se efectuará con el fin de verificar los resultados de las acciones
correctivas a las observaciones determinadas en la inspección anterior; y, se efectuará en el tiempo
determinado por la Comisión en el informe de inspección. Las visitas de seguimiento con el fin de
verificar que los laboratorios farmacéuticos cumplen las normas de BPM, se podrán efectuar durante
el período de vigencia del Certificado.
Si el laboratorio farmacéutico no salva en dos reinspecciones consecutivas las observaciones
generadas durante la inspección inicial, se solicitará la suspensión o cancelación del permiso de
funcionamiento del establecimiento a las instancias correspondientes, hasta que una nueva
inspección demuestre que cumple con las normas de Buenas Prácticas de Manufactura.
Si el laboratorio farmacéutico fuere objeto de cancelación o suspensión del permiso de
funcionamiento, no podrá fabricar ni comercializar los productos elaborados por dicha empresa, y se
solicitará al Instituto Nacional de Higiene y Medicina Tropical "Dr. Leopoldo Izquieta Pérez"
suspendan o cancelen los registros sanitarios de los productos que fabrican, según corresponda.
Nota: Inciso primero sustituido por Acuerdo Ministerial No. 2881, publicado en Registro Oficial 889 de
8 de Febrero del 2013 .
Art. 12.- Para obtener el Certificado de BPM los laboratorios farmacéuticos deberán presentar una
solicitud dirigida a la Dirección de Control y Mejoramiento en Vigilancia Sanitaria conteniendo los
siguientes datos:
1. Nombre o razón social del laboratorio farmacéutico.
2. Dirección del establecimiento.
3. Nombre del representante legal del establecimiento.
4. Nombre del químico farmacéutico o bioquímico farmacéutico responsable técnico del
establecimiento.
A la solicitud deberá adjuntar lo siguiente:
a) Copia del permiso de funcionamiento vigente del establecimiento;
REGLAMENTO DE BUENAS PRACTICAS PARA LABORATORIOS FARMACEUTICOS - Página 3
eSilec Profesional - www.lexis.com.ec
b) Guía de verificación de buenas prácticas de manufactura debidamente llenada en lo que
corresponda a las condiciones de la empresa, declarando de manera expresa su veracidad con la
firma del profesional responsable del laboratorio;
c) Planos de las instalaciones;
d) Lista de medicamentos que elabora la empresa, incluyendo los productos fabricados a terceros,
debiendo constar el nombre, forma farmacéutica, concentración del principio activo, presentación y
número de registro sanitario;
e) Organigramas: General de Producción y de Control de Calidad;
f) Archivo Maestro del Laboratorio Farmacéutico; y,
g) Pago por derecho de servicios de inspecciones y Certificación de Buenas Prácticas de
Manufactura.
Art. 13.- El procedimiento para que los laboratorios farmacéuticos puedan obtener el Certificado de
BPM, será el indicado a continuación:
Ingresar vía electrónica al sistema automatizado para que realice la solicitud, previa obtención de su
clave, y agregar la información solicitada en el formulario de Solicitud de Certificado de BPM.
1. El usuario debe escanear e ingresar en el sistema, todos los documentos adjuntos que se
describen en el Art. 12 del presente Reglamento.
En el término de un día, la Agencia Nacional de Regulación, Control y Vigilancia Sanitaria-ARCSA, o
quien ejerza sus competencias, revisará que la documentación se encuentre completa y que la
información constante en la solicitud sea correcta.
2. Si la documentación no está completa y correcta, vía electrónica se devolverá el trámite al usuario,
indicando los inconvenientes encontrados en su solicitud. El usuario corregirá la solicitud ingresada
de acuerdo a las observaciones recibidas y tendrá un término de ocho (8) días para realizar esta
actividad, antes de que cambie el estado del proceso. En caso de que vuelva a ingresar
erróneamente la solicitud, o no la ingrese en el tiempo establecido, el proceso será cancelado y el
sistema le notificará los motivos de la cancelación.
3. Una vez completa y correcta la documentación, se autorizará el pago de Certificación de BPM. El
sistema notificará al usuario la cantidad a pagar y el plazo para efectuar dicho pago, así como las
formas previstas para el mismo.
4. Una vez que el usuario realiza el pago y éste es verificado por la Agencia Nacional de Regulación,
Control y Vigilancia Sanitaria-ARCSA, o quien ejerza sus competencias, se generará la factura
electrónica en el sistema y se enviará automáticamente al usuario para su impresión.
5. Luego de este proceso, se distribuirá los documentos a la instancia responsable de la revisión, y
en el término de tres (3) días se notificará a la empresa la fecha en que se realizará la inspección
para verificar el cumplimiento de las normas de BPM.
6. La Agencia Nacional de Regulación, Control y Vigilancia Sanitaria - ARCSA, o quien ejerza sus
competencias, establecerá una Comisión Técnica Inspectora conformada por mínimo dos
profesionales Químicos Farmacéuticos o Bioquímicos Farmacéuticos de acuerdo a lo establecido en
el artículo 7 del presente Reglamento; la Comisión realizará las inspecciones de conformidad con el
cronograma elaborado, y evaluará las instalaciones, equipos y documentación del establecimiento.
Si del resultado de la visita se concluye que el establecimiento no cumple con las normas de BPM
vigentes, en la reunión de cierre de la inspección la Comisión informará sobre los incumplimientos o
no conformidades detectados (as).
Luego de realizada la inspección, en el término de diez (10) días, se elaborará el informe de la
misma y si se establece que el establecimiento cumple con las normas de BPM, se emitirá el
Certificado de BPM.
7. El Certificado de BPM será publicado en el sistema informático y se lo dejará disponible para que
el usuario pueda tener acceso a éste, a través de su clave personal.
REGLAMENTO DE BUENAS PRACTICAS PARA LABORATORIOS FARMACEUTICOS - Página 4
eSilec Profesional - www.lexis.com.ec
8. En caso de incumplimiento de las normas de BPM, la Agencia Nacional de Regulación, Control y
Vigilancia Sanitaria - ARCSA, o quien ejerza sus competencias, determinará un plazo para que el
establecimiento farmacéutico implemente las acciones correctivas detalladas en el informe de
inspección, el mismo que se contará a partir de la fecha de emisión y disponibilidad del citado
informe en el sistema.
Este plazo se establecerá en función de las acciones que deba tomar la empresa para corregir las no
conformidades.
Si en dos reinspecciones consecutivas, el establecimiento farmacéutico o salva las observaciones
generadas durante la inspección inicial, se solicitará a las instancias correspondientes la suspensión
o cancelación del Permiso de Funcionamiento del establecimiento, hasta que una nueva inspección
demuestre que cumple con las normas de BPM.
9. Una vez expedido el Certificado de BPM, el expediente con toda la documentación será enviado
automáticamente a la Unidad responsable de realizar la vigilancia y el control del respectivo
establecimiento, para que éste sea incluido dentro de su planificación, a fin de realizar el control de
seguimiento en el momento que lo crea conveniente.
Nota: Artículo sustituido por Acuerdo Ministerial No. 2881, publicado en Registro Oficial 889 de 8 de
Febrero del 2013 .
Art. 14.-
Nota: Artículo derogado por Acuerdo Ministerial No. 2881, publicado en Registro Oficial 889 de 8 de
Febrero del 2013 .
Art. 15.-
Nota: Artículo derogado por Acuerdo Ministerial No. 2881, publicado en Registro Oficial 889 de 8 de
Febrero del 2013 .
Art. 16.- El Certificado de BPM tendrá una vigencia de tres años contados a partir de la fecha de su
concesión.
Art. ...- En el Certificado de BPM deberá constar lo siguiente:
1. Nombre de la Empresa;
2. Areas de fabricación;
3. Tipo de medicamento/s y formas farmacéuticas que elabora;
4. Número de certificado;
5. Dirección del establecimiento;
6. Fecha de emisión y fecha de vigencia del Certificado;
7. Número de permiso de funcionamiento vigente del establecimiento;
8. Nombre del responsable técnico;
9. Nombre del representante legal; y,
10. Firma/s de responsabilidad del/os funcionario/s competente/s de la Agencia Nacional de
Regulación, Control y Vigilancia Sanitaria - ARCSA, o quien ejerza sus competencias.
Nota: Artículo agregado por Acuerdo Ministerial No. 2881, publicado en Registro Oficial 889 de 8 de
Febrero del 2013 .
Art. ...- La renovación del Certificado de BPM se lo realizará por un período igual al de su vigencia,
para lo cual se aplicará el procedimiento establecido para la certificación, mismo que se encuentra
detallado en este Reglamento.
REGLAMENTO DE BUENAS PRACTICAS PARA LABORATORIOS FARMACEUTICOS - Página 5
eSilec Profesional - www.lexis.com.ec
Nota: Artículo agregado por Acuerdo Ministerial No. 2881, publicado en Registro Oficial 889 de 8 de
Febrero del 2013 .
Art. ...- Para reinspecciones y salvar objeciones, la empresa deberá cumplir con los requisitos
descritos en el Art. 12 de este Reglamento, excepto el pago por derecho de servicio de inspección y
Certificación de Buenas Prácticas de Manufactura (literal g); para lo que se aplicará el procedimiento
descrito en el Art. 13.
Nota: Artículo agregado por Acuerdo Ministerial No. 2881, publicado en Registro Oficial 889 de 8 de
Febrero del 2013 .
CAPITULO IV
De los derechos por servicios
Art. 17.- Conforme dispone la Ley Orgánica de Salud en la disposición general primera, los servicios
de control, inspecciones, autorizaciones, permisos, licencias, registros y otros de similar naturaleza
que preste la autoridad sanitaria nacional, satisfarán el pago de derechos de conformidad con los
reglamentos respectivos.
Para efectos de este reglamento se establece, los siguientes derechos por servicios de inspecciones
para la Certificación de Buenas Prácticas de Manufactura:
Por inspección para Certificación de Buenas Prácticas de Manufactura por primera vez y renovación
se requiere la cancelación previa de doce y medio (12,5) Salarios Básicos Unificados del Trabajador
en General vigente a la fecha del pago.
Por inspección para Certificación de Buenas Prácticas de Manufactura para ampliación de áreas se
requiere la cancelación de ocho (8) salarios básicos unificados del trabajador en general vigente a la
fecha del pago.
En el caso de inspección para verificación de cumplimiento de Buenas Prácticas de Manufactura por
denuncia, por seguimiento o reinspección, el laboratorio inspeccionado no deberá cancelar el
derecho por servicio de inspección.
Art. 18.- Los valores recaudados por concepto de derechos de inspecciones para Certificación de
Buenas Prácticas de Manufactura, serán asignados específica y exclusivamente para el
fortalecimiento del programa de BPM y actividades relacionadas como: capacitación, movilización,
transporte entre otros.
CAPITULO V
De las Sanciones
Art. 19.- Los laboratorios farmacéuticos que no cumplan con las normas de Buenas Prácticas de
Manufactura, serán sancionados de conformidad con lo previsto en la Ley Orgánica de Salud y el
presente reglamento, sin perjuicio de las sanciones civiles, administrativas y penales a que hubiere
lugar.
Art. 20.- La Dirección General de Salud dependiendo de la gravedad del incumplimiento podrá:
a) Suspender o cancelar el Certificado de Buenas Prácticas de Manufactura (BPM); y,
b) Solicitar al Instituto Nacional de Higiene y Medicina Tropical "Dr. Leopoldo Izquieta Pérez", la
suspensión o cancelación de los registros sanitarios.
DISPOSICIONES GENERALES
PRIMERA.- Derógase el Reglamento de Buenas Prácticas de Manufactura, expedido mediante
REGLAMENTO DE BUENAS PRACTICAS PARA LABORATORIOS FARMACEUTICOS - Página 6
eSilec Profesional - www.lexis.com.ec
Acuerdo Ministerial No. 4640 publicado en Registro Oficial No. 486 de 19 de julio de 1994 y toda otra
norma de igual o menor jerarquía que se le oponga.
Nota: Denominación de Disposición reformada por Acuerdo Ministerial No. 2881, publicado en
Registro Oficial 889 de 8 de Febrero del 2013 .
SEGUNDA.- Los laboratorios farmacéuticos establecidos en el territorio de la República del Ecuador
que sean sujetos de inspección o auditorías externas conformadas por autoridades de salud de otros
países, deberán notificar y solicitar autorización para la realización de la misma a la Dirección
General de Salud, a fin de que éstas, según el caso, sean acompañadas por inspectores nacionales
de Buenas Prácticas de Manufactura, en calidad de observadores o según corresponda.
Nota: Denominación de Disposición reformada por Acuerdo Ministerial No. 2881, publicado en
Registro Oficial 889 de 8 de Febrero del 2013 .
TERCERA.- Los laboratorios farmacéuticos que dispongan de Certificado de BPM, obtendrán el
permiso de funcionamiento anual automáticamente, presentando como únicos requisitos los
siguientes:
1. El Certificado de BPM vigente;
2. El permiso otorgado por el Cuerpo de Bomberos vigente; y, en el caso del Distrito Metropolitano
de Quito, con la presentación de la Licencia Unica de Actividades Económicas LUAE;
3. El certificado de salud ocupacional vigente, otorgado por un Centro de Salud del Ministerio de
Salud Pública, del personal que labora en el establecimiento.
Para la obtención del permiso de funcionamiento anual, el establecimiento que posea el Certificado
de BPM, no tendrá que cancelar los valores determinados en el Reglamento para Otorgar Permisos
de Funcionamiento a los Establecimientos Sujetos a Vigilancia y Control Sanitario, por considerarse
incluidos en el pago del Certificado de BPM.
Nota: Disposición agregada por Acuerdo Ministerial No. 2881, publicado en Registro Oficial 889 de 8
de Febrero del 2013 .
DISPOSICIONES TRANSITORIAS
PRIMERA.- Al existir laboratorios farmacéuticos que no han ejecutado el Plan Gradual de
Implementación de las normas de BPM presentado en el año 2011, y por consiguiente no han
cumplido con las mismas en el plazo establecido de 18 meses, este Portafolio amplía el mismo por
seis (06) meses adicionales, contados a partir de la suscripción del presente Acuerdo Ministerial, con
el fin de que estos laboratorios cumplan con las normas de BPM y obtengan la Certificación
correspondiente.
Nota: Disposición sustituida por Acuerdo Ministerial No. 2881, publicado en Registro Oficial 889 de 8
de Febrero del 2013 .
SEGUNDA.- Los laboratorios farmacéuticos que elaboran medicamentos en el país, a partir de la
vigencia del presente reglamento, como requisito para obtener el permiso de funcionamiento anual
deberán presentar en la Dirección de Control y Mejoramiento en Vigilancia Sanitaria, el plan gradual
de implementación de las normas de BPM al que se hace referencia en la primera disposición
transitoria.
TERCERA.- Para el caso de las empresas que no dispongan de la autorización de uso de suelo que
otorgan los Municipios, la Agencia Nacional de Regulación, Control y Vigilancia Sanitaria - ARCSA, o
quien ejerza sus competencias, realizará un análisis individual de cada una de ellas y se
determinarán las causas para otorgar o negar una modificación del plazo establecido en este
Acuerdo Ministerial.
REGLAMENTO DE BUENAS PRACTICAS PARA LABORATORIOS FARMACEUTICOS - Página 7
eSilec Profesional - www.lexis.com.ec
Nota: Disposición agregada por Acuerdo Ministerial No. 2881, publicado en Registro Oficial 889 de 8
de Febrero del 2013 .
CUARTA.- Hasta que la Agencia Nacional de Regulación, Control y Vigilancia Sanitaria-ARCSA, o
quien ejerza sus competencias, culmine su proceso de implementación del sistema automatizado,
los requisitos técnicos y legales establecidos en el presente Reglamento para la obtención del
Certificado de BPM, serán ingresados en una carpeta de manera física por los usuarios, requisitos
que estarán debidamente foliados y rubricados por el técnico responsable, y una copia de dichos
documentos escaneados en un CD. De la misma forma se receptarán las solicitudes para
reinspecciones y se retirarán los informes y notificaciones de las inspecciones en la Agencia
Nacional de Regulación, Control y Vigilancia Sanitaria-ARCSA, o quien ejerza sus competencias.
Nota: Disposición agregada por Acuerdo Ministerial No. 2881, publicado en Registro Oficial 889 de 8
de Febrero del 2013 .
QUINTA.- Los establecimientos farmacéuticos que dispongan de áreas para realizar
reacondicionamiento y que dispongan del Certificado de BPM, podrán efectuar las actividades
contempladas en el mencionado Certificado hasta su caducidad, mismo que no será objeto de
renovación.
Nota: Disposición agregada por Acuerdo Ministerial No. 2881, publicado en Registro Oficial 889 de 8
de Febrero del 2013 .
Art. FINAL.- De la ejecución del presente reglamento que entrará en vigencia a partir de su
suscripción sin perjuicio de su publicación en el Registro Oficial, encárguese a la Dirección General
de Salud, a través de la Dirección de Control y Mejoramiento en Vigilancia Sanitaria.
Dado en el Distrito Metropolitano de la ciudad de Quito, a 21 de diciembre del 2010.
f.) Dr. David Chiriboga, Ministro de Salud Pública.
Es fiel copia del documento que consta en el archivo del Proceso de Asesoría Jurídica al que me
remito en caso necesario.- Lo certifico.- Quito, a 21 de diciembre del 2010.- f.) Dra. Nelly Cecilia
Mendoza Orquera, Secretaría General, Ministerio de Salud Pública.
REGLAMENTO DE BUENAS PRACTICAS PARA LABORATORIOS FARMACEUTICOS - Página 8
eSilec Profesional - www.lexis.com.ec
Das könnte Ihnen auch gefallen
- Preparación, transporte y almacenamiento de biocidas y productos fitosanitarios. SEAG0110Von EverandPreparación, transporte y almacenamiento de biocidas y productos fitosanitarios. SEAG0110Noch keine Bewertungen
- Seguridad e Higiene en un obrador de panadería y bollería. INAF0108Von EverandSeguridad e Higiene en un obrador de panadería y bollería. INAF0108Noch keine Bewertungen
- Resolución 1160Dokument4 SeitenResolución 1160johana lopezNoch keine Bewertungen
- Resolucion 1160 2016 PDFDokument128 SeitenResolucion 1160 2016 PDFDavid MontañezNoch keine Bewertungen
- Resolucion 1160 2016 1 59Dokument59 SeitenResolucion 1160 2016 1 59Diamantes Cuenta 1Noch keine Bewertungen
- Resolucionn 1160 de 2016Dokument128 SeitenResolucionn 1160 de 2016fatimaNoch keine Bewertungen
- Resolucion Minsaludps 1160 2016Dokument114 SeitenResolucion Minsaludps 1160 2016euserodriguezNoch keine Bewertungen
- Decreto 919 EXENTO - 09 OCT 2015Dokument2 SeitenDecreto 919 EXENTO - 09 OCT 2015maritzaNoch keine Bewertungen
- Disposición 6967-2022Dokument7 SeitenDisposición 6967-2022piabNoch keine Bewertungen
- 5 E 6osiz 203: T InctDokument51 Seiten5 E 6osiz 203: T InctlufjardNoch keine Bewertungen
- Manual BPM Informe 45 OmsDokument128 SeitenManual BPM Informe 45 OmsAndres Urrego100% (1)
- PreguntasDokument7 SeitenPreguntascpinedaNoch keine Bewertungen
- Resolucion - Minsaludps - 3619 - 2013 BPL Ind Farmaceutica PDFDokument65 SeitenResolucion - Minsaludps - 3619 - 2013 BPL Ind Farmaceutica PDFPOSSDNoch keine Bewertungen
- Resolucion 3619 de 2013Dokument95 SeitenResolucion 3619 de 2013andres zuluagaNoch keine Bewertungen
- Anteproyecto de Reglamento de BPM para Productos CosméticosDokument37 SeitenAnteproyecto de Reglamento de BPM para Productos CosméticosDATTA & QUALITYNoch keine Bewertungen
- IE-B.3.2.3-LF-01 BPM Laboratorios NacionalesDokument1.228 SeitenIE-B.3.2.3-LF-01 BPM Laboratorios NacionalesGuiss LemaNoch keine Bewertungen
- Resolucion 5402 de 2015 - Manual BPM Medicamentos BiologicosDokument43 SeitenResolucion 5402 de 2015 - Manual BPM Medicamentos BiologicosSara SánNoch keine Bewertungen
- 1.guia de BPLRM - 506-2019Dokument45 Seiten1.guia de BPLRM - 506-2019Ricardo Jackichan Barzola LopezNoch keine Bewertungen
- Resolucion Minsaludps 1160 2016Dokument78 SeitenResolucion Minsaludps 1160 2016Alexandra Arroyave BoteroNoch keine Bewertungen
- Decreto 335 Del 8 de Marzo de 2022Dokument8 SeitenDecreto 335 Del 8 de Marzo de 2022EDWIN CALDERONNoch keine Bewertungen
- Disposicion 2819-2004Dokument141 SeitenDisposicion 2819-2004lobosabio5997Noch keine Bewertungen
- REGLAMENTO DEESTABLECIMIENTOS FARMACEUTICOS Modificatoria 2012Dokument8 SeitenREGLAMENTO DEESTABLECIMIENTOS FARMACEUTICOS Modificatoria 2012cocorealNoch keine Bewertungen
- Validation Standard Operating ProceduresDokument20 SeitenValidation Standard Operating ProceduresSANDYNoch keine Bewertungen
- PRESENTACIONHISGTORIADokument22 SeitenPRESENTACIONHISGTORIAMelanie Vélez BasurtoNoch keine Bewertungen
- MEDICAMENTODokument25 SeitenMEDICAMENTOFELINoch keine Bewertungen
- Aspectos Legales en FarmaciaDokument10 SeitenAspectos Legales en FarmaciaBartolome Riveros EcheverreNoch keine Bewertungen
- Permiso BotiquinDokument9 SeitenPermiso BotiquinClaudia Seguel OlivaresNoch keine Bewertungen
- Directiva BPMDokument18 SeitenDirectiva BPMpocampor8607Noch keine Bewertungen
- DS N°009-2015-SaDokument3 SeitenDS N°009-2015-SaMily Qui CaNoch keine Bewertungen
- Resolucion 5402 Del 17 de Diciembre de 2015Dokument43 SeitenResolucion 5402 Del 17 de Diciembre de 2015marcelitaeNoch keine Bewertungen
- Reglamento de BPM Gases MedicinalesDokument22 SeitenReglamento de BPM Gases Medicinalesceelbero79Noch keine Bewertungen
- Norma Técnica 09-2021 V 2 Registro Sanitario OficinalesDokument7 SeitenNorma Técnica 09-2021 V 2 Registro Sanitario OficinalesarbizudanielNoch keine Bewertungen
- RM Reglamento Dirimenciasn1853-2002-Sa - DMDokument7 SeitenRM Reglamento Dirimenciasn1853-2002-Sa - DMEdith PimentelNoch keine Bewertungen
- ANMAT Disposicion 727-2013Dokument34 SeitenANMAT Disposicion 727-2013planeriNoch keine Bewertungen
- Poes-6-Droguerias, Laboratorios Farmacias y BoticasDokument116 SeitenPoes-6-Droguerias, Laboratorios Farmacias y BoticasYanina Mendoza Mestanza0% (1)
- Marco LegalpmDokument7 SeitenMarco LegalpmMaryssNoch keine Bewertungen
- Gaceta Oficial No 38 009 Del 26 - Ago - 2004 BPMDokument58 SeitenGaceta Oficial No 38 009 Del 26 - Ago - 2004 BPMMaria SalinasNoch keine Bewertungen
- Guia Ejemplos Fuentes de Ampliaciones BPXDokument5 SeitenGuia Ejemplos Fuentes de Ampliaciones BPXjefe.calidadNoch keine Bewertungen
- Normativa Técnica Sanitaria para Productos Higiénicos de Uso IndustrialDokument29 SeitenNormativa Técnica Sanitaria para Productos Higiénicos de Uso IndustrialOscar MartínezNoch keine Bewertungen
- Manual Farmacia FarmasaludDokument86 SeitenManual Farmacia FarmasaludRenzo Walther Bustamante Huayta100% (2)
- ManualDokument164 SeitenManualchrystin2009Noch keine Bewertungen
- Disposicion 3266 2013Dokument24 SeitenDisposicion 3266 2013bprzNoch keine Bewertungen
- Reglamento Productos FarmaceuticosDokument70 SeitenReglamento Productos FarmaceuticosLeonardo Serrano CalistoNoch keine Bewertungen
- Grupo A4 - Actividad 3 - Asuntos R.Dokument8 SeitenGrupo A4 - Actividad 3 - Asuntos R.Ana Karen Lopez LozanoNoch keine Bewertungen
- Clase - Seminario LegislacionDokument37 SeitenClase - Seminario LegislacionfarmaciaemergenciavotoNoch keine Bewertungen
- Ejemplo DossierDokument26 SeitenEjemplo DossieryorkNoch keine Bewertungen
- BPM Productos Farmacéuticos DS-021-2018Dokument3 SeitenBPM Productos Farmacéuticos DS-021-2018Jhon Cabezas moranNoch keine Bewertungen
- Evidencia 5 Matriz de ComparacionDokument6 SeitenEvidencia 5 Matriz de Comparacionzuame comunidadNoch keine Bewertungen
- Normatividad de La Atencion FarmaceuticaDokument11 SeitenNormatividad de La Atencion FarmaceuticaLAURA PAOLA RIVERA VILLAMILNoch keine Bewertungen
- 2do TrabajoDokument3 Seiten2do TrabajoFredy FernandezNoch keine Bewertungen
- ANMAT - Regulacion Productos MedicosDokument71 SeitenANMAT - Regulacion Productos MedicosMaximilianoGabrielColazo50% (2)
- Control de procesos y seguridad e higiene. INAV0109Von EverandControl de procesos y seguridad e higiene. INAV0109Noch keine Bewertungen
- Elaboración de curados y salazones cárnicos. INAI0108Von EverandElaboración de curados y salazones cárnicos. INAI0108Noch keine Bewertungen
- Calidad, seguridad y protección ambiental en restauración. HOTR0309Von EverandCalidad, seguridad y protección ambiental en restauración. HOTR0309Noch keine Bewertungen
- Comisión del Codex Alimentarius: Manual de Procedimiento 26 edicionVon EverandComisión del Codex Alimentarius: Manual de Procedimiento 26 edicionNoch keine Bewertungen
- Instalaciones, maquinaria y equipos de la explotación ganadera. AGAP0108Von EverandInstalaciones, maquinaria y equipos de la explotación ganadera. AGAP0108Noch keine Bewertungen
- Mantenimiento correctivo de instalaciones frigoríficas. IMAR0108Von EverandMantenimiento correctivo de instalaciones frigoríficas. IMAR0108Noch keine Bewertungen
- Higiene general en la industria alimentaria. INAQ0108Von EverandHigiene general en la industria alimentaria. INAQ0108Noch keine Bewertungen
- Anexo 011-2015 Final PDFDokument48 SeitenAnexo 011-2015 Final PDFVane VillamarinNoch keine Bewertungen
- BPF Manual de Capacitación para Manipuladores de Alimentos OPAS OMSDokument44 SeitenBPF Manual de Capacitación para Manipuladores de Alimentos OPAS OMSbrunanut100% (3)
- Bpadt Situaciones Q No Deseas EncontrarDokument14 SeitenBpadt Situaciones Q No Deseas EncontrarLeonardoNoch keine Bewertungen
- ARCSA-De-36-2020-MAFG-NTS para Registro Sanitario y BPM de Productos Procesados Naturales de Uso MedicinalDokument34 SeitenARCSA-De-36-2020-MAFG-NTS para Registro Sanitario y BPM de Productos Procesados Naturales de Uso MedicinalLeonardoNoch keine Bewertungen
- Reglamento RecetasDokument48 SeitenReglamento RecetasFernando Vallejo ChoezNoch keine Bewertungen
- Buenas Practica Almacenamiento PDFDokument160 SeitenBuenas Practica Almacenamiento PDFcarmen100% (1)
- Buenas Practica Almacenamiento PDFDokument160 SeitenBuenas Practica Almacenamiento PDFcarmen100% (1)
- Reglamento de Manejo Gases UdeC PDFDokument42 SeitenReglamento de Manejo Gases UdeC PDFXimena TorresNoch keine Bewertungen
- Monografia O2 UPS 38 NF 33Dokument2 SeitenMonografia O2 UPS 38 NF 33LeonardoNoch keine Bewertungen
- Arcsa de 010 2016 GGGDokument6 SeitenArcsa de 010 2016 GGGLeonardoNoch keine Bewertungen
- 33749FT-BOLSA ANTIG - BL IMP 17x17Dokument1 Seite33749FT-BOLSA ANTIG - BL IMP 17x17LeonardoNoch keine Bewertungen
- Nte Inen 811-2Dokument7 SeitenNte Inen 811-2LeonardoNoch keine Bewertungen
- Evolucion de Centrales de MezclasDokument34 SeitenEvolucion de Centrales de MezclasjheisonNoch keine Bewertungen
- Nutricion Emulsiones PDFDokument6 SeitenNutricion Emulsiones PDFGustavo PobleteNoch keine Bewertungen
- GuiavalidacionmetodosanaliticosDokument18 SeitenGuiavalidacionmetodosanaliticossheriffe23Noch keine Bewertungen
- Ley de Comercio Electronico Firmas y Mensajes de DatosDokument17 SeitenLey de Comercio Electronico Firmas y Mensajes de DatosUchihaElkinNoch keine Bewertungen
- Guía de V..Dokument43 SeitenGuía de V..Cesar Sp100% (5)
- A 4872 Reglamento de BPADT para Establecimientos Farmacéuticos PDFDokument18 SeitenA 4872 Reglamento de BPADT para Establecimientos Farmacéuticos PDFErick Lara Yance0% (1)
- Produccion de Oxigeno Metodo PSA PDFDokument56 SeitenProduccion de Oxigeno Metodo PSA PDFAhonny LarpNoch keine Bewertungen
- Aplicativo Firma Ec Parte 4 PDFDokument9 SeitenAplicativo Firma Ec Parte 4 PDFLeonardoNoch keine Bewertungen
- Sustento Legal Parte 2Dokument5 SeitenSustento Legal Parte 2LeonardoNoch keine Bewertungen
- Guia Técnica 1 Validación de Métodos y Determinación de La Incertidumbre de La Medición - 1Dokument70 SeitenGuia Técnica 1 Validación de Métodos y Determinación de La Incertidumbre de La Medición - 1Yoselin Saldivia CasanovaNoch keine Bewertungen
- Manual Usuario FirmaEC PDFDokument34 SeitenManual Usuario FirmaEC PDFLeonardoNoch keine Bewertungen
- Certificado Digital Parte 3Dokument8 SeitenCertificado Digital Parte 3LeonardoNoch keine Bewertungen
- Aplicativo Firma Ec Parte 4Dokument9 SeitenAplicativo Firma Ec Parte 4LeonardoNoch keine Bewertungen
- Ley de Comercio Electronico Firmas y Mensajes de DatosDokument17 SeitenLey de Comercio Electronico Firmas y Mensajes de DatosUchihaElkinNoch keine Bewertungen
- Manual Usuario FirmaEC PDFDokument34 SeitenManual Usuario FirmaEC PDFLeonardoNoch keine Bewertungen
- Miv 19Dokument41 SeitenMiv 19LeonardoNoch keine Bewertungen
- Ley Orgánica de Incentivos para Asociaciones Público PrivadasDokument23 SeitenLey Orgánica de Incentivos para Asociaciones Público PrivadasLeonardoNoch keine Bewertungen
- Contrato de Concesión ComercialDokument11 SeitenContrato de Concesión ComercialJennifer Orellana100% (1)
- Examen Final - Semana 8 - RA - PRIMER BLOQUE-IMPUESTOS DE RENTA - COSTOS Y DEDUCCIONES - (GRUPO3) PDFDokument11 SeitenExamen Final - Semana 8 - RA - PRIMER BLOQUE-IMPUESTOS DE RENTA - COSTOS Y DEDUCCIONES - (GRUPO3) PDFLauraLorenaMarentesNoch keine Bewertungen
- MOFDokument26 SeitenMOFAnyi Romero SebastianNoch keine Bewertungen
- Ordenanza Regulacion de Remisse en Municipio de NecocheaDokument22 SeitenOrdenanza Regulacion de Remisse en Municipio de NecocheaAlfredo BarrosNoch keine Bewertungen
- Palamas MagisterialesDokument44 SeitenPalamas MagisterialesEUSEBHIO666Noch keine Bewertungen
- Anexo 9 - Facilitación PDFDokument61 SeitenAnexo 9 - Facilitación PDFGonzalo Alberto Gonzalez AlcalaNoch keine Bewertungen
- Contrato de Adquisicion de Una Camioneta Hilux 4x4 CDokument5 SeitenContrato de Adquisicion de Una Camioneta Hilux 4x4 CCésar Belisario Gutiérrez ToledoNoch keine Bewertungen
- T Uce 0013 Jur 120Dokument118 SeitenT Uce 0013 Jur 120Andres SalasNoch keine Bewertungen
- Cierre de Faenas MinerasDokument56 SeitenCierre de Faenas MinerasMiguel Sisniegas0% (1)
- Boe A 2018 4694Dokument5 SeitenBoe A 2018 4694LuisJoséCastillaRomeroNoch keine Bewertungen
- Contrato A PruebaDokument6 SeitenContrato A PruebaJoelMontenegro100% (1)
- Servidores PúblicosDokument9 SeitenServidores PúblicosEIBAR FARIDTH GUTIERREZ PEREZNoch keine Bewertungen
- El Contrato TuristicoDokument4 SeitenEl Contrato TuristicomerryNoch keine Bewertungen
- Norma GE 030Dokument8 SeitenNorma GE 030ofdevil l100% (1)
- Bases Cp0372018seal 20180717 141337 417Dokument76 SeitenBases Cp0372018seal 20180717 141337 417TigreAmazonicoNoch keine Bewertungen
- Regla de La CadenaDokument1 SeiteRegla de La CadenaDiego Andres Ramirez0% (1)
- Nom J 467Dokument96 SeitenNom J 467Eliseo NeriNoch keine Bewertungen
- Trabajadoras Del Hogar Ministerio de Trabajo Prom D EmpleoDokument21 SeitenTrabajadoras Del Hogar Ministerio de Trabajo Prom D EmpleoBill Alan Del CastilloNoch keine Bewertungen
- ComplaiceDokument19 SeitenComplaiceJose Gildardo Parra BarcoNoch keine Bewertungen
- Procedimiento de Trabajo SeguroDokument6 SeitenProcedimiento de Trabajo SeguroPablo Renee Alva VillacortaNoch keine Bewertungen
- Acta de Consejo 147Dokument9 SeitenActa de Consejo 147Wilson Jose García MateusNoch keine Bewertungen
- Cuadro ComparativoDokument4 SeitenCuadro ComparativoYency Viviana DIAZ ATEHORTUANoch keine Bewertungen
- Reglamento de Tránsito en Carreteras y PuentesDokument10 SeitenReglamento de Tránsito en Carreteras y PuentesFrancisco LlamasNoch keine Bewertungen
- Contrato de ConcesiónDokument6 SeitenContrato de ConcesiónRonald MunozNoch keine Bewertungen
- Bitácora de ObraDokument36 SeitenBitácora de ObraJesús GkNoch keine Bewertungen
- Concepto de Derecho BancarioDokument3 SeitenConcepto de Derecho BancarioJuan Hernandez FloresNoch keine Bewertungen
- Manual Del Inspector Del TrabajoDokument260 SeitenManual Del Inspector Del TrabajoAnonymous GFXQQQENoch keine Bewertungen
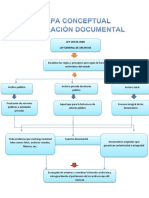
- Mapa Conceptual Legislacion DocumentalDokument2 SeitenMapa Conceptual Legislacion DocumentalClaudia Molano83% (6)
- Régimen Jurídico de La Gestión y Del Control en La Hacienda PúblicaDokument17 SeitenRégimen Jurídico de La Gestión y Del Control en La Hacienda PúblicaMaria Ines Galarza0% (1)
- Rama EjecutivaDokument18 SeitenRama EjecutivaNicolasNoch keine Bewertungen