Beruflich Dokumente
Kultur Dokumente
Cuestionario práctica #2: Solubilidad de compuestos en disolventes
Hochgeladen von
AnelPeña0%(1)0% fanden dieses Dokument nützlich (1 Abstimmung)
290 Ansichten2 SeitenEste documento presenta las respuestas a un cuestionario sobre la solubilidad de un compuesto en diferentes disolventes orgánicos y activos. El compuesto tiene una alta polaridad y es soluble en agua fría, lo que la hace ideal para su recristalización. Pertenece al grupo S1 de solubilidad y es ácido. Aunque la información de solubilidad obtenida de disolventes orgánicos y activos es similar, se logró a diferentes temperaturas. Debido a la toxicidad de algunos disolventes, estos fueron almacen
Originalbeschreibung:
inmunología
Originaltitel
Cuestionario Practica 2
Copyright
© © All Rights Reserved
Verfügbare Formate
DOCX, PDF, TXT oder online auf Scribd lesen
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenEste documento presenta las respuestas a un cuestionario sobre la solubilidad de un compuesto en diferentes disolventes orgánicos y activos. El compuesto tiene una alta polaridad y es soluble en agua fría, lo que la hace ideal para su recristalización. Pertenece al grupo S1 de solubilidad y es ácido. Aunque la información de solubilidad obtenida de disolventes orgánicos y activos es similar, se logró a diferentes temperaturas. Debido a la toxicidad de algunos disolventes, estos fueron almacen
Copyright:
© All Rights Reserved
Verfügbare Formate
Als DOCX, PDF, TXT herunterladen oder online auf Scribd lesen
0%(1)0% fanden dieses Dokument nützlich (1 Abstimmung)
290 Ansichten2 SeitenCuestionario práctica #2: Solubilidad de compuestos en disolventes
Hochgeladen von
AnelPeñaEste documento presenta las respuestas a un cuestionario sobre la solubilidad de un compuesto en diferentes disolventes orgánicos y activos. El compuesto tiene una alta polaridad y es soluble en agua fría, lo que la hace ideal para su recristalización. Pertenece al grupo S1 de solubilidad y es ácido. Aunque la información de solubilidad obtenida de disolventes orgánicos y activos es similar, se logró a diferentes temperaturas. Debido a la toxicidad de algunos disolventes, estos fueron almacen
Copyright:
© All Rights Reserved
Verfügbare Formate
Als DOCX, PDF, TXT herunterladen oder online auf Scribd lesen
Sie sind auf Seite 1von 2
Cuestionario practica #2:
1. Solubilidad en disolventes orgánicos:
a) De acuerdo con las pruebas de solubilidad, ¿Cuál es el grado de
polaridad de su compuesto?
El grado de polaridad de la muestra problema es alto, porque se disolvió con la
mayoría de los reactivos, por la formación de puentes de hidrogeno.
b) ¿Cuándo un disolvente es el ideal para efectuar la recristalización de un
sólido?, explique. En base a su respuesta, ¿Cuál disolvente seleccionaría
para recristalizar su problema?
Cuando no disuelve nuestro compuesto a temperatura ambiente, pero su se
disuelve a temperatura de ebullición y la temperatura de ebullición del
disolvente es menor que la del compuesto a cristalizar.
Tomaría el agua como disolvente por que la solubilidad en frio del compuesto
es baja, lo que nos permite la formación de cristales y la solubilidad en caliente
es alta, para que las impurezas se disuelvan y se pueda purificar.
c) ¿Un sólido que es soluble en determinado disolvente frio, puede ser
recristalizado en dicho disolvente? ¿Por qué?
No puede, a que al cristalizar la sustancia ya no tiene que estar disuelta en el
disolvente se tiene que separar cuando se pone a una temperatura fría. Esto
impide que cristalice ya que esta en lugar de separarse y formar cristales se
disuelve.
d) ¿Un sólido que es insoluble en un disolvente caliente, puede
recristalizarse en él? ¿Por qué?
No es posible porque primero la sustancia se tiene que disolver lo cual se hace
a temperatura caliente para posteriormente pasa a temperatura fría, así se
logra que se separe de su disolvente y cristalice. Al no disolverse no se puede
cristalizar.
2.- Solubilidad en disolventes activos.
a) ¿Qué observa cuando una sustancia es soluble en un disolvente
activo? Y ¿Cuándo no lo es?
Al entrar en contacto el soluto se disuelve al instante y cuando no lo es no
se disuelve.
b) ¿Diga a que grupo de solubilidad es su problema y/o clasifique como
acida, básica o neutra?
Pertenece al grupo S1 (compuestos monofuncionales de bajo peso
molecular) debido a que tienen ácidos carboxílicos y se clasifica como
acido.
c) ¿Explique la razón por la cual no se debe calentar, al realizar las
pruebas en disolventes activos?
Es porque puede provocar una reacción muy intensa y puede llegar a ser
flamable.
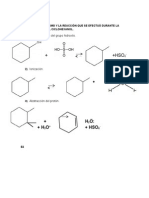
d) Dibuje el diagrama correspondiente a la resolución de su problema.
e) La información obtenida de la solubilidad en disolventes orgánicos,
¿es la misma que la obtenida de la solubilidad en disolventes activos?
Explique de acuerdo a sus resultados.
Si se obtuvo los resultados, los cuales eran lograr que se solubilizaran, sin
embargo, esto se logró a temperaturas diferentes.
f) Consulte la toxicidad de los disolventes utilizados en este
experimento, diga cuál será la mejor manera de desecharlos.
Debido a que algunos de estos son algo tóxicos fueron almacenados en un
recipiente para su posterior tratamiento, y otros desechados en las tarjas.
Das könnte Ihnen auch gefallen
- CristalizacionDokument8 SeitenCristalizacionMonse Gomez RNoch keine Bewertungen
- Laboratorio de Química Orgánica - Cristalización y Recristalización (Juan Pabon)Dokument5 SeitenLaboratorio de Química Orgánica - Cristalización y Recristalización (Juan Pabon)Santiago SanchezNoch keine Bewertungen
- Reacciones de PrecipitaciónDokument4 SeitenReacciones de PrecipitaciónVP LeonelNoch keine Bewertungen
- Informe de Recristalizacion 1.Dokument3 SeitenInforme de Recristalizacion 1.braulio tobarNoch keine Bewertungen
- Cuestionario de Orhánica 3Dokument2 SeitenCuestionario de Orhánica 3Luis CorderoNoch keine Bewertungen
- Síntesis de Bromuro de N-Butilo Por Reacción SN2.Dokument8 SeitenSíntesis de Bromuro de N-Butilo Por Reacción SN2.Glenia ArroyaveNoch keine Bewertungen
- EXTRACCIÓN Simple, Multiple y SelectivaDokument6 SeitenEXTRACCIÓN Simple, Multiple y Selectiva.:("*"BLacK BuLLeT"*"):.100% (8)
- P NitroacetanilidaDokument18 SeitenP NitroacetanilidaAngelo S VelNoch keine Bewertungen
- Informe 1 Pruebas de SolubilidadDokument16 SeitenInforme 1 Pruebas de SolubilidadAndresTobarNoch keine Bewertungen
- Informe 6 Extracción L-L.Dokument20 SeitenInforme 6 Extracción L-L.Maria Del CarmenNoch keine Bewertungen
- Practica2. - Determinacion-Del-Punto-De-EbullicionDokument24 SeitenPractica2. - Determinacion-Del-Punto-De-EbullicionKaren CerdaNoch keine Bewertungen
- Marco Teórico 4 To LABDokument5 SeitenMarco Teórico 4 To LABBruno GonzálezNoch keine Bewertungen
- Informe RecristalizaciónDokument7 SeitenInforme RecristalizaciónJuan Jose HermosaNoch keine Bewertungen
- PRÁCTICA 3. Saponificación de Una GrasaDokument11 SeitenPRÁCTICA 3. Saponificación de Una Grasamaria fernanda moralesNoch keine Bewertungen
- Informe Extraccion Con Disolventes OrganicosDokument8 SeitenInforme Extraccion Con Disolventes Organicosdianis07Noch keine Bewertungen
- Reactivo de LucasDokument1 SeiteReactivo de LucasAnonymous 7HPe30Noch keine Bewertungen
- Info Practica 3. FeSO4 7H2ODokument13 SeitenInfo Practica 3. FeSO4 7H2Onetflix netflixNoch keine Bewertungen
- Epímero (Química)Dokument1 SeiteEpímero (Química)Luisana Isabel DoranteNoch keine Bewertungen
- Practica 5 Naranja IIDokument7 SeitenPractica 5 Naranja IIkarensitogordisNoch keine Bewertungen
- Ácido FenoxiaceticoDokument2 SeitenÁcido FenoxiaceticoGammaCSNoch keine Bewertungen
- Obtención de rojo de metilo mediante acoplamiento de sales de diazonioDokument8 SeitenObtención de rojo de metilo mediante acoplamiento de sales de diazonioErnesto ZavalaNoch keine Bewertungen
- Informe #2 Cristalizacion SimpleDokument14 SeitenInforme #2 Cristalizacion SimpleDaniel BV0% (1)
- Informe Química Orgánica Lab08Dokument29 SeitenInforme Química Orgánica Lab08EccRodoNoch keine Bewertungen
- SecadoDokument5 SeitenSecadoasriel owoNoch keine Bewertungen
- Practica INORGANICA12Dokument13 SeitenPractica INORGANICA12betsy cadena tenorio100% (1)
- El Naranja II Es Un Colorante AzoicoDokument2 SeitenEl Naranja II Es Un Colorante AzoicoMerry MarieNoch keine Bewertungen
- Informe SN2Dokument3 SeitenInforme SN2lorenaNoch keine Bewertungen
- Preparación de Sulfato de Cobre y Sulfito de SodioDokument3 SeitenPreparación de Sulfato de Cobre y Sulfito de SodioMariana Buritica Naranjo100% (1)
- Proyecto CoordinacionDokument16 SeitenProyecto CoordinacionDaniel HernándezNoch keine Bewertungen
- Informe de Quimica de Acidos CarboxilicosDokument4 SeitenInforme de Quimica de Acidos CarboxilicosRamirez JuanNoch keine Bewertungen
- Resultados Práctica 3 Preparación de Sulfato Ferroso HetahidratadoDokument7 SeitenResultados Práctica 3 Preparación de Sulfato Ferroso HetahidratadoLAURA MERCEDES TELLEZ IBA�EZ100% (1)
- Previo 2 Pruebas de Solubilidad en Disolventes OrgánicosDokument4 SeitenPrevio 2 Pruebas de Solubilidad en Disolventes OrgánicosSophie Evans100% (2)
- Síntesis y Caracterización Del Ácido BóricoDokument4 SeitenSíntesis y Caracterización Del Ácido BóricoAlexisCruz100% (1)
- Practica 3 "Cristalización Por Par de Disolventes"Dokument2 SeitenPractica 3 "Cristalización Por Par de Disolventes"Ithalya OlveraNoch keine Bewertungen
- Deshidratación CiclohexanolDokument5 SeitenDeshidratación CiclohexanolDiana Laura Bautista MontejoNoch keine Bewertungen
- Cuestionario 1 DestilacionDokument15 SeitenCuestionario 1 DestilacionLuis Fernando UrionaNoch keine Bewertungen
- Isomeria Cis PracticaDokument9 SeitenIsomeria Cis PracticaVargas Soriano MaRcela100% (1)
- Determinacion de Sulfato Por GravimetriaDokument8 SeitenDeterminacion de Sulfato Por GravimetriaPierina Sulca LoliNoch keine Bewertungen
- Grafica de Solubilidad de KNO3Dokument9 SeitenGrafica de Solubilidad de KNO3Edwin Rodriguez Dzul0% (1)
- Resultados y DiscusionesDokument2 SeitenResultados y Discusioneselvisescorpio95100% (2)
- Diferencia Entre Punto de Equivalencia y Punto FinalDokument2 SeitenDiferencia Entre Punto de Equivalencia y Punto FinalJORDAN100% (1)
- Informe Nº2 SolubilidadDokument9 SeitenInforme Nº2 SolubilidadNatalia Salgado Aviléz89% (9)
- Práctica 5. Preparación de La Sal de MohrDokument3 SeitenPráctica 5. Preparación de La Sal de MohrDaniel Santos GarciaNoch keine Bewertungen
- Practica 3 Cristalización Por Par de DisolventesDokument5 SeitenPractica 3 Cristalización Por Par de DisolventesAnonymous WtLEdM2ioNoch keine Bewertungen
- Metodo de Rast 2Dokument6 SeitenMetodo de Rast 2Mendoza EiraNoch keine Bewertungen
- Anteproyecto Velocidad de ReacciónDokument4 SeitenAnteproyecto Velocidad de ReacciónAlexis Gael Peralta LozanoNoch keine Bewertungen
- Purificación ácido benzóicoDokument5 SeitenPurificación ácido benzóicoWR SalasNoch keine Bewertungen
- Informe Sobre Determinació de Acido Citrico de Jugo de Frutas ComercialDokument7 SeitenInforme Sobre Determinació de Acido Citrico de Jugo de Frutas ComercialCésar Bermúdez50% (4)
- Cuestionario Grupo I Cationes AnaliticaDokument4 SeitenCuestionario Grupo I Cationes AnaliticaIsrael NarvastaNoch keine Bewertungen
- Reporte Cristalizacio - N AcetanilidaDokument4 SeitenReporte Cristalizacio - N AcetanilidaandresNoch keine Bewertungen
- Sintesis Yodo AnilinaDokument4 SeitenSintesis Yodo AnilinaSebastianAntaresNoch keine Bewertungen
- Informe Lab 8 KJHGJDFDokument3 SeitenInforme Lab 8 KJHGJDFMishell BetancourtNoch keine Bewertungen
- LABORATORIO 11 (Complejos)Dokument16 SeitenLABORATORIO 11 (Complejos)jeanette_ih71% (21)
- TP SublimaciónDokument6 SeitenTP Sublimacióntere_figueroa0% (1)
- Informe Inorgánica Quimica Del Grupo 13 Aluminio y Boro 14 de MayoDokument4 SeitenInforme Inorgánica Quimica Del Grupo 13 Aluminio y Boro 14 de MayoPablo AndrésNoch keine Bewertungen
- Taller Estequiometría en GeneralDokument3 SeitenTaller Estequiometría en GeneralnataliaNoch keine Bewertungen
- Informe 7 Labo InorganicaDokument4 SeitenInforme 7 Labo InorganicaDiego Montenegro100% (1)
- Laboratorio de Química Orgánica IDokument2 SeitenLaboratorio de Química Orgánica IragdediasNoch keine Bewertungen
- Cuestionario SolubilidadDokument3 SeitenCuestionario SolubilidadAlejandra CéspedesNoch keine Bewertungen
- Práctica 1 de OrgánicaDokument6 SeitenPráctica 1 de OrgánicaArturo Vargas0% (2)
- Suspensiones OralesDokument19 SeitenSuspensiones OralesAnelPeñaNoch keine Bewertungen
- Análisis compartimental en farmacocinéticaDokument8 SeitenAnálisis compartimental en farmacocinéticaAnel Jareth Peña IndaNoch keine Bewertungen
- Participación 4 Cartas de ControlDokument3 SeitenParticipación 4 Cartas de ControlAnelPeñaNoch keine Bewertungen
- Dengue 2Dokument9 SeitenDengue 2AnelPeñaNoch keine Bewertungen
- El Origen Genético Del Cáncer de MamaDokument15 SeitenEl Origen Genético Del Cáncer de MamaAnelPeñaNoch keine Bewertungen
- Impacto del castor en Tierra del FuegoDokument4 SeitenImpacto del castor en Tierra del FuegoAnelPeñaNoch keine Bewertungen
- Condiciones InsegurasDokument10 SeitenCondiciones InsegurasAnelPeñaNoch keine Bewertungen
- Resumen - Análisis CompartimentalDokument3 SeitenResumen - Análisis CompartimentalAnelPeñaNoch keine Bewertungen
- Participación 4 Cartas de ControlDokument3 SeitenParticipación 4 Cartas de ControlAnelPeñaNoch keine Bewertungen
- Trabajos de GraficasDokument11 SeitenTrabajos de GraficasAnelPeñaNoch keine Bewertungen
- Control AdministracionDokument11 SeitenControl AdministracionAnelPeñaNoch keine Bewertungen
- Trabajos de GraficasDokument11 SeitenTrabajos de GraficasAnelPeñaNoch keine Bewertungen
- Control AdministracionDokument20 SeitenControl AdministracionAnelPeñaNoch keine Bewertungen
- Control AdministracionDokument20 SeitenControl AdministracionAnelPeñaNoch keine Bewertungen
- Reporte BioquimicaDokument4 SeitenReporte BioquimicaAnelPeñaNoch keine Bewertungen
- Miller, G. Tyler CIENCIA-AMBIENTAL-DESARROLLO-SOSTENIBLE 8ed PDFDokument385 SeitenMiller, G. Tyler CIENCIA-AMBIENTAL-DESARROLLO-SOSTENIBLE 8ed PDFJuan Biblio71% (21)
- La Medicina Tradicional en NayaritDokument10 SeitenLa Medicina Tradicional en NayaritAnelPeñaNoch keine Bewertungen
- Contaminación AtmosféricaDokument20 SeitenContaminación AtmosféricaAnelPeñaNoch keine Bewertungen
- Legalización de La MarihuanaDokument5 SeitenLegalización de La MarihuanaAnelPeñaNoch keine Bewertungen
- Calentamiento GlobalDokument7 SeitenCalentamiento GlobalAnelPeña100% (1)
- Nucleótidos de La ZanahoriaDokument1 SeiteNucleótidos de La ZanahoriaAnelPeñaNoch keine Bewertungen
- Calentamiento GlobalDokument7 SeitenCalentamiento GlobalAnelPeña100% (1)
- Medicina TradicionalDokument34 SeitenMedicina TradicionalLuis MorfeNoch keine Bewertungen
- TB TiDokument106 SeitenTB TiAnelPeñaNoch keine Bewertungen
- Resumen de La Paráfrasis de La Fiebre Puerperal Por Ignaz SemmelweisDokument2 SeitenResumen de La Paráfrasis de La Fiebre Puerperal Por Ignaz SemmelweisAnelPeña67% (3)
- Diseno de Estructuras Metalicas Normativa ANSI AISC 360 ASCE 7 10Dokument65 SeitenDiseno de Estructuras Metalicas Normativa ANSI AISC 360 ASCE 7 10Luis R TurnerNoch keine Bewertungen
- Curso AcoplesDokument40 SeitenCurso AcoplespepitoNoch keine Bewertungen
- Diseño de Fundaciones de RiostraDokument9 SeitenDiseño de Fundaciones de Riostraantonio_holguin_2Noch keine Bewertungen
- Paz Rojas, Anderson JavierDokument206 SeitenPaz Rojas, Anderson JavierVictor Peralta CabreraNoch keine Bewertungen
- Diagramas EjemplosDokument16 SeitenDiagramas EjemplossebastianNoch keine Bewertungen
- Inventarios Mapa ConceptualDokument1 SeiteInventarios Mapa ConceptualCamilo Andres Hernández Petro100% (1)
- Diseno Geometrico de CarreterasDokument5 SeitenDiseno Geometrico de CarreterasRaul Madrigal BravoNoch keine Bewertungen
- Ejemplo Plan de Control de Calidad UnifamiliarDokument138 SeitenEjemplo Plan de Control de Calidad UnifamiliarJ Cesar QuispeNoch keine Bewertungen
- Unidad 6.3.Pptx GorditoDokument15 SeitenUnidad 6.3.Pptx GorditoLópez De La Cruz Francisco100% (1)
- Bitacora de Mantenimiento de Maquinaria PesadaDokument403 SeitenBitacora de Mantenimiento de Maquinaria PesadaMauricio FachinNoch keine Bewertungen
- McCormack 4.2Dokument3 SeitenMcCormack 4.2SVGC870Noch keine Bewertungen
- Manual lavadora chata OPPICI LC0450Dokument13 SeitenManual lavadora chata OPPICI LC0450Robert Patricio Medina SarmientoNoch keine Bewertungen
- Vanti CoguaDokument2 SeitenVanti CoguaaliciaNoch keine Bewertungen
- Cartilla Mampostería Confinada PDFDokument68 SeitenCartilla Mampostería Confinada PDFWilmer Alexander Sanchez GomezNoch keine Bewertungen
- Reconocimiento Nitrógeno: Potasio MetálicoDokument21 SeitenReconocimiento Nitrógeno: Potasio MetálicoEdgar Huanca AguilarNoch keine Bewertungen
- Feria de Proyectos - Construcciones en Edificaciones (Columnas) - JoeDokument68 SeitenFeria de Proyectos - Construcciones en Edificaciones (Columnas) - JoeJoe Owen TicahuancaNoch keine Bewertungen
- Memoria Miranda SKATE PARKDokument30 SeitenMemoria Miranda SKATE PARKerikapereira_89Noch keine Bewertungen
- El PlanímetroDokument13 SeitenEl PlanímetroOmar CariNoch keine Bewertungen
- Tipos de Reacciones QuimicasDokument4 SeitenTipos de Reacciones QuimicasSanti AvareceNoch keine Bewertungen
- Fuerzas en El PlanoDokument41 SeitenFuerzas en El PlanoHugo BaldeonNoch keine Bewertungen
- 6 Metodo Esfuerzos PermisiblesDokument29 Seiten6 Metodo Esfuerzos PermisiblesVICTOR ROLANDO CASTRO DEL CARPIONoch keine Bewertungen
- Expresiones Regulares en JSDokument3 SeitenExpresiones Regulares en JSpatNoch keine Bewertungen
- 1er ParcialDokument2 Seiten1er ParcialBerna Aguilar MondragonNoch keine Bewertungen
- Manual de Ingenierias en La EdificacionDokument131 SeitenManual de Ingenierias en La EdificacionJorge Abraham DevoNoch keine Bewertungen
- Plataformas Virtuales de Aprendizaje - TICAPDokument17 SeitenPlataformas Virtuales de Aprendizaje - TICAPTICAPNoch keine Bewertungen
- Simulación de cascada neumática para secuencia A+B+A-BDokument7 SeitenSimulación de cascada neumática para secuencia A+B+A-BAndres SoriaNoch keine Bewertungen
- Room and Pillar Estabilidad de MacizoDokument58 SeitenRoom and Pillar Estabilidad de MacizobenjaminNoch keine Bewertungen
- Síntesis y caracterización de compuestos de coordinación simplesDokument13 SeitenSíntesis y caracterización de compuestos de coordinación simplesyouly xiomara cano correaNoch keine Bewertungen
- Practica 2 El Perfil Del SueloDokument3 SeitenPractica 2 El Perfil Del SueloPablo Muñoz CastellanosNoch keine Bewertungen
- Clasificacion de PavimentosDokument4 SeitenClasificacion de PavimentosmoisesNoch keine Bewertungen