Beruflich Dokumente
Kultur Dokumente
Evaluación
Hochgeladen von
Marcos Jimvel0 Bewertungen0% fanden dieses Dokument nützlich (0 Abstimmungen)
8 Ansichten3 SeitenQuímica general
Copyright
© © All Rights Reserved
Verfügbare Formate
DOCX, PDF, TXT oder online auf Scribd lesen
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenQuímica general
Copyright:
© All Rights Reserved
Verfügbare Formate
Als DOCX, PDF, TXT herunterladen oder online auf Scribd lesen
0 Bewertungen0% fanden dieses Dokument nützlich (0 Abstimmungen)
8 Ansichten3 SeitenEvaluación
Hochgeladen von
Marcos JimvelQuímica general
Copyright:
© All Rights Reserved
Verfügbare Formate
Als DOCX, PDF, TXT herunterladen oder online auf Scribd lesen
Sie sind auf Seite 1von 3
Evaluación: Química I, “Teoría atómica y cuántica”.
Nombre__________________________________________ 2° semestre, grupo ________
Subraya o responde cada inciso, según el caso.
1.- Establece que los elementos se pueden combinar en más de un conjunto de proporciones, y
cada conjunto corresponde a un compuesto diferente:
a) Continuidad de la materia. b) Ley de proporciones múltiples. c) Ley de proporciones definidas.
d) Ley de la conservación de la materia.
2.- Haz luminoso descubierto por Eugen Goldstein que le permitió descubrir el protón:
a) Rayos alfa. b) Rayos canales. c) Cuanto. d) Rayos catódicos.
3.- Es el rayo propio de la radiación de los elementos radiactivos, el cual está cargado doblemente
positivo y que permitió el descubrimiento del núcleo atómico y del neutrón:
a) Rayos alfa. b) Rayos beta. c) Rayos Gamma. d) Rayos canales.
4.- Se define como la cantidad de energía necesaria que requiere o emite un electrón para pasar
de un nivel energético a otro (órbita):
a) Coulombio. b) Unidad de masa atómica. c) Cuanto. d) Radiactividad.
5.- Cuando los electrones de un átomo no se encuentran en sus niveles más bajos de energía
decimos que está en:
a) Reposo. b) Estado excitado. c) Estado basal. d) Discontinuidad.
6.- Relaciona las características con el modelo atómico correspondiente:
Características Modelo atómico
a) Representa al núcleo, en el cual se encuentra la carga positiva
del átomo y a su alrededor se posicionan los electrones ( ) Modelo de Rutherford.
formando una nube, nube electrónica.
b) Representa el núcleo, incluyendo en él las partículas
subatómicas correspondientes (protones y neutrones) y,
( ) Modelo de Thomsom.
posteriormente distribuye los electrones en niveles
energéticos (órbitas).
c) Se representa mediante un círculo de masa positiva, en el cual
( ) Modelo de Dirac–Jordan.
se encuentran los electrones inmersos distribuidos de forma
( ) Modelo de Bohr.
7.- Representa el átomo de aluminio mediante el modelo de Bohr y el modelo de Thomsom,
incluye los cálculos realizados para lograrlo.
Evaluación: Química I, “Teoría atómica y cuántica”.
Nombre__________________________________________ 2° semestre, grupo ________
Subraya o responde cada inciso, según el caso.
1.- Establece que los elementos se pueden combinar en más de un conjunto de proporciones, y
cada conjunto corresponde a un compuesto diferente:
a) Continuidad de la materia. b) Ley de proporciones múltiples. c) Ley de proporciones definidas.
d) Ley de la conservación de la materia.
2.- Haz luminoso descubierto por Eugen Goldstein que le permitió descubrir el protón:
a) Rayos alfa. b) Rayos canales. c) Cuanto. d) Rayos catódicos.
3.- Es el rayo propio de la radiación de los elementos radiactivos, el cual está cargado doblemente
positivo y que permitió el descubrimiento del núcleo atómico y del neutrón:
a) Rayos alfa. b) Rayos beta. c) Rayos Gamma. d) Rayos canales.
4.- Se define como la cantidad de energía necesaria que requiere o emite un electrón para pasar
de un nivel energético a otro (órbita):
a) Coulombio. b) Unidad de masa atómica. c) Cuanto. d) Radiactividad.
5.- Cuando los electrones de un átomo no se encuentran en sus niveles más bajos de energía
decimos que está en:
a) Reposo. b) Estado excitado. c) Estado basal. d) Discontinuidad.
6.- Relaciona las características con el modelo atómico correspondiente:
Características Modelo atómico
a) Representa al núcleo, en el cual se encuentra la carga positiva
del átomo y a su alrededor se posicionan los electrones ( ) Modelo de Rutherford.
formando una nube, nube electrónica.
b) Representa el núcleo, incluyendo en él las partículas
subatómicas correspondientes (protones y neutrones) y,
( ) Modelo de Thomsom.
posteriormente distribuye los electrones en niveles
energéticos (órbitas).
c) Se representa mediante un círculo de masa positiva, en el cual
( ) Modelo de Dirac–Jordan.
se encuentran los electrones inmersos distribuidos de forma
d) Este modelo representa los niveles energéticos de un átomo
mediante los subniveles y estos a su vez mediante sus
( ) Modelo de Bohr.
orbitales, el núcleo es representado únicamente por un
círculo.
7.- Representa el átomo de aluminio mediante el modelo de Bohr.
8.- Es la región de espacio que rodea al núcleo de un átomo, en la que existe una alta posibilidad
de hallar un máximo de dos electrones.
a) Principio de incertidumbre. b) Número cuántico principal. c) Nivel energético.
d) Orbital.
9.- En un subnivel de tipo “p”, ¿Qué valores toma el número cuántico m? Realiza el cálculo y
representa estos de forma gráficas.
10.- ¿Cuántos electrones caben en el subnivel “p”? Explica el porqué con base en las preguntas
anteriores.
11.- Define la configuración electrónica:
Das könnte Ihnen auch gefallen
- Cuestionario Ingeniería de CostosDokument7 SeitenCuestionario Ingeniería de CostosMarcos JimvelNoch keine Bewertungen
- Práctica de Análisis para La LecheDokument14 SeitenPráctica de Análisis para La LecheMarcos Jimvel0% (1)
- Práctica de Análisis para La LecheDokument14 SeitenPráctica de Análisis para La LecheMarcos Jimvel0% (1)
- Sistemas Contra IncendiosDokument11 SeitenSistemas Contra IncendiosAle RamosNoch keine Bewertungen
- Holman Solucionario MultidiDokument50 SeitenHolman Solucionario MultidiOlfer Claros63% (19)
- Cuadro SinópticoDokument3 SeitenCuadro SinópticoMarcos Jimvel100% (2)
- Caida de Presión en Lechos EmpacadosDokument3 SeitenCaida de Presión en Lechos EmpacadosMarcos Jimvel100% (1)
- Repaso Balanceo de Ecuaciones QuímicasDokument2 SeitenRepaso Balanceo de Ecuaciones QuímicasSaraNoch keine Bewertungen
- NomenclaturaDokument6 SeitenNomenclaturaMarcos JimvelNoch keine Bewertungen
- Tecnología de SalsasDokument17 SeitenTecnología de SalsasMarcos JimvelNoch keine Bewertungen
- Secado por aspersión de lecheDokument8 SeitenSecado por aspersión de lecheMarcos JimvelNoch keine Bewertungen
- Aceite de MangoDokument28 SeitenAceite de MangoMarcos Jimvel75% (4)
- Protocolo de Investigación.Dokument27 SeitenProtocolo de Investigación.Marcos JimvelNoch keine Bewertungen
- Lugar de Circulación de Los FluidosDokument3 SeitenLugar de Circulación de Los FluidosMarcos JimvelNoch keine Bewertungen
- FisicoquímicaDokument25 SeitenFisicoquímicaMarcos JimvelNoch keine Bewertungen
- Aplicaciones de Los EmpaquesDokument1 SeiteAplicaciones de Los EmpaquesMarcos JimvelNoch keine Bewertungen
- CristalizadoresDokument8 SeitenCristalizadoresMarcos JimvelNoch keine Bewertungen
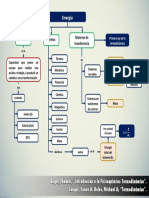
- EnergíaDokument1 SeiteEnergíaMarcos JimvelNoch keine Bewertungen
- Servicios AmbientalesDokument2 SeitenServicios AmbientalesMarcos JimvelNoch keine Bewertungen
- La Historia de Las CosasDokument2 SeitenLa Historia de Las CosasMarcos JimvelNoch keine Bewertungen
- Análisis SensorialDokument14 SeitenAnálisis SensorialMarcos JimvelNoch keine Bewertungen
- Resumen de TesisDokument4 SeitenResumen de TesisMarcos JimvelNoch keine Bewertungen
- PolímerosDokument2 SeitenPolímerosMarcos JimvelNoch keine Bewertungen
- Cuadro de Tipos de Investigaciones.Dokument2 SeitenCuadro de Tipos de Investigaciones.Marcos JimvelNoch keine Bewertungen
- Determinación humedad alimentosDokument3 SeitenDeterminación humedad alimentosMarcos Jimvel100% (1)
- Descripción de ProcesosDokument2 SeitenDescripción de ProcesosMarcos JimvelNoch keine Bewertungen
- Esterilización de MaterialesDokument13 SeitenEsterilización de MaterialesMarcos JimvelNoch keine Bewertungen
- PotabilizaciónDokument10 SeitenPotabilizaciónMarcos JimvelNoch keine Bewertungen
- Determinación de CT y MADokument3 SeitenDeterminación de CT y MAMarcos JimvelNoch keine Bewertungen
- Trinitrotolueno EnsayoDokument7 SeitenTrinitrotolueno EnsayoMarcos JimvelNoch keine Bewertungen
- Compuestos aromáticos intermediarios químicosDokument1 SeiteCompuestos aromáticos intermediarios químicosMarcos JimvelNoch keine Bewertungen
- Cuestionarios de BiologíaDokument45 SeitenCuestionarios de BiologíaValeryPicoNoch keine Bewertungen
- Agua fría caliente instalacionesDokument64 SeitenAgua fría caliente instalacionesMartín Soriano JuliánNoch keine Bewertungen
- Modelo AtomicoDokument1 SeiteModelo AtomicoFacundo TrocheNoch keine Bewertungen
- Catalogo Convic 60 PDFDokument28 SeitenCatalogo Convic 60 PDFRamon RieraNoch keine Bewertungen
- Herramientas Básicas de La QuímicaDokument2 SeitenHerramientas Básicas de La QuímicaAmy XiomiNoch keine Bewertungen
- Estructura y características del átomoDokument16 SeitenEstructura y características del átomoPedro Rafael Hurtado AlvaradoNoch keine Bewertungen
- Aminoácidos y estructura proteínasDokument8 SeitenAminoácidos y estructura proteínasAlexa MacielNoch keine Bewertungen
- Informe de CraDokument13 SeitenInforme de CraAngie More SolanoNoch keine Bewertungen
- Evidencia Análisis de Caso Productos Químicos en Una Empresa IBIS PALMADokument31 SeitenEvidencia Análisis de Caso Productos Químicos en Una Empresa IBIS PALMAibis palmaNoch keine Bewertungen
- Oxoacidos Presentacion CompletaDokument14 SeitenOxoacidos Presentacion CompletaMarianela Carina PaternoNoch keine Bewertungen
- C Previo4Dokument10 SeitenC Previo4David RodriguezNoch keine Bewertungen
- Historia de La QuímicaDokument10 SeitenHistoria de La QuímicaOmar Tallacagua LaimeNoch keine Bewertungen
- Calor y TrabajoDokument5 SeitenCalor y TrabajoVALERIA SARAY LOPEZ LUNARNoch keine Bewertungen
- Taller de Guía de ToxicologíaDokument15 SeitenTaller de Guía de ToxicologíaLaura Sofia Andrade HerreraNoch keine Bewertungen
- TesisDokument174 SeitenTesisJorgito PazNoch keine Bewertungen
- INSTRUMENTALDokument20 SeitenINSTRUMENTALLisselotte RamirezNoch keine Bewertungen
- Aplicaciones de La Nanotecnología A La Industria de La Construcción - Nuevas Tecnologías y MaterialesDokument11 SeitenAplicaciones de La Nanotecnología A La Industria de La Construcción - Nuevas Tecnologías y Materialespaula posadaNoch keine Bewertungen
- Atacama-Introducciín A La HidrometalurgiaDokument19 SeitenAtacama-Introducciín A La HidrometalurgiaLourdesNoch keine Bewertungen
- Informe Tecnico de Infirmacion QuimicaDokument35 SeitenInforme Tecnico de Infirmacion QuimicagermanNoch keine Bewertungen
- 6004 CartuchosDokument1 Seite6004 CartuchosGleydid AltamarNoch keine Bewertungen
- Ejercicio Resuelto Cu Con EdtaDokument7 SeitenEjercicio Resuelto Cu Con EdtaMarqítos Ü Sánchez FloresNoch keine Bewertungen
- Paper - Estudio Sobre La Disolucion de Fase Sigma en Un Acero Duplex S31803Dokument8 SeitenPaper - Estudio Sobre La Disolucion de Fase Sigma en Un Acero Duplex S31803Elmostro2Noch keine Bewertungen
- Clasificación de procesos de conformado en frío y calienteDokument4 SeitenClasificación de procesos de conformado en frío y calienteFeelipe Hdz.Noch keine Bewertungen
- Hoja de Trabajo Quim IIDokument1 SeiteHoja de Trabajo Quim IIClodoveo MartinezNoch keine Bewertungen
- DiferenciasC3C4plantasDokument5 SeitenDiferenciasC3C4plantasMARIANA MEJIA VERGARANoch keine Bewertungen
- Practica 3Dokument10 SeitenPractica 3caroNoch keine Bewertungen
- Rutinas de diagnóstico para espectrofotómetro UV-VisDokument11 SeitenRutinas de diagnóstico para espectrofotómetro UV-VisLeninNoch keine Bewertungen