Beruflich Dokumente
Kultur Dokumente
Métodos de Rompimiento Celular Y Purificacion Parcial para Extraccion Y Concentracion de La Enzima Tirosinasa de Agaricus Bisporus
Hochgeladen von
María Lisette RamosOriginalbeschreibung:
Originaltitel
Copyright
Verfügbare Formate
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
Verfügbare Formate
Métodos de Rompimiento Celular Y Purificacion Parcial para Extraccion Y Concentracion de La Enzima Tirosinasa de Agaricus Bisporus
Hochgeladen von
María Lisette RamosCopyright:
Verfügbare Formate
VIII CAIQ2015 y 3 JASP
MÉTODOS DE ROMPIMIENTO CELULAR Y PURIFICACION
PARCIAL PARA EXTRACCION Y CONCENTRACION DE LA
ENZIMA TIROSINASA DE AGARICUS BISPORUS
V. P.S dos Santos, C. H. Mendonça, F.C.S.S Mihos, A. G. Torres, K. S. Pereira, A. M.
Salgado
Escola de Química - EQ
(Universidade Federal do Rio de Janeiro – UFRJ)
Av. Horácio Macedo, 2030, Edifício do Centro de Tecnologia, Bloco E.
Cidade Universitária - CEP: 21941-909) Rio de Janeiro – RJ – Brasil
paulassalviano@ufrj.br
Resumen. La enzima tirosinasa cataliza reacciones que son ampliamente
usadas en procesos biotecnológicos, como en bioremediación, biosensores.
Siendo abundantemente encontrada en plantas y microrganismos, la
extracción de la enzima a partir de fuentes alternativas constituye una
opción económicamente ventajosa frente a las enzimas comerciales
purificadas que son aún de alto costo. El macro hongo Agaricus bisporus es
una de las principales fuentes de la enzima tirosinasa intracelular. El
presente trabajo tuvo como objetivos comparar métodos de rompimiento
celular combinados para la extracción de la enzima tirosinasa y métodos de
purificación parcial buscando la concentración del extracto enzimático del
macro hongo Agaricus bisporus. Fueron probados y comparados métodos
combinados de rompimiento celular parcial con solvente acetona, detergente
triton X-100 y congelamiento/descongelamiento y el método de
rompimiento celular total utilizando el congelamiento/descongelamiento con
nitrógeno líquido. La purificación parcial fue realizada por medio de
métodos de precipitación secuencial de proteínas utilizando sal sulfato de
amonio (en los rangos de 0-20%, 20-40%, 40-60% de saturación (w/v)) y
acetona (entre el 20% -125% (v/v) de saturación). La estabilidad de los
extractos bruto y parcialmente purificado fue evaluada durante 96h (25°C,
4°C y -6°C). La permeabilización con acetona resultó en los extractos con
AAIQ Asociación Argentina de Ingenieros Químicos - CSPQ
VII CAIQ 2015 y 2das JASP
menores volúmenes y mayor actividad enzimática, en cuanto a la
precipitación con sulfato de amonio confirió la mayor eficiencia de
recuperación de la actividad enzimática. La mejor temperatura de
almacenamiento fue de -6°C.
Palabras clave: tirosinasa, enzima, intracelular
1. Introducción
El uso de extractos como fuente de enzimas para aplicación en processos
biotecnológicos y una alternativa económicamente ventajosa frente a las enzimas
comerciales (Nagodawithana & Reed 2013). La enzima tirosinase de Agaricus bisporus
es extensamente aplicada en el desarrollo de procesos biotecnológicos, principalmente
en la construcción de biosensores (Faria et al. 2007). Estando ampliamente distribuída
en plantas, animales y microrganismos, la tirosinasa fúngica es intracelular, necesitando,
por lo tanto de un proceso de rompimiento celular total o parcial (permeabilización)
para su extracción (Bridge et al. 2004).
Métodos físicos (sonicación, homogenización, prensado, congelamiento-
descongelamiento), químicos (permeabilización con solventes orgánicos o detergentes)
o combinados acostumbran ser utilizados para la extracción de productos intracelulares.
El extracto crudo contiene diversos contaminantes y fragmentos celulares que pueden
ser removidos por medio de métodos de precipitación de proteínas utilizando sales,
solventes o polímeros. Esta etapa de purificación parcial reduce el volumen de extracto
enzimático, posibilitando el control de la concentración de la enzima de acuerdo con la
aplicación (Harrison et al. 2015).
El objetivo de este trabajo es comparar métodos de rompimiento celular para la
extracción de la enzima tirosinasa y de purificación parcial para la concentración y
estabilización del extracto enzimático del macrohongo Agaricus bisporus, así como la
estabilidad de almacenamiento en diferentes temperaturas.
AAIQ, Asociación Argentina de Ingenieros Químicos - CSPQ
VII CAIQ 2015 y 2das JASP
2. Métodos
2.1. Preparación de las muestras de Agaricus bisporus
Los lotes de setas destinados a los ensayos de rompimiento celular, pasaran por un
proceso de disminución de tamaño de los cuerpos fructíferos, por medio de un
procesamiento manual seguido de la homogeneización de las partículas. Este proceso
busca minimizar la heterogenicidad de los lotes de setas y posibilitar la comparación de
la eficiencia entre los métodos probados. Muestras de masas iguales (500 g) fueron
retiradas aleatoriamente de la muestra principal, para ser utilizadas en todas las
metodologías de rompimiento celular.
2.2. Rompimiento celular a partir de métodos combinados
Permeabilización celular química con solvente (acetona) seguido de
congelamiento e descongelamiento: procedimiento modificado de (Kameda et al.
2006). En una licuadora industrial, fueron triturados 500 g de cuerpos fructíferos de
Agaricus bisporus com 1 L acetona helada. La mezcla fue filtrada a vacío con papel de
filtro Watman n°1. El residuo de seta fue congelado por 24 horas. El residuo de seta fue
resuspenso con 80 mL de tampón fosfato 0,1 M pH 6 y congelado por otras 24 horas. El
residuo fue centrifugado a 4000 rpm por 10 minutos, dos veces consecutivas. El
material flotante obtenido constituye el primer extracto enzimático. Las etapas de re-
suspensión y centrifugación fueron repetidas con el residuo de la primera centrifugación
para la obtención del segundo extracto enzimático. Los extractos fueron mesclados y
almacenados en frascos oscuros en congelador de refrigerador doméstico, a temperatura
abajo de - 6 °C.
Permeabilización con detergente (Triton X-100) seguido de congelamiento y
descongelamiento: 500 g de cuerpos frutificación de Agaricus bisporus, fueron
triturados con solución de Triton X-100 5% (v/v) en tampón fosfato de sódio pH 6.
Posterior a la filtración a vacío el resíduo de seta fue sometido a los mismos
procedimientos de la permeabilización con acetona.
Congelamiento/descongelamiento con nitrógeno líquido: En una caja de unicel de
10 L fueron colocados 500 g de setas y nitrógeno líquido en cantidad suficiente para
AAIQ, Asociación Argentina de Ingenieros Químicos - CSPQ
VII CAIQ 2015 y 2das JASP
cubrir las setas, siendo estos, dejados por 10 minutos. El exceso de nitrógeno líquido fue
retirado y las setas fueron dejadas a temperatura ambiente hasta el total
descongelamiento. Posterior al descongelamiento la masa de setas fue homogeneizada
usando una licuadora industrial y el homogeneizado obtenido, sometido a
centrifugación refrigerada a 4 °C a 4000 rpm durante 10 minutos, siendo este proceso
realizado 2 x. El extracto fue almacenado en frasco obscuro en congelador doméstico a
temperatura abajo de -6°C.
2.3. Métodos de precipitación de proteínas para concentración de los extractos
enzimáticos
Precipitación con sal sulfato de amonio: muestras de extracto enzimático de 50 mL
(558 U/mL) fueron sometidas a precipitación secuencial en los intervalos de 0-20%, 20-
40%, 40-60%, de saturación. La muestra permaneció en baño de hielo, a 0 °C, bajo
agitación por 60-90 minutos. Después fueron centrifugados a 9000 rpm a 2 °C durante
30 minutos. Los precipitados de cada intervalo fueron resuspendidos en 5 mL de
tampón fosfato de sódio pH 6 a temperatura de -6°C.
Precipitación con solvente acetona: muestras del extracto enzimático fueron
sometidas a precipitación secuencial en los intervalos de 20%-125% (v/v) de saturación.
La muestra permaneció en baño de hielo, a 0 °C, sobre agitación por 20 minutos.
Después fue centrífugada a 9000 rpm a 2 °C durante 30 minutos. Los precipitados de
cada intervalo fueron resuspendidos en 5 mL de tampón fosfato de sódio pH 6 a
temperatura de -6°C.
La eficiencia de la precipitación en relación a la concentración de los extractos
enzimáticos, el factor de recuperación, dados fue calculado por la ecuación:
(1)
Donde, FR: factor de recuperación
UTr: actividad total recuperada
Uti : actividad total inicial
AAIQ, Asociación Argentina de Ingenieros Químicos - CSPQ
VII CAIQ 2015 y 2das JASP
2.4. Determinación de la actividad enzimática
La medición de la actividad enzimática de la tirosinasa fue realizada por
determinación espectrofotométrica según el procedimiento adaptado de Campos et al.
(1996). Los extractos fueron diluídos en la proporción de 1:10, en solución tampón de
fosfato de sódio 0.1 M pH 6. En tubos de ensayo de 20 cm fueron agregados 5.5 mL de
la solución del tampón fosfato de sódio 0.2M a pH 6, 1.5 mL de solución de L-tirosina
2.4 mM y 1 mL del extracto enzimático previamente diluído. La mezcla fue agitada en
un agitador vortex por 3s e inmediatamente vertida en cubeta y llevada al
espectrofotometro para análisis, donde la variación de la absorbencia resultante de la
reacción de la enzima del extracto enzimatico con el substrato L-tirosina, fue leida en
280 nm en intervalos de 30 segundos durante 870 s.
Una unidad de actividad enzimática fue definida como siendo la cantidad de enzima
que provoca el aumento de 0.001 en la absorbencia a 280 nm por minuto.
Para el cálculo de la actividad total (U/mL), la siguiente fórmula fue utilizada:
Ecuación (2)
Dónde, Abs1: absorbencia inicial
Abs2: absorbencia final
T1 : tiempo inicial
T2 : tiempo final
DE : Volúmen de solución enzimática
VE : factor de dilución de la solución enzimática
2.5. Determinación de proteínas totales
La concentración de proteínas totales fue determinada mediante el método de
Bradford (1976). La curva de calibración y análisis de las muestras de los extractos
siguieron el protocolo de método de reactivo de Bradford (Sigma-Aldrich)(Sigma-
AAIQ, Asociación Argentina de Ingenieros Químicos - CSPQ
VII CAIQ 2015 y 2das JASP
Aldrich 2013). A partir de soluciones padrón de BSA (albumina de suero bovino) (0.1-
1.4 mg/mL), se construyó una curva analítica sumándose 3 mL del reactivo de Bradford
(Sigma-Aldrich) a 0.1 mL de las soluciones padrón de proteína en tubos de ensayo que
fueron agitados en un vórtex. Pasados 10 minutos de reacción las muestras padrón
fueron llevadas a lectura en espectrofotómetro a 595 nm (Fentom X 800).
Después de la construcción de la curva analítica, una alícuota de 0.1 mL de los
extractos enzimáticos, previamente diluída 1:10, en tampón fosfato de sódio pH 6, fue
adicionada a un tubo de ensayo conteniendo 3 mL do reactivo de Bradford y llevada a
lectura en espectrofotómetro después de 10 minutos de reacción.
El cálculo do concentración de proteínas fue hecho en base a la ecuación de la
reta de la curva de calibración linear:
Ecuación (3)
Donde, [P]: concentración de proteínas
Abs: absorbencia
FD: factor de dilución
a e b: constantes da ecuación de la recta
2.6. Estabilidad de almacenamiento en relación a temperatura
La actividad enzimática de los extractos bruto y parcialmente purificados fue
evaluada en 3 temperaturas de almacenamiento: 25°C, 4°C e -6°C, durante 96 horas a
cada 24 horas.
3 Resultados y discusión
3.1. Rompimiento celular: actividad enzimática y concentración de proteínas de los
extractos
La tabla 1 presenta las actividades enzimáticas y las concentraciones de proteínas de
los extractos, resultantes de las extracciones utilizando los métodos de rompimiento
AAIQ, Asociación Argentina de Ingenieros Químicos - CSPQ
VII CAIQ 2015 y 2das JASP
celular, químicos con solventes acetona y el detergente Triton-X100, ambos seguidos de
congelamiento/descongelamiento y físico, con congelamiento/descongelamiento
utilizando nitrógeno líquido.
Tabla 1 – Actividad enzimática y concentración de proteínas de los extractos de los
métodos de rompimiento celular.
Método Volúmen (mL) Actividad total (U/mL) Proteínas totales
rompimiento celular (mg/mL)
Permeabilización con
acetona/congelamiento- 90 ±7,1 2363 ± 64,4 0,51 ±0,01
descongelamiento
Permeabilización con
Trito X-
100/congelamiento-
410 ±14,1 169 ± 22,9 0,11 ±0,01
descongelamiento
Congelamiento-
descongelamiento con 230 ±28,3 63 ± 8,8 0,69 ±0,02
N2 líquido
La permeabilización con acetona combinada al congelamiento/descongelamiento
en congelador doméstico, produjo los extractos con mayores actividades enzimáticas y
menores concentraciones de proteínas debido, probablemente al rompimiento celular
parcial ocasionado por la acetona. La permeabilización con detergente Triton X-100
seguida del congelamiento/descongelamiento resultó en extractos con actividades
enzimáticas y concentraciones de proteínas menores que con la acetona, siendo por lo
tanto, menos eficiente.
La extracción por congelamiento/descongelamiento con nitrógeno líquido originó
extractos con actividades enzimáticas menores que con la permeabilización con acetona.
Sin embargo, la concentración de proteínas de esos extractos fue mayor, posiblemente
debido a la presencia de una mayor concentración de fragmentos celulares originados
por el rompimiento celular total debido al drástico congelamiento con nitrógeno líquido.
La permeabilización con acetona permitió el control sobre el volumen y
concentración del extracto producido, una vez que estos están condicionados al volumen
de tampón adicionado en las etapas de resuspensión. Al contrário de la extracción por
AAIQ, Asociación Argentina de Ingenieros Químicos - CSPQ
VII CAIQ 2015 y 2das JASP
congelamiento/descongelamiento con nitrógeno líquido donde el volumen de extracto
depende del agua contenida en los cuerpos fructíferos del macro hongo Agaricus
bisporus, lo que produjo volúmenes de extractos cerca de 2.5x mayores que en la
extracción con acetona, conforme a los resultados de la Tabla 1.
De este modo, la extracción con acetona se mostró más ventajosa, debido a la
producción de extractos con concentraciones menores de fragmentos celulares en
función de un rompimiento celular parcial y por tanto, más selectivo, más allá de la
producción de volúmenes menores de extracto, lo que lleva a una mayor relación de
costo-benefício de la etapa de purificación parcial.
3.2 Purificación parcial: actividad enzimática, concentración de proteínas y
eficiencia de concentración
Los resultados de los métodos de purificación parcial con sulfato de amonio y acetona
están sumarizados en la Tabla 2:
Tabla 2 – Resultados de los métodos de purificación parcial de los extractos enzimáticos
Extracto Actividad total (U/mL) Proteínas totales (mg/mL) FR (%)
Bruto
558 2,27 100
Parcialmente
purificado con
sulfato de 5286 ±75,6 4,5 ±0,06 94,73
amonio
Parcialmente
purificado con 4812 ±149,8 3,8 ±0,08 86,25
acetona
Ambos resultados de purificación parcial con acetona y sulfato de amonio fueron
satisfactorios, teniendo que este último presentó un porcentual mayor de recuperación
de la actividad enzimática con 94,73% de actividad recuperada, además de remover
proteínas contaminantes de alto peso molecular (Scopes 1994).
AAIQ, Asociación Argentina de Ingenieros Químicos - CSPQ
VII CAIQ 2015 y 2das JASP
3.3 Estabilidad de almacenamiento
Los resultados de la estabilidad de los extractos bruto y parcialmente purificado en las
temperaturas de 25°C, 4°C e -6°C, durante 96 horas, pueden ser verificados en los
gráficos 1 y 2.
Gráfico 1- Estabilidad del extracto bruto en período de 96 h.
Gráfico 2 – Estabilidad del extracto parcialmente purificado en período de 96 h.
AAIQ, Asociación Argentina de Ingenieros Químicos - CSPQ
VII CAIQ 2015 y 2das JASP
A temperatura de 25 °C los extractos brutos y parcialmente purificados tuvieron
perdida de cerca de 50% de la actividad pasadas 24h y pérdida total de la actividad en
48 h. A 4 °C los extractos se mantuvieron estables en su actividad por hasta 24h. La
mayor estabilidad de los extractos fue con almacenamiento a -6°C. En temperaturas más
altas, en general, enzimas tienden a sufrir desnutrición debido al desequilibrio entre las
diversas interacciones en su estructura, tales como, puentes de hidrógeno ,
interacciones hidrofóbicas, fuerzas de Van der Vaals y pariamento de íons. En elevadas
concentraciones de sal y bajas temperaturas enzimas pueden ser estabilizadas debido a
inhibición de la acción de proteasas y de la acción bacteriana en consecuencia de la
reducción de la actividad de agua (Gomes et al. 2007).
4. Conclusión
De entre los métodos de extracción de la enzima tirosinasa a partir del macro hongo
Agaricus bisporus, probados, la permeabilización con acetona fue el más eficiente,
resultando en extractos con las mayores actividades enzimáticas, con menor volumen de
extracto, lo que resulta en mejor relación costo benefício para la etapa de precipitación
de proteínas. Los ensayos de purificación parcial indicaron la mayor eficiencia en
términos de actividad recuperada para el método con la sal sulfato de amonio. La mejor
temperatura de almacenamiento fue a -6 °C con poca variación de la actividad total a lo
largo de 96h.
Agradecimientos: Los autores agradecen al CNPq (Conselho Nacional de
Desenvolvimento Científico e Tecnológico) por el apoyo y las becas concedidas.
Referencias Bibliográficas
Bradford, M.M., 1976. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing
the principle of protein-dye binding. Analytical biochemistry, 72, pp.248–54. Available at:
http://www.ncbi.nlm.nih.gov/pubmed/942051 [Accessed November 11, 2013].
Bridge, P.D., Kokubun, T. & Simmonds, M.S.J., 2004. Protein Extraction From Fungi. In P. Cutler, ed. Protein
Purification Protocols. Humana Press, p. 484. Available at:
http://books.google.com/books?id=_wibShTmB5IC&pgis=1 [Accessed March 27, 2014].
AAIQ, Asociación Argentina de Ingenieros Químicos - CSPQ
VII CAIQ 2015 y 2das JASP
Campos, C.F. et al., 1996. Chemical composition, enzyme activity and effect of enzyme inactivation on flavor quality
of green coconut water. Journal of Food Processing and Preservation, 20(6), pp.487–500. Available at:
http://doi.wiley.com/10.1111/j.1745-4549.1996.tb00761.x [Accessed December 3, 2013].
Faria, R.O. de et al., 2007. The Biotechnological Potential of Mushroom Tyrosinases. Food Technology and
Biotechnology, 45(3), pp.287–294.
Gomes, E. et al., 2007. Enzimas termoestáveis: fontes, produção e aplicação industrial. , 30(1), pp.136–145.
Harrison, R.G. et al., 2015. Bioseparations Science and Engineering, Oxford University Press. Available at:
https://books.google.com/books?id=Q5IKBgAAQBAJ&pgis=1 [Accessed May 25, 2015].
Kameda, E., Langone, M.A.P. & Coelho, M.A.Z., 2006. Tyrosinase extract from Agaricus bisporus mushroom and its
in natura tissue for specific phenol removal. Environmental technology, 27(11), pp.1209–15. Available at:
http://www.ncbi.nlm.nih.gov/pubmed/17203602 [Accessed December 3, 2013].
Nagodawithana, T. & Reed, G., 2013. Enzymes in Food Processing, Elsevier. Available at:
https://books.google.com/books?id=RabYBAAAQBAJ&pgis=1 [Accessed March 13, 2015].
Scopes, R.K., 1994. Protein Purification: Principles and Practice , Springer. Available at:
http://books.google.com/books?id=byi_lK0gk6cC&pgis=1 [Accessed December 3, 2013].
Sigma-Aldrich, 2013. Technical bulletin. , pp.3–8.
AAIQ, Asociación Argentina de Ingenieros Químicos - CSPQ
Das könnte Ihnen auch gefallen
- Análisis de Alimentos. Fundamentos y TécnicasVon EverandAnálisis de Alimentos. Fundamentos y TécnicasNoch keine Bewertungen
- For-Tc-040 Registro de Lecturas Transmisores de PresionDokument1 SeiteFor-Tc-040 Registro de Lecturas Transmisores de Presionpedro colllahuazoNoch keine Bewertungen
- Tecnología de las conservas de frutas y vegetales. Segunda parteVon EverandTecnología de las conservas de frutas y vegetales. Segunda parteNoch keine Bewertungen
- Capitulo 2 PsicoacusticaDokument6 SeitenCapitulo 2 PsicoacusticaAdamo O'ByrneNoch keine Bewertungen
- Charla Seguridad en Los OjosDokument2 SeitenCharla Seguridad en Los OjosYANETH SOTONoch keine Bewertungen
- Análisis Granulométrico Por Tamizado Astm D-422Dokument5 SeitenAnálisis Granulométrico Por Tamizado Astm D-422Christian Yvan100% (1)
- Obtencion Enzimatica de Colorante A Partir de PaprikaDokument12 SeitenObtencion Enzimatica de Colorante A Partir de PaprikaSandro Bustamante MunivesNoch keine Bewertungen
- Control de Calidad SubrasantesDokument21 SeitenControl de Calidad SubrasantesCa SoPre100% (1)
- 9 y 25Dokument19 Seiten9 y 25María Lisette Ramos100% (1)
- El cianuro en la minería. Efectos sobre las plantas acuaticasVon EverandEl cianuro en la minería. Efectos sobre las plantas acuaticasNoch keine Bewertungen
- 2010 Matematicas 60 13 PDFDokument30 Seiten2010 Matematicas 60 13 PDFkudasai_sugoiNoch keine Bewertungen
- Biodetergentes Se Prefieren Sobre Los Detergentes Sintéticos Convencionales en Vista de Su Mejor LimpiezaDokument9 SeitenBiodetergentes Se Prefieren Sobre Los Detergentes Sintéticos Convencionales en Vista de Su Mejor LimpiezaJorge Carlos Vazquez SanchezNoch keine Bewertungen
- Yadira, CARACTERIZACIÓN PARCIAL DE UNA LIPASA EXTRACELULAR DE Marinobacter Sp. Empleando La Metodologia de Superficie Respuesta PDFDokument6 SeitenYadira, CARACTERIZACIÓN PARCIAL DE UNA LIPASA EXTRACELULAR DE Marinobacter Sp. Empleando La Metodologia de Superficie Respuesta PDFLeonardo Barrios SotoNoch keine Bewertungen
- Optimización de Néctar de Lactosuero Enriquecido Con Zumo de Naranja y Controlado Con Radiación Ultraviolet1Dokument13 SeitenOptimización de Néctar de Lactosuero Enriquecido Con Zumo de Naranja y Controlado Con Radiación Ultraviolet1Kevin Yengle PerezNoch keine Bewertungen
- 4 A Materiales y Métodos MetodologiaDokument11 Seiten4 A Materiales y Métodos MetodologiaKarla Alessandra Miranda VargasNoch keine Bewertungen
- Synadenium GrantiiDokument9 SeitenSynadenium GrantiiJose Roberto Salazar SalazarNoch keine Bewertungen
- Práctica 3. Extracción de Adn BacterianoDokument5 SeitenPráctica 3. Extracción de Adn BacterianoCAMILO ERNESTONoch keine Bewertungen
- 02 Mothe and Reddy 2016 - Production Purification and Characterization-Protease-Bacillus - En.esDokument10 Seiten02 Mothe and Reddy 2016 - Production Purification and Characterization-Protease-Bacillus - En.esArturo PeñablassiNoch keine Bewertungen
- Caracterización Bioquímica de AmiJ33, Una Amilasa de Bacillus Amyloliquefaciens Aislada de Suelos CuDokument22 SeitenCaracterización Bioquímica de AmiJ33, Una Amilasa de Bacillus Amyloliquefaciens Aislada de Suelos CuHanylu AvilaNoch keine Bewertungen
- Datos CompletosDokument11 SeitenDatos CompletosDaniel DelgadoNoch keine Bewertungen
- TECNICAS de Evalución de La Cascarilla de CacaoDokument6 SeitenTECNICAS de Evalución de La Cascarilla de CacaoJhoana Espin LedesmaNoch keine Bewertungen
- RECUPERACIÓN, CONCENTRACIÓN Y PURIFICACIÓN DESUPEROXIDODISMUTASA HUMANA RECOMBINANTE (rhSOD)Dokument12 SeitenRECUPERACIÓN, CONCENTRACIÓN Y PURIFICACIÓN DESUPEROXIDODISMUTASA HUMANA RECOMBINANTE (rhSOD)Fernanda MartinezNoch keine Bewertungen
- Optimización de La Producción de Ácido IndolacéticoDokument33 SeitenOptimización de La Producción de Ácido IndolacéticoErik LiiñanNoch keine Bewertungen
- Extracciòn de Carotenos Del ChileDokument11 SeitenExtracciòn de Carotenos Del ChileLilia Tierrablanca SanchezNoch keine Bewertungen
- DocumentoDokument8 SeitenDocumentoJonathan MatusNoch keine Bewertungen
- Arqueas HalófilasDokument6 SeitenArqueas HalófilasAna0402Noch keine Bewertungen
- Trabajo de Investigación EnzimáticaDokument5 SeitenTrabajo de Investigación EnzimáticaJuan C. RamirezNoch keine Bewertungen
- Guia Laboratorio Inmovilizacion Alfa-AmilasaDokument4 SeitenGuia Laboratorio Inmovilizacion Alfa-AmilasaFAUSTO GABRIEL YEPEZ CALDERONNoch keine Bewertungen
- Prã Ctica 3Dokument5 SeitenPrã Ctica 3Carolina RamírezNoch keine Bewertungen
- BIOTECNOLOGIADokument17 SeitenBIOTECNOLOGIAReynaldo Carlos MendozaNoch keine Bewertungen
- LipasaDokument15 SeitenLipasaPaula RamirezNoch keine Bewertungen
- Antecedentes (Randy)Dokument9 SeitenAntecedentes (Randy)SargentoBobNoch keine Bewertungen
- Trabajo II de Osbel Núñez, Atagua (1) - 0410113159Dokument11 SeitenTrabajo II de Osbel Núñez, Atagua (1) - 0410113159Joyssi LopezNoch keine Bewertungen
- Actifivad en Clase 1 Fi9nalDokument20 SeitenActifivad en Clase 1 Fi9nalSantiStalinNoch keine Bewertungen
- 005 Apaisado Journal 1CAA 2016 2pag Por HojaDokument3 Seiten005 Apaisado Journal 1CAA 2016 2pag Por HojarcabanaNoch keine Bewertungen
- Produccion de Papaina Purificada Liofilizada A Partir de La PapayaDokument10 SeitenProduccion de Papaina Purificada Liofilizada A Partir de La PapayaJa VikiõNoch keine Bewertungen
- Práctica Lab #4 EnzimasDokument4 SeitenPráctica Lab #4 EnzimasSergioNoch keine Bewertungen
- Metabolitos en CoralesDokument9 SeitenMetabolitos en CoraleshaydelbatrinidadNoch keine Bewertungen
- Evaluacion Tres Caracteristicas de La EnzimaDokument8 SeitenEvaluacion Tres Caracteristicas de La EnzimaRafaela AcostaNoch keine Bewertungen
- Metodología EjemploDokument5 SeitenMetodología EjemploYoha GiveNoch keine Bewertungen
- Articulo EspanishDokument11 SeitenArticulo EspanishRICHERSON HAROLD PISCOCHE CHINCHAYNoch keine Bewertungen
- Articulo EspanishDokument7 SeitenArticulo EspanishRICHERSON HAROLD PISCOCHE CHINCHAYNoch keine Bewertungen
- Articulo CarotenoidesDokument15 SeitenArticulo Carotenoidesdmz_92Noch keine Bewertungen
- Ficha Técnica EnzimologíaDokument5 SeitenFicha Técnica EnzimologíaLuz IzaNoch keine Bewertungen
- Selección de Un Hongo Filamentoso Altamente Productor de Amilasas para Ser Usadas en Detergentes BiodegradablesDokument9 SeitenSelección de Un Hongo Filamentoso Altamente Productor de Amilasas para Ser Usadas en Detergentes BiodegradablesMaría Belén VecchioneNoch keine Bewertungen
- Sachapapa Quia de PracticaDokument4 SeitenSachapapa Quia de PracticaCinthya Stefanie Vara ArrateaNoch keine Bewertungen
- Metodologia para La Determinación de La Carga Organica en El BiodigestorDokument2 SeitenMetodologia para La Determinación de La Carga Organica en El BiodigestorJoshua SusanibarNoch keine Bewertungen
- Pruebas de Aislamiento de ADN y Evaluación de Su CalidadDokument34 SeitenPruebas de Aislamiento de ADN y Evaluación de Su Calidadcristian david londoño riverNoch keine Bewertungen
- Enzimas de Uso Industrial - Amilasa y CelulasaDokument5 SeitenEnzimas de Uso Industrial - Amilasa y CelulasaChristian CarreraNoch keine Bewertungen
- 19 - Caracterizacion Molecular PDFDokument7 Seiten19 - Caracterizacion Molecular PDFWendy PeñaNoch keine Bewertungen
- Actividad Antioxidante, Polifenoles Totales Y Contenido de Taninos de Extractos de TaraDokument7 SeitenActividad Antioxidante, Polifenoles Totales Y Contenido de Taninos de Extractos de TaraSharon JimenezNoch keine Bewertungen
- Actividad Antioxidante, Polifenoles Totales Y Contenido de Taninos de Extractos de TaraDokument7 SeitenActividad Antioxidante, Polifenoles Totales Y Contenido de Taninos de Extractos de TaraSharon JimenezNoch keine Bewertungen
- Materiales y ReactivosDokument7 SeitenMateriales y ReactivosLiliana Cruz de JulianNoch keine Bewertungen
- La Yerba Mate Posee Alto Nivel de AntioxidantesDokument12 SeitenLa Yerba Mate Posee Alto Nivel de AntioxidantesmanfenixNoch keine Bewertungen
- Dialnet OptimizacionDeUnProtocoloDeExtraccionDeQuitinaYQui 4320335 PDFDokument7 SeitenDialnet OptimizacionDeUnProtocoloDeExtraccionDeQuitinaYQui 4320335 PDFRenan Gonzalez GutierrezNoch keine Bewertungen
- Investigación de Metabolitos Secundarios Producidos Por Hongos Filamentosos Recuperados de Tucumán y Su Potencial en La IndustriaDokument8 SeitenInvestigación de Metabolitos Secundarios Producidos Por Hongos Filamentosos Recuperados de Tucumán y Su Potencial en La IndustriaTomas5102Noch keine Bewertungen
- Caroteno en Mago de Azúcar ( Mangifera Indica ) Por Medio de LasDokument11 SeitenCaroteno en Mago de Azúcar ( Mangifera Indica ) Por Medio de LasAlfredo Arroyo SanchezNoch keine Bewertungen
- Práctica No. 4 Extracción y Cuantificación de ProteínasDokument4 SeitenPráctica No. 4 Extracción y Cuantificación de ProteínasCyberlosophy BlogNoch keine Bewertungen
- Práctica 2. Extracción de Adn BacterianoDokument4 SeitenPráctica 2. Extracción de Adn BacterianoCristina Fajardo100% (1)
- Cascara Camu Camu Tomate de ArbolDokument8 SeitenCascara Camu Camu Tomate de Arboljamilena817Noch keine Bewertungen
- Protocolo de Micropropagacion de PiñaDokument3 SeitenProtocolo de Micropropagacion de PiñaJulieth RomeroNoch keine Bewertungen
- Trabajo de Aislamiento y Selección de Microorganismos Eymar CorreaDokument6 SeitenTrabajo de Aislamiento y Selección de Microorganismos Eymar CorreaEnrrique Correa ValverdeNoch keine Bewertungen
- Articulo Ambiental (Autoguardado)Dokument5 SeitenArticulo Ambiental (Autoguardado)laurasantos2369Noch keine Bewertungen
- Bioquímica - Informe 3Dokument57 SeitenBioquímica - Informe 3Tizy LynNoch keine Bewertungen
- 11.11 García SenosiainDokument4 Seiten11.11 García SenosiainJORGE PACHECONoch keine Bewertungen
- Aprovechamiento de Las Cascaras de Mango Como Soporte para La Produccion de PolisacaridasasDokument5 SeitenAprovechamiento de Las Cascaras de Mango Como Soporte para La Produccion de PolisacaridasasFabioAGM11Noch keine Bewertungen
- Procesamiento de semen porcino para uso en inseminación artificial: Metabolismo espermático, almacenamiento y control de calidadVon EverandProcesamiento de semen porcino para uso en inseminación artificial: Metabolismo espermático, almacenamiento y control de calidadNoch keine Bewertungen
- Diseño Deber 5Dokument3 SeitenDiseño Deber 5María Lisette RamosNoch keine Bewertungen
- Determinación de PiruvatoDokument4 SeitenDeterminación de PiruvatoMaría Lisette RamosNoch keine Bewertungen
- 1967-Cu-P-2018 Reglamento para La Obtención Del Título de Tercer NivelDokument15 Seiten1967-Cu-P-2018 Reglamento para La Obtención Del Título de Tercer NivelMaría Lisette RamosNoch keine Bewertungen
- Modelo Lineal General: NotasDokument54 SeitenModelo Lineal General: NotasMaría Lisette RamosNoch keine Bewertungen
- Informe de Microbiologia II Estudio de L PDFDokument28 SeitenInforme de Microbiologia II Estudio de L PDFMaría Lisette RamosNoch keine Bewertungen
- Aceite de Sacha InchiDokument4 SeitenAceite de Sacha InchiMaría Lisette RamosNoch keine Bewertungen
- Art 1. Produccion de AcidoDokument18 SeitenArt 1. Produccion de AcidoYuchiruNoch keine Bewertungen
- Familias de Polimerasas AdnDokument218 SeitenFamilias de Polimerasas AdnGreiner Duràn DiazNoch keine Bewertungen
- REACTIVOSDokument2 SeitenREACTIVOSMaría Lisette RamosNoch keine Bewertungen
- Guias PaeDokument2 SeitenGuias PaeKrito Pérez AldasNoch keine Bewertungen
- Taller ExposiciónDokument3 SeitenTaller ExposiciónMaría Lisette RamosNoch keine Bewertungen
- FQ RatasDokument4 SeitenFQ RatasMaría Lisette RamosNoch keine Bewertungen
- Modelo Lineal General: NotasDokument54 SeitenModelo Lineal General: NotasMaría Lisette RamosNoch keine Bewertungen
- BacillusDokument4 SeitenBacillusMaría Lisette RamosNoch keine Bewertungen
- 19-Ramos LisetteDokument6 Seiten19-Ramos LisetteMaría Lisette RamosNoch keine Bewertungen
- 19 Ramos Lisette.Dokument21 Seiten19 Ramos Lisette.María Lisette RamosNoch keine Bewertungen
- Bioquimica, Materiales y MetodosDokument1 SeiteBioquimica, Materiales y MetodosMaría Lisette RamosNoch keine Bewertungen
- El Agar SalmonellaDokument1 SeiteEl Agar SalmonellaMaría Lisette RamosNoch keine Bewertungen
- 5.1 Taller. Calidad y Sus PrincipiosDokument2 Seiten5.1 Taller. Calidad y Sus PrincipiosMaría Lisette RamosNoch keine Bewertungen
- Ciclo Del NitrógenoDokument6 SeitenCiclo Del NitrógenoMaría Lisette RamosNoch keine Bewertungen
- El Agar SalmonellaDokument1 SeiteEl Agar SalmonellaMaría Lisette RamosNoch keine Bewertungen
- Sobrealimentacion en Motores Termicos PDFDokument6 SeitenSobrealimentacion en Motores Termicos PDFAldo AlexanderNoch keine Bewertungen
- 01.06-1 ETR ProblemasDokument48 Seiten01.06-1 ETR ProblemasLuisAlcantaraEstevesNoch keine Bewertungen
- FaewsdxDokument23 SeitenFaewsdxqqNoch keine Bewertungen
- Monturas TelescopioDokument4 SeitenMonturas TelescopioZaleth rocio Villanueva ramosNoch keine Bewertungen
- Evaluación Unidad 3 OkiDokument4 SeitenEvaluación Unidad 3 OkiVerónicaAlejandraAriasRodriguezNoch keine Bewertungen
- Calculos AcometidaDokument16 SeitenCalculos AcometidaFelipe MejiasNoch keine Bewertungen
- Práctica Módulo IIIDokument3 SeitenPráctica Módulo IIIWilliam Beder Sandi ChavezNoch keine Bewertungen
- Guía 1Dokument6 SeitenGuía 1Vania MenaresNoch keine Bewertungen
- Suelos Arcillosos y Susceptibles de Problemas de ExpansiónDokument18 SeitenSuelos Arcillosos y Susceptibles de Problemas de ExpansiónDante NinaNoch keine Bewertungen
- Guía Octavo Periodo 1 PrefísicaDokument5 SeitenGuía Octavo Periodo 1 Prefísicasandramenco institucionalNoch keine Bewertungen
- Yjruedao - Clase - 29 - Convección Natural - Parte 4Dokument14 SeitenYjruedao - Clase - 29 - Convección Natural - Parte 4Jose Daniel Caicedo ManriqueNoch keine Bewertungen
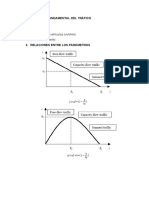
- Ecuación Fundamental Del TráficoDokument5 SeitenEcuación Fundamental Del TráficoPATYNoch keine Bewertungen
- James Clerk Maxwel BiografiaDokument2 SeitenJames Clerk Maxwel BiografiamaryjozeeNoch keine Bewertungen
- Primera Prueba de Avance - Ciencias Naturales - Primer Año de Bachillerato - Praem 2012Dokument15 SeitenPrimera Prueba de Avance - Ciencias Naturales - Primer Año de Bachillerato - Praem 2012Willian CativoNoch keine Bewertungen
- Estudio de Combustion LatenteDokument16 SeitenEstudio de Combustion LatenteVincent EscalaNoch keine Bewertungen
- 3.-Criterios de Gestion de AlmacenDokument56 Seiten3.-Criterios de Gestion de AlmacenKOBRINJA100% (2)
- Abbe5 - ESMANUAL DE USODokument15 SeitenAbbe5 - ESMANUAL DE USOAna Rosa MartinezNoch keine Bewertungen
- VisualizacionesDokument11 SeitenVisualizacionesRoxana VialeNoch keine Bewertungen
- Se Denomina Fuerza ElectromotrizDokument6 SeitenSe Denomina Fuerza ElectromotrizJoseph StamuckNoch keine Bewertungen
- Medición de Flujo de Hidrocarburos. Artículo FinalDokument17 SeitenMedición de Flujo de Hidrocarburos. Artículo FinalOmar David Ochoa RemolinaNoch keine Bewertungen
- John Berger Poemas de EmigracionDokument4 SeitenJohn Berger Poemas de EmigracionBel SalNoch keine Bewertungen
- Difusion de Dopantes para Dispositivos SemiconductoresDokument19 SeitenDifusion de Dopantes para Dispositivos SemiconductoresCarlos Bravo100% (1)
- Guia 1 Am1c23Dokument10 SeitenGuia 1 Am1c23Vieja Chadetu LaconNoch keine Bewertungen
- Guia 3 Estatica Del SolidoDokument11 SeitenGuia 3 Estatica Del SolidoBrayan SNoch keine Bewertungen