Beruflich Dokumente
Kultur Dokumente
Unidad 2 TEST
Hochgeladen von
mtbf2014Copyright
Verfügbare Formate
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
Verfügbare Formate
Unidad 2 TEST
Hochgeladen von
mtbf2014Copyright:
Verfügbare Formate
El enlace químico
02 TEST
Nombre: Fecha:
Apellidos: Curso:
1. Clasifica las siguientes sustancias según su tipo de enlace:
NaCl, HCl, Cl2, Na, CaCl2, Cl2O
2. Ordena las siguientes sustancias por orden creciente de su energía de disociación:
a) O2 > N2 > F2
b) N2 > O2 > F2
c) F2 > O2 > N2
3. Ordena las siguientes sustancias por orden creciente de sus distancias interatómicas:
a) O2 > N2 > F2
b) N2 > O2 > F2
c) F2 > O2 > N2
4. Ordena las siguientes sustancias por orden de polaridad creciente:
a) Cl2 > HCl > NaCl > CCl4
b) HCl> Cl2 > CCl4 >NaCl
c) NaCl> HCl> CCl4> Cl2
d) NaCl >CCl4 > HCl> Cl2
5. ¿Por qué las redes iónicas al golpearlas y tratar de deformarlas se rompen, mientras
que las redes metálicas si pueden deformarse?
6. Ordena las siguientes sustancias por orden creciente de sus puntos de fusión:
a) NaCl > Na>HCl>Cl2
b) Cl2 >Na>HCl> NaCl
c) HCl>Cl2 > Na > NaCl
7. Ordena las siguientes sustancias por orden creciente de sus puntos de fusión:
a) TeH2 > SeH2 > SH2> H2O
b) H2O> TeH2 >SeH2 >SH2
c) H2O> SH2 > SeH2 > TeH2
Química 2.º Bachillerato 1-2
El enlace químico
02 TEST
8. Razona si las siguientes afirmaciones son verdaderas o falsas:
a) Todas las sustancias polares tienen enlaces polares.
b) Todas las sustancias con enlaces polares son polares.
c) Todas las sustancias con enlaces polares y carentes de simetría son polares.
d) Todas las sustancias apolares carecen de enlaces polares.
9. Indica la forma geométrica de las siguientes moléculas:
H2O, NH3, BF3 y BeCl2.
¿Cuáles de las sustancias anteriores son polares?
10. Para las siguientes moléculas: BCl3 , NH3, H2S, y PH3 determina:
a) La geometría de cada molécula según la teoría de la repulsión de pares de electrones de
la capa de valencia.
b) La hibridación que presenta el átomo central en cada una de las moléculas.
c) ¿Cuáles de las moléculas anteriores son polares?
11. Explica razonadamente la conductividad eléctrica de los siguientes sistemas:
a) Un hilo de cobre.
b) Un cristal de Cu (NO3)2.
c) Una disolución de Cu (NO3)2.
Indica un disolvente adecuado para las sustancias anteriores.
12. En función del tipo de enlace explica por qué:
a) El NH3 tiene un punto de ebullición mas alto que el CH4.
b) El KCl tiene un punto de fusión mayor que el Cl2.
c) El CH4 es insoluble en agua y el KCl es soluble.
13. a) Realiza un esquema del ciclo de Born-Habern para el NaCl
b) Calcula la energía reticular del NaCl a partir de los siguientes datos:
Entalpías de sublimación del sodio = 108 KJ/mol.
Energía de disociación del cloro = 243,2 KJ/mol.
Energía de ionización del sodio = 495,7 KJ/mol.
Afinidad electrónica del cloro = -348 KJ/mol.
Entalpía de formación del cloruro de sodio = -401,8 KJ/mol.
14. Define energía reticular. Si las energías de Ionización del NaF es –914 KJ/mol y las del
NaBr es –728 Kjul/mol ¿cómo varia para el NaF, NaCl y Na Br el punto de fusión? ¿Y su
solubilidad en agua?
Química 2.º Bachillerato 2-2
Das könnte Ihnen auch gefallen
- Unidad 2 TESTDokument2 SeitenUnidad 2 TESTMarta MarquesNoch keine Bewertungen
- CuestionesDokument5 SeitenCuestionesBRENDA JIMENEZ PEINADONoch keine Bewertungen
- Ejercicios Tema 2. Enlace QuímicoDokument3 SeitenEjercicios Tema 2. Enlace QuímicohebronambrosioNoch keine Bewertungen
- Ebau - Bloque 2.Dokument3 SeitenEbau - Bloque 2.Javier Sánchez SánchezNoch keine Bewertungen
- Problemas Pevau Enlace Químico y Fuerzas IntermolecularesDokument4 SeitenProblemas Pevau Enlace Químico y Fuerzas IntermolecularespaulaaaNoch keine Bewertungen
- 3 Prob Enlace 2010-11Dokument2 Seiten3 Prob Enlace 2010-11Lorenzo R. RamirezNoch keine Bewertungen
- Q03 Enlace Químico DefDokument12 SeitenQ03 Enlace Químico DefDENZILITONoch keine Bewertungen
- 083 EnlacequimicoDokument3 Seiten083 EnlacequimicoAlicia Conti0% (1)
- 1Dokument4 Seiten1Saúl Corona CarrilloNoch keine Bewertungen
- Selectividad Murcia EnlaceDokument5 SeitenSelectividad Murcia EnlaceJose Manuel Sanchez MasNoch keine Bewertungen
- Problemas Repaso Selectividad 2020. Enlace QuímicoDokument5 SeitenProblemas Repaso Selectividad 2020. Enlace QuímicoscribdNoch keine Bewertungen
- Problemas 3Dokument3 SeitenProblemas 3Mario Andres B.Noch keine Bewertungen
- 2 Enlace Qui ProDokument3 Seiten2 Enlace Qui ProalfonsocerezoNoch keine Bewertungen
- Relación Tema 3 Enlace QuimicoDokument4 SeitenRelación Tema 3 Enlace QuimicoCarlos Castaño RuizNoch keine Bewertungen
- Tema 2 Cuestiones y ProblemasDokument12 SeitenTema 2 Cuestiones y ProblemasGuillermo Martínez RamónNoch keine Bewertungen
- Pau Sept17 QuimicaDokument2 SeitenPau Sept17 QuimicalincecitaNoch keine Bewertungen
- Seminar Enlace Quimico I IIDokument4 SeitenSeminar Enlace Quimico I IIAdrian Benites CarranzaNoch keine Bewertungen
- Ejercicios Propuestos de Enlace QuimicoDokument18 SeitenEjercicios Propuestos de Enlace QuimicoLazloNoch keine Bewertungen
- Seminar Enlace Quimico I II S - RespDokument4 SeitenSeminar Enlace Quimico I II S - RespCristhian GuzmanNoch keine Bewertungen
- QUÍMICA 2º Bachillerato: Ejercicios: Enlace QuímicoDokument9 SeitenQUÍMICA 2º Bachillerato: Ejercicios: Enlace QuímicoperrobastardoNoch keine Bewertungen
- Enlace Químico Ebau 22-23Dokument3 SeitenEnlace Químico Ebau 22-23Viqui R.Noch keine Bewertungen
- Ejercicios Sobre EnlaceDokument1 SeiteEjercicios Sobre EnlaceJorgeAguilarNoch keine Bewertungen
- Guia de Trabajo ENLACE QUIMICODokument2 SeitenGuia de Trabajo ENLACE QUIMICOkarinNoch keine Bewertungen
- S 3 Q1216 (10-1)Dokument4 SeitenS 3 Q1216 (10-1)los sabiosNoch keine Bewertungen
- Enlace Quimico.Dokument5 SeitenEnlace Quimico.Adri_RondanNoch keine Bewertungen
- S 3 Q1210 (10-1)Dokument8 SeitenS 3 Q1210 (10-1)los sabios100% (1)
- Ejercicios Átomos, Elementos y CompuestosDokument13 SeitenEjercicios Átomos, Elementos y CompuestosDavid Gasco DobonNoch keine Bewertungen
- Trabajo NoviembreDokument4 SeitenTrabajo NoviembreSilvano Salvador ondo ndongNoch keine Bewertungen
- Taller No 2 de Química GeneralDokument5 SeitenTaller No 2 de Química Generalestiven alvarezNoch keine Bewertungen
- Boletã N 3. - Enlace Quã MicoDokument4 SeitenBoletã N 3. - Enlace Quã MicoMartin FNoch keine Bewertungen
- Ejercicios Pau Enlace Quimico - 0Dokument11 SeitenEjercicios Pau Enlace Quimico - 0Mirian VivarNoch keine Bewertungen
- Examen de Estructura Atómica y EnlacesDokument1 SeiteExamen de Estructura Atómica y EnlacesFlavia González LimaNoch keine Bewertungen
- Cuestionesenlace PaumadridDokument54 SeitenCuestionesenlace Paumadridhuman100% (1)
- 02 Enlace PevauDokument5 Seiten02 Enlace PevaupatinojulianereaNoch keine Bewertungen
- Propuesta de Ejercicios Bloque 2Dokument4 SeitenPropuesta de Ejercicios Bloque 2ciencia250Noch keine Bewertungen
- DFKJD DF FSDDokument31 SeitenDFKJD DF FSDGabriel Díaz VidalNoch keine Bewertungen
- Ejercicios Born HaberDokument9 SeitenEjercicios Born Haberlb_BotsNoch keine Bewertungen
- Ejercicios PapaDokument7 SeitenEjercicios Papanaca05 lapaNoch keine Bewertungen
- Tabla - EnlaceDokument2 SeitenTabla - Enlacemjymc9z5vsNoch keine Bewertungen
- Ejercicios T2 El EnlaceDokument7 SeitenEjercicios T2 El EnlacealexmadoareNoch keine Bewertungen
- Taller 4Dokument3 SeitenTaller 4XJR150Noch keine Bewertungen
- Enlace QuimicoDokument3 SeitenEnlace QuimicoAlfredo FernandezNoch keine Bewertungen
- Repaso GeneralDokument28 SeitenRepaso GeneralMiriam M GNoch keine Bewertungen
- Guia de Problemas Quimica I 2016Dokument42 SeitenGuia de Problemas Quimica I 2016tomiespi50% (2)
- Cuestiones Tema 2-PpiosDokument5 SeitenCuestiones Tema 2-PpiosJavier OrtuñoNoch keine Bewertungen
- Enlace QuímicoDokument2 SeitenEnlace QuímicoVictor Manuel Ambroa MagariñosNoch keine Bewertungen
- Cepre Uni Exfinal 2002 2Dokument17 SeitenCepre Uni Exfinal 2002 2rosherNoch keine Bewertungen
- Tema 1.2 Enlace Quimico FICHA DE TRABAJO PDFDokument8 SeitenTema 1.2 Enlace Quimico FICHA DE TRABAJO PDFJoaquin Rodrigo CuevaNoch keine Bewertungen
- 2 - Taller 02 - Semana 2 - 2017 - 01Dokument10 Seiten2 - Taller 02 - Semana 2 - 2017 - 01Anonymous IX1cuqR0% (1)
- FICHA - 3 Enlace QuimicoDokument1 SeiteFICHA - 3 Enlace QuimicoRuben FraguelNoch keine Bewertungen
- Cuestiones y Problemas Del Tema 3: Enlace Químico y Propiedades de Las SustanciasDokument19 SeitenCuestiones y Problemas Del Tema 3: Enlace Químico y Propiedades de Las SustanciasjujujujuuajajjajajjsjajajNoch keine Bewertungen
- EnlaceDokument12 SeitenEnlaceAlba Megías MartínezNoch keine Bewertungen
- Deber de Enlaces QuimicosDokument11 SeitenDeber de Enlaces QuimicosJose Bladimir SarchiNoch keine Bewertungen
- Tema 3 - Cuestiones y ProblemasDokument8 SeitenTema 3 - Cuestiones y ProblemasDeme CueVerNoch keine Bewertungen
- Caracterización química, morfológica y estructural de materialesVon EverandCaracterización química, morfológica y estructural de materialesNoch keine Bewertungen
- Estudio de La FundaciónDokument10 SeitenEstudio de La Fundaciónmtbf2014Noch keine Bewertungen
- MATEMATICAS 2 º BACHILLERATO EXAMEN FINAL - Profesor10dematesDokument11 SeitenMATEMATICAS 2 º BACHILLERATO EXAMEN FINAL - Profesor10dematesmtbf2014Noch keine Bewertungen
- Ejercicios Resueltos de Matrices, Ecuaciones 2ob PDFDokument4 SeitenEjercicios Resueltos de Matrices, Ecuaciones 2ob PDFmtbf2014Noch keine Bewertungen
- Explica Las Diferencias Entre Denotación y Connotación A Partir de Las Siguientes PalabrasDokument1 SeiteExplica Las Diferencias Entre Denotación y Connotación A Partir de Las Siguientes Palabrasmtbf20140% (1)
- CUESTIONES DE LÉXICO Sin SolucionesDokument53 SeitenCUESTIONES DE LÉXICO Sin Solucionesmtbf2014Noch keine Bewertungen
- Cantar de Mío Cid Cantar de Mío CidDokument6 SeitenCantar de Mío Cid Cantar de Mío Cidmtbf2014100% (1)
- Refuerzo Pendientes 3 EsoDokument62 SeitenRefuerzo Pendientes 3 Esomtbf2014Noch keine Bewertungen
- Exámenes. Reacciones Orgánicas. Isomería. FormulaciónDokument97 SeitenExámenes. Reacciones Orgánicas. Isomería. Formulaciónmtbf2014Noch keine Bewertungen
- Repaso - Estadistica 2 Eso PDFDokument6 SeitenRepaso - Estadistica 2 Eso PDFmtbf2014Noch keine Bewertungen
- 3º ESO Sintaxis. Ejercicios. 2017 WebDokument13 Seiten3º ESO Sintaxis. Ejercicios. 2017 Webmtbf2014Noch keine Bewertungen
- Certamenes AlgebraDokument22 SeitenCertamenes AlgebraMarcela Santos GarridoNoch keine Bewertungen
- Rta FisicaDokument22 SeitenRta Fisicaandreylawrence1122Noch keine Bewertungen
- Cómo y Con Qué Se Hace El VidrioDokument11 SeitenCómo y Con Qué Se Hace El VidrioCristina Acosta PierolaNoch keine Bewertungen
- Informe de Laboratorio N1Dokument2 SeitenInforme de Laboratorio N1DanielRuizNoch keine Bewertungen
- Termofluencia en PolímerosDokument7 SeitenTermofluencia en PolímerosRomanMartinezzNoch keine Bewertungen
- 003 Memoria ElectricidadDokument9 Seiten003 Memoria ElectricidadsamuelelingenieroNoch keine Bewertungen
- Transformaciones en El PlanoDokument1 SeiteTransformaciones en El PlanoVíctor Huerta Rojas0% (2)
- Mecanica Ejercicios 6Dokument10 SeitenMecanica Ejercicios 6OmarNoch keine Bewertungen
- Electromagnetism oDokument4 SeitenElectromagnetism odaniel gutierrez torresNoch keine Bewertungen
- Ensayo Evaporador de Doble EfectoDokument4 SeitenEnsayo Evaporador de Doble EfectomargaritaNoch keine Bewertungen
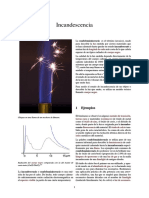
- La candoluminiscencia es el término (arcaico), usado para describir la luz emitida por ciertos materiales que sehancalentadohastaquedarenestadoincandescentey emitenluzdelongituddeondamáscortadeloquecabría esperardeuntípicoradiadordecuerponegro. Lacalidaddelaluzemitidadependedirectamentedela temperatura del cuerpo caliente, un cuerpo ligeramente caliente (alrededor de 1600 °C), emite luz roja-naranja, mientrasqueuncuerpomuycaliente(alrededorde5000 °C),emiteluzmuyblancaeinclusopuedellegaralblanco azuladoatemperaturasextremas(de8000-9000°C). Deahílaexpresiónredhoto“rojocaliente”paradescribir elestadodeunmetalenlafragua.Deahítambiénelbrillo delalavadelosvolcanes(larocafundidaestátancaliente queemiteluz). Para medir el estado de incandescencia de un objeto o describir la luz que emite, se utiliza un modelo teórico llamadocuerponegro.Dokument3 SeitenLa candoluminiscencia es el término (arcaico), usado para describir la luz emitida por ciertos materiales que sehancalentadohastaquedarenestadoincandescentey emitenluzdelongituddeondamáscortadeloquecabría esperardeuntípicoradiadordecuerponegro. Lacalidaddelaluzemitidadependedirectamentedela temperatura del cuerpo caliente, un cuerpo ligeramente caliente (alrededor de 1600 °C), emite luz roja-naranja, mientrasqueuncuerpomuycaliente(alrededorde5000 °C),emiteluzmuyblancaeinclusopuedellegaralblanco azuladoatemperaturasextremas(de8000-9000°C). Deahílaexpresiónredhoto“rojocaliente”paradescribir elestadodeunmetalenlafragua.Deahítambiénelbrillo delalavadelosvolcanes(larocafundidaestátancaliente queemiteluz). Para medir el estado de incandescencia de un objeto o describir la luz que emite, se utiliza un modelo teórico llamadocuerponegro.Kimberly PalmerNoch keine Bewertungen
- Taller. Unidad IDokument8 SeitenTaller. Unidad IVanessa Rodriguez AyalaNoch keine Bewertungen
- Inspección, Mantenimiento Y Operación Del Sistema de Bombeo de Agua Por Afloramiento en La Barrera Del Desvío Del Río AsanaDokument4 SeitenInspección, Mantenimiento Y Operación Del Sistema de Bombeo de Agua Por Afloramiento en La Barrera Del Desvío Del Río AsanaGelber PactaNoch keine Bewertungen
- Recuperacion Enlaces QuimicosDokument2 SeitenRecuperacion Enlaces Quimicoskelly escorcia100% (1)
- Potenciales de Liénard-WiechertDokument4 SeitenPotenciales de Liénard-WiechertAndrea ValderramaNoch keine Bewertungen
- Resumen de Movimiento Rectilíneo UniformeDokument6 SeitenResumen de Movimiento Rectilíneo Uniformeevelynbrianna70% (10)
- Mecánica RacionalDokument4 SeitenMecánica RacionalYolandaNoch keine Bewertungen
- Formacion de Mezclas Homogenias y HeterogeniasDokument4 SeitenFormacion de Mezclas Homogenias y HeterogeniasHenry Vizcarra0% (1)
- Informe 6 Carga de Un Condensador UTPDokument12 SeitenInforme 6 Carga de Un Condensador UTPE. R. Reinoso Núñez40% (5)
- Ciencias 2 Puente ColganteDokument12 SeitenCiencias 2 Puente ColganteTorices Uriel100% (1)
- Unidad IV Transformaciones Lineales PDFDokument25 SeitenUnidad IV Transformaciones Lineales PDFDavid GarciaNoch keine Bewertungen
- 1.7.7 Desigualdades Tipo CocienteDokument5 Seiten1.7.7 Desigualdades Tipo CocienteJ Luis MlsNoch keine Bewertungen
- AscensoresDokument15 SeitenAscensoresCristian Salinas MurilloNoch keine Bewertungen
- Cristalizaciòn Del Nitrato de PotasioDokument9 SeitenCristalizaciòn Del Nitrato de Potasioपेट्रीसिया पाटीNoch keine Bewertungen
- Determinación de Dióxido de NitrógenoDokument3 SeitenDeterminación de Dióxido de NitrógenoMaria Teresa Asmat BautistaNoch keine Bewertungen
- Topografia AngulosDokument4 SeitenTopografia AngulosAlexFernandoAlmacheNoch keine Bewertungen
- Cinemática Inversa de RobotsDokument5 SeitenCinemática Inversa de RobotsAcus Xelor Imperium TemporeNoch keine Bewertungen
- PAU - 2002 - 2010 - Aleaciones y Diagramas de FasesDokument11 SeitenPAU - 2002 - 2010 - Aleaciones y Diagramas de FasesjmbravomNoch keine Bewertungen
- Trabajo Concreto Pretensado 2Dokument25 SeitenTrabajo Concreto Pretensado 2Maxs Delgado BuitrónNoch keine Bewertungen
- Guia 1. Fundamentos de Quimica AnaliticaDokument10 SeitenGuia 1. Fundamentos de Quimica AnaliticaWilley100% (1)