Beruflich Dokumente
Kultur Dokumente
Propiedades de los gases
Hochgeladen von
Valentina Castaño0 Bewertungen0% fanden dieses Dokument nützlich (0 Abstimmungen)
33 Ansichten15 SeitenEl documento describe las propiedades de los gases. Los gases no tienen fuerzas de atracción entre sus moléculas y adoptan la forma de su contenedor. Según la teoría cinética molecular, las moléculas de gas se mueven al azar y chocan entre sí y con las paredes, lo que explica la presión y mezcla de los gases. Las moléculas rebotan con la misma velocidad durante los choques elásticos.
Originalbeschreibung:
Originaltitel
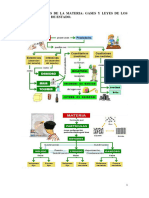
Estados de la materia 2.0
Copyright
© © All Rights Reserved
Verfügbare Formate
PDF, TXT oder online auf Scribd lesen
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenEl documento describe las propiedades de los gases. Los gases no tienen fuerzas de atracción entre sus moléculas y adoptan la forma de su contenedor. Según la teoría cinética molecular, las moléculas de gas se mueven al azar y chocan entre sí y con las paredes, lo que explica la presión y mezcla de los gases. Las moléculas rebotan con la misma velocidad durante los choques elásticos.
Copyright:
© All Rights Reserved
Verfügbare Formate
Als PDF, TXT herunterladen oder online auf Scribd lesen
0 Bewertungen0% fanden dieses Dokument nützlich (0 Abstimmungen)
33 Ansichten15 SeitenPropiedades de los gases
Hochgeladen von
Valentina CastañoEl documento describe las propiedades de los gases. Los gases no tienen fuerzas de atracción entre sus moléculas y adoptan la forma de su contenedor. Según la teoría cinética molecular, las moléculas de gas se mueven al azar y chocan entre sí y con las paredes, lo que explica la presión y mezcla de los gases. Las moléculas rebotan con la misma velocidad durante los choques elásticos.
Copyright:
© All Rights Reserved
Verfügbare Formate
Als PDF, TXT herunterladen oder online auf Scribd lesen
Sie sind auf Seite 1von 15
El Estado Gaseoso
LOS GASES
Sus fuerzas de atracción intermoleculares son nulas, es
decir, no existe fuerza de atracción ni de repulsión entre
sus moléculas.
LOS GASES
Teoría cinético molecular de tos gases
La teoría cinética de los gases intenta explicar el
comportamiento de los gases a partir de los siguientes
enunciados:
• Están constituidos por partículas muy
pequeñas denominadas moléculas, cuyo volumen es
despreciable comparado con la distancia
que existe entre ellas. Debido a lo anterior, no se
evidencian fuerzas de atracción entre las moléculas; esto
explicaría la alta compresibilidad y la baja
densidad de los gases.
• Las moléculas de los gases se encuentran en continuo
movimiento. Dicho movimiento es al azar
y de forma desordenada, chocando unas contra
otras y con las paredes del recipiente que las contiene. Este
postulado explicaría por qué los gases
tienden a mezclarse completamente; además, los
choques de las moléculas contra las paredes del
LOS GASES
recipiente serían la razón de la presión ejercida
por los gases.
• Los choques de las moléculas de los gases son
elásticos; en consecuencia, durante los choques
no se pierde energía, pues las moléculas rebotan
con la misma velocidad.
• La temperatura de un sistema gaseoso es una
medida del movimiento de las partículas.
LOS GASES
FIG. 5 El movimiento de tas moléculas del gas puede compararse
con el de los balotas de un bingo; sin embargo, las balotas pierden
energía en cada choque y por rozamiento con el aire hasta
detenerse, mientras que las moléculas de los gases no.
Propiedades de los gases
• No tienen forma definida sino que adoptan la forma del
recipiente que los contiene.
•No tienen volumen definido debido a que sus moléculas se
mueven continuamente, se expanden y se contraen.
LOS GASES
•Son fácilmente compresibles, es decir, su volumen disminuye
ante un aumento de la presión.
•Tienen densidades muy bajas comparados con los sólidos y
los líquidos.
•Se difunden fácilmente, mezclándose por completo en forma
espontánea.
Propiedades que identifican a un gas
Aunque el gas y el vapor son dos
expresiones que a usan indistintamente,
tienen significados diferentes.
Un gas es una sustancia que a
temperatura ambiente y a presión normal
LOS GASES
se encuentra en estado gaseso. Algunos
ejemplos son el O2 y el N2. El vapor y la
forma gaseosa de una sustancia que
normalmente se encuentra en estado
líquido. Sin embargo, al calentar dicho
líquido, parte o todo el líquida si:
convierte en vapor.
FIG. 6 El agua es un líquido que
El agua de los ríos, lagos y mares se transforma en vapor al
continuamente es sometida a este evaporarse. Durante la
proceso. Para describir un sistema evaporación, las moléculas se
desprenden de lo superficie
gaseoso se usan tres propiedades: el
líquida sin alcanzar la
volumen, la temperatura y la presión. temperatura de ebullición.
PRESIÓN
P= F
A
• Definición: es la fuerza perpendicular que se ejerce por
unidad del área.
• Unidades:
[P]=[F]/[L]2=[N]/[m2]= Pa (Pascales)
1 Pa = N/m2
• Otras unidades:
• atm: 1 atm = 101 325 Pa = 1013,2 HPa
• mm Hg: 760 mm Hg = 1 atm
Das könnte Ihnen auch gefallen
- Matemáticas 1 s00332 Edit Trillas Fortino EscareñoDokument256 SeitenMatemáticas 1 s00332 Edit Trillas Fortino Escareñooctavio alvarez100% (2)
- Teoría Del Gas Real: La Relación Exacta Para Gases RealesVon EverandTeoría Del Gas Real: La Relación Exacta Para Gases RealesNoch keine Bewertungen
- Hidraulica ExperimentalDokument34 SeitenHidraulica ExperimentalWilliam Juarez Lozano100% (7)
- Guía Aprendizaje 7° BásicoDokument6 SeitenGuía Aprendizaje 7° BásicoMassiel VergaraNoch keine Bewertungen
- Propiedades de Los GasesDokument26 SeitenPropiedades de Los GasesNelly Vargas MontilvaNoch keine Bewertungen
- TALLER DE QUÍMICA ResueltoDokument52 SeitenTALLER DE QUÍMICA ResueltoSanti Maya86% (7)
- MIII 001 006 Prelindice PDFDokument6 SeitenMIII 001 006 Prelindice PDFMaría Isabel Ordóñez0% (2)
- TALLER DE QUÍMICA ResueltoDokument52 SeitenTALLER DE QUÍMICA ResueltoSanti Maya100% (5)
- Estados de la materia: gases, líquidos y sólidosDokument12 SeitenEstados de la materia: gases, líquidos y sólidosLoreto BlancoNoch keine Bewertungen
- Masa Molecular de Una Sustancia VolátilDokument7 SeitenMasa Molecular de Una Sustancia VolátilAmadeus MüllerNoch keine Bewertungen
- 2018 - Propiedad de Gases Ideales y RealesDokument118 Seiten2018 - Propiedad de Gases Ideales y RealesambientalgelogyNoch keine Bewertungen
- Boletin 6Dokument9 SeitenBoletin 6Jonathan AgueroNoch keine Bewertungen
- Tema GasesDokument12 SeitenTema GasesbimboNoch keine Bewertungen
- Taller Estado GaseosoDokument14 SeitenTaller Estado GaseosoMelissa PinedaNoch keine Bewertungen
- Los gases y su comportamientoDokument94 SeitenLos gases y su comportamientoCarlos XavierNoch keine Bewertungen
- Física y química 1o bachillerato: Leyes de los gasesDokument13 SeitenFísica y química 1o bachillerato: Leyes de los gasesDaniel SaavedraNoch keine Bewertungen
- Intensivo Uni - Química Semana 07Dokument28 SeitenIntensivo Uni - Química Semana 07leodu2712Noch keine Bewertungen
- Química I: Estados de la materia y leyes de los gasesDokument7 SeitenQuímica I: Estados de la materia y leyes de los gasesAlejandro Nicolas SchunkeNoch keine Bewertungen
- Estado GaseosoDokument3 SeitenEstado GaseosoManuela ReyesNoch keine Bewertungen
- Propiedades de Los GasesDokument47 SeitenPropiedades de Los GasesHarlan SimonettiNoch keine Bewertungen
- Características y leyes de los gasesDokument11 SeitenCaracterísticas y leyes de los gasesJ Benjamiin Hdez MatNoch keine Bewertungen
- Taller de GasesDokument13 SeitenTaller de GasesSteven CastañedaNoch keine Bewertungen
- Gases Ideales 2Dokument33 SeitenGases Ideales 2MelodyNoch keine Bewertungen
- QUIMICADokument9 SeitenQUIMICANathaly ChaconNoch keine Bewertungen
- Estados de La MateriaDokument35 SeitenEstados de La MateriaCarmen ChirinosNoch keine Bewertungen
- Quimica Expo 3Dokument16 SeitenQuimica Expo 3Charlton H. Pretel D.Noch keine Bewertungen
- 4 La Materia. Gases - Disoluciones Fyq3esoDokument16 Seiten4 La Materia. Gases - Disoluciones Fyq3esozkkbydzh2wNoch keine Bewertungen
- Guia 7 Quimica 10 GasesDokument9 SeitenGuia 7 Quimica 10 GasesBrayan Steven Patiño NarvaezNoch keine Bewertungen
- Los 3 Estados de Agregación de La MateriaDokument4 SeitenLos 3 Estados de Agregación de La MateriaJM TiqueNoch keine Bewertungen
- Trabajo de QuímicaDokument20 SeitenTrabajo de QuímicaMariangel IzarraNoch keine Bewertungen
- Estados de la materiaDokument4 SeitenEstados de la materiaTqm MillardNoch keine Bewertungen
- Taller QuimicaDokument40 SeitenTaller QuimicamilibethNoch keine Bewertungen
- Diseño ExperimentalDokument12 SeitenDiseño ExperimentalJose Luis Jose LuisNoch keine Bewertungen
- Taller de QuimicaDokument49 SeitenTaller de QuimicaDaniel DíazNoch keine Bewertungen
- Taller de QuimicaDokument30 SeitenTaller de QuimicaAna Yulieth CaceresNoch keine Bewertungen
- Trabajo de Química-2Dokument17 SeitenTrabajo de Química-2Yeison Armando Bravo BravoNoch keine Bewertungen
- GT 2021 CN g7 Cuales Son Los Estados de La MateriaDokument6 SeitenGT 2021 CN g7 Cuales Son Los Estados de La MateriaSoene FernandezNoch keine Bewertungen
- Estados de La MateriaDokument26 SeitenEstados de La MateriaHilde GuerraNoch keine Bewertungen
- Diapositiva Estado Gaseoso - Proceso GeneralDokument33 SeitenDiapositiva Estado Gaseoso - Proceso GeneralPedro Luis Almeyda RamírezNoch keine Bewertungen
- Lectura Modelo Corpuscular MaterialDokument3 SeitenLectura Modelo Corpuscular MaterialPilo Hernandez50% (2)
- Semana 9 Quimica 10 2021Dokument7 SeitenSemana 9 Quimica 10 2021Amadora RNoch keine Bewertungen
- GasesDokument17 SeitenGasesDiego YPNoch keine Bewertungen
- Estado GaseosoDokument17 SeitenEstado GaseosoCiro Alejandro Pacheco CardenasNoch keine Bewertungen
- Evaluación para QuímicaDokument6 SeitenEvaluación para QuímicarodrigoNoch keine Bewertungen
- El Estado Gaseoso Es Un Estado Disperso de La MateriaDokument9 SeitenEl Estado Gaseoso Es Un Estado Disperso de La MateriaMaria Jose Prieto GonzalezNoch keine Bewertungen
- Informe QuímicaDokument6 SeitenInforme Químicagbkgyc52dhNoch keine Bewertungen
- Quimica Enviar PDFDokument6 SeitenQuimica Enviar PDFnahumelyNoch keine Bewertungen
- Modelo Cinetico MolecularDokument28 SeitenModelo Cinetico MolecularGoergieNoch keine Bewertungen
- Estados de La MateriaDokument60 SeitenEstados de La MateriaPaul PeñaNoch keine Bewertungen
- Integrantes: - Carmen Rosa Samame. - Dayhann Valer. Profesor: Wilmer JaramilloDokument7 SeitenIntegrantes: - Carmen Rosa Samame. - Dayhann Valer. Profesor: Wilmer Jaramillodayhann179Noch keine Bewertungen
- Los GasesDokument8 SeitenLos GasesDanna Michell Gualdron MuñozNoch keine Bewertungen
- Guia No. 10 de Quimica Ciclo 5Dokument5 SeitenGuia No. 10 de Quimica Ciclo 5JuanC.RomeroNoch keine Bewertungen
- Propiedades de Los GasesDokument13 SeitenPropiedades de Los GasesIrlanda Yareth De Leon HuertaNoch keine Bewertungen
- Los Fluidos y Sus PropiedadesDokument4 SeitenLos Fluidos y Sus PropiedadesJohn Jhonatan Herrera SaavedraNoch keine Bewertungen
- U2 Tema3. Gases IdealesDokument11 SeitenU2 Tema3. Gases IdealesRICHARD JAMES ROCANO YUPANoch keine Bewertungen
- Estado Gaseoso 1Dokument33 SeitenEstado Gaseoso 1davis100% (1)
- Propiedades de Los GasesDokument11 SeitenPropiedades de Los GasesSamuel Tobar100% (2)
- 9 Cambios de Estado, Leyes de GasesDokument6 Seiten9 Cambios de Estado, Leyes de Gasesmiriammedina344Noch keine Bewertungen
- Trabajo de QuimicaDokument14 SeitenTrabajo de QuimicajoseNoch keine Bewertungen
- Infografía Listado de Propiedades Químicas Doodle Ilustrativo Naranja y AzulDokument9 SeitenInfografía Listado de Propiedades Químicas Doodle Ilustrativo Naranja y Azulcarlos.vargasNoch keine Bewertungen
- Fuerzas de Atracción Entre MoleculasDokument5 SeitenFuerzas de Atracción Entre MoleculasVELA CNoch keine Bewertungen
- Estados de La MateriaDokument8 SeitenEstados de La MateriajehilliNoch keine Bewertungen
- Torta de Banan1Dokument2 SeitenTorta de Banan1Valentina CastañoNoch keine Bewertungen
- Pensum Administracion Negocios Internacionales CEIPADokument1 SeitePensum Administracion Negocios Internacionales CEIPAValentina CastañoNoch keine Bewertungen
- GUION RADIALlDokument2 SeitenGUION RADIALlValentina CastañoNoch keine Bewertungen
- Directorio DocenteDokument1 SeiteDirectorio DocenteValentina CastañoNoch keine Bewertungen
- Investigación de Operaciones IDokument3 SeitenInvestigación de Operaciones IJuan NegretteNoch keine Bewertungen
- Ejercicio1 Fisica GeneralDokument2 SeitenEjercicio1 Fisica GeneralRicardo SanchezNoch keine Bewertungen
- Resumen Capitulo 4 FELDERDokument5 SeitenResumen Capitulo 4 FELDERSEBASTIAN RIVAS CALDERONNoch keine Bewertungen
- DM-03-2022 GeometríaDokument6 SeitenDM-03-2022 Geometríamaria ignacia correaNoch keine Bewertungen
- Guía 1-Punto y Recta (Mar2016)Dokument4 SeitenGuía 1-Punto y Recta (Mar2016)luis estradaNoch keine Bewertungen
- Introducción a la programación paso a paso y GRAFCETDokument7 SeitenIntroducción a la programación paso a paso y GRAFCETJosé ValenzuelaNoch keine Bewertungen
- Reporte de investigación de operacionesDokument8 SeitenReporte de investigación de operacionesAntonio LopezNoch keine Bewertungen
- Elementos A Flexo CompresionDokument61 SeitenElementos A Flexo CompresionErik VivancoNoch keine Bewertungen
- Probabilidad Condicional2Dokument12 SeitenProbabilidad Condicional2Lester Zarate RodriguezNoch keine Bewertungen
- 2240 Ea Matematica Aplicada A Los Negocios Diurno g1dn 00 Et 1 Guillermo Romero MendezDokument5 Seiten2240 Ea Matematica Aplicada A Los Negocios Diurno g1dn 00 Et 1 Guillermo Romero Mendezmontejomanuel12Noch keine Bewertungen
- Resumen Mario BungeDokument4 SeitenResumen Mario BungeOscar ChinchayNoch keine Bewertungen
- Dosificacion Metodos Numericos 2018Dokument2 SeitenDosificacion Metodos Numericos 2018Anonymous Qj9JOFONoch keine Bewertungen
- Perfil del Egresado de la Unefa: Capaz de programar equiposDokument8 SeitenPerfil del Egresado de la Unefa: Capaz de programar equiposJavier FalconNoch keine Bewertungen
- Norma Coguanor NTG 41051 h2 Astm C 1314 - 09Dokument27 SeitenNorma Coguanor NTG 41051 h2 Astm C 1314 - 09Emilio Beltranena MatheuNoch keine Bewertungen
- Laboratorio Transportes Asignación y TransbordoDokument3 SeitenLaboratorio Transportes Asignación y TransbordoNereaNoch keine Bewertungen
- Prueba de HipotesisDokument9 SeitenPrueba de Hipotesisl_fitoNoch keine Bewertungen
- Aritmética 13Dokument4 SeitenAritmética 13Oswaldo Aguirre MendozaNoch keine Bewertungen
- Temarios - Física - Esgrum - Esdeim 2018Dokument2 SeitenTemarios - Física - Esgrum - Esdeim 2018Joselo LópezNoch keine Bewertungen
- 051 Libros Matematicas CapDokument54 Seiten051 Libros Matematicas CapМаурисио Торрес РамиресNoch keine Bewertungen
- Taller de Quimica 3Dokument11 SeitenTaller de Quimica 3josé Mestre Lara100% (1)
- Perforacion DireccionalDokument23 SeitenPerforacion DireccionaljorgillooNoch keine Bewertungen
- Componentes de Un VectorDokument6 SeitenComponentes de Un VectorAngelica Perez RozasNoch keine Bewertungen
- Clase 5 de Cálculo IIIDokument25 SeitenClase 5 de Cálculo IIIjulio100% (1)
- EL Manejo de La DiscalculiaDokument13 SeitenEL Manejo de La DiscalculiaLiceth Herrera MartinezNoch keine Bewertungen
- A Journey Around Alpha and Omega To Estimate Internal Consistency ReliabilityDokument28 SeitenA Journey Around Alpha and Omega To Estimate Internal Consistency ReliabilityMateus EstevamNoch keine Bewertungen