Beruflich Dokumente
Kultur Dokumente
Cinetique Chimique PDF
Hochgeladen von
ياسين السعدانيOriginaltitel
Copyright
Verfügbare Formate
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
Verfügbare Formate
Cinetique Chimique PDF
Hochgeladen von
ياسين السعدانيCopyright:
Verfügbare Formate
CINETIQUE CHIMIQUE.
A) CINETIQUE FORMELLE:
La cinétique chimique étudie l’évolution d’un système physico-chimique au cours du temps.
Sur le plan macroscopique, on détermine des lois de vitesse de réaction, et on analyse les divers facteurs
optimisant les conditions industrielles .
Sur le plan microscopique, on détermine le mécanisme de la réaction à l’échelle élémentaire.
On se limite aux réactions thermodynamiquement possible .
I) DIFFERENTES VITESSES :
1) Vitesse de disparition, de formation. Vitesse de réaction:
Soit une réaction chimique donnée :
∑ν A
i
i i =0
ν i > 0 pour les produits
ν i < 0 pour les réactifs
dni
On définit la vitesse de disparition d’un réactif i, dont la quantité est ni, par : -
dt
dni
La vitesse de formation d’un produit est définie par + .
dt
1 dni d ξ
On définit alors la vitesse de la réaction, appelée vitesse globale, par : υ = =
ν i dt dt
Cette vitesse s’exprime en mol/s .
2) Vitesse de réaction pour un système fermé isochore :
Dans un système fermé, il n’y a pas d’échange de matière avec l’extérieur. Par conséquent,
la variation des quantités de matière n’est due qu’à la réactivité chimique. Pour un système
fermé à volume V constant, on définit la vitesse volumique υ par :
1 d ξ 1 dCi
υ= =
V dt ν i dt
Ci représente la concentration du composé i dans le milieu. C’est une grandeur intensive,
dont l’évolution est plus facile à suivre lors du déroulement de la réaction.
Cette vitesse s’exprime en mol/L.s.
Pi
Remarque : pour les gaz supposés parfaits on remplace Ci par ou Pi représente la pression
RT
partielle du gaz i ( N.B : Ptot = ∑ Pi pour un mélange idéal de gaz parfaits ).
i
1 A.NARJIS CRMEF 2016-2017
II) FACTEURS CINETIQUES :
On appelle facteurs cinétiques les paramètres qui influent sur la vitesse d’une réaction, exemples :
– les concentrations des réactifs ;
– la température ;
– la présence éventuelle d’un catalyseur ou d’un initiateur ;
– l’éclairement ...
1) Influence de la concentration - ordre d'une réaction :
Pour un certain nombre de réactions chimiques, on observe expérimentalement que la
vitesse peut s’exprimer par une relation de type :
p q
υ = k [ A] [ B ]
k est la constante de vitesse,(positive) dont la dimension dépend des valeurs de p et q.
p et q sont les ordres partiels par rapport aux composés A et B respectivement qui peuvent être
entières ou fractionnaires. Leur valeurs numériques différentes souvent des coefficients
stœchiométriques . Sauf dans le cas des actes élémentaires où les ordres partiels seront égaux aux
coefficients stoechiométriques .
L’ordre global de la réaction r est la somme des ordres partiels : r = p + q .
Exemple : la réaction d’oxydation des ions iodure par les ions peroxodisulfate :
S 2 O82 − + 2 I − 2 SO42 − + I 2
admet la loi de vitesse : υ = k S2 082− I − . Les ordres partiels sont égaux à 1 par
rapport aux deux réactifs et l’ordre global est égal à 2.
Remarque : la plupart des réactions chimiques n’admettent pas d’ordre . On ne peut établir une
relation simple entre la vitesse et les concentrations des réactifs. Exemple :
Br2 + H 2 2 HBr
1
υ=k
[ H 2 ][ Br ]2
1+ k '
[ HBr ]
[ Br2 ]
2) Influence de la température :
Pour la plupart des réactions chimiques, la vitesse augmente quand la température augmente.
La vitesse fait intervenir une constante de vitesse k qui dépend de la température k (T).
Arrhenius proposa une relation empirique liant la constante de vitesse à la température :
− Ea
k = A exp (Loi d’Arrhénius )
RT
Ea : l’énergie d’activation de la réaction (kJ/mol). C'est l'énergie que doivent franchir les
réctifs pour que la réaction se produise .
R: la constante des gaz parfaits ( 8,314 L.k.mol-1) .
T: la température absolue T(K) = t(°C) + 273,15 .
A: Facteur préexponentiel appelée facteur de fréquence .
2 A.NARJIS CRMEF 2016-2017
III)
III) CINÉTIQUE FORMELLE. ÉTUDE DES RÉACTIONS AVEC ORDRES
1) Cinétique formelle. Lois cinétiques .
L’étude expérimentale de la vitesse d’une réaction permet de déterminer s’il existe une
relation simple liant la vitesse et les concentrations des réactifs.
La cinétique formelle tente d’établir l’évolution des concentrations des réactifs en fonction
du temps, les relations Ci = f (t). Ces relations, appelées lois cinétiques, dépendent de
l’ordre de la réaction. Elles sont caractéristiques pour une valeur numérique de l’ordre.
2) Dégénérescence de l’ordre d’une réaction .
Soit la réaction : αA + βB δC + γ D
a b
admettant la loi de vitesse υ = k [ A] [ B ] .
Dans certaines conditions expérimentales, la concentration d’un des deux réactifs, B par exemple,
peut rester quasiment constante au cours du temps.( B est introduit en très grand excès)
a
υ = kapp [ A] avec kapp la constante apparente : kapp = k. [B]b. L’ordre global apparent de la réaction
se réduit à la seule valeur a. On dit qu’il y a dégénérescence de l’ordre global de la réaction.
Expérimentalement, la méthode de dégénérescence de l’ordre est couramment utilisée pour
déterminer les ordres partiels. Par une première étude, on détermine l’ordre partiel
a par rapport au réactif A et la constante apparente kapp. Puis on recommence l’expérience
avec une quantité initiale du réactif B différente. La détermination de la nouvelle valeur
de k'app permet de déduire la valeur de l’ordre partiel b par rapport au réactif B. (voir TD).
3) Temps de demi-réaction.
Définition : Le temps de demi-réaction, t1/2, est le temps au bout duquel la moitié de la quantité
du réactif limitant a disparu ( ou bien lorsque l'avancement est égale à l'avancement maximale
divisée par deux).
On peut également définir le temps de tiers de réaction, de quart de réaction, etc...
4) Réaction d’ordre 0 .
Temps de demi-réaction :
( dépend de la concentration initiale )
3 A.NARJIS CRMEF 2016-2017
5) Réaction d’ordre 1 .
Temps de demi-réaction :
( ne dépend pas de la concentration initiale )
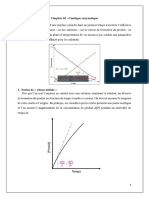
Pour obtenir une représentation affine ( ou pour
justifier l'ordre 1 ), il faut tracer l’évolution de
la fonction Ln [A] = f (t).
6) Réaction d’ordre 2 .
Premier cas :
Soit la réaction α A → produits . La vitesse de réaction est d’ordre 2 par rapport à A :
Temps de demi-réaction :
( dépend de la concentration initiale )
4 A.NARJIS CRMEF 2016-2017
Deuxième cas :
Soit la réaction α A + β B → produits . On considère le cas d’une réaction d’ordre 1 par
rapport aux deux réactifs et d’ordre global 2. On se limite au cas d’un mélange initial des deux réactifs
en proportions stœchiométriques. À t = 0 .
Temps de demi-réaction :
( dépend de la concentration initiale )
Exercice :
Refaites le calcul dans le cas où le mélange initiale n'est pas stoechiométrique et déterminer le
temps de la demi réaction.
7) Tableau récapitulatif .
5 A.NARJIS CRMEF 2016-2017
IV) MÉTHODES EXPÉRIMENTALES DE LA CINÉTIQUE
L’étude cinétique des réactions chimiques a pour but de déterminer les ordres de la réaction quand
ils existent et l’énergie d’activation . Pour cela on doit suivre l’évolution de la concentration d’un
constituant au cours du temps. On distingue les méthodes chimiques et les méthodes physiques.
1) Les méthodes chimiques
On effectue des prises d’essai au cours du temps à intervalles réguliers , puis on dose le constituant
sélectionné avec une réaction adaptée.
Exemple : pour l’étude de la réaction de décomposition de l’eau oxygénée, on suit l’évolution de la
concentration en H2O2 en dosant des prises d’essai par une solution de permanganate de potassium.
La manipulation demande du temps . Il faut donc bloquer la cinétique de la réaction étudiée soit en :
– diluant fortement la prise d’essai ;
– plongeant cette prise d’essai dans un bain de glace (trempe) ;
– ajoutant un nouveau constituant chimique qui bloque la cinétique (inhibiteur adapté) .
2) Les méthodes physiques
On enregistre l’évolution dans le temps d’une grandeur physique convenable. Ces méthodes
présentent l’avantage de moins perturber le milieu réactionnel .
Les principales techniques physiques utilisées sont :
– la spectrophotométrie ;
– la conductimétrie ;
– la potentiométrie, la pH-métrie ;
– la calorimétrie ;
– la mesure de la pression dans le réacteur...
V) MÉTHODES
MÉTHODES DE DETERMINATION DE L'ORDRE .
1) Les méthodes d’intégration ( pour un seul réactif)
On se limite le plus souvent à vérifier que l’ordre est égal à 0, 1 ou 2. On doit donc :
- Tracer en fonction [ A] = f (t ) pour vérifier si, l'ordre est égale à 0 .
- Tracer en fonction Ln [ A] = f (t ) pour vérifier si, l'ordre est égale à 1 .
1
- Tracer en fonction = f (t ) pour vérifier si, l'ordre est égale à 2 .
[ A]
2) Les méthodes de vitesse instantanées .
Cette méthode moins précise puisqu'il demande de précise la concentration d'une espèce à chaque
instant . On trace Ln (υ (t ) ) = f ([ A]) . A partir de la pente on détermine l'ordre .
3) Les méthodes de vitesse initiales .
On trace Ln (υo ) = f ([ A]o ) (pour différentes valeur de la concentration initiale de A) .
Pour déterminer les ordres partiels on utilise la méthode des vitesses initiales( voir exo4 :TD)
6 A.NARJIS CRMEF 2016-2017
VI) ETUDE DE QUELQUES REACTIONS ELEMENTAIRES.
Une réaction chimique résulte de la succession ou la superposition de plusieurs étapes au cours
d’un processus complexe. Parmi ces étapes, on peut distinguer des réactions opposées , des
réactions successives et des réactions compétitives ou parallèles .
On suppose dans la suite de ce paragraphe que tous les processus respectent la loi de Van't Hoff.
1) Les réactions parallèles :
Soient les deux processus suivant et partons initialement uniquement de A:
k1
A → B
k2
A → C
Montrer que [ ] = k1 ∀t ( on parle de contrôle cinétique : le plus rapide se forme en excès )
B
[A ] k2
2) Les réactions opposées
Il y a réaction à la fois entre les réactifs et entre les produits , mais globalement la composition du
mélange reste constante :
3) Les réactions successives
k1 k2
Soit le mécanisme : A → B → C .
Les actes élémentaires respectent la loi de Van't Hoff, :
d[A ]
= − v1 = −k1[A ]
dt
d[B]
= v1 - v 2 = k1 [A ] - k 2 [B]
dt
d[C]
= v 2 = k 2 [B]
dt
7 A.NARJIS CRMEF 2016-2017
Soit :
d[A ]
+ k1 [A ] = 0 (1)
dt
d[B]
+ k 2 [B] = k1 [ A] (2)
dt
d[C]
= k 2 [B] (3)
dt
Solution:
- [A] = C × e - k1×t = [ A]0 e - k1×t .
k1 [ A]0 - k1t - k2t
- [ B] =
k 2 − k1
(e − e ) .
( k1e- k2t − k2e- k1t )
- [C ] = [ A]0 1 + .
k2 − k1
k2
1 k k 2 −k 1
tM = ln 1 [B](t M ) = a k 1
k1 − k 2 k 2 k2
4) Principe de l'état quasi stationnaire (AEQS):
Prenons l'intermédiaire réactionnel précèdent " B ". Dans le cas ou k1 << k2 , B est une espèce très
d[B ]
réactive. (2) donne ≈ 0 . La concentration de B est alors dans un état quasi stationnaire.
dt
Elle s’applique aux intermédiaires réactionnels . La concentration de l’I.R. reste très faible et quasi
constante au bout d'une courte durée . On parle de l’approximation de l’état quasi stationnaire ou du
principe de Bodenstein :
8 A.NARJIS CRMEF 2016-2017
B) MECANISME REACTIONNEL:
I) INTRODUCTION :
L’équation-bilan d’une réaction chimique est une description macroscopique de la transformation
de la matière. Au contraire le mécanisme réactionnel décrit la réalité microscopique en indiquant
les transformations se produisant à l’échelle moléculaire. Elles se produisent en plusieurs étapes,
appelés actes élémentaires.
L’équation-bilan de la réaction chimique est une combinaison de ces processus élémentaires.
1) Acte élémentaire et molécularité
On appelle acte élémentaire, une réaction se produisant réellement en une seule étape .
On appelle molécularité d’un acte élémentaire le nombre d’entités réactives mises en jeu.
Ce nombre est faible : (acte monomoléculaire), (acte bimoléculaire), 3 (acte trimoléculaire (rare)).
Pour qu’un acte élémentaire puisse se produire, il faut qu’il y ait rencontre énergétiquement (ou
choc efficace ) pour pouvoir franchir un certain niveau énergétique ( énergie d'activation)
2) Loi de Van’t Hoff - Loi d'Arrhénius .
Les actes élémentaires admettent toujours des ordres entiers en respectant les loi suivantes:
- Loi de Van’t Hoff : les ordres partiels sont égaux aux coefficients stœchiométriques et
l’ordre global est égal à la molécularité".
- Loi d’Arrhénius : La constante de vitesse d’un acte élémentaire suit la loi k = A exp
− Ea
.
RT
3) Intermédiaires réactionnels.
Un intermédiaire réactionnel (IR) est une espèce chimique peu stable qui apparaît dans un acte
élémentaire et disparaît dans un autre sans figurer dans l'équation bilan . On l'appelle aussi un centre
actif sa durée de vie est brève . On peut détecter sa présence et, parfois, l'isoler pour l' identifier.
Formée au cours d’étapes lentes et consommée au cours d’étapes rapides.
Un intermédiaire de réaction peut être :
• un radical (molécule ayant au mois un electron celibataire) ( Cl. , R. .....)
• un ion
- tel qu’un carbocation : ( Charge positive sur un atome de carbone ) ;
- ou tel qu’un carbanion : ( charge négative sur un atome de carbone).
4) Principe de l’étape limitante ou cinétiquement déterminante
Lorsqu’un mécanisme réactionnel se décompose en une succession d’actes élémentaires ,
Si un acte élémentaire possède une constante de vitesse très faible devant toutes les autres,
sa vitesse sera beaucoup plus petite . On dit que cet acte constitue l’étape limitante du mécanisme
réactionnel ( Il impose sa vitesse à la réaction globale).
9 A.NARJIS CRMEF 2016-2017
II) PROFILS ENERGETIQUES (voir annexe):
annexe):
1) Profil énergétique simple :
Le profil énergétique, ou profil réactionnel, d’une
transformation représente l’évolution de l’énergie
potentielle du système au cours de son avancement
de l’état initial jusqu'à l’état final .
IL présente un maximum énergétique, une barrière
que doit franchir les réactifs pour que la réaction
aura lieu . L'apport d’énergie peut provenir de chocs
« efficaces » entre les entités présentes, sous l'effet de
l’agitation thermique , photochimique ou autres.
Le maximum énergétique "col énergétique" est appelé complexe activé, C.A., ou état de transition.
Il correspond à un arrangement spatial des atomes intermédiaire entre les réactifs et les produits. C'est
une espèce qui n'est ni isolable ni détectable au cours du mécanisme de structure hypothétique notée
(A….B….C) . Ea est appelée énergie potentielle d’activation.
Exemple 1 : la SN2
Exemple 2 : cassure d'une liaison:
la réaction est endothermique ; une molécule
énergétique (M*) appelée partenaire du choc
fourni l'énergie à la molécule :
A-B + M* ----> A + B + M
La formation de liaison est le processus inverse qui est exothermique , l'énergie libérée est absorbée
par un atome M appelée partenaire du choc:
A + B + M ----> A-B + M*
10 A.NARJIS CRMEF 2016-2017
2) Profil énergétique double :
Avec le mécanisme : A -----> B ----> C
la transformation globale de A en C se produit en deux étapes avec
apparition d’un IR . À chaque étape du mécanisme est associé le
franchissement d’une barrière énergétique.
L’intermédiaire réactionnel B correspond à un minimum d’énergie,
contrairement aux deux complexes activés. De manière générale,
tout minimum d’énergie sur le profil réactionnel autre que l’état
initial et l’état final est appelé IR .
L’IR est donc une espèce relativement stable, qui peut être isolée au cours de la transformation.
C’est la grande différence par rapport aux complexes activés qui sont des maxima énergétiques.
L’énergie de l’IR est supérieure à celles de l’état initial A et de l’état final C.
Les deux barrières énergétiques ont des valeurs très différentes : La disparition de B est beaucoup plus
rapide que sa formation. Cela justifie le fait qu’il ne s’accumule pas dans le milieu et reste en faible
quantité par rapport aux espèces A et C. On retrouve le principe de l’AEQS applicable IR.
Exemple : la SN1
11 A.NARJIS CRMEF 2016-2017
III) DIFFERENTS TYPES DE MECANISMES :
Suivant l’enchaînement des actes élémentaires lors du processus réactionnel, on peut distinguer
deux types de mécanisme :
– les mécanismes en séquence ouverte ou par stades ;
– les mécanismes en séquence fermée ou en chaîne.
1) Mécanisme par stade ( ou en séquence ouverte) ou en cascades .
Constitué d'un ensemble de processus élémentaire dans lesquelles tout intermédiaire formé dans une
étape sera consommé dans une autre sans être régénéré. Le mécanisme se déroule donc selon une
cascade de réactions successives.
Le passage du réactif au produit de fait selon une successions d'actes élémentaires ( renversable ou
non) se déroulant toujours dans le même ordre . On peut appliquer l'AECD à ce mécanisme .
Exemple : la réaction de substitution nucléophile ( SN1)
Equation bilan : RCl + OH − → ROH + Cl − .
k1
Mécanisme : RCl ⇌ R + + Cl −
k −1
k2
R + + OH − → ROH
Exemple 2 : décomposition thermique du diazote : N2O5 (g) -----> 1/2 O2 (g) + 2NO2(g)
Le mécanisme proposé est le suivant :
Montrer que la vitesse suit une loi cinetique d'ordre 1 . Exprimer la constante cinétique:
Loi de Van't Hoff:
12 A.NARJIS CRMEF 2016-2017
Les vitesses de formation et de disparition:
Approximation de l'état quasistationnaire:
Vitesse d'après l'équation bilan:
On trouve la loi de vitesse :
13 A.NARJIS CRMEF 2016-2017
2) Mécanisme en chaîne ( ou en séquence fermée).
Constitué d'un ensemble de processus élémentaire dans lesquelles certain intermédiaire formé dans
une étape sera consommé puis régénéré permettant ainsi la mise au place d'un processus cyclique.
Certaines étapes du mécanisme se répètent donc cycliquement indépendamment du premier
processus ( c'est pour cela qu'on l'appelée mécanisme en séquence fermé) .
Ce type de mécanisme est constitué de 3 étapes ( Initiation , propagation et rupture ).
Initiation (amorçage) : Formation du Per IR , amorcée par voie thermique ou photochimique
Propagation : Formation des produits et régénération des IR ;
Terminaison : Recombinaison et disparition des IR.
Exercice : Bromation méthane.
Soit la réaction entre le méthane et le brome dont le bilan est :
Le mécanisme chimique observé pour cette réaction est composé de 5 étapes élémentaires:
Ce mécanisme fait intervenir une étape d'activation par irradiation ultraviolette (photon hν) et une
étape de terminaison avec partenaire de choc (M). On admet que la première étape se fait avec une
constante de vitesse ka , proportionnelle aux photons efficaces. On suppose connue et constante la
concentration des partenaires de chocs [M] = [M]₀. On définit la vitesse de la réaction comme la
vitesse d'apparition de CH₃Br.
1. Nommer les différentes étapes du mécanisme. Comment qualifier ce mécanisme ?
2. Écrire la loi de van 't Hoff pour chaque étape.
. .
3. Établir la loi de vitesse pour cette réaction en appliquant l'AEQS à Br et CH3 .
4. La réaction admet-elle un ordre global ? Un ordre initial ? Quels sont les ordres partiels ?
5. Comment évolue la vitesse de réaction lorsque l'irradiation (donc ka) augmente ?
Solution :
1) La réaction élémentaire 1 est l'étape d'amorçage. Les étapes 2 - 3 - 4 sont des
propagations. L'étape 5 est la terminaison ; C'est un mécanisme en chaînes.
2) On note [X] la concentration de l'espèce X en mole/L. Les vitesses de réaction sont:
v1 = ka × [Br2] ,
v2 = k2 × [CH4] × [Br•] ,
v3 = k3 × [Br2] × [CH3•] ,
v4 = k4 × [HBr] × [CH3•] ,
v5 = k5 × [Br•]2 × [M] .
14 A.NARJIS CRMEF 2016-2017
3) On demande d’établir la loi de vitesse pour cette réaction et on nous a précisé que la
vitesse de la réaction est la vitesse d'apparition de CH₃Br.
On aura: + d[CH₃Br]/dt = v3 = k3 × [Br2] × [CH3•]
L' AEQS nous donne :
Comme [M] reste constante avec [M] ~ [M]0, alors on pose k5' = k5.[M] ~ k5.[M]0 . Soit:
On remplace la concentration des atomes Br• dans la deuxième relation:
d'où
On a alors,
4) Le mécanisme de la réaction est complexe et on n'a pas d'ordre cinétique.
Pour t = 0, on aura [HBr] = 0 et la vitesse initiale est alors:
On a donc un ordre partiel 1 pour le méthane et 0,5 pour le brome; ce qui donne un ordre
global de 1,5 pour la vitesse initiale (t=0).
5)
15 A.NARJIS CRMEF 2016-2017
C) LA CATALYSE:
CATALYSE:
La catalyse est classée parmi les facteurs cinétiques influençant sur la vitesse d’une transformation
chimique. On peut accélérer la vitesse d’une réaction en utilisant une substance appelée catalyseur.
I) GENERALITES :
1) Définitions:
Un catalyseur est une substance qui augmente la vitesse d'une réaction thermodynamiquement
possible sans intervenir dans l'équation bilan. Il est régénéré en fin de réaction et donc on l'utilise en
faible quantité . On distingue trois grands catégories :
Catalyse homogène : (réactifs + catalyseur dans la même phase liquide ou gazeuse) .
Catalyse hétérogène : (souvent le catalyseur est solide tandis que les réactifs et les produits sont
en phase gazeuses ou liquide) .
Catalyse enzymatique : (protéine ; molécule très grande, possèdent une cavité (site actif) dans
laquelle la réaction se déroule. La cavité est généralement spécifique à
une molécule d’un réactif donné (appelé substrat).
2) Mode d’action du catalyseur
Le catalyseur accélère la réaction en abaissant la
barrière énergétique à franchir. Le catalyseur offre
une autre voie ou un autre mécanisme réactionnel.
Le catalyseur n’apparaît pas dans le bilan de la
réaction. Celui-ci est donc inchangé de même pour
les grandeurs caractéristiques ∆rH., ∆rS., ∆rG. et en
particulier K(T). Le catalyseur permet juste
d’atteindre plus vite l’état d’équilibre.
Un catalyseur accélère aussi bien la transformation directe que la transformation inverse . Par exemple,
un catalyseur d’hydrogénation pourra également servir de catalyseur de déshydrogénation.
II) LES TROIS TYPES DE CATALYSEURS:
1) Catalyse homogène:
Le mécanisme en présence du catalyseur se produit en deux étapes, une première étape où celui-ci est
consommé, et une deuxième étape où il est régénéré. La concentration du catalyseur va donc intervenir
dans la vitesse de la réaction, c’est une caractéristique importante de la catalyse homogène.
Exemple de catalyses homogènes :
- catalyse acido-basique (réaction d’estérification catalysée par H2SO4) .
- catalyse redox (oxydation des ions iodure I- par les ions peroxodisulfate S2O82- par l'ion Fe2+).
- catalyse enzymatique présente dans les réactions biologiques ; Le catalyseur est alors une
protéine appelée enzyme. Son action est due à la présence d’une partie bien précise de la
molécule appelée site actif.
16 A.NARJIS CRMEF 2016-2017
2) Catalyse hétérogène:
2.1) Définition:
Il s’agit le plus souvent d’un catalyseur solide en contact avec un fluide, contenant les réactifs.
L’activité du catalyseur est liée à sa surface ; La réaction est d'autant plus rapide que la surface du
catalyseur est plus grande (poudres, fils métalliques , matériaux poreux, mousse ( pots catalytique
d'une voiture)).
Exemple : Hydrogénation de l’éthylène:
La catalyse hétérogène est très sélective. Dans le cas de réactions compétitives, on peut favoriser
l’une ou l’autre en employant le catalyseur approprié.
Exemple : La déshydratation ou la déshydrogénation catalytique d’un alcool par chauffage
en phase vapeur dépend de la nature du catalyseur solide utilisé :
2.2) Mode de fonctionnement :
Les molécules des réactifs se fixent à la surface du catalyseur par un phénomène d’adsorption.
Suivant le type d’interaction entre le catalyseur et les molécules réagissantes, on parle de :
– l’adsorption physique ou physisorption .
– l’adsorption chimique ou chimisorption.
La physisorption : se produit à basse température. Il y a une faible interaction entre les
molécules du fluide et le catalyseur. Ce sont des interactions de type van der Waals. Le phénomène
est réversible, l’adsorption et la désorption se produisent rapidement.
La chimisorption : se produit à température plus élevée. Il se forme une interaction
forte entre les molécules et le catalyseur, de véritables liaisons chimiques nouvelles. Ces
molécules adsorbées sont alors beaucoup plus réactives que dans le fluide.
Le mécanisme de l'adsorption peut être décomposé en trois étapes :
– l'adsorption des réactifs ;
– les réactions entre les réactifs adsorbés rendus plus actifs ;
– la désorption des produits obtenus.
diffusion des réactifs adsorption formation des produit désorption des produits
17 A.NARJIS CRMEF 2016-2017
Exemples de catalyses hétérogènes :
– catalyse redox : oxydation de l’ammoniac lors de la synthèse industrielle de l’acide
nitrique (catalyseur Pt)
hydrogénation du diazote lors de la synthèse industrielle de l’ammoniac
(catalyseur Feα)
oxydation du dioxyde de soufre lors de la synthèse industrielle de l’acide sulfurique
(catalyseur V2O5 : penta oxyde de vanadium)
– catalyse acido-basique : déshydratation d’un alcool en alcène (catalyseur Al2O3).
2.3) Autres applications de la catalyse hétérogène:
2.3.1) Hydrogénation catalytique des acides gras:
Les acides gras sont des acides carboxyliques : ils sont saturés lorsqu’ils ne contiennent que de
simples liaisons carbone-carbone et insaturés lorsqu’ils comptent au moins une double liaison. A
température ordinaire, les acides gras insaturés sont liquides (huiles) et les acides gras saturés sont
solides (graisses)
Des huiles peuvent être transformées en graisses par hydrogénation catalytique ( Nickel de Raney).
Cette opération est utilisée pour obtenir les margarines à partir d’huiles végétales.
2.3.2) Pot à catalyseur d'une voiture :
Les gaz d’échappement des moteurs à explosion contiennent des hydrocarbures non brûlés (HC : 0.5
- 1%), du monoxyde de carbone (CO: 0.1-6%) et des oxydes d’azote (NOx : 0.04 - 0.4 %). Leur
conversion en gaz non toxiques se fait sur des particules de Rh et de Pd (env. 2 g), dispersées sur
une grille d’alumine.
2 CO (g) + O2 (g) → 2 CO2 (g)
HC (g) + O2 (g) → CO2 (g), H2O (g)
2 CO (g) + 2 NO (g) → 2 CO2 (g) + N2 (g)
HC (g) + NO (g) → CO2 (g), N2 (g), H2O (g)
CO (g) + H2O (g) → CO2 (g) + H2 (g)
2 NO (g) + 2 H2 (g) → N2 (g) + 2 H2O (g)
Pour le bon fonctionnement du système, il faut un apport suffisant en oxygène .
18 A.NARJIS CRMEF 2016-2017
3) Catalyse enzymatique:
3.1) Définition:
Les enzymes sont protéines; molécules de masse molaire élevée qui catalysent des réactions
importantes en biologie et en biochimie . L'espèce sur laquelle réagit l'enzyme est appelée
substrat . Le comportement d'un très grand nombre d'enzyme est décrit par le mécanisme :
k1 k2
E + S ⇌ ES → P + S
k−1
L'enzyme E réagit avec le substrat S pour donner de manière réversible le complexe enzyme-
substrat (ES) . Ce complexe se décompose de manière irréversible pour donner le produit P et
régénère l'enzyme E
Produit
Substrat
site actif
Enzyme
Enzyme
Complexe
Enzyme-substrat
Dans le cas général , les vitesse des deux étapes ( formation et décomposition ) du complexe sont de
même ordre de grandeur , ES se décompose aussi rapidement qu'il se forme (état quasi-stationnaire)
On peut considérer sa concentration est faible et relativement constante .
d [ ES ]
= k1 [ E ][ S ] − k−1 [ ES ] − k2 [ ES ] ≈ 0
dt
d [ P] k2 [ E ]o [ S ]
On montre que : V = = avec [ E ]o , la concentration totale de l'enzyme
dt k −1 + k2
+ [S ]
k1
Cette équation est appelée équation de Michaelis-Menten.
k−1 + k2 [ E ][ S ]
On pose : K m = = appelée constante de Michaelis
k1 [ ES ]
k2
Si [S] << Km on aura une réaction du 1er ordre : V = [ E ]o [ S ] .
Km
Si [S] >> Km on aura une réaction d'ordre zéro : V = k2 [ E ]o = Vmax .
Vmax
Si [S] = Km on aura une réaction du 1er ordre : V = .
2
d [ P]
dt
Vmax
V max
2
Km
19 A.NARJIS CRMEF 2016-2017
3.2) Inhibition des enzymes:
Les inhibiteurs sont des substances successible de bloquer l'action des enzymes en fixant dessus de
façon irréversible . On distingue deux types :
Inhibiteur compétitif: ressemble au substrat et entre en compétition avec lui pour s'introduire dans
le site actif. Si le site actif est bloqué par un inhibiteur compétitif, l'enzyme ne peut plus fonctionner.
L'inhibiteur compétitif a souvent une action réversible. Il peut se retirer du site actif si sa
concentration devient faible dans le milieu. Beaucoup de poisons sont des inhibiteurs compétitifs
d'enzymes essentielles à la survie.
réaction
site actif pas de réaction
Inhibiteur
20 A.NARJIS CRMEF 2016-2017
Le cyanure est un inhibiteur compétitif d'une enzyme appelée cytochrome oxydase. Cette enzyme
est essentielle à la dernière étape de la respiration cellulaire. Sans elle, la respiration cesse, c'est la
mort!!
La neurotoxine s'explique par le blocage de la transmission du flux nerveux aux muscles . C'est
donc des poisons de catalyseur .
Inhibiteur incompétitif : Il n'entre pas en compétition avec un substrat sur son site de fixation. Il
ne se fixe jamais à l'enzyme libre mais seulement à l'enzyme complexée avec le substrat ES et
empêche la formation des produits. L'inhibiteur modifie la forme du site actif de l'enzyme, le site
devient inactif. L'enzyme a alors perdu ses propriétés catalytiques,
réaction
Inhibiteur
site inactif
S ne se
fixe pas
pas de réaction
3.3) Le cofacteur:
Un cofacteur est une substance simple organique ou inorganique qui rend une enzyme active en
transportant ou en complétant le substrat .
Beaucoup d’enzymes ont besoin de la présence de cofacteurs pour jouer leur rôle de catalyseur.
Ce sont souvent des ions comme le calcium, le fer, le magnésium ou le manganèse, qui se lient à
l’enzyme pour lui permettre d’acquérir sa forme fonctionnelle.
21 A.NARJIS CRMEF 2016-2017
Das könnte Ihnen auch gefallen
- Cinétique ChimiqueDokument10 SeitenCinétique Chimiquearfpower100% (2)
- Cours DR BENAMIRA MESSAOUD Cinétique Chimique Master 2 Chimie Des MatériauxDokument66 SeitenCours DR BENAMIRA MESSAOUD Cinétique Chimique Master 2 Chimie Des MatériauxamineNoch keine Bewertungen
- TD Cinétique Et Catalyse SMC5Dokument92 SeitenTD Cinétique Et Catalyse SMC5Regele ZăpeziiNoch keine Bewertungen
- Cinetique ExercicesDokument15 SeitenCinetique ExercicesAyyoub Dahbi100% (1)
- P2016 CM11 TP FasciculeDokument44 SeitenP2016 CM11 TP FasciculeRochdi BAATINoch keine Bewertungen
- Correction To CinetiqueDokument5 SeitenCorrection To CinetiquejaywalkNoch keine Bewertungen
- Etude Cinetique D'Une Reaction Du 2 Ordre TP N°1Dokument2 SeitenEtude Cinetique D'Une Reaction Du 2 Ordre TP N°1Ikram GrNoch keine Bewertungen
- TD N°2-Chapitre II. Mécanismes RéactionnelsDokument6 SeitenTD N°2-Chapitre II. Mécanismes RéactionnelsJojo BoubNoch keine Bewertungen
- TP N° 5 SolutionsDokument6 SeitenTP N° 5 SolutionsMohamed EL AmineNoch keine Bewertungen
- M28 Thermo TD3 CorrectionDokument3 SeitenM28 Thermo TD3 CorrectionHassan Driouach100% (1)
- Compte Rendu 2 RésolutionDokument5 SeitenCompte Rendu 2 Résolutionchouchou baNoch keine Bewertungen
- TD Cinetique ChimiqueDokument2 SeitenTD Cinetique Chimiquemomos55100% (3)
- TP PH Metre ATHIR - New1Dokument8 SeitenTP PH Metre ATHIR - New1samibenhabileNoch keine Bewertungen
- C03 Cinetique ReactionDokument2 SeitenC03 Cinetique ReactionmohNoch keine Bewertungen
- Chapitre II Influence Des Concentrations Et de La Température Sur La VitesseDokument4 SeitenChapitre II Influence Des Concentrations Et de La Température Sur La VitesseroffaaNoch keine Bewertungen
- TP Chimie 02Dokument6 SeitenTP Chimie 02Rayane BEKKOUCHENoch keine Bewertungen
- TP Electrochimie L3 PDFDokument1 SeiteTP Electrochimie L3 PDFmadNoch keine Bewertungen
- TP Chimie Analytique Et Instrumentale Manip1 FinalDokument16 SeitenTP Chimie Analytique Et Instrumentale Manip1 FinalHamed AbbassiNoch keine Bewertungen
- Vérification KDokument11 SeitenVérification KWassini BensNoch keine Bewertungen
- Chimie TD 3 Cinétique ChimiqueDokument4 SeitenChimie TD 3 Cinétique ChimiqueFranck Momo100% (1)
- FDS - TD Cinétique Chimique - 2013Dokument6 SeitenFDS - TD Cinétique Chimique - 2013Lenz Daniel Jean Paul100% (1)
- CONDUCTIMETRIE TPDokument11 SeitenCONDUCTIMETRIE TPOUMAIMA SAKHINoch keine Bewertungen
- MANGANIMÉTRIEDokument2 SeitenMANGANIMÉTRIEDiallo100% (1)
- Des Ex Cour de Chimie ElectrochimieDokument21 SeitenDes Ex Cour de Chimie ElectrochimieImene GhmrNoch keine Bewertungen
- Nombre de TransportDokument15 SeitenNombre de TransportČhįfaâ BęnNoch keine Bewertungen
- Méthodes Electrochimiques (Partie 2)Dokument12 SeitenMéthodes Electrochimiques (Partie 2)Lina BahazNoch keine Bewertungen
- Polycopie Travaux Pratique Chimie Organique III L3Dokument30 SeitenPolycopie Travaux Pratique Chimie Organique III L3rayanezianimalakNoch keine Bewertungen
- Fascicule TP2012-13Dokument58 SeitenFascicule TP2012-13Moustapha BelmoudenNoch keine Bewertungen
- BUT DE TP Determination de Lordre Dune RDokument7 SeitenBUT DE TP Determination de Lordre Dune RÃßdø SãñføürNoch keine Bewertungen
- Cinetique Tpn°1 2020 GP 2eme Annee LicenceDokument4 SeitenCinetique Tpn°1 2020 GP 2eme Annee LicenceChouYa OsNoch keine Bewertungen
- Compte Rendu TP2 Cinétique ChimiqueDokument12 SeitenCompte Rendu TP2 Cinétique ChimiquePONDIKPA KondiNoch keine Bewertungen
- Cryoscopie AlmemaDokument9 SeitenCryoscopie AlmemaCheikh Ismaïla BA0% (1)
- Cinetique en Phase LiquideDokument10 SeitenCinetique en Phase LiquideKARIMA BNoch keine Bewertungen
- Thermodynamique Des Solutions Master Chapitre2Dokument41 SeitenThermodynamique Des Solutions Master Chapitre2Abde Tam100% (2)
- Chapitre 5 - Oxydoréduction - PilesDokument12 SeitenChapitre 5 - Oxydoréduction - PilesBeatrice Florin100% (3)
- TP Cinétique 2023 L2Dokument5 SeitenTP Cinétique 2023 L2dihia didaNoch keine Bewertungen
- Grandeurs Molaires PartiellesDokument53 SeitenGrandeurs Molaires Partiellesmradid7930100% (2)
- Chimie B Chap8 Titrage - Acidobasique PDFDokument6 SeitenChimie B Chap8 Titrage - Acidobasique PDFMouloud IssaadNoch keine Bewertungen
- TP s6 2017 2018 PR .Guenoun Ferhat - PR Kholtei AbdelilahDokument22 SeitenTP s6 2017 2018 PR .Guenoun Ferhat - PR Kholtei AbdelilahBella BenzNoch keine Bewertungen
- Master Cmba: Rapport de Travaux Pratiques: SYNTHESE TOTALEDokument15 SeitenMaster Cmba: Rapport de Travaux Pratiques: SYNTHESE TOTALEAli BoutaharNoch keine Bewertungen
- Extraction D Especes Chimiques Exercices CorrigesDokument2 SeitenExtraction D Especes Chimiques Exercices CorrigesMalika BENHAMADANoch keine Bewertungen
- Site TS C 12 CatalyseDokument3 SeitenSite TS C 12 CatalysePecorellaNoch keine Bewertungen
- Melange Ethanol EauDokument8 SeitenMelange Ethanol EauImi LouzaNoch keine Bewertungen
- Potentiel Chimique ExercicesDokument4 SeitenPotentiel Chimique ExercicesYassine RakchoNoch keine Bewertungen
- Expose Usto - Version 1Dokument8 SeitenExpose Usto - Version 1riadNoch keine Bewertungen
- TP .Avancement .4sc - Exp.2022Dokument6 SeitenTP .Avancement .4sc - Exp.2022Med Brini100% (1)
- TP Chimie n1Dokument2 SeitenTP Chimie n1Oussoufi Mze Kaanbi100% (2)
- Synthese Du Diphenyl-1,3 Epoxypropan-1-OneDokument5 SeitenSynthese Du Diphenyl-1,3 Epoxypropan-1-OneHoussem Eddine KAFI100% (1)
- Chapitre 4 Cinétique ÉlectrochimiqueDokument17 SeitenChapitre 4 Cinétique ÉlectrochimiqueClosed WayNoch keine Bewertungen
- TP4 La Reaction Persulfate IodureDokument4 SeitenTP4 La Reaction Persulfate IodureSellam Anis100% (1)
- Catalyse Hétérogène Partie3Dokument25 SeitenCatalyse Hétérogène Partie3abdarxNoch keine Bewertungen
- TP Volume MolaireDokument9 SeitenTP Volume MolaireTaourite AmelNoch keine Bewertungen
- TP Dosage Complexometrie1Dokument4 SeitenTP Dosage Complexometrie1Sellam AnisNoch keine Bewertungen
- Cinetique ChimiqueDokument27 SeitenCinetique Chimiquelopir120100% (6)
- Applications de la spectrophotomérie en phytochimie: sciencesVon EverandApplications de la spectrophotomérie en phytochimie: sciencesNoch keine Bewertungen
- CP I Chapitre I. Vitesse Et Lois de Vitesse 1 1Dokument17 SeitenCP I Chapitre I. Vitesse Et Lois de Vitesse 1 1Section E GPNoch keine Bewertungen
- Cinétique Chimique MPSI Et MPDokument23 SeitenCinétique Chimique MPSI Et MPmomoadamso07Noch keine Bewertungen
- La Cinétique ChimiqueDokument7 SeitenLa Cinétique ChimiqueAS asNoch keine Bewertungen
- Chapitre 1 Cours Cinétique - 2021Dokument40 SeitenChapitre 1 Cours Cinétique - 2021Li NaNoch keine Bewertungen
- M1 CinetiqueDokument39 SeitenM1 CinetiquePenda FayeNoch keine Bewertungen
- Exercices Python3Dokument49 SeitenExercices Python3Devin Ramos100% (1)
- dm13 PolynomesDokument6 Seitendm13 Polynomesياسين السعدانيNoch keine Bewertungen
- Sec CCP 2007 Phy2c MP PDFDokument19 SeitenSec CCP 2007 Phy2c MP PDFabdelbarrNoch keine Bewertungen
- TP Goniometre CorrectionDokument4 SeitenTP Goniometre CorrectionMatthieu Caron100% (7)
- Capes 2010 M2 EnonceDokument7 SeitenCapes 2010 M2 Enonceياسين السعدانيNoch keine Bewertungen
- DM12b PolyDokument8 SeitenDM12b Polyياسين السعدانيNoch keine Bewertungen
- EzgrDokument1 SeiteEzgrياسين السعدانيNoch keine Bewertungen
- Calcul D'intégrale 1Dokument2 SeitenCalcul D'intégrale 1Karime AmineNoch keine Bewertungen
- JKHGDokument1 SeiteJKHGياسين السعدانيNoch keine Bewertungen
- Calcul D'intégrale 1Dokument2 SeitenCalcul D'intégrale 1Karime AmineNoch keine Bewertungen
- PB 096Dokument1 SeitePB 096ToufikJalalEddineNoch keine Bewertungen
- Centrale MP 2007 - Epreuve de Physique-Chimie: Problème 1: Analyseur de Monoxyde de CarboneDokument10 SeitenCentrale MP 2007 - Epreuve de Physique-Chimie: Problème 1: Analyseur de Monoxyde de CarboneMihnea GamanNoch keine Bewertungen
- CNC MP 2009 Physique 2 CorrigeDokument7 SeitenCNC MP 2009 Physique 2 Corrigeياسين السعدانيNoch keine Bewertungen
- Génie Chimique Partie II-2Dokument44 SeitenGénie Chimique Partie II-2khaoula khaoulaNoch keine Bewertungen
- EXERCICEs CinétiqDokument8 SeitenEXERCICEs Cinétiqhicham bouatlaouiNoch keine Bewertungen
- Td-Évolution Temporelle D'un Systeme Et Mecanisme Reactionnel - Prepa-Mpsi 2023-2024Dokument2 SeitenTd-Évolution Temporelle D'un Systeme Et Mecanisme Reactionnel - Prepa-Mpsi 2023-2024hermannibetowaNoch keine Bewertungen
- TD (1) Cinétique ChimieDokument3 SeitenTD (1) Cinétique ChimieAnass ZaouiNoch keine Bewertungen
- Bioch1an16-Enzymologie GhoualiDokument67 SeitenBioch1an16-Enzymologie Ghoualiahlemm100% (1)
- Cine 4Dokument4 SeitenCine 4AliAliNoch keine Bewertungen
- M1 CinetiqueDokument39 SeitenM1 CinetiquePenda FayeNoch keine Bewertungen
- TD Meca Reactionnelscorrige PDFDokument13 SeitenTD Meca Reactionnelscorrige PDFAyyoub Dahbi100% (1)
- TD GRC 2 HydrolyseDokument6 SeitenTD GRC 2 HydrolyseChristian AmadouNoch keine Bewertungen
- CoursExercices 01Dokument65 SeitenCoursExercices 01phytanja100% (4)
- Cinetique CDokument6 SeitenCinetique CAyoub KhoyaNoch keine Bewertungen
- Vitesse Et Lois Des VitessesDokument10 SeitenVitesse Et Lois Des Vitessesamiira bouzouadaNoch keine Bewertungen
- Travaux Dirigés Série 2Dokument1 SeiteTravaux Dirigés Série 2abdell bmqNoch keine Bewertungen
- TD N1 Enzymologie PR ChernaneDokument2 SeitenTD N1 Enzymologie PR ChernaneZineb Dahmani100% (1)
- Fiche TD Enzymologie Réactions Enzymatiques - CopieDokument2 SeitenFiche TD Enzymologie Réactions Enzymatiques - Copiebenali anfalNoch keine Bewertungen
- 7 Mecanismes Bibi PDFDokument9 Seiten7 Mecanismes Bibi PDFOussama IdrissNoch keine Bewertungen
- Cinétique EnzymatiqueDokument3 SeitenCinétique EnzymatiqueChaka TraoreNoch keine Bewertungen
- Examen RPADokument13 SeitenExamen RPALENOVO PCNoch keine Bewertungen
- Cours - MAOUCHE Nassima - Réacteurs Homogènes IdéauxDokument73 SeitenCours - MAOUCHE Nassima - Réacteurs Homogènes IdéauxFaiza FaizaNoch keine Bewertungen
- Examen de Cin Et Cat Avec Correction Session Normale 2018-2019Dokument6 SeitenExamen de Cin Et Cat Avec Correction Session Normale 2018-2019Chai Mae100% (1)
- Ds 2 CorrigéDokument22 SeitenDs 2 CorrigéSouad BouafiaNoch keine Bewertungen
- TDmecanismeDokument2 SeitenTDmecanismeSouad Bouafia100% (1)
- (PDF) Etude Experimentale de La Phosphataase Alcaline - Enzymologie 2 PDFDokument17 Seiten(PDF) Etude Experimentale de La Phosphataase Alcaline - Enzymologie 2 PDFRastateNoch keine Bewertungen
- CHAPITRE II - Réacteurs Chimiques - M1 G.Pétr PDFDokument5 SeitenCHAPITRE II - Réacteurs Chimiques - M1 G.Pétr PDFAmel ChalabiNoch keine Bewertungen
- C R - TP-II-S BelkessamDokument6 SeitenC R - TP-II-S BelkessamAmmar GouasmiaNoch keine Bewertungen
- Chap5 Reacteurouvert1solutionDokument14 SeitenChap5 Reacteurouvert1solutionMokhtaria ReguigNoch keine Bewertungen
- Chapitre 02 Cinétique EnzymatiqueDokument5 SeitenChapitre 02 Cinétique Enzymatiqueamina44Noch keine Bewertungen
- CinétiqueDokument112 SeitenCinétiqueRodolphe YoboNoch keine Bewertungen
- Correction TD TM4Dokument2 SeitenCorrection TD TM4Clovis KamNoch keine Bewertungen
- TDBR-P21 Corrige1Dokument11 SeitenTDBR-P21 Corrige1Alejandro Domingo NúñezNoch keine Bewertungen