Beruflich Dokumente
Kultur Dokumente
05 Spectroscopie Par Resonance Magnetique Nucleaire (RMN 13C)
Hochgeladen von
Hamza El-ghrirCopyright
Verfügbare Formate
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
Verfügbare Formate
05 Spectroscopie Par Resonance Magnetique Nucleaire (RMN 13C)
Hochgeladen von
Hamza El-ghrirCopyright:
Verfügbare Formate
Compléments - Chapitre 5
Spectroscopie
Spectroscopie par résonance magnétique nucléaire (RMN 13C)
Tandis que la spectroscopie RMN 1H fournit des données sur la disposition des atomes
d'hydrogène dans une molécule, la spectroscopie RMN 13C nous renseigne sur le
squelette carboné. L’isotope le plus abondant du carbone, soit le carbone 12, ne possède
pas de spin nucléaire à l’inverse du carbone 13. Or, le carbone 13 ne constitue que 1,1 %
des atomes de carbone trouvés dans la nature. Par ailleurs, la différence d’énergie entre
les états de spin de haut et de bas niveau du 13C est très petite. Pour ces deux raisons, les
spectromètres RMN 13C doivent être extrêmement sensibles. Heureusement, les
spectromètres RMN-TF (à transformée de Fourier) à haut champ d’aujourd’hui sont assez
puissants et sensibles ; c’est pourquoi la spectroscopie RMN 13C est devenue une
technique courante.
Une molécule m’a dit…
La RMN en biologie et en médecine
L’imagerie par résonance magnétique (IRM) est une technologie utilisée pour
produire une image du cerveau.
Dans le chapitre 5 et ses compléments, nous nous sommes arrêtés à présenter les
rudiments de la spectroscopie RMN et des exemples de détermination de structure.
Toutefois, en appliquant la technologie des ordinateurs, particulièrement celle des
microprocesseurs, à l’instrumentation RMN, le domaine s’est rapidement développé et de
nombreuses techniques de pointes se sont ajoutées*. Par exemple, il est possible de
produire des spectres en faisant varier la température (de −180 °C à 200 °C) et de
quantifier ainsi la vitesse de phénomènes comme la rotation autour des liaisons simples,
le basculement des conformations chaises du cyclohexane, l’inversion de l’azote dans les
amines et les réactions radicalaires (voir l’halogénation radicalaire au chapitre 6).
*Pour d’excellentes descriptions de ces techniques, voir :Mohan, J. Organic Spectroscopy, 2ème édition
Harrow, U.K., Alpha Science International Ltd., 2004.
Chimie organique 1 – Chapitre 5 – Complément © 2008 Les Éditions de la Chenelière inc. 1
À l’aide d’autres techniques, il est possible d’obtenir non seulement des spectres 13C pour
tous les atomes de carbone d’une molécule, mais aussi ceux des groupes CH3 uniquement
(ou des groupes CH2 ou CH), ce qui facilite considérablement la détermination de la
structure des molécules biologiques complexes.
Certaines autres techniques permettent de localiser les groupes voisins les uns des autres
dans l’espace au sein d’une même molécule, malgré leur éloignement dans la chaîne
carbonée, ce qui s’avère précieux pour étudier la conformation des molécules complexes.
On a maintenant réalisé le plein potentiel de la spectroscopie RMN pour contourner
certaines difficultés en biologie et en médecine. En effet, les appareils sont désormais
suffisamment sensibles pour analyser des liquides biologiques entiers comme l’urine, le
plasma sanguin, le sperme, le liquide céphalo-rachidien et les liquides oculaires. La
protéine créatinine, par exemple, est un métabolite normal excrété dans l’urine à une
concentration de l’ordre du millimolaire. Les singulets, correspondant à ses groupes CH3
(δ = 3,1 ppm) et CH2 (δ = 4,2 ppm), sont facilement observables à cette faible
concentration à l’aide d’un spectromètre à haute résolution (500 MHz), malgré la
présence de tous les autres constituants de l’urine. Sa concentration, qui peut être mesurée
en quelques minutes, est un bon indicateur de la fonction rénale. La spectroscopie RMN
sert aussi à déceler les maladies héréditaires du métabolisme dans l’urine des nourrissons.
CH3
N
NH
H2C C
C NH
créatinine
D’autres liquides biologiques fournissent aussi des renseignements utiles en médecine. La
surveillance continue de la présence des lipoprotéines de faible et de haute densité dans le
plasma sanguin permet de comprendre l’évolution des maladies cardiaques. L’analyse du
sperme pourrait servir à traiter les problèmes d’infertilité. Les spectres RMN du liquide
céphalo-rachidien des nourrissons sont étudiés par les neurologues et révèleront peut-être
de nouvelles pistes sur les troubles du cerveau**.
Le 31P, le 23Na et le 19F figurent parmi les noyaux ayant un spin et jouant un rôle
important en biologie. Des appareils ont été développés pour obtenir des spectres RMN
de parties anatomiques intactes chez l’humain et l’animal. Par exemple, des spectres 31P
d’un muscle de l’avant-bras d’un humain (l’avant-bras est placé directement dans le
champ magnétique) mesurés avant, pendant et après un exercice ont permis de suivre
dans le temps plusieurs constituants du tissu musculaire contenant du phosphore dont
notamment l’adénosine triphosphate (ATP), la phosphocréatine et le phosphate
inorganique. En comparant les variations de concentration de ces constituants chez des
** Pour de l’information supplémentaire, voir : Bell, J. D., J. C. Brown et P. J. Sadler. « RMN spectroscopy
of Body Fluids », Chemistry in Britain, 1988, p. 1021-1024.
Chimie organique 1 – Chapitre 5 – Complément © 2008 Les Éditions de la Chenelière inc. 2
gens normaux par rapport aux patients souffrant de maladies musculaires, on peut en
apprendre plus sur la nature de la maladie et concevoir des traitements†. En RMN
topique, l’aimant de l’appareil est amené jusqu’à l’objet d’étude et non l’inverse. Une
sorte de sonde magnétique placée sur l’objet induit alors une résonance des molécules
situées en surface et c’est ainsi qu’on peut obtenir des spectres 1H, 13C ou 31P de
molécules in vivo. Cette technique a été employée, par exemple, pour observer les effets
de divers médicaments sur le métabolisme.
L’imagerie par résonance magnétique (IRM) est une technique utilisée sur des patients
en milieu hospitalier depuis le milieu des années 1980. Elle permet d’obtenir des images
de l’intérieur de parties corporelles entières et offre plusieurs avantages par rapport aux
rayons X. Pour les uns, elle est beaucoup moins dangereuse puisqu’elle n’endommage
pas les tissus par les radiations. Pour les autres, elle donne des images claires des tissus
mous, ce qui est très difficile avec les rayons X. Comment l’IRM fonctionne-t-elle ? Un
grand pourcentage du corps humain est constitué d’eau. Dans la plupart des techniques
d’IRM, on mesure le spectre 1H de l’eau de divers tissus (le 31P est aussi employé) pour
créer des images. Toutefois, l’aimant doit être très gros : son diamètre intérieur doit être
d’au moins 25 cm pour que la tête d’un humain puisse y être logée, voire même
l’organisme entier ! Heureusement, le champ magnétique n’a pas besoin d’être uniforme
comme c’est le cas lorsqu’on détermine la structure à l’aide de la RMN à haute
résolution, si bien qu’il est concevable de construire de tels aimants. La présence d’un
gradient de champ plutôt que d’un champ uniforme est cruciale. L’intensité du champ
peut aussi être considérablement plus faible que celle utilisée en recherche, ce qui est une
chance vu le coût élevé de ces gros aimants.
La durée d’une séance d’IRM varie de 30 secondes à 10 minutes, avec une moyenne
d’environ 2 minutes. Les images sont constituées en choisissant des coupes dans
différents plans du corps ou des images en trois dimensions. L’illustration au début de la
présente rubrique montre l’image d’un cerveau humain obtenue par IRM.
La principale utilité de l’IRM est sans contredit le diagnostic médical, mais l’IRM peut
notamment servir en science des aliments pour évaluer les conditions nécessaires à la
cueillette, au stockage et à la mise en marché des aliments, en agriculture pour étudier la
germination des graines, et dans le bâtiment lorsqu’il s’agit d’évaluer la concentration et
la distribution de l’eau dans le bois de charpente‡.
† Pour de plus amples détails, voir :
Radda, G. K. « The Use of RMN Spectroscopy for the Understanding of Disease », Science, 1986, 233, p.
640-645.
‡Pour en savoir plus sur l’IRM, voir :
Morris, P. G. Nuclear Magnetic Resonance in Medicine and Biology, Oxford, England, Clarendon Press,
1986.
Ross R., B. Goodpaster, D. Kelley et F. Boada. « Magnetic resonance imaging in human body composition
research. From quantitative to qualitative tissue measurement », Annals of the New York Academy of
Sciences, 2000, 12(7), p. 904.
Chimie organique 1 – Chapitre 5 – Complément © 2008 Les Éditions de la Chenelière inc. 3
La résonance magnétique nucléaire, découverte par des physiciens, a été développée par
des chimistes et elle est aujourd’hui mise en application par des biologistes et d’autres
scientifiques. À ses débuts, nul ne pouvait soupçonner les bienfaits de ses applications.
Son histoire démontre bien qu’il peut être très sage de s’engager en recherche
fondamentale sans se préoccuper immédiatement des applications pratiques.
Les spectres du carbone 13 diffèrent des spectres du 1H sur plusieurs points. Les
déplacements chimiques (δ) en RMN 13C sont plus étendus que ceux de la RMN 1H. Ces
déplacements sont mesurés à partir du même composé de référence, le TMS, dont tous les
atomes de carbone méthyliques sont équivalents et produisent un signal bien défini. Les
déplacements chimiques du 13C sont aussi mesurés en unités de δ, mais ils apparaissent
habituellement dans la région située environ de 0 ppm à 200 ppm vers les champs plus
faibles par rapport au TMS (au lieu d’une plus petite région variant de 0 ppm à 13 ppm
pour le 1H). Grâce à cette gamme étendue de déplacements chimiques, les spectres 13C
sont moins complexes que les spectres 1H.
À cause de la rareté naturelle du 13C, la probabilité de rencontrer deux atomes de 13C
adjacents dans une même molécule est faible. C’est la raison pour laquelle le couplage
spin–spin 13C–13C n’a habituellement pas lieu. Cet état de fait simplifie les spectres 13C.
En revanche, le couplage spin–spin 13C–1H peut survenir. On peut prendre le balayage
d’un spectre de manière à ce que le couplage figure ou non sur le tracé, selon les besoins.
La figure 5.a présente le spectre RMN 13C du butan-2-ol mesuré avec et sans couplage
13
C–1H. Le spectre sans couplage 1H (appelé spectre avec découplage du proton)
présente quatre singulets bien définis, un pour chacun des types d’atomes de carbone. Le
signal de l’atome de carbone portant le groupe hydroxyle apparaît à des champs plus
faibles (δ = 69,3 ppm), et les signaux des deux atomes de carbone méthyliques sont bien
séparés (δ = 10,8 ppm et 22,9 ppm). Dans le spectre avec couplage 13C–1H, la règle n + 1
s’applique. Le signal de chaque type de noyau de 13C est scindé à cause des noyaux de 1H
qui leur sont directement liés. Le signal des deux groupes CH3 est un quadruplet (trois
atomes d'hydrogène, par conséquent, n + 1 = 4), l’atome de carbone du CH2 donne un
triplet et celui du CH un doublet.
Remarque : Dans un spectre RMN 13C avec découplage du proton, chaque type d’atome de
carbone est représenté par un singulet.
Chimie organique 1 – Chapitre 5 – Complément © 2008 Les Éditions de la Chenelière inc. 4
Figure 5.a Spectre RMN 13C du butan-2-ol avec (en haut) et sans (en bas) couplage
13
C–1H. Les valeurs de δ sont affichées dans le spectre du bas. Le solvant
utilisé est le CDCl3.
Chimie organique 1 – Chapitre 5 – Complément © 2008 Les Éditions de la Chenelière inc. 5
Exemple 5.a
Décrivez le spectre RMN 13C du CH3CH2OH.
Solution
Le spectre RMN 13C avec découplage 13C–1H est constitué de deux signaux, car deux
atomes de carbone non équivalents sont présents (leur signal correspond à
δCH3 = 18,2 ppm et δCH2 = 57,8 ppm). Sans le découplage 13C–1H, le signal à
δ = 18,2 ppm se manifeste par un quadruplet (trois H liés au C) et celui qui est à
δ = 57,8 ppm par un triplet (2 H liés au C).
Exercice 5.a
Quelles sont les principales caractéristiques du spectre RMN 13C de CH3CH2CH2OH ?
Exercice 5.b
13
À combien de signaux peut-on s’attendre dans le spectre RMN C avec découplage du
proton du :
a) 2-méthylpropan-2-ol ? c) 2-méthylpropan-1-ol ?
b) cyclopentanone ? d) cis-1,3-diméthylcyclopentane ?
Solutionnaire des exercices du complément
5.a. Le spectre sans couplage avec les hydrogènes présente trois signaux sous forme de
singulets dont les déplacements chimiques sont :
δ =65 ppm δ =32 ppm δ = 11 ppm
CH3 CH2 CH2 OH
3 2 1
Le spectre avec couplage des hydrogènes présente trois signaux, dont les
déplacements chimiques sont les mêmes que pour le spectre RMN 13C sans
couplage, mais où la multiplicité change. En effet, les signaux du carbone 1 et du
carbone 2 sortent sous la forme d’un triplet et celui du carbone 3 sous la forme
d’un quadruplet, respectant ainsi la règle du n + 1.
5.b a) Deux signaux seront observés, un pour les trois carbones C du groupement
méthyle et l’autre pour le carbone C lié à l’oxygène :
CH3
H3C C OH
CH3
Chimie organique 1 – Chapitre 5 – Complément © 2008 Les Éditions de la Chenelière inc. 6
b) Trois signaux seront observés :
O
C
C C
C C
c) Trois signaux seront observés :
CH3 CH CH2 OH
CH3
d) Quatre signaux seront observés:
CH3
C
C C
C C
CH3
Chimie organique 1 – Chapitre 5 – Complément © 2008 Les Éditions de la Chenelière inc. 7
Das könnte Ihnen auch gefallen
- TP CPG15Dokument15 SeitenTP CPG15ismail bd100% (17)
- Techniques D'analyseDokument7 SeitenTechniques D'analysesusCities75% (4)
- TP CPG15Dokument15 SeitenTP CPG15ismail bd100% (17)
- TP CPG15Dokument15 SeitenTP CPG15ismail bd100% (17)
- TP CPG15Dokument15 SeitenTP CPG15ismail bd100% (17)
- Techniques D'analyseDokument7 SeitenTechniques D'analysesusCities75% (4)
- Incertitudes Lors D'un Dosage Acide BaseDokument11 SeitenIncertitudes Lors D'un Dosage Acide BaseHamza El-ghrirNoch keine Bewertungen
- Déchets SolidesDokument39 SeitenDéchets SolidesYasmine Cohen100% (2)
- La Gestion Des DéchetsDokument10 SeitenLa Gestion Des DéchetsLuca Cantarella100% (1)
- 04-Gestion Des DechetsDokument65 Seiten04-Gestion Des DechetsFatima Zahra Rarhoute0% (1)
- La Gestion Des DéchetsDokument10 SeitenLa Gestion Des DéchetsLuca Cantarella100% (1)
- Chimie: - Chimie en Solution AqueuseDokument35 SeitenChimie: - Chimie en Solution AqueuseAyoub Maverick100% (1)
- La Gestion Des DéchetsDokument10 SeitenLa Gestion Des DéchetsLuca Cantarella100% (1)
- Incertitudes Lors D'un Dosage Acide BaseDokument11 SeitenIncertitudes Lors D'un Dosage Acide BaseHamza El-ghrirNoch keine Bewertungen
- 4-Suite Réaction de Complexation Et de PrécipitationDokument11 Seiten4-Suite Réaction de Complexation Et de PrécipitationHamza El-ghrirNoch keine Bewertungen
- La Pratique D'audit Interne PDFDokument120 SeitenLa Pratique D'audit Interne PDFMimi Meriem100% (9)
- Incertitudes Lors D'un Dosage Acide BaseDokument11 SeitenIncertitudes Lors D'un Dosage Acide BaseHamza El-ghrirNoch keine Bewertungen
- Chapitre 2 Erreurs MesuresDokument9 SeitenChapitre 2 Erreurs MesuresyayaNoch keine Bewertungen
- Chapitre 2 Erreurs MesuresDokument9 SeitenChapitre 2 Erreurs MesuresyayaNoch keine Bewertungen
- Chapitre 2 Erreurs MesuresDokument9 SeitenChapitre 2 Erreurs MesuresyayaNoch keine Bewertungen
- Chimie: - Chimie en Solution AqueuseDokument35 SeitenChimie: - Chimie en Solution AqueuseAyoub Maverick100% (1)
- Chimie: - Chimie en Solution AqueuseDokument35 SeitenChimie: - Chimie en Solution AqueuseAyoub Maverick100% (1)
- Chimie: - Chimie en Solution AqueuseDokument35 SeitenChimie: - Chimie en Solution AqueuseAyoub Maverick100% (1)
- La Pratique D'audit Interne PDFDokument120 SeitenLa Pratique D'audit Interne PDFMimi Meriem100% (9)
- 02 Rousseau PDFDokument95 Seiten02 Rousseau PDFchmimoy4421Noch keine Bewertungen
- Chimie: - Chimie en Solution AqueuseDokument35 SeitenChimie: - Chimie en Solution AqueuseAyoub Maverick100% (1)
- Chimie: - Chimie en Solution AqueuseDokument35 SeitenChimie: - Chimie en Solution AqueuseAyoub Maverick100% (1)
- Chimie: - Chimie en Solution AqueuseDokument35 SeitenChimie: - Chimie en Solution AqueuseAyoub Maverick100% (1)
- Chimie: - Chimie en Solution AqueuseDokument35 SeitenChimie: - Chimie en Solution AqueuseAyoub Maverick100% (1)
- Chimie: - Chimie en Solution AqueuseDokument35 SeitenChimie: - Chimie en Solution AqueuseAyoub Maverick100% (1)
- 55-1-2 PhysicsDokument15 Seiten55-1-2 PhysicsAli GadaNoch keine Bewertungen
- Modélisation en 2 Dimensions D'une Poutre de Forme Rectangulaire Trouée, Homogène Et Isotrope en Élastoplasticité Sous Sollicitation StatiqueDokument8 SeitenModélisation en 2 Dimensions D'une Poutre de Forme Rectangulaire Trouée, Homogène Et Isotrope en Élastoplasticité Sous Sollicitation StatiqueYOUNES KABBAJNoch keine Bewertungen
- Etude Des Pendules Couplés Par Une Barre de Torsion: I-But Du TravailDokument5 SeitenEtude Des Pendules Couplés Par Une Barre de Torsion: I-But Du TravailSamado Tips46Noch keine Bewertungen
- Exercice 1Dokument6 SeitenExercice 1Houssam FerrahNoch keine Bewertungen
- WWW - Cours Gratuit - Com Id 10654Dokument87 SeitenWWW - Cours Gratuit - Com Id 10654Zakaria HaouariNoch keine Bewertungen
- Dans Les Secrets de L UniversDokument165 SeitenDans Les Secrets de L UniversNihad FarahNoch keine Bewertungen
- Cours S4 Edp 08Dokument81 SeitenCours S4 Edp 08Guy Gildas DjemNoch keine Bewertungen
- 636116bfcb71b - Magazine1 ÉnoncéDokument5 Seiten636116bfcb71b - Magazine1 ÉnoncéAmine MohamedNoch keine Bewertungen
- Correction Examen PC Juin 2016 2bac SVT FRDokument7 SeitenCorrection Examen PC Juin 2016 2bac SVT FRhassan ibnahmadNoch keine Bewertungen
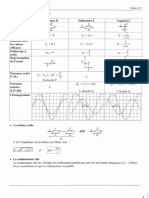
- Formulaire Dipoles ParfaitsDokument1 SeiteFormulaire Dipoles ParfaitsDavid100% (1)
- Chap I I Biomedical eDokument26 SeitenChap I I Biomedical eZOUHAIR KADDIOUINoch keine Bewertungen
- Chapitre1-Vecteurs Torseurs PDFDokument19 SeitenChapitre1-Vecteurs Torseurs PDFIlies GourriNoch keine Bewertungen
- Ens ScientDokument1 SeiteEns ScientfachaferreroNoch keine Bewertungen
- S2 1011 Mecanique Des Fluides TD CorrectionDokument9 SeitenS2 1011 Mecanique Des Fluides TD Correctiontarif ashtarNoch keine Bewertungen
- RPFE (Récupération de L'énergie Biomécanique) 2023Dokument38 SeitenRPFE (Récupération de L'énergie Biomécanique) 2023Loffy AyouNoch keine Bewertungen
- M Ecanique Quantique II - Corrig e S Erie 2: 1 Delta de Dirac IDokument9 SeitenM Ecanique Quantique II - Corrig e S Erie 2: 1 Delta de Dirac Iaba armelNoch keine Bewertungen
- Correction Ex1 - TD2 Cinématique FST-BM 20-21Dokument3 SeitenCorrection Ex1 - TD2 Cinématique FST-BM 20-21Oussama SafiNoch keine Bewertungen
- Les Ondes Mécaniques Progressives PDFDokument6 SeitenLes Ondes Mécaniques Progressives PDFMarøøen Bouabid100% (2)
- TD1Dokument1 SeiteTD1DjamalNoch keine Bewertungen
- QCM Phisique-ChimieDokument2 SeitenQCM Phisique-ChimieklowkerNoch keine Bewertungen
- B00U9J23CUDokument10 SeitenB00U9J23CUMohammadNoch keine Bewertungen
- C4 2Dokument22 SeitenC4 2Hoang-Vu BuiNoch keine Bewertungen
- Programme Instrumentation Et Métrologie LEEA2 - S3 PDFDokument2 SeitenProgramme Instrumentation Et Métrologie LEEA2 - S3 PDFParfumerie Actu'ElleNoch keine Bewertungen
- Les Transformations PhysiquesDokument6 SeitenLes Transformations Physiquesbcmdata bcmdata100% (1)
- Mounir Desité ApparenteDokument5 SeitenMounir Desité ApparenteMounir Alcapone100% (3)
- Chap M2Dokument33 SeitenChap M2Kader MilanoNoch keine Bewertungen
- Control Non DestructifDokument7 SeitenControl Non Destructifhouyam hamdiNoch keine Bewertungen
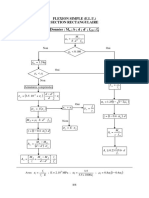
- Organigrame BaelDokument5 SeitenOrganigrame BaelKaram HoussamNoch keine Bewertungen
- FT Vide InertieDokument5 SeitenFT Vide InertielaurynNoch keine Bewertungen