Beruflich Dokumente
Kultur Dokumente
Activación de Linfocitos
Hochgeladen von
elizabeth890716Originaltitel
Copyright
Verfügbare Formate
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
Verfügbare Formate
Activación de Linfocitos
Hochgeladen von
elizabeth890716Copyright:
Verfügbare Formate
Activacin de linfocitos
L. Castro, L. Montes, M. Cobo y J. Pea
Una vez que los linfocitos reconocen mediante sus receptores de membrana las estructuras especficas a travs de las interacciones moleculares adecuadas, se inicia el proceso de activacin de los mismos. Este proceso implica una serie de eventos en cadena que se inician en la membrana celular, prosiguen en el citoplasma y terminan en el ncleo. En este captulo abordaremos el estudio de todo lo referente a la activacin de los principales linfocitos implicados en la respuesta inmune, como son: -- Los linfocitos T -- Los linfocitos B -- Las clulas NK De esta manera despus podremos estudiar con detalle la respuesta innata, humoral y celular.
Activacin de linfocitos T
La activacin de los linfocitos T se inicia cuando el receptor de los linfocitos T (TCR) reconoce a un pptido transportado por la molcula HLA. La unin entre el TCR y el pptido, junto a la molcula HLA, tanto de clase I como II, es especfica. El proceso de reconocimiento vara si el TCR est formado por el heterodmero alfa/beta presente en clulas T alfa/beta o si es del tipo gamma/delta presente en clulas T gamma/delta. Sin embargo para que la activacin se inicie adecuadamente, se requiere adems de la participacin de TCR de otras molculas presentes en la membrana de los linfocitos T. Una vez activados los linfocitos T, stos producirn prioritariamente citocinas o factores citotxicos, segn se trate de linfocitos Th o Tc respectivamente. De esta manera estos linfocitos intervienen en la respuesta inmune en la que estn implicados. (Figura, activacin linfocitos T).
En resumen la secuencia de eventos en la activacin de linfocitos T son: el proceso de interaccin celular, la intervencin del complejo TCR/CD3, la cascada de seales intracelulares y la activacin de diferentes factores de transcripcin celular.
Interaccin intercelular
La unin del antgeno con el es TCR, suficiente eficaz estudiado para de la los en captulos anteriores, no activacin linfocitos T. Para que esta respuesta se lleve a cabo se requiere la participacin de una serie de molculas conocidas como globalmente
accesorias, y cuya funcin es la de contribuir al desarrollo de una respuesta inmune efectiva, facilitando la interaccin entre las distintas clulas. Se forma as lo que se denomina sinapsis entre linfocitos T y clula presentadora de antgeno (Figura, requerimiento activacin). De estas molculas destacan: Las molculas CD4 y CD8. Las molculas CD28 y CTLA-4 y sus ligandos. Otras molculas como CD2, CD45 entre otras. Molculas CD4 y CD8. Estas molculas facilitan la unin intercelular y adems potencian la transmisin de seales al interior celular. Son glicoprotenas cuyos ligandos naturales son las molculas dehistocompatibilidad clase II y I respectivamente. Ambas molculas pertenecen a la superfamilia de las inmunoglobulinas, pero mientras el CD4 est formado por una sola cadena, el CD8 lo est por dos cadenas, alfa y beta. El CD4 se expresa en la mayora de los linfocitos T colaboradores, el CD8 lo hace, principalmente, en linfocitos T con funcin citotxica. Molculas CD28 y CTLA-4. La molcula CD28 es de especial importancia, incrementando la estabilidad de las interacciones intercelulares de linfocitos. El CD28 se expresa en todos los linfocitos CD4 y aproximadamente en el 50% de los linfocitos CD8 y sus ligandos naturales pertenecen a la familia B7 (B71, CD80; B72, CD86). El CD28, adems de su papel en el proceso de adhesin, tambin participa transmitiendo seales de activacin de la clula T. Una variante de esta molcula es el CTL4 que, a diferencia del CD28, se expresa slo de modo transitorio despus de la activacin de las clulas confiere una seal inhibidora al linfocito, a diferencia del CD28 que, como hemos dicho, confiere seales de activacin. Esta posibilidad de la presencia diferencial de CD28 o CTL4 define que el linfocito se active o se inhiba, lo que tiene gran trascendencia regulando el proceso de la activacin de los linfocitos T.
Molcula CD2. La molcula CD2 es una glicoprotena de adhesin que contribuye a la unin del linfocito T a la clula presentadora. Su ligando natural es el CD58 ( LFA3) y se expresan en la superficie de todas las clulas con funcin presentadora de antgenos. CD45. El CD45, es una de las glicoprotenas ms abundantemente expresadas en la superficie de linfocitos y en general en las clulas hematopoyticas, pudindose detectar hasta un milln de molculas por clula y cuyo ligando no se conoce con precisin. Pertenece a la familia de protenas con varios miembros y con mltiples alelos,con actividad fosfatasa (PTP), como son el CD45Ra y el CD45RB. Concretamente la parte citoplasmtica de esta molcula es muy extensa y en accin fosfatasa puede eliminar grupos fosfato a las tirosin kinasas LcT y Fyn, tal como veremos despus con ms detalle.
Transmisin de seales en linfocitos T
Los linfocitos T, al igual que los linfocitos B y NK, poseen mecanismos a travs de los cuales los estmulos externos son procesados y enviados al ncleo a travs de una serie de mediadores bioqumicos intracelulares conocidos como segundos mensajeros.
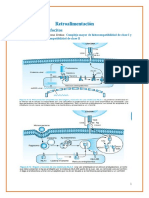
stos son capaces de regular la transcripcin especfica de un amplio nmero de genes, que participan en los procesos de crecimiento, divisin y diferenciacin celular. En la activacin de esta cadena de segundos mensajeros intervienen seales procedentes tanto del TCR/CD3 como de las molculas accesorias, de molculas que participan en la interaccin celular y receptores de citocinas presentes en la membrana de los linfocitos (Figura, cascada activacin).
Un mecanismo fundamental en la regulacin de la actividad y la funcin de estos mensajeros son los ciclos de fosforilacin y defosforilacin a los que estn sometidos mediante cinasas y fosfatasasrespectivamente. Bsicamente existen dos tipos de cinasas, dependiendo de su actividad fosfotransferasa, que se manifiesta fosforilando protenas en aminocidos serina y treonina(serina/treonina cinasas) o bien en aminocidos tirosina (tirosina cinasas). Igualmente hay dos tipos de fosfatasas que defosforilan especficamente protenas fosforiladas bien en serina/treonina o en tirosina. Una propiedad general de los linfocitos es la de necesitar dos tipos de seales distintas para inducir su activacin y proliferacin. Como se ha comentado anteriormente:
La La
primera seal la proporciona la unin del complejo pptido MHC al TCR (y a los
correceptores CD4 y CD8), esta seal est potenciada por la participacin de molculas de adhesin, tales como CD2, LFA1, CD26 y otras. segunda seal es suministrada por molculas coestimuladoras del tipo CD28, que de alguna manera complementan las seales de activacin inducidas por el TCR permitiendo una activacin celular completa (Figura, cascada activacin). Estas seales coestimuladoras son necesarias para la activacin del linfocito, ya que en su ausencia la seal mediada por el TCR puede conducir al linfocito a la muerte celular o a un estado de anergia (en la que el linfocito no responde a nuevas estimulaciones). En esta ltima dcada se est realizando un gran esfuerzo para identificar los componentes celulares y moleculares que estn involucrados en dicha activacin celular y determinar la secuencia de eventos bioqumicos que ocurren despus del reconocimiento del antgeno.
Mediadores intracitoplasmticos de la activacin celular
Uno de los primeros eventos bioqumicos que ocurren en los linfocitos T despus de la interaccin HLA-pptido-TCR, es la fosforilacin en tirosina, principalmente de las cadenas zeta no polimrficas del CD3. Estas cadenas poseen en sus dominios intracitoplasmticos unas regiones denominadas ITAM (Immunoreceptor Tyrosinebased Activation Motifs) que se fosforilan por la accin de las tirosina cinasas clck y cfyn. Ello se debe a que existe una estrecha asociacin fsica del CD4 y del CD8 con el TCR/CD3, de tal manera que cuando se produce la unin TCR-pptido-HLA, hace que la cLck asociada a estas molculas se aproxime a la porcin citoplsmica de las protenas del complejo CD3, donde puede fosforilar en tirosina a sus regiones ITAM. As mismo, todo ello es posible porque la tirosina cinasa cLck se encuentra localizada precisamente en la parte intracelular de la membrana plasmtica unida a la bicapa lipdica, por un proceso de miristilacin de su regin aminoterminal. Una vez que los ITAM son fosforilados en sus residuos tirosina, se convierten en sitios especficos de acoplamiento donde se une a la protena citoplsmica ZAP70, que pertenecen a la familia de enzimas proteincinasas. Ejerce as el ZAP70, que se encuentra tanto en clulas T como NK, un papel crtico en cascada fosforizando de sealizacin nuevos substratos. la intracelular (fFgura,
fosforilacin ITAM). El ZAP70 acta fosforilizando sobre ciertos adaptadores, con lo cual prosigue la cascada de transmisin de seal de activacin. Entre estos adaptadores se encuentran el estabilizador de clulas T activadas (LAT) y la protena especfica de leucocito que contiene SH2 (SLP76). Despus de la activacin de estos adaptadores se producir la fosforilacin en tirosina de la enzima fosfolipasa C gamma (PLCgamma) que es crucial en todo el proceso de la cascada de transmisin de seales. Como consecuencia, la PLCgamma se activa e induce la hidrlisis de su substrato especfico, elfosfatidilinositol bifosfato (PIP2), generndose los metabolitos inositol trifosfato (IP3) ydiacilglicerol (DAG) . De esta manera es como se inician las dos vas de transduccin de suma importancia que es la iniciada por el IP3 y la otra la iniciada por el DAG, y que son conocidas como va mediada por calcio y va mediada por la proteincinasa C (PKC) respectivamente. Va mediada por calcio. Cuando el IP3 se une a un receptor especfico (IP3R) localizado en el retculo endoplsmico, facilita la liberacin del calcio intracelular de sus compartimentos, este aumento de la concentracin de estos iones en el espacio libre intracelular acta estimulando la enzima calmodulina, que es una serina/treonina cinasa. Posteriormente se induce la formacin de calcineurina que despus activar el factor de transcripcin activador de clulas T (NFAT).
Va mediada por la protena cinasa C. Por otra parte el DAG formado activa la PKC que terminar activando el factor de transcripcin de clulas B (NFkB). Las PKCs, en condiciones de reposo celular, se encuentra localizada en el citosol donde es inactiva, pero una vez que recibe el estmulo del DAG ejerce conjuntamente su funcin con de iones cinasa Ca ++ (dependiendo de protenas en del isotipo enzimtico) se transloca a la membrana celular, donde en presencia de fosfolpidos (fundamentalmente fosfatidilserina) aminocidos serina y treonina. Va mediada por APRAS. Otra va importante de activacin es en la que interviene el Ras, que hace que Raf se active y acte como una cinasa de MAPc que interviene en la regulacin por fosforilacin delfactor de transcripcin activador de protena (AP1).
Factores de transcripcin en linfocitos T
Como consecuencia del desarrollo de la cascada de los mensajeros citoplasmticos analizados ms arriba, se activan ciertos factores que tienen como funcin la de activar la transcripcin, conocidos comofactores de transcripcin, de un gran nmero de genes implicados en la respuesta inmune. Entre estos factores de transcripcin destacan:
El factor nuclear de la cadena K de clulas B El factor activador de protena 1 El factor nuclear de clulas T
Factor nuclear de la cadena K de clulas B El factor nuclear de la cadena Kappa de clulas B (NFB), fue caracterizado por primera vez como un factor especfico de clulas B (de ah su nombre), pero ahora sabemos que se encuentra en muchosotros tipos celulares, incluyendo los linfocitos T. Este factor est formado por cinco componentes que presentan una alta homologa entre s y que son las protenas p50, p52, p65, RelB y crel. Estas protenas pueden estar formando distintos complejos entre ellos siendo los ms comunes: p50/p50 y p50/p65. El complejo p50/p65, se encuentra retenido en el citoplasma por molculas llamadas inhibidores de NFB o IB, bloquendose as su llegada al ncleo. Ser slo despus de la activacin de la PKC cuando el IkB terminar degradndose y como consecuencia se liberan los componentes del NF-kB, que pueden ahora pasar del citoplasma al ncleo en donde ejerce su funcin (Figura: Factores transcripcin).
Este factor puede participar en la transcripcin de la IL2 y de su receptor y tambin en un amplio nmero de genes de linfocitos T tales como los de MHC, ciertas molculas de adhesin, protooncogenes c myc y otros. Factor activador de protena 1 El factor activador protein 1 (AP1), a diferencia del NFKB, es un factor de transcripcin exclusivamente nuclear que se activa por fosforilacin mediada por cinasas que se translocan al ncleo e inducen en este factor una modificacin postranslacional que le hace activo. Este factor est formado por protenas ubicuas pertenecientes a las familias de genes de expresin temprana Jun (c Jun, vJun, JunB y JunD) y Fos (c Fos, FosB, Fra1 y Fra2) capaces de regular la transcripcin de un alto nmero de genes, incluyendo el de IL2. Factor nuclear de clulas T activadas La familia de factores nucleares de clulas T activadas (NFAT), se encuentran en su estado fosforilado en el citoplasma y pasa al ncleo cuando se desfosforila. En este proceso interviene directamente la calcineurina que, a su vez, aparece cuando sobre la calmodulina se une el ion Ca++ como consecuencia de su movilizacin tras la activacin del TCR. En gran parte el NFAT necesita de la cooperacin de AP1 para activar los genes donde acta.
Inmunopatologa
Se han observado alteraciones de muchas de la cinasas que intervienen en la activacin de los linfocitos T. Entre ellas ZAP70 que se asocia a valores muy bajos o ausentes de linfocitos T CD8+ en sangre perifrica y sus linfocitos no proliferan en respuesta a lectinas, a anticuerpos monoclonales antiCD3, y a antgenos y a clulas alognicas.
Activacin de linfocitos B
Los linfocitos B utilizan como receptor las inmunoglobulinas de membrana (mIgs), de tal manera que cuando se produce la unin mIg-Ag se inicia el proceso de activacin de los mismos. Posteriormente proliferan y diferencian a clulas plasmticas, productoras de anticuerpos y clulas memoria, listas para una pronta activacin en caso de la entrada de nuevo del mismo antgeno.
Para que los linfocitos B respondan tienen que haber sufrido un proceso madurativo que en el adulto ocurre en la mdula sea de tal manera, que a continuacin estudiaremos en primer lugar el proceso de maduracin de estos linfocitos y despus la serie de eventos conducentes a la activacin, proliferacin y diferenciacin de los mismos.
Proceso madurativo de linfocitos B
El proceso madurativo de los linfocitos B o linfopoyesis B, se produce a partir de progenitores linfoides derivados de las clulas hematopoyticas primordiales (HSC), que se convertirn en linfocitos B maduros capaces de producir Igs. Este proceso madurativo es independiente del estmulo antignico, durante el cual se reordenan los genes de las cadenas pesadas y ligeras de las inmunoglobulinas. Tambin durante este proceso se produce la seleccin del repertorio de linfocitos B no autorreactivos y la eliminacin de aquellos clones que reconcoen antgneso propios, que pueden ser lesivos para el organimo en el futuro. (Figura desarrollo B).
Etapas del proceso madurativo B El proceso madurativo los linfocitos B pasa por una serie de fases caracterizadas por la expresin diferencial de genes de Igs y de otras protenas de superficie. Las clulas ms primitivas son lasclulas proB, que no producen Igs, pero si expresan molculas de superficie propias de la estirpe B, tales como CD19. Se produce tambin la recombinacin de segmentos gnicos D con J. Despus se formarn las clulas preB, que tienen capacidad de sintetizar la cadena pesada mu que al ser slo citoplasmtica no acta como receptor y no puede reconocer ni responder a antgenos. En esta clula ya se han reorganizado los complejos gnico VDJ. El siguiente estado madurativo y corresponde cadenas a los linfocitos los ligeras, genes, que B inmaduros, las a la que se caracterizan por reordenar completamente producir bien de asocindose cadenas cadena
ligeras Kappa o lambda,
pesada mu se forma la IgM de manera completa. Despus se formarn los linfocitos B maduros que se caracterizan por expresar las cadenas pesadas mu y delta que, asociandose con sus cadenas ligeras, hacen que estas clulas coexpresan en su membrana IgM e IgD, que poseen la misma regin V y consecuentemente la misma especificidad por el antgeno.
Estos procesos madurativos de los linfocitos B inmaduros en la mdula requieren de la presencia de clulas estromales que interactan con los lifocitos inmaduros y a los que ayudan a travs de laIL7 que producen y que facilita el proceso madurativo de los linfocitos. La interaccin entre clula estromal y clula B se lleva a cabo con la participacin de las molculas VLA4 y su ligando VCAM1, presentes en clulas B y estromales, respectivamente y la molcula cKit, presente en los linfocitos y que interacta con otra molcula presente en las clulas estromales, el factor de clulas madre o SCF (Figura, Linfopoyesis B). Generacin del repertorio de anticuerpos Como se ha comentado en captulos anteriores, los genes V de las Ig se distribuyen clonalmente, es decir, que cada linfocito B exprese una nica regin VH y VL. Basado en ello, cada grupo de linfocitos (clon) posee una nica especificidad antignica distinta de la expresada por los otros linfocitos B, constituyendo el punto esencial de la teora de la seleccin clonal, segn la cual el
Ag exgeno se une (selecciona) a los linfocitos B, cuyas Ig de membrana sean especficas (complementarias) para l. El conjunto de especificidades de anticuerpo distribuidas entre los linfocitos B recientemente formados y que no han tenido contacto todava con el Ag, se denomina repertorio primario. Despus, y como consecuncia de los estimulos antignicos y diferenciacin de los linfocitos, aparecen hipermutaciones somticas que son responsables de las mltiples posibilidades de generacin de un repertorio casi infinito de anticuerpos, calculndose que, pueda ser de aprox. 109. Ello garantiza que cualquier Ag exgeno de los mltiples (potencialmente millones) presentes de forma natural o artificialmente creados por el hombre, que entre en el organismo pueda tener oportunidad de encontrar linfocitos B que lo reconozcan. Eliminacin de linfocitos B autorreactivos en la mdula El desarrollo del sistema inmune necesita compaginar dos fenmenos casi contradictorios; a) generar una enorme diversidad de receptores que reconozcan diferentes antgenos y b) seleccionar de todas estas especificidades generadas al azar las no dainas para el propio organismo. De no ser as, los autoanticuerpos generados produciran, inflamaciones destructivas en los tejidos propios. Por ello las clulas B inmaduras que interaccionen con antgenos son eliminados por un proceso denominado apoptosis, proceos por el cual mueren los linfocitos debido a una fragmentacin de su DNA.
Reconocimiento del antgeno y activacin de linfocitos B
Los linfocitos B maduros, pueden reconocer al antgeno por su receptor BCR (Figura, BCR simple) y transmitirse las seales en la ayuda de Igalfa otras e molculas, Igbeta tambin que en la
poseen residuos tirosina, presentes membra 4). Los residuos de tirosina de las colas citoplasmticas de los componentes del BCR pueden fosforilarse por enzimas protentirosncinasas (PTK), que son de importancia capital en la transduccin de seales activadoras al interior de la clula tras la unin del Ag a las mIg. Entre esas PTK se encuentran las molculas lyn, fyn y blk entre otras (Figura, Activacin BCR). Adems existe tambin lo que se conoce como correceptor de clulas B, que acta asociado con las molcuas anteriores formando un gran complejo de activacin. Estas molculas son el CD21 (CR2), el CD19 y el CD81. De ellas, el CD19 posee gran nmero de tirosinas en el tallo citoplasmtico y la CD21 tiene la posibilidad de unirse a C3d que es un producto del catabolismo celular (Figura,
del complemento e importante en el proceso de identificacin de clulas y bacterias que se requieren destruir del receptor del Ag de las clulas B (BCR) (Figura, BCR completo).
Teora de seleccin clonal No todos los linfocitos B se activan frente a un antgeno, sino que lo hacen slo aquellos clonos que poseen el receptor adecuado y por tanto lo reconocen (Figura , seleccin clonal). Esto se debe a que los receptores de los linfocitos B estan distribuidos clonalmente, esto es, cada uno de los diversos tipos de linfocitos slo reconocera y en consecuencia se estimulara por un determinado tipo de antgeno. De esta manera, tras el contacto con el antgeno, los linfocitos B se activaran y diferencian a clulas secretoras de inmunoglobulinas, las cuales tienen una especificidad casi idntica, a la expresada en la membrana de las clulas B que originariamente reconocieron al antgeno.
Activacin B, dependiente de linfocitos T Para la activacin de la mayoria de los linfocitos B se requiere adems del reconocimiento de un determinado antgeno por el complejo BCR (primera seal), la presencia de linfocitos T, que facilitaran una segunda seal necesaria para una ptima activacin de los mismos. A este proceso se conoce como activacin B, dependiente de linfociots T. Por otra parte, sabemos que en ciertas cinrcunstancias tambien los lifocitos B pueden activarse en ausencia de linfocitos T. Esto ocurre ante antgenos con epitopos muy repetitivos y en este caso sa habla activacin B, independiente de linfocitos T. Veamos como se desarrolla la activacin dependiente de linfocitos T para despus analizar la respuesta B independiente de T. Hoy sabemos como los linfocitos B, al igual que los linfocitos T, precisan de al menos dos seales para su activacin.
La primera seal es dada por el complejo BCR de los linfocitos B tras su unin al antgeno con lo que se pone en marcha la cascada de segundos mensajeros en estos linfocitos. Sin embargo, hoy sabemos que esta seal por s sola no es suficiente para una activacin completa de los linfocitos B. Para ello es necesaria al menos una segunda seal proveniente de los linfocitos T y que es mediada por ciertas citocinas que propiciaran la proliferacin y diferenciacin de las clulas B. Para ello tambin se requiere la adecuada interaccin entre ambos tipos de linfocitos, T y B, mediante molculas conocidas como accesorias. As, las clulas B expresan las molculas de activacin CD80 y CD86 que interactan con la molcula CD28 de linfocitos T para una buena activacin de los primeros. Tambien es de gran importancia que las molculas CD40L se unan a CD40 presentes en linfocitos T y B respectivamente para que estos ltimos puedan activarse y diferenciarse de manera adecuada (Figura, antgenos T dependientes). Activacin B, independiente de linfocitos T Por otra parte, sabemos que hay antgenos que en ausencia de clulas T pueden producir una respuesta de linfocitos B, conocida como activacin B, independiente de linfocitos T. Este tipo de Ags se denominan antgenos T independientes y pueden ser de dos tipos: a) Ciertos
antgenos de paredes bacterianas, como es el LPS, que inducen activacin y diferenciacin de linfocitos B sin interaccionar con el BCR y b) ciertos antgenos formados por estructuras repetitivas, normalmente hidratos de carbono, que son reconocidos simultaneamente por muchos complejos BCR, dando lugar a la activacin de clulas B sin necesidad de la interaccin con las T.
Linfocitos B como clulas presentadoras de antgenos
Por ltimo, es de destacar que los linfocitos B pueden actuar como clulas presentadoras de Ags. Efectivamente cuando un linfocito B interacciona a travs de su BCR con un antgeno, ste puede ser endocitado y procesado en sus pptidos, que a su vez pueden ser presentados posteriormente unidos a sus molculas MHC de membrana a los linfocitos T. Los linfocitos B que interaccionarn a travs de su Igm con un antgeno, denominado por ejemplo X, lo procesaran y presentaran unidos a MHC pptidos del mismo antgeno X (pptidosX). Los linfocitos T con especificidad anti (pptidosX) que han interaccionado previamente con el antgeno en clulas accesorias clsicas, reconoceran el complejo MHCpptido en la membrana de la clula B, transmitiendo las segundas seales necesarias para la diferenciacin de clulas B (factores solubles ms interaccin membranamembrana). Es importante destacar que las partes del antgeno X reconocidas por linfocitos T y B pueden ser muy distintas. Las clulas B pueden interaccionar con los hidratos de carbono de la glicoprotena X, mientras que los linfocitos T antiX slo reconocen pptidos de esta protena X (Figura, eptopo).
Diferenciacin de linfocitos B
Los linfocitos B activados se diferencian en clulas plasmticas, pueden permanecer aos produciendo un mismo tipo de anticuerpos desde los lugares donde normalmente se asientan, que es la pulpa roja del bazo, ganglios linfticos y la propia mdula sea. (Figura, diferenciacin B)
Durante el proceso madurativo de la respuesta inmune B, se produce un cambio de isotipo de las cadenas pesadas de las inmunoglobulinas, de tal forma que los linfocitos que originariamente expresan en su membrana mIgM o mIgD, pasan a sintetizar IgG, IgA IgE. En este proceso intervienen ciertas citocinas producidas por linfocitos T, entre las que destacan la IL4, IL5 e IFN. Por otra parte los por linfocitos B memoria, se caracterizan permanecer largo tiempo en el organismo y cuando se activan producen IgG de o IgA o bien de IgE que son inmunoglobulinas larespuesta de respuesta) La mayora de los linfocitos B memoria, en virtud de los mecanismos de recombinacin de la parte constante de de los genes de las Igs, han cambiado la regin constante de su mIg, de forma que deja de expresar IgD para prooducir IgG o IgA o bien IgE. secundaria.(Figura, inmune tipos
Es de destacar que estas Igs que se producen como consecuencia de la activacin de las clulas memoria, siguen expresando el mismo tipo de regiones variables. Esto hace que sigan reconociendo los mismos antigenos aunque sean de distitnto isotipo que las clulas originarias pero con un aumento de la afinidad entre ellos. Ello se debe a las modificadas aparecidas debido a las mutaciones de los genes que las codifican.
Activacin de clulas NK
Las
clulas
NK
son
esenciales como
parte
de
la
respuesta inmune innata y tambin por su colaboracin en el inicio de la respuesta inmune adaptativa en la defensa del organismos frente al desarrollo de clulas tumorales como frente a patgenos. (Figura, NK/Clula tumoral). En las primeras fases de la infeccin, las clulas NK actan especialmente frente a virus, de ah que cuando estas clulas no actan correctamente, el individuo se hace vulnerable sobre todo a infecciones de tipo viral. Adems de las acciones defensivas frente a agentes externos, las clulas NK, tienen la propiedad de respetar las clulas propias de cada individuo, reconociendo as su identidad biologica por la presencia en las clulas de molculas HLA-I. Sin embargo cuando las propias clulas pierden estas molculas, son destruidas por las clulas NK, actuando as como "clulas escoba" eliminando todo aquello que pierde la identidad propia definida por las molculas HLA-I. La accin de las clulas NK se debe a su potente capacidad y clulas destructora malignas. una en (citotxica) de clulas infectadas por microorganismos Adems estas clulas de poseen citocinas,
potente capacidad secretora tanto de quimiocinas como especial de interferngamma. Debido a su produccin de quimiocinas poseen gran capacidad inflamatoria y debido a la secrecin de citocinas pueden influir facilitando el NK) Las clulas NK constituyen la tercera estirpe de clulas de tipo linfoide y se caracterizan por carecer de TCR y de BCR y, en su mayora, expresar en su superficie las molculas CD16 y CD56. Se encuentran en sangre, bazo, mdula sea y en muy baja proporcin en ganglios linfticos.Existen grandes diferencias funcionales entre las clulas NK y los linfocitos T (Tabla diferencias: NK/CTL). inicio de la respuesta inmune adaptativa. (Figura, funciones
Receptores de las clulas NK
La funcin destructora de las clulas NK fue la primera accin asignada a estas clulas y es de donde deriva su nombre.
Para que las clulas NK ejerzan sus funciones citotxicas se requiere que las clulas blanco sean identificadas, a travs de receptores adecuados, de las clulas a destruir. Entre estos receptores destacan
1. Receptores del extremo Fc de Igs conocido
como CD16 y
2. Receptores de citotoxicidad natural (NCRs)
Adems de estos receptores de citotoxicicdad, existen otros cuya funcin es reguladora y que actan bien en forma activante como inhibidora y lo hacen reconociendo molculas HLA de clase I. Son los receptores NK de HLA (NKRs). Receptores CD16 en NK Los receptores CD16 en clulas NK median los procesos de lisis denominados citotoxicidad proceso implica la presencia dependiente de anticuerpos (ADCC) en estas clulas. Este de anticuerpos que se unen, por una parte, a antgenos presentes en las clulas blanco y por extremo FC son reconocidos por los receptores CD16 presentes en las clulas NK, que como consecuencia se activan y destruyen la clula blanco implicada en este proceso (Tabla: Receptores activantes). Receptores de citotoxicidad natural en NK Los receptores de citotoxicidad natural (NCKs) en clulas NK, han sido descritos recientemente y son responsables de la citotoxicidad natural de las clulas NK (CN), esto es la lisis espontnea y directa de las clulas blanco con las que interatan. Entre estos receptores de citotoxicidad natural, destacan tres molculas conocidas como: Nkp46, Nkp30 y Nkp44. No se conoce bien las molculas que reconocen en la clula blanco pero la mayora lo hacen a travs de la hemaglutinia, presente en muchos microorganismos.
Receptores NK de molculas HLA
Recientemente se han descubierto receptores presentes en clulas NK que reconociendo molculas de histocompatibilidad clase I y que tienen capacidad de activar o de inhibir sus funciones. Precisamente del equilibrio de estas acciones, activadoras/inhibidoras, resultar la accin final de las clulas NK, bien desarrollando sus funciones citolticas y secretoras o bien bloquendolas.
Estos datos provienen de las observaciones de Krre, quien utilizando variantes de una misma lnea celular tumoral, encontr distinto grado de sensibilidad a la lisis NK, que se correlacionaba inversamente con la expresin de molculas de histocompatibildiad clase I. As fue propuesta la teora de "prdida de lo propio" (missing self theory) para explicar los fenmenos por los cuales las molculas HLA propias inhiben la destruccin por las clulas NK de aquellas otras clulas que han perdido sus molculas de histocompatibildiad. Estos receptores pertenecen a distintas familias de glicoprotenas que adems de expresarse en clulas NK, se encuentran tambin en ciertos linfocitos T (Figura y Tabla: Receptores NK).
Entre estas familias de receptores destacan tres: 1. Receptores tipo KIR (killer cell Iglike receptors)
2. Receptores ILTs (immunoglobulin like transcripts) y 3. Receptores tipo lectinas
Receptores NK tipo KIR Estos receptores fueron descubiertos porque estaban implicados en la inhibicin de la lisis al interaccionar especficamente con determinadas molculas HLA de clase I de la clula blanco. Pertenecen a la familia de las inmunoglobulinas originariamente. (Figura, ITAM/ITIM en KIRs y ILTs).
A la palabra KIR, se aaden los sufijos 2D y 3D, que indican el nmero de los dominios de inmunoglobulina que poseen y la letra L (long) o S (short) segn la cola citoplasmtica de estas molculas sea larga o corta respectivamente. Estos receptores pueden ser de tipo inhibidor o de tipo activante. La distribucin de estos receptores en las clulas NK no es homognea y cada clon NK puede expresar uno o varios tipos de estos receptores. Se aprecian claras diferencias en la expresin de cada receptor cuando se
estudian distintos individuos, y hay indicios en los que el repertorio de receptores est regulado durante el desarrollo por factores genticos, incluyendo presumiblemente la influencia del propio MHC. Receptores NK tipo ILT Otro grupo de receptores, que tambin pertenece a la superfamilia de las inmunoglobulinas, se conocen como ILTs (immunoglobulin like transcripts) CD85. Algunos de estos receptores reconocen molculas HLAG y la protena UL18, presente en citomegalovirus. Estos receptores se distribuyen en diferentes tipos de clulas, adems de las clulas NK, como monocitos y ciertas clulas de tipo polimorfonuclear Receptores NK tipo lectina La tercera familia de estos receptores est formada por a) las molculas CD94 que se encuentran unidas covalentemente de manera alternativa a diferentes molculas pertenecientes a la familia NKG2 (A, B, C, E y H) formando el complejo CD94/NKG2 y b) tambin por dmeros de la molcula NKG2D. El primer grupo de receptores (CD94/NKG2) poseen la capacidad de reconocer y unirse a HLA-E, mientras que los segundos (NKG2D), se unen a una molcula de histocompatibilidad especial conocida como MICA. La molcula CD94, que es una lectina, fue identificada originalmente por M. LpezBotet en el laboratorio del Hospital de Princesa de Madrid. Las molculas de HLA-E se caracterizan porque se producen en asociacin con pptidos derivados de la secuencia lder de las otras molculas HLA-I (Figura, ITAM/ITIM en receptores lectina)
Consideramos a estos receptores de especial importancia en los procesos de regulacin de la accin de clulas NK in vivo, debido a la extensa distribucin de las molculas de histocompatibilidad HLAE que reconocen y sobre todo por el hecho de encontrarse presentes en
un amplio nmero de clulas NK (6080 %) y ciertos linfocitos T. La expresin de CD94 es regulada principalmente por las citocinas IL15 IL10 y TGFbeta.
Transduccin de seales de NKRs
Los receptores KIR, ILT como el homodmero de CD94 con distintos miembros de la familia de NKG2, pueden ejercer acciones inhibidoras como activantes. El que ejerzan una u otra accin depende de la cola citoplasmtica de dichas molculas y de las cinasas con las cuales se asocien. Mecanismos de inhibicin Los receptores inhibidores se caracterizan por poseer en sus dominios intracitoplasmticos los motivos YxxL26YxxL, denominados ITIM (immunoreceptor tyrosinebased inhibitory motives) (Figura, inhibicin/activacin).
Estos motivos tiene la propiedad de unirse al dominio SH2 que contiene las tirosn-fosfatasas y as producir inhibicin de la citotoxicidad por la desfosforilacin que producen. Se representa un ejemplo de cada uno de los dos tipos de receptores, inhibidores y activadores. Es de destacar que esta accin inhibidora, ejercida por los receptores inhibidores despus de reconocer a su ligando (HLA clase I) en la clulas, tiene una gran importancia fisiolgica, pues esto evita la destruccin de las clulas normales del husped. Esto se debe a que, como se sabe, la mayora de las clulas del organismo expresan molculas de histocompatibilidad clase I, incluidas las molculas HLAE.
De esta manera, cuando una clula deja de expresar molculas de histocompatibilidad clase I, por ejemplo como consecuencia de una infeccin viral, entonces puede ser destruida por las clulas NK al no ser frenada su actividad por no actuar los receptores de tipo inhibidor que reconocen a estas molculas (Figura, prdida proteccin).
Mecanismos de activacin Los receptores NK carecen de la secuencias ITAMs pero muchas de ellas tienen la propiedad de asociarse a las molcula DAP12 que s forma secuencias ITAMs de tipo estimulante. Estos receptores son KIRD2S, NKG2C, NKG2E y NKG2H. El DAP12 es un homodmero, gracias al cual se lleva a cabo la transmisin de seales en el citoplasma de la clula de los receptores arriba indicados.
Finalmente hemos de decir que las clulas NK, tal como se ha indicado anteriormente, forman parte de la primera barrera defensiva del individuo junto con macrfagos, clulas dendrticas y polimorfonucleares, constituyendo as parte de la respuesta inmune innata. En ello intervienen ciertas citocinas, que potencian el efecto de stas clulas y son producidas precisamente por
macrfagos en las primeras fases de la infeccin. A su vez, gracias al IFN-gamma que producen, pueden intervenir facilitando la respuesta inmune adaptativa. (Figura, NK en la respuesta inmune).
Das könnte Ihnen auch gefallen
- Cascadas de Activación de Células T y BDokument57 SeitenCascadas de Activación de Células T y BFERNANDANoch keine Bewertungen
- GUIA CLASE 12 2023-1 - Activacion Linfocitos TDokument8 SeitenGUIA CLASE 12 2023-1 - Activacion Linfocitos TVale AlvarezNoch keine Bewertungen
- Activación de Linfocitos TDokument26 SeitenActivación de Linfocitos TFernandho Cruz BaciiliioNoch keine Bewertungen
- Maduración y Activación de Linfocitos TDokument59 SeitenMaduración y Activación de Linfocitos TVioleta Tello MedinaNoch keine Bewertungen
- Activación de Linfocitos TDokument16 SeitenActivación de Linfocitos Tclarafra628Noch keine Bewertungen
- Generación de Linfocitos T EfectoresDokument11 SeitenGeneración de Linfocitos T EfectoresMariano Félix DemasiNoch keine Bewertungen
- Linfocitos T y Su Receptor (TCR)Dokument8 SeitenLinfocitos T y Su Receptor (TCR)Giovanna B100% (11)
- Activacion Del Linfocito TDokument8 SeitenActivacion Del Linfocito TMANUEL ALBERTO VERA PIMINCHUMONoch keine Bewertungen
- Sinapsis InmunologicaDokument12 SeitenSinapsis InmunologicaFaraTatiNoch keine Bewertungen
- Cap. 5 - Inmunidad Mediada Por Linfocitos TDokument30 SeitenCap. 5 - Inmunidad Mediada Por Linfocitos TDaviid A'SNoch keine Bewertungen
- Cap 10Dokument7 SeitenCap 10Natalia Espíndola BalderasNoch keine Bewertungen
- Moléculas AccesoriasDokument15 SeitenMoléculas AccesoriasPaola PintoNoch keine Bewertungen
- Linfocitos T y Su Receptor de Antígeno (TCR)Dokument8 SeitenLinfocitos T y Su Receptor de Antígeno (TCR)Mariano Félix DemasiNoch keine Bewertungen
- Activacion de Los Linfoncitos T.Dokument6 SeitenActivacion de Los Linfoncitos T.Lis Juli MenReNoch keine Bewertungen
- INMUNIDAD CELULAR Estudiantes PDFDokument49 SeitenINMUNIDAD CELULAR Estudiantes PDFlordgimli77100% (3)
- Taller de InmunologíaDokument5 SeitenTaller de InmunologíamayleNoch keine Bewertungen
- Linfocito T CD4+ - Wikipedia, La Enciclopedia LibreDokument13 SeitenLinfocito T CD4+ - Wikipedia, La Enciclopedia LibreShowerNoch keine Bewertungen
- Unidad 6 Linfocitos TDokument45 SeitenUnidad 6 Linfocitos Tkarina trejoNoch keine Bewertungen
- Activación de Linfocitos T y B: Reconocimiento Antigénico y SeñalizaciónDokument22 SeitenActivación de Linfocitos T y B: Reconocimiento Antigénico y SeñalizaciónDove CameronNoch keine Bewertungen
- Clase 5Dokument4 SeitenClase 5Jesus Yepes martinezNoch keine Bewertungen
- Inmunología - T10.Abril_GómezDokument5 SeitenInmunología - T10.Abril_Gómezlgomez04Noch keine Bewertungen
- Rol MHC presentación antigénicaDokument3 SeitenRol MHC presentación antigénicaLeandroCayaoNoch keine Bewertungen
- Inmunidad Celular e HumoralDokument5 SeitenInmunidad Celular e HumoralYony Galeano EspinozaNoch keine Bewertungen
- Linfocitos T 2reDokument52 SeitenLinfocitos T 2reesalivorNoch keine Bewertungen
- Activacion de Los Linfocitos Clase IIDokument72 SeitenActivacion de Los Linfocitos Clase IIOlga Meléndez MayorquinNoch keine Bewertungen
- Activación, diferenciación y memoria de células T: Receptores coestimuladoresDokument14 SeitenActivación, diferenciación y memoria de células T: Receptores coestimuladoresFabian Acosta ReyesNoch keine Bewertungen
- 2.1 Clases de HomeroDokument34 Seiten2.1 Clases de HomeroAndres Ignacio Aguilar AndradeNoch keine Bewertungen
- Generación de linfocitos T efectoresDokument22 SeitenGeneración de linfocitos T efectoresCarLiita CruzNoch keine Bewertungen
- Activacion de Linfocitos TDokument18 SeitenActivacion de Linfocitos TVictor Fabian Uribe Olmos100% (1)
- Activacion Del Linfocitos TH y TCDokument25 SeitenActivacion Del Linfocitos TH y TCJose Efraím Olvera LopezNoch keine Bewertungen
- Respuesta Funcional de Linfocito T Activados Fase de Contracciã N de La Respuesta de Cã© Lulas T SuperantigenosDokument13 SeitenRespuesta Funcional de Linfocito T Activados Fase de Contracciã N de La Respuesta de Cã© Lulas T SuperantigenosPabsNoch keine Bewertungen
- Capitulo 11 InmunoDokument26 SeitenCapitulo 11 InmunoJonatan PintoNoch keine Bewertungen
- Sesion 5Dokument83 SeitenSesion 5Diego LópezNoch keine Bewertungen
- Resumen Del Capítulo 9 de AbbasDokument7 SeitenResumen Del Capítulo 9 de AbbasMaría Alejandra Peña100% (1)
- Inmunologia (1) Lizzzz - OdtDokument10 SeitenInmunologia (1) Lizzzz - Odtwilber carvajalNoch keine Bewertungen
- Linfocito T y CitocinasDokument28 SeitenLinfocito T y CitocinasAlfredo VidalesNoch keine Bewertungen
- RESPUESTA INMUNE CELULARDokument28 SeitenRESPUESTA INMUNE CELULARraziel boxNoch keine Bewertungen
- Primera Parte Taller de InmunologiaDokument13 SeitenPrimera Parte Taller de Inmunologiajuan ariasNoch keine Bewertungen
- Proteínas Cd1 - Cd8 y TCR (Alfa y betaDokument5 SeitenProteínas Cd1 - Cd8 y TCR (Alfa y betaJorge VargasNoch keine Bewertungen
- Linfocitos TDokument15 SeitenLinfocitos TIGNACIO SALVADOR FERNANDEZ GIRONNoch keine Bewertungen
- Linfocitos TDokument10 SeitenLinfocitos Tisrael tulcanazaNoch keine Bewertungen
- Maduración de Linfocitos TDokument41 SeitenMaduración de Linfocitos TVicToRia50% (2)
- Presentación de AntígenoDokument5 SeitenPresentación de AntígenoFernanda QuilachaminNoch keine Bewertungen
- InmunologiaDokument58 SeitenInmunologiaSantiago PerezNoch keine Bewertungen
- Seminario 6Dokument5 SeitenSeminario 6Rubén HNoch keine Bewertungen
- Expoooo Receptores para Antígeno e InmunoglobulinaDokument25 SeitenExpoooo Receptores para Antígeno e InmunoglobulinaCdcgs PWinNoch keine Bewertungen
- Desarrollo Linfocitos TDokument82 SeitenDesarrollo Linfocitos TVALENTINA ESCOBAR QUINTERONoch keine Bewertungen
- linfocito T virgenDokument3 Seitenlinfocito T virgensofiarodavilNoch keine Bewertungen
- PreguntasDokument9 SeitenPreguntasSerCL1Noch keine Bewertungen
- Resumen-Activación Del Linfocito T (Corregido)Dokument4 SeitenResumen-Activación Del Linfocito T (Corregido)alisson louridoNoch keine Bewertungen
- Sistema Inmune AdaptativoDokument6 SeitenSistema Inmune AdaptativoJose FernandezNoch keine Bewertungen
- Respuesta Inmune AdaptativaDokument11 SeitenRespuesta Inmune Adaptativaalessandra.sandoval.93Noch keine Bewertungen
- MORFO2Dokument8 SeitenMORFO2ValeriaNadjarNoch keine Bewertungen
- RESPUESTA INMUNE CELULAR CompletaDokument96 SeitenRESPUESTA INMUNE CELULAR CompletaJazmin Sanchez SanchezNoch keine Bewertungen
- Dinámica de ClusteringDokument2 SeitenDinámica de ClusteringPacaya Astulla JamesNoch keine Bewertungen
- Inmunología E InmunopatologíaDokument24 SeitenInmunología E InmunopatologíaBanu TeamNoch keine Bewertungen
- Regulacion de La Exprecion Genica, Sistema InmunitarioDokument17 SeitenRegulacion de La Exprecion Genica, Sistema InmunitarioKleverxithoDiazCiezaNoch keine Bewertungen
- Linfocitos T IDokument9 SeitenLinfocitos T IFrancisca BaezaNoch keine Bewertungen
- Las Hormigas - Texto y Compreension LectoraDokument1 SeiteLas Hormigas - Texto y Compreension LectoraMichelle Chiarelli100% (1)
- Silabo Del CursoDokument14 SeitenSilabo Del CursoJP VdlcNoch keine Bewertungen
- Introducción a la anatomía clínicaDokument82 SeitenIntroducción a la anatomía clínicaAllana FrósNoch keine Bewertungen
- Guia Sistema CirculatorioDokument3 SeitenGuia Sistema CirculatoriosebastkmNoch keine Bewertungen
- Clave dicotómica filos animalesDokument5 SeitenClave dicotómica filos animalesManuelVidalLópez100% (2)
- Solucionario Ecología Temario Sem 16Dokument2 SeitenSolucionario Ecología Temario Sem 16Angeles Guerra FloresNoch keine Bewertungen
- Triptico AracnidosDokument3 SeitenTriptico AracnidosJaneth Cajachagua Leon0% (1)
- Clasificación de Los Animales Según Su AlimentaciónDokument11 SeitenClasificación de Los Animales Según Su AlimentaciónAbraham CosworthNoch keine Bewertungen
- Cuestionario 1 HematologíaDokument4 SeitenCuestionario 1 HematologíaMichelle AvalosNoch keine Bewertungen
- Dibujos de ForenseDokument5 SeitenDibujos de ForenseMichael Javier Cerda TijerinoNoch keine Bewertungen
- 1º - Guía de Estudio DigestiónDokument14 Seiten1º - Guía de Estudio DigestiónvickylicoNoch keine Bewertungen
- Manual ParamedicoDokument299 SeitenManual Paramedicogusarx100% (1)
- Diapositivas de OrganogenesisDokument14 SeitenDiapositivas de OrganogenesisYojara Herrera LeyvaNoch keine Bewertungen
- Ontogenia en MamíferosDokument24 SeitenOntogenia en Mamíferoslucia herediaNoch keine Bewertungen
- TP C. AmbDokument1 SeiteTP C. AmbPaula Fernanda TiseraNoch keine Bewertungen
- ACTIVIDAD DE APRENDIZAJE N 1 - Experiencia 5 - 2doDokument11 SeitenACTIVIDAD DE APRENDIZAJE N 1 - Experiencia 5 - 2doLuciana León Luján 6FNoch keine Bewertungen
- Anatomia y Fisiologia de Los InsectosDokument12 SeitenAnatomia y Fisiologia de Los InsectosJuan Baudilio López LópezNoch keine Bewertungen
- Tejidos nervioso y muscular: estructura, tipos y funcionesDokument21 SeitenTejidos nervioso y muscular: estructura, tipos y funcionesDilan TorresNoch keine Bewertungen
- Odontogenesis: Etapa de CampanaDokument22 SeitenOdontogenesis: Etapa de Campanaabigailreri1822Noch keine Bewertungen
- 2021.07.17 - Kendall, Canino, Hemograma +BDokument1 Seite2021.07.17 - Kendall, Canino, Hemograma +BGilvert vasquez DIAZNoch keine Bewertungen
- InmunologiaDokument43 SeitenInmunologiatitoxxxyyy100% (1)
- NeuroanatomiaDokument16 SeitenNeuroanatomiasofia MontufarNoch keine Bewertungen
- Médula Ósea y Maduración de LBDokument109 SeitenMédula Ósea y Maduración de LBCasandra Castillo100% (1)
- Procesos Que Se Dan en El CadaverDokument1 SeiteProcesos Que Se Dan en El Cadaversuyuana4sayas100% (2)
- Material Didactico 2010-I-Sesion 1Dokument8 SeitenMaterial Didactico 2010-I-Sesion 1Romina Sequeiros DejoNoch keine Bewertungen
- Definición y etapas del desarrollo embrionarioDokument4 SeitenDefinición y etapas del desarrollo embrionarioCelso HernandezNoch keine Bewertungen
- Taller de MoluscosDokument8 SeitenTaller de MoluscosClaudia GuerreroNoch keine Bewertungen
- Crucigrama biología respiratoria reproducciónDokument1 SeiteCrucigrama biología respiratoria reproducciónMauro Hernandez MendozaNoch keine Bewertungen
- Histología y EmbriologíaDokument2 SeitenHistología y EmbriologíaLuis SueroNoch keine Bewertungen
- Clasificación de Animales VertebradosDokument10 SeitenClasificación de Animales VertebradosYésica CLNoch keine Bewertungen