Beruflich Dokumente
Kultur Dokumente
Previo 6 Sintesis de Hantzsch para Piridinas
Hochgeladen von
Julio Cesar Venegas MuñozOriginaltitel
Copyright
Verfügbare Formate
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
Verfügbare Formate
Previo 6 Sintesis de Hantzsch para Piridinas
Hochgeladen von
Julio Cesar Venegas MuñozCopyright:
Verfügbare Formate
UNIVERSIDAD NACIONAL AUTONOMA DE MEXICO FACULTA DE ESTUDIOS SUPERIORES CUAUTITLAN CAMPO 1 QUIMICO FARMACEUTICO BIOLOGO QUIMICA ORGANICA III
PREVIO 6
EQUIPO: 6
SINTESIS DE HANTZSCH PARA PIRIDINAS OBJETIVO.
Obtencin de dihidropiridina por la reaccin de Hantzsch, y su consiguiente oxidacin para dar piridinas polisustitudas.
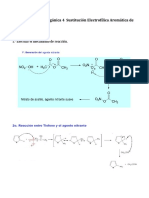
1.- Sntesis de Hantzsch. La Sntesis de pirroles de Hantzsch es un mtodo de sntesis orgnica que consiste en la preparacin de pirroles sustituidos (3) a partir de -cetosteres (1) con -halocetonas (2) en presencia de amoniaco (o aminas primarias). La describi por primera vez el qumico Arthur Rudolf Hantzsch. El mtodo consiste en 4 etapas:[] 1) Se forma de la base de Schiff entre el amoniaco y el -cetoster. La imina se encuentra en equilibrio con su enamina. 2) La enamina se condensa con el carbonilo de la -halocetona, formando la imina ,insaturada. 3) El nitrgeno de la imina reacciona con el carbono unido al halgeno en una reaccin de SN2 4)Se elimina el protn disponible en la posicin 2 del pirrol formado para dar el producto aromtico.
2.- Formacin y reaccin de enaminas, condensacin de Knoevenagel, adicin tipo Michael, mtodo de sntesis de piridinas. Las enaminas se obtienen por reaccin de aldehdos o cetonas con aminas secundarias. Mecanismo de formacin de enaminas Despus del ataque inicial de la amina secundaria al carbonilo, se elimina agua formndose el doble enlace entre el carbono carbonilo y el alfa del carbonilo de partida. La condensacin o reaccin de Knoevenagel es una reaccin en la que se produce la adicin nuclefila sobre el carbonilo, de un aldehdo o cetona, de un carbono activado (cido) situado entre dos grupos aceptores de electrones por resonancia, grupo seguido por una reaccin de deshidratacin en el que se elimina una molcula de agua. La condensacin o reaccin de Knoevenagel es una reaccin qumica orgnica en la que se produce la adicin nuclefila sobre el carbonilo, de un aldehdo o cetona, de un carbono activado (cido) situado entre dos grupos aceptores de electrones por resonancia, por ejemplo un compuesto -dicarbonlico, seguida a continuacin de deshidratacin (prdida de una molcula de agua), en lo que sera globalmente una reaccin de tipo condensacin aldlica, obtenindose un producto ,-insaturado. La reaccin es catalizada por una amina, en la forma de hidrocloruro o acetato de la misma. Ejemplo de reaccin de Knoevenagel
En general, el papel como catalizador de la amina, dada adems su relativa debilidad como base, no es tanto el de desprotonar el metileno activo (cido) para generar el enolato como s el de adicionarse al carbonilo del aldehdo o cetona para formar la sal de iminio, un buen electrfilo. La reaccin de Michael o adicin de Michael consiste en una adicin nuclefila de un carbanin a un compuesto carbonlico ,-insaturado. Pertenece a la clase ms grande de las adiciones conjugadas. Es uno de los mtodos ms tiles de formacin de enlaces C-C en condiciones suaves. Existen muchas variantes asimtricas. Mecanismo general de la reaccin de Michael
En este esquema los sustituyentes R y R' en el nuclefilo son grupos electroaceptores tales como los acilo y ciano convirtiendo al hidrgeno metilnico en cido, que al reaccionar con la base B: da lugar al carbanin. El sustituyente en el alqueno activado es normalmente una cetona, lo que la convierte en una enona, pero puede ser tambin un grupo nitro. Tal como fue definida originalmente por Michael,3 la reaccin es una adicin de un enolato de una cetona o aldehdo sobre el carbono de un compuesto carbonlico ,-insaturado (el "aceptor" de Michael). Una definicin posterior, propuesta por Kohler,4 es la adicin 1,4 de un carbono nuclefilo doblemente estabilizado a un compuesto carbonlico ,-insaturado. Algunos ejemplos de nuclefilos incluyen a beta-cetoesteres, malonatos y beta-cianoesteres. El producto resultante contiene un altamente til patrn de dos carbonilos (C=O) en 1,5. El mecanismo de reaccin es esbozado a continuacin con un compuesto 1,3-dicarbonilo 1, (siendo p.ej. R un residuo alcoxi), como nuclefilo:
Mecanismo de la reaccin de Michael
La desprotonacin de 1 por la base conduce al carbanin 2 estabilizado por sus grupos electroaceptores. Las estructuras 2a a 2c son tres estructuras de resonancia que pueden ser dibujadas para esta especie, dos de las cuales son iones enolato. Este nuclefilo reacciona con el alqueno eletroflico 3 dando 4 en una reaccin de adicin conjugada. La abstraccin del protn de la base protonada (o del solvente) por el enolato conduce al producto 5, siendo este el paso final. 3.- Importancia y aplicacin de piridinas La piridina y los compuestos relacionados con ella encuentran gran utilidad como disolventes, en anlisis qumicos, y como reactivos para la sntesis de frmacos, insecticidas, herbicidas, saborizantes, colorantes, adhesivos, pinturas, explosivos, desinfectantes y qumicos para el caucho. Tambin es utilizada junto con las picolinas como desnaturalizante en mezclas anticongelantes y en el alcohol etlico, en fungicidas, y en la tincin de textiles. REFERENCIAS: Fundamentos de quimica heterociclica, Leo Paquete 1 edicin, editorial limusa Quimica Organica , Mc Macmurry, 6-edicion, Editorial Tomson, Mexico 1999. http://www.academiaminasonline.com/aldehidos-cetonas/198-formacion-enaminas.html
Das könnte Ihnen auch gefallen
- Cálculo de parámetros de rapidez en cinética química, cinética enzimática y catálisis heterogéneaVon EverandCálculo de parámetros de rapidez en cinética química, cinética enzimática y catálisis heterogéneaBewertung: 5 von 5 Sternen5/5 (1)
- Previo HidantoínasDokument9 SeitenPrevio HidantoínasUriel RamosNoch keine Bewertungen
- Previo 5 Q.O IIIDokument2 SeitenPrevio 5 Q.O IIIMichell Maximiliano Santillan HerrejonNoch keine Bewertungen
- Reporte 5 PirazolonasDokument4 SeitenReporte 5 PirazolonasAnonymous enA4SSNoch keine Bewertungen
- Previo 2 NitrotiofenoDokument4 SeitenPrevio 2 NitrotiofenoAngelicaBaezNoch keine Bewertungen
- Carbonylchlorohydridotris (Triphenylphosphine) RutheniumDokument6 SeitenCarbonylchlorohydridotris (Triphenylphosphine) RutheniumatomsformeNoch keine Bewertungen
- Formación de CumarinasDokument6 SeitenFormación de CumarinasJessica BMNoch keine Bewertungen
- PRÁCTICA No. 4: OBTENCIÓN DE 5,5-DIFENILHIDANTOINADokument7 SeitenPRÁCTICA No. 4: OBTENCIÓN DE 5,5-DIFENILHIDANTOINADiana HMNoch keine Bewertungen
- Dibenzalacetona PracticaDokument4 SeitenDibenzalacetona PracticaBrayan Efrain Orozco SoteloNoch keine Bewertungen
- 2 Nitro TiofenoDokument7 Seiten2 Nitro TiofenoAngel HernándezNoch keine Bewertungen
- Investigación Previa Obtención de Hidantoinas OrgánicaDokument8 SeitenInvestigación Previa Obtención de Hidantoinas OrgánicaDaniel Romano100% (1)
- Previo 2-NitrotiofenoDokument5 SeitenPrevio 2-NitrotiofenoEdgar Armando100% (5)
- Formacion de IndolesDokument4 SeitenFormacion de IndolesMariana CervanteesNoch keine Bewertungen
- 2-Nitrotiofeno PrevioDokument5 Seiten2-Nitrotiofeno PrevioLyn Quinn Mim100% (1)
- Previo de Orgánica III Práctica 2Dokument4 SeitenPrevio de Orgánica III Práctica 2ChirinoNoch keine Bewertungen
- Previo Org Acetanilida.Dokument27 SeitenPrevio Org Acetanilida.Anonymous wGV7fYXgNoch keine Bewertungen
- NitrotiofenoDokument3 SeitenNitrotiofenoGaby RodriguezNoch keine Bewertungen
- Aldair 201 Q Qo4 Vi B Hidantoinas 1° Intento PDokument9 SeitenAldair 201 Q Qo4 Vi B Hidantoinas 1° Intento PAldair HernandezNoch keine Bewertungen
- BenciloDokument3 SeitenBenciloLily LeroNoch keine Bewertungen
- Qoiii Rep 01 MenadionaDokument2 SeitenQoiii Rep 01 MenadionaFrancisco QuirozNoch keine Bewertungen
- Reporte Practica 3Dokument5 SeitenReporte Practica 3Daniel OlveraNoch keine Bewertungen
- AspirinaDokument7 SeitenAspirinaFernanda GómezNoch keine Bewertungen
- Previo 4 Q O III PirrolDokument4 SeitenPrevio 4 Q O III PirrolAngel ZurielNoch keine Bewertungen
- Previo BenciloDokument6 SeitenPrevio BenciloHeber Daniel Andrade Rivera100% (1)
- Previo 10Dokument6 SeitenPrevio 10Carlos CastilloNoch keine Bewertungen
- Síntesis Del CiclohexenoDokument14 SeitenSíntesis Del CiclohexenophtalicNoch keine Bewertungen
- Cuestionario Previo 16 BenciloDokument5 SeitenCuestionario Previo 16 BenciloDavid AquinoNoch keine Bewertungen
- Sintesis de 6-MetiltiouraciloDokument3 SeitenSintesis de 6-MetiltiouraciloKarenNoch keine Bewertungen
- Practica 6 ADokument6 SeitenPractica 6 AMiguel Angel LlunaNoch keine Bewertungen
- Previo 3 Orgánica 4Dokument5 SeitenPrevio 3 Orgánica 4dany_289Noch keine Bewertungen
- Reporte Práctica 9 - Obtención de BenzimidazolDokument8 SeitenReporte Práctica 9 - Obtención de BenzimidazolMelissa Galan100% (1)
- 2,4 DinitroclorobencenoDokument5 Seiten2,4 DinitroclorobencenoFanny Arvizu AgNoch keine Bewertungen
- NitroanilinaDokument4 SeitenNitroanilinaDiana MoedanoNoch keine Bewertungen
- Organo Pre VioDokument17 SeitenOrgano Pre VioJonathan VillafañeNoch keine Bewertungen
- Compuestos de RU (Ii) Organomet.Dokument11 SeitenCompuestos de RU (Ii) Organomet.Tommy Chente MartinezNoch keine Bewertungen
- Reporte Practica 2 - Sintesis de AzocompuestosDokument7 SeitenReporte Practica 2 - Sintesis de AzocompuestosNicte Llanes0% (1)
- p1 Obtencion Del Epoxido de MenadionaDokument6 Seitenp1 Obtencion Del Epoxido de MenadionadanielNoch keine Bewertungen
- 2 Nitrotiofeno 2Dokument7 Seiten2 Nitrotiofeno 2anon_506134490Noch keine Bewertungen
- Efecto Del NaF Sobre La Actividad Glucolítica...Dokument9 SeitenEfecto Del NaF Sobre La Actividad Glucolítica...Danae LezcanoNoch keine Bewertungen
- Practicas QOIII 2020-IDokument72 SeitenPracticas QOIII 2020-IUriel RamosNoch keine Bewertungen
- Bencilo ReporteDokument2 SeitenBencilo ReporteDavid Ramirez50% (2)
- Investigacion Previa Practica Sintesis de Acido BarbituricoDokument3 SeitenInvestigacion Previa Practica Sintesis de Acido BarbituricoDaniel RomanoNoch keine Bewertungen
- Reacción de Condensación de PechmannDokument6 SeitenReacción de Condensación de PechmannNubia PorrasNoch keine Bewertungen
- Reacción de KnoevenagelDokument12 SeitenReacción de KnoevenagelKatherine RamírezNoch keine Bewertungen
- Síntesis de Pirazolona 1Dokument3 SeitenSíntesis de Pirazolona 1Mónica MedinaNoch keine Bewertungen
- Sintesis Acido CinamicoDokument8 SeitenSintesis Acido Cinamicodavid mateusNoch keine Bewertungen
- Acido Fenoxiacetico Previo y ReporteDokument5 SeitenAcido Fenoxiacetico Previo y Reportebrayan gutierrezNoch keine Bewertungen
- Reporte 7 Sintesis de HantzschDokument7 SeitenReporte 7 Sintesis de Hantzschangelreyes7gpapirrinNoch keine Bewertungen
- Perkin Acido CinamicoDokument5 SeitenPerkin Acido CinamicoFernanda DomínguezNoch keine Bewertungen
- Identificacion de Aldehidos y CetonasDokument48 SeitenIdentificacion de Aldehidos y CetonasUriel Ramos100% (1)
- Sustitución Electrófilica Aromática en Tiofeno.2Dokument2 SeitenSustitución Electrófilica Aromática en Tiofeno.2dany_289Noch keine Bewertungen
- Informe 7 Preparación de 3-CarbetoxicumarinaDokument11 SeitenInforme 7 Preparación de 3-CarbetoxicumarinaDani SantoyoNoch keine Bewertungen
- AcetanilidaDokument7 SeitenAcetanilidaLiLiana Niño100% (1)
- Benzoxazoles Benzotiazoles Bencimidazoles 3FM1Dokument32 SeitenBenzoxazoles Benzotiazoles Bencimidazoles 3FM1Pamela Adkins50% (2)
- Cuestionario OrganometalicaDokument2 SeitenCuestionario OrganometalicaOSMIN DURAN VILLEDANoch keine Bewertungen
- Tarea Clase 13 - 10 - 2021Dokument6 SeitenTarea Clase 13 - 10 - 2021Romel Esteban ReyesNoch keine Bewertungen
- Alquenos y AlquinosDokument7 SeitenAlquenos y AlquinosJesúsHenriquezNoch keine Bewertungen
- Reacciones de AlquinosDokument8 SeitenReacciones de AlquinoskarinaNoch keine Bewertungen
- Muchas de Las Reacciones de Los Alquinos SonDokument13 SeitenMuchas de Las Reacciones de Los Alquinos SonFrank Pitalua BarbosaNoch keine Bewertungen
- Aldehídos y Cetonas 2022Dokument18 SeitenAldehídos y Cetonas 2022eliana vegaNoch keine Bewertungen
- Curso Energía FotovoltaicaDokument71 SeitenCurso Energía FotovoltaicaLuisNoch keine Bewertungen
- Ejercicios Fluidos en ReposoDokument3 SeitenEjercicios Fluidos en ReposoMateo Ortega PalenciaNoch keine Bewertungen
- MC - Sem 02 - Ses 04 - Tabla PeriódicaDokument5 SeitenMC - Sem 02 - Ses 04 - Tabla PeriódicaJulio SurfNoch keine Bewertungen
- Practica 9 Práctica Obtención de Biodisel A Partir de Aceite de CocinaDokument4 SeitenPractica 9 Práctica Obtención de Biodisel A Partir de Aceite de CocinaDaniel MartínezNoch keine Bewertungen
- TEMA 9. Técnicas Luminiscentes.Dokument29 SeitenTEMA 9. Técnicas Luminiscentes.Daniel MontealegreNoch keine Bewertungen
- Propiedades ElasticasDokument5 SeitenPropiedades ElasticasFrank Gomer Gonzales ArroyoNoch keine Bewertungen
- 7 Unidad VII. QMA-103Dokument10 Seiten7 Unidad VII. QMA-103Omar SantosNoch keine Bewertungen
- Practica Calificada SsDokument4 SeitenPractica Calificada Ssmartin alvaradoNoch keine Bewertungen
- Expociencia DefinitivaDokument17 SeitenExpociencia DefinitivaAlexNoch keine Bewertungen
- LABORATORIO #2 Clasificación de SuelosDokument16 SeitenLABORATORIO #2 Clasificación de SuelosbrayanNoch keine Bewertungen
- Portafolio PDFDokument40 SeitenPortafolio PDFHander Gudiel Palacios LópezNoch keine Bewertungen
- QUÍMICADokument22 SeitenQUÍMICADaniel AvendañoNoch keine Bewertungen
- Cristalografía y MineralogiaDokument29 SeitenCristalografía y MineralogiaJhonatan romuchoNoch keine Bewertungen
- Cuadro Conductividad y ResistividadDokument4 SeitenCuadro Conductividad y ResistividadRuben RubenNoch keine Bewertungen
- Diseño de Plantas - Coagulación-FloculaciónDokument7 SeitenDiseño de Plantas - Coagulación-FloculaciónJUAN VICTOR VALDIVIA FARFANNoch keine Bewertungen
- Reactor CSTRDokument21 SeitenReactor CSTRDavid Ramirez TorresNoch keine Bewertungen
- Preparatorio 1.1 Fisica Mendez Arias LatexDokument8 SeitenPreparatorio 1.1 Fisica Mendez Arias LatexLupita MéndezNoch keine Bewertungen
- CJ01 Cajamarca v3.0Dokument4 SeitenCJ01 Cajamarca v3.0Demetrio Carranza Peña100% (2)
- Red Escalera R2R.Dokument10 SeitenRed Escalera R2R.Daniel Gómez RodríguezNoch keine Bewertungen
- Practica Final Oscurecimiento EnzimáticoDokument12 SeitenPractica Final Oscurecimiento EnzimáticoYare BGNoch keine Bewertungen
- 2014A Roberto Paz - Silabo Mecanica de Fluidos e Hidraulica BDokument10 Seiten2014A Roberto Paz - Silabo Mecanica de Fluidos e Hidraulica BChristian DanyNoch keine Bewertungen
- Copia de Copia de Desechos TóxicosDokument8 SeitenCopia de Copia de Desechos TóxicosAngie De la PazNoch keine Bewertungen
- Criogenia AlimentariaDokument7 SeitenCriogenia AlimentariaDavid Parado0% (1)
- Guia 1 Periodo 2Dokument3 SeitenGuia 1 Periodo 2ELIANANoch keine Bewertungen
- Taller 2 Calor 2014-02Dokument1 SeiteTaller 2 Calor 2014-02sanpornuNoch keine Bewertungen
- Rejilla de Biología (Energía Celular)Dokument7 SeitenRejilla de Biología (Energía Celular)EstebanNoch keine Bewertungen
- Clase 8 - Trans - CalorDokument72 SeitenClase 8 - Trans - Calormundo de diamantinasNoch keine Bewertungen
- Ja 2006Dokument457 SeitenJa 2006Estefany SanchezNoch keine Bewertungen
- PolimerosDokument32 SeitenPolimerosCristina GonzálezNoch keine Bewertungen
- T02 - Aguilar Hidrogo Manuel AlejandroDokument8 SeitenT02 - Aguilar Hidrogo Manuel AlejandroManuel AlejandroNoch keine Bewertungen
- Cómo hacer que te pasen cosas buenas: Entiende tu cerebro, gestiona tus emociones, mejora tu vidaVon EverandCómo hacer que te pasen cosas buenas: Entiende tu cerebro, gestiona tus emociones, mejora tu vidaBewertung: 5 von 5 Sternen5/5 (1875)
- La revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaVon EverandLa revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaBewertung: 5 von 5 Sternen5/5 (203)
- Psicología oscura: Una guía esencial de persuasión, manipulación, engaño, control mental, negociación, conducta humana, PNL y guerra psicológicaVon EverandPsicología oscura: Una guía esencial de persuasión, manipulación, engaño, control mental, negociación, conducta humana, PNL y guerra psicológicaBewertung: 4.5 von 5 Sternen4.5/5 (766)
- Recupera tu mente, reconquista tu vidaVon EverandRecupera tu mente, reconquista tu vidaBewertung: 5 von 5 Sternen5/5 (9)
- Yo Pude, ¡Tú Puedes!: Cómo tomar el control de tu bienestar emocional y convertirte en una persona imparable (edición revisada y expandida)Von EverandYo Pude, ¡Tú Puedes!: Cómo tomar el control de tu bienestar emocional y convertirte en una persona imparable (edición revisada y expandida)Bewertung: 5 von 5 Sternen5/5 (8)
- Batidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoVon EverandBatidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoBewertung: 5 von 5 Sternen5/5 (2)
- Tus Zonas Erroneas: Guía Para Combatir las Causas de la InfelicidadVon EverandTus Zonas Erroneas: Guía Para Combatir las Causas de la InfelicidadBewertung: 4.5 von 5 Sternen4.5/5 (1833)
- Resetea tu mente. Descubre de lo que eres capazVon EverandResetea tu mente. Descubre de lo que eres capazBewertung: 5 von 5 Sternen5/5 (196)
- El poder del optimismo: Herramientas para vivir de forma más positivaVon EverandEl poder del optimismo: Herramientas para vivir de forma más positivaBewertung: 5 von 5 Sternen5/5 (16)
- Resumen de Pensar rápido pensar despacio de Daniel KahnemanVon EverandResumen de Pensar rápido pensar despacio de Daniel KahnemanBewertung: 4.5 von 5 Sternen4.5/5 (64)
- La violencia invisible: Identificar, entender y superar la violencia psicológica que sufrimos (y ejercemos) en nuestra vida cotidianaVon EverandLa violencia invisible: Identificar, entender y superar la violencia psicológica que sufrimos (y ejercemos) en nuestra vida cotidianaBewertung: 4 von 5 Sternen4/5 (2)
- DMT: La molécula del espíritu (DMT: The Spirit Molecule): Las revolucionarias investigaciones de un medico sobre la biologia de las experiencias misticas y cercanas a la muerteVon EverandDMT: La molécula del espíritu (DMT: The Spirit Molecule): Las revolucionarias investigaciones de un medico sobre la biologia de las experiencias misticas y cercanas a la muerteBewertung: 4.5 von 5 Sternen4.5/5 (19)
- La metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceVon EverandLa metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceBewertung: 5 von 5 Sternen5/5 (8)
- Contra la ansiedad: Una guía completa para manejar emociones difícilesVon EverandContra la ansiedad: Una guía completa para manejar emociones difícilesBewertung: 5 von 5 Sternen5/5 (58)
- Tu cerebro emocional: Saca partido de lo que sientes y transforma tu vidaVon EverandTu cerebro emocional: Saca partido de lo que sientes y transforma tu vidaBewertung: 5 von 5 Sternen5/5 (2)
- Influencia. La psicología de la persuasiónVon EverandInfluencia. La psicología de la persuasiónBewertung: 4.5 von 5 Sternen4.5/5 (14)
- The Coaching Habit: Las 7 preguntas clave para liderar equipos y organizaciones del siglo XXIVon EverandThe Coaching Habit: Las 7 preguntas clave para liderar equipos y organizaciones del siglo XXIBewertung: 4.5 von 5 Sternen4.5/5 (166)
- Liberación del trauma: Perdón y temblor es el caminoVon EverandLiberación del trauma: Perdón y temblor es el caminoBewertung: 4 von 5 Sternen4/5 (4)
- Homo antecessor: El nacimiento de una especieVon EverandHomo antecessor: El nacimiento de una especieBewertung: 5 von 5 Sternen5/5 (1)
- Sistema nervioso y osteopatía: Nervios periféricos, meninges craneales y espinales, y sistema nervioso vegetativo (Color)Von EverandSistema nervioso y osteopatía: Nervios periféricos, meninges craneales y espinales, y sistema nervioso vegetativo (Color)Bewertung: 5 von 5 Sternen5/5 (9)
- Una mente en calma: Técnicas para manejar los pensamientos intrusivosVon EverandUna mente en calma: Técnicas para manejar los pensamientos intrusivosBewertung: 4.5 von 5 Sternen4.5/5 (143)
- Yo, ego. Una guía para dejar de sufrir, conectar contigo mismo y alcanzar la paz mentalVon EverandYo, ego. Una guía para dejar de sufrir, conectar contigo mismo y alcanzar la paz mentalBewertung: 4.5 von 5 Sternen4.5/5 (7)
- Escritura terapéutica. El poder curativo de la expresión escritaVon EverandEscritura terapéutica. El poder curativo de la expresión escritaBewertung: 5 von 5 Sternen5/5 (2)
- El Tesoro Escondido (Hidden Treasure): La vida interior de niños y adolescentes. Terapia infanto-juvenilVon EverandEl Tesoro Escondido (Hidden Treasure): La vida interior de niños y adolescentes. Terapia infanto-juvenilBewertung: 5 von 5 Sternen5/5 (4)
- Terapia cognitivo-conductual (TCC) y terapia dialéctico-conductual (TDC): Cómo la TCC, la TDC y la ACT pueden ayudarle a superar la ansiedad, la depresión, y los TOCSVon EverandTerapia cognitivo-conductual (TCC) y terapia dialéctico-conductual (TDC): Cómo la TCC, la TDC y la ACT pueden ayudarle a superar la ansiedad, la depresión, y los TOCSBewertung: 5 von 5 Sternen5/5 (1)