Beruflich Dokumente
Kultur Dokumente
Aula 9 QA Classica KMB
Hochgeladen von
Ancelmo Queiroz JúniorCopyright
Verfügbare Formate
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
Verfügbare Formate
Aula 9 QA Classica KMB
Hochgeladen von
Ancelmo Queiroz JúniorCopyright:
Verfügbare Formate
UNIVERSIDADE FEDERAL DA PARABA
Centro de Cincias Exatas e da Natureza Departamento de Qumica Qumica Analtica Clssica
Equilbrio de solubilidade
Profa. Ktia Messias Bichinho 2010/2
UNIVERSIDADE FEDERAL DA PARABA
Centro de Cincias Exatas e da Natureza Departamento de Qumica Qumica Analtica Clssica
Contedo
1. Solubilidade
2. Soluo saturada, insaturada e supersaturada 3. Equilbrio de solubilidade 4. Produto de solubilidade 5. Produto de solubilidade e Kps 6. Clculos Kps e solubilidade 7. Fatores que afetam a solubilidade
Qumica Analtica Clssica
Solubilidade
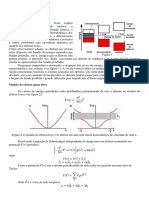
A uma dada temperatura, existe uma quantidade limite de uma dada substncia que se consegue dissolver num determinado volume de solvente, e que se denomina solubilidade dessa substncia nesse solvente. A solubilidade representada por S. Por exemplo, temperatura de 25 C, possvel dissolver cerca de 36 gramas de cloreto de sdio) em 100 mL de gua, sendo, portanto 36 g/100 mL a solubilidade do cloreto de sdio em gua.
Qumica Analtica Clssica
Classificao de solues Solubilidade do soluto no solvente
Saturada: Exemplos: contm a mxima quantidade de soluto dissolvido em um dado volume de solvente a uma dada temperatura. acar possui solubilidade de 200g /100 mL ( 20C ). CaSO4 possui solubilidade de 0,2 g /100 mL ( 20C ). contm uma quantidade de soluto dissolvido inferior solubilidade possvel a uma dada temperatura. contm mais soluto dissolvido e tende a precipitar parte do soluto, formando uma soluo saturada.
Insaturada:
Supersaturada:
Qumica Analtica Clssica
Equilbrio de Solubilidade
Considerando uma soluo saturada de cloreto de prata, AgCl. Se continuarmos a adicionar AgCl a uma soluo saturada, verificamos que h formao de precipitado, e passamos a ter uma soluo heterognea com uma fase lquida e uma fase slida. Nestas condies, ocorre um equilbrio entre estas duas fases, designado por equilbrio em solues saturadas de sais, e que, neste caso, pode ser representado por: AgCl (s) AgCl (aq) O momento em que a velocidade de dissoluo iguala-se velocidade de precipitao, corresponde ao instante em que se estabelece o equilbrio de solubilidade do sal em estudo.
Qumica Analtica Clssica
Equilbrio de solubilidade
Equilbrio entre um eletrlito pouco solvel e os ons que este eletrlito libera em soluo. Ex: soluo de AgCl ocorrem os seguintes equilbrios: AgCl (s) AgCl (aq) Ag+(aq) + Cl-(aq) Ks Kd Kps = Ks.Kd
Qumica Analtica Clssica
Equilbrio de solubilidade MA(s) MA(aq) M+ + AS = S0 + [M+]
S0 = solubilidade intrnseca ou molecular
M+ MA(aq) M+ AAM+ AM+ AM+ A- MA (aq)
MA(s)
Obs: os haletos de prata agem como eletrlitos fracos, dissociando-se apenas parcialmente em gua.
Qumica Analtica Clssica
Equilbrio de solubilidade
Exerccio 1 Calcular a solubilidade do AgCl em gua destilada. Ks = 3,6 x 10-7. Solubilidade = S = [AgCl(aq)] + [Ag+] [Ag+] = [Cl-] [Ag+] [Cl-] = Kps 1,82 x 10-10 [Ag+] = 1,82 x 10-10 = 1,35 x 10-5 Sabendo que S = 3,6 x 10-7 S = 1,35 x 10-5 + 3,6 x 10-7 = 1,38 10-5 mol L-1
Qumica Analtica Clssica
Equilbrio de solubilidade
No entanto, a maioria dos sais pouco solveis encontra-se essencial e totalmente dissociado em solues aquosas saturadas. [Ba2 ][IO3 ]2 K Ba(IO3)2(s) = Ba2+(aq) + 2IO3-
Ba(IO3 )2 (s )
K Ba(IO3 )2 (s ) K ps [Ba2 ][IO3 ]2
Obs: quando dizemos que um sal pouco solvel est completamente dissociado, no significa que todo o sal se dissolve. Ao contrrio, a pequena quantidade que realmente solubiliza dissocia-se totalmente.
Qumica Analtica Clssica
Qumica Analtica Clssica
Constante do Produto de Solubilidade Kps MA(s) M+(aq) + A-(aq)
Keq
M+ MA(aq) M+ AAM+ AM+ AM+ A- MA (aq)
aM a A aMA(s )
MA(s)
[ M ][ A ] Keq [ MAs ]
Qumica Analtica Clssica
Constante do Produto de Solubilidade Kps
Exemplo 1. Soluo de Ba(IO3)2(s) ocorre o seguinte equilbrio:
Ba(IO3)2(s) = Ba2+(aq) + 2IO3-
Keq
aBa 2 aIO
3
aBa ( IO3 ) 2 ( s )
Kps= aBa2+ aIO3-
Obs: Ba(IO3)2(s) estado padro a=1
Portanto, o equilbrio independe da quantidade de slido em contato com a soluo.
Qumica Analtica Clssica
Constante do Produto de Solubilidade Kps
Quando o eletrlito pouco solvel e a fora inica baixa:
Kps = [Ba2+][IO3-]2
Exemplo 2: Ag2S 2Ag+ + 1S2Kps = [Ag+]2 [S2-]1
Qumica Analtica Clssica
Importncia da solubilidade
As estalactites e estalagmites encontradas em grutas e cavernas, no so mais do que equilbrios de solubilidade entre os depsitos subterrneos, constitudos essencialmente por carbonato de clcio (CaCO3), e as guas naturais, como por exemplo a gua da chuva. Outro exemplo o sulfato de brio (BaSO4), sal insolvel e opaco aos raios X, que usado em meios de diagnstico de problemas do tubo digestivo.
Qumica Analtica Clssica
Princpio do produto de solubilidade
Em uma soluo saturada de um eletrlito pouco solvel, o produto das concentraes molares dos ons (molL-1),
elevadas a potncias apropriadas constante, para uma
dada temperatura, independentemente de outros
eletrlitos presentes na soluo.(Nernst 1889)
Qumica Analtica Clssica
Produto de Solubilidade e Solubilidade
Ex.: AgCl
S representa a solubilidade (em molL-1) do AgCl em gua 1AgCl(s) 1Ag+ + 1ClComo um mol de Ag+ formado para cada mol de AgCl, a S do AgCl = [Ag+] e sei que [Ag+] = [Cl-]:
Kps = [Ag+][Cl-] Kps = S S
S Kps
Kps = S2
Qumica Analtica Clssica
Produto de Solubilidade e Solubilidade
Em geral, para sais moderadamente solveis:
S ( xy )
K ps x y
x y
Qumica Analtica Clssica
Produto de Solubilidade e Solubilidade
Ex. CaF2 Ca2+ + 2FComo um mol de Ca2+ formado para cada mol de CaF2, a S do CaF2 = [Ca2+] e [F-] = 2S. Kps = [Ca2+]1 [F-]2 Kps = S1 (2S)2 = 4S3 Kps = 4S3
Kps 4
Qumica Analtica Clssica
Produto de Solubilidade e Solubilidade
Qumica Analtica Clssica
Clculo de Kps a partir da solubilidade Exerccio 2. A solubilidade do AgCl a 25C 1,9x10-4 g por 100 mL. Calcular seu Kps. a) Escrever a equao inica para o equilbrio de solubilidade AgCl(s) Ag+ + Clb) Formular a expresso de Kps Kps= [Ag+][Cl-] c) Calcular as concentraes molares dos ons S = 1,9x10-4 g em 100 mL , ou seja, S =1,9x10-3 gL-1 Massa molar do AgCl = 143,32 g mol-1
Qumica Analtica Clssica
Clculo de Kps a partir da solubilidade Exerccio 2. A solubilidade do AgCl a 25C 1,9x10-4 g por 100 mL. Calcular seu Kps. d) Massa molar do AgCl = 143,32 g mol-1 A solubilidade molar S ser:
0,0019 1,33 10 5 molL1 143 ,32
S = [Ag+] = [Cl-] = 1,33x10-5 mol L-1
e) Substituir os valores na expresso do Kps Kps = [Ag+][Cl-] = (1,33x10-5)2 = 1,82 x 10-10 (mol L-1)2
Qumica Analtica Clssica
Clculo de Kps a partir da solubilidade
Exerccio 3. A solubilidade do AgCl a 10oC 0,000089 g/100 mL. O peso molecular do AgCl 143,32 g mol-1. Qual a solubilidade molar e o produto de solubilidade nesta temperatura? a)n = massa(g) / mol(g) n = 8,9 x 10-5 / 143,32 n = 6,21 x 10-7 mol c) S = (Kps)1/2 b) 6,21 x 10-7 mol 100 mL mol 1000 mL S = 6,21 x 10-6 mol L-1
6,21 x 10-6 = (Kps)1/2 Kps = (6,21 x 10-6 )2 Kps = 3,86 x 10-11
Qumica Analtica Clssica
Clculo de Kps a partir da solubilidade Exerccio 4. A solubilidade do Ag3PO4 0,20 mg por 100mL. Calcular seu Kps. a) Ag3PO4 3Ag+ + PO43b) Kps = [Ag+]3 [PO43-] c) 0,20 mg em 100mL ou 2x10-3 gL-1 d) Massa molar do Ag3PO4 = 419 g mol-1
0,0020 S 4,8 106 molL1 419
Qumica Analtica Clssica
Clculo de Kps a partir da solubilidade Exerccio 4. A solubilidade do Ag3PO4 0,20 mg por 100ml. Calcular seu Kps. e) Lembrando, Ag3PO4 3Ag+ + PO43[Ag+] = 3 x 4,8x10-6 = 1,44x10-5 [PO43-] = 4,8x10-6
Kps = [Ag+]3[PO43-] = (1,44x10-5)3(4,8x10-6)
Kps Ag3PO4= 1,4x10-20 (mol L-1)4
Qumica Analtica Clssica
Clculo de solubilidade a partir de Kps Exerccio 5.
O produto de solubilidade do CaF2 4,0 x 10-11. Calcule a solubilidade S. CaF2 Ca2+ + 2FS 2S Kps = [Ca2+][F-]2 S = (4,0 x 10-11 /4)1/3 Kps = S . (2S)2 Kps = 4S3
S = 2,2 x 10-4 mol L-1
Qumica Analtica Clssica
Kps e formao de precipitado
Kps de um eletrlito pouco solvel estabelece o critrio para a formao de um precipitado. Kps constante para uma dada temperatura. Se o produto das concentraes molares dos ons, com seus expoentes correspondentes (PI), menor que Kps a soluo no est saturada, ou seja, no haver formao de precipitado.
Qumica Analtica Clssica
Kps e formao de precipitado
Se PI < Kps , soluo no saturada, no haver ppt
Se PI = Kps , soluo saturada, no haver ppt
Se PI > Kps , forma-se ppt ou a soluo est supersaturada (metaestvel).
H precipitao do soluto quando o valor de KPS ultrapassado.
Qumica Analtica Clssica
Kps e formao de precipitado
Exerccio 6
O Kps para o BaSO4 1,0 x 10-10. Se em 1L de soluo existem 0,0010 mol de Ba2+ e 0,00010 mol de SO42- haver precipitao de BaSO4?
Soluo: a) BaSO4 Ba2+ + SO42b) KpsBaSO4= [Ba2+] [SO42-] = 1,0x10-10 c) Antes de alcanar o equilbrio: [Ba2+] = 1,0 x 10-3 [SO42-] = 1,0 x 10-4
d) PI = ( 1,0x10-3)(1,0x10-4) = 1,0x10-7 PI >> Kps=1,0x10-10 precipitar BaSO4
Qumica Analtica Clssica
Kps e formao de precipitado
Exerccio 7
Calcular a concentrao de on sulfeto necessria para iniciar a precipitao de FeS em uma soluo 1,0x10-4 molL-1 em Fe2+(Kps= 5x10-18).
Soluo: a) FeS Fe2+ + S2b) Kps = [Fe2+] [S2-] c) [Fe2+] = 1,0x10-4 d) [S2-] = Kps/1,0x10-4 = 5,0x10-14
saturao da soluo
Portanto, para precipitar FeS necessrio que a [S2-] > 5,0x10-14
Qumica Analtica Clssica
Fatores que afetam a solubilidade
1. Efeito da Presso A presso sobre o equilbrio de solues no exerce efeito significativo e prtico, pois os lquidos sofrem menos o efeito da presso do que gases. Alm disso, em geral as solues so trabalhadas sob presso atmosfrica.
Qumica Analtica Clssica
Fatores que afetam a solubilidade
2. Efeito da Temperatura O grau de dissociao de um sal solvel aumentar com o aumento da temperatura, em geral. Assim, a solubilidade molar aumentar.
Qumica Analtica Clssica
Fatores que afetam a solubilidade
3. Efeito da natureza do solvente A natureza polar da molcula de gua exerce efeitos de solvatao sobre nions e ctions do soluto, formando ons hidratados. Esta fora de atrao supera as foras que mantm ctions e nions na estrutura cristalina do sal. Solventes orgnicos no apresentam estas foras de atrao inicas da mesma forma que a gua. Ento muitos sais inorgnicos so pouco solveis nesses solventes.
Qumica Analtica Clssica
Fatores que afetam a solubilidade
4. Efeito do pH A solubilidade de precipitados contendo um nion com propriedades bsicas ou um ction com propriedades cidas ou ambos depende do pH. Os precipitados que contm nions do tipo base conjugada de um cido fraco so mais solveis em pH mais baixo.
Qumica Analtica Clssica
Fatores que afetam a solubilidade
5. Efeito do on comum O efeito do on uma consequncia da Lei das Ao das Massas descrita no princpio de Le Chatelier. O efeito do on comum responsvel pela reduo da solubilidade de um precipitado inico quando um composto solvel contendo um dos ons do precipitado adicionada soluo que est em equilbrio com o precipitado.
Exemplo: a solubilidade do AgCl em soluo 1,0 x 10-3molL-1 em Cl- cerca de 100 vezes menor que em H2O.
Qumica Analtica Clssica
Fatores que afetam a solubilidade
5. Efeito do on estranho Medidas de solubilidade de diferentes eletrlitos pouco solveis indicam que a solubilidade em soluo salina maior do que em gua. Exemplo AgCl e BaSO4 so mais solveis em soluo de KNO3 do que em gua.
Qumica Analtica Clssica
Exerccios 7) Calcular a solubilidade molar do Mg(OH)2 em gua. R. 1,2 x 10-4 mol L-1.
Kps e formao de precipitado
8) Sabendo que a solubilidade molar S do Ba(IO3)2 7,32 x 10-4 mol L-1, calcule o produto de solubilidade, Kps. R. 1,57 x 10-9.
9) Sabendo que Kps 1,57 x 10-9, calcule a solubilidade molar S do Ba(IO3)2. Quantos gramas de Ba(IO3)2 (487 g/mol) podem ser dissolvidos em 500 mL de gua a 25C? R. 0,178g 10) Diferente da maioria dos sais, o sulfato de clcio dissocia-se apenas parcialmente em soluo aquosa. Sabendo que Kd = 5,2 x 10-3 e que a constante do produto de solubilidade do sulfato de clcio 2,6 x 10-5, calcule a solubilidade do CaSO4 em gua. R. 1,01 x 10-2 mol L-1.
Das könnte Ihnen auch gefallen
- Industrias Do Ácido SulfuricoDokument25 SeitenIndustrias Do Ácido SulfuricogandramichaelNoch keine Bewertungen
- Mat111111eriais e Mét333333odosDokument1 SeiteMat111111eriais e Mét333333odosAncelmo Queiroz JúniorNoch keine Bewertungen
- Folder Bomba 407 Português 2021Dokument9 SeitenFolder Bomba 407 Português 2021Ancelmo Queiroz JúniorNoch keine Bewertungen
- Esforços M N QDokument28 SeitenEsforços M N Qpaniago44Noch keine Bewertungen
- MS Software MDSolids Problema 2Dokument1 SeiteMS Software MDSolids Problema 2Ancelmo Queiroz JúniorNoch keine Bewertungen
- Convolução2 PDFDokument3 SeitenConvolução2 PDFAncelmo Queiroz JúniorNoch keine Bewertungen
- Esforços M N QDokument28 SeitenEsforços M N Qpaniago44Noch keine Bewertungen
- TDQ - Cap 14Dokument37 SeitenTDQ - Cap 14Ancelmo Queiroz JúniorNoch keine Bewertungen
- Trocadores de Calor e Torres de ResfriamentoDokument1 SeiteTrocadores de Calor e Torres de ResfriamentoAncelmo Queiroz JúniorNoch keine Bewertungen
- PedrasDokument1 SeitePedrasAncelmo Queiroz JúniorNoch keine Bewertungen
- 203-Estudos de Corrosao em Meio de EtanolDokument8 Seiten203-Estudos de Corrosao em Meio de EtanolAncelmo Queiroz JúniorNoch keine Bewertungen
- Resolução de Todos Os CapítulosDokument2 SeitenResolução de Todos Os CapítulosAncelmo Queiroz JúniorNoch keine Bewertungen
- PedrasDokument1 SeitePedrasAncelmo Queiroz JúniorNoch keine Bewertungen
- Trocadores de Calor e Torres de ResfriamentoDokument1 SeiteTrocadores de Calor e Torres de ResfriamentoAncelmo Queiroz JúniorNoch keine Bewertungen
- Resolução de Todos Os CapítulosDokument2 SeitenResolução de Todos Os CapítulosAncelmo Queiroz JúniorNoch keine Bewertungen
- Padrão de Um Relatório - ExemploDokument3 SeitenPadrão de Um Relatório - ExemploWarlley Batista de DeusNoch keine Bewertungen
- Destilacao SimplesDokument5 SeitenDestilacao SimplesAncelmo Queiroz JúniorNoch keine Bewertungen
- Determin OuDokument1 SeiteDetermin OuAncelmo Queiroz JúniorNoch keine Bewertungen
- Sistemas OperacionaisDokument12 SeitenSistemas Operacionaishacker100% (2)
- Bloco 05Dokument56 SeitenBloco 05Ancelmo Queiroz JúniorNoch keine Bewertungen
- So LinuxDokument23 SeitenSo LinuxAncelmo Queiroz JúniorNoch keine Bewertungen
- So LinuxDokument23 SeitenSo LinuxAncelmo Queiroz JúniorNoch keine Bewertungen
- Constante de Equilíbrio e Energia Livre de Gibbs de Uma ReaçãoDokument12 SeitenConstante de Equilíbrio e Energia Livre de Gibbs de Uma ReaçãoAncelmo Queiroz Júnior100% (1)
- So LinuxDokument23 SeitenSo LinuxAncelmo Queiroz JúniorNoch keine Bewertungen
- ArtigoDokument3 SeitenArtigoAncelmo Queiroz JúniorNoch keine Bewertungen
- Bloco 06Dokument16 SeitenBloco 06Ancelmo Queiroz JúniorNoch keine Bewertungen
- Receita - Arroz MisturadoDokument1 SeiteReceita - Arroz MisturadoAncelmo Queiroz JúniorNoch keine Bewertungen
- A Europa TerezaDokument12 SeitenA Europa TerezaAncelmo Queiroz JúniorNoch keine Bewertungen
- 7ºano CiênciasDokument2 Seiten7ºano CiênciasLeda Maria da SilvaNoch keine Bewertungen
- Ligações iônicas e exercícios de químicaDokument4 SeitenLigações iônicas e exercícios de químicaAíla LimaNoch keine Bewertungen
- Aula 5 - Eb01007 - Quimica Geral E Experimental: DisciplinaDokument77 SeitenAula 5 - Eb01007 - Quimica Geral E Experimental: DisciplinaJuliane AlmeidaNoch keine Bewertungen
- Amperometria: princípios e aplicações em titulaçõesDokument38 SeitenAmperometria: princípios e aplicações em titulaçõeswalas joãoNoch keine Bewertungen
- Hidro A09 - Evaporação Evapotranspiração 1Dokument47 SeitenHidro A09 - Evaporação Evapotranspiração 1Alex BarbosaNoch keine Bewertungen
- NBR16057-Projeto Sistema Aquecimento A Gas r8 271011 PDFDokument37 SeitenNBR16057-Projeto Sistema Aquecimento A Gas r8 271011 PDFAndré Luis RosaNoch keine Bewertungen
- Escola Estadual José SeffairDokument4 SeitenEscola Estadual José SeffairAlexandre RochaNoch keine Bewertungen
- Determinação Do Ponto Isoelétrico Da CaseínaDokument6 SeitenDeterminação Do Ponto Isoelétrico Da CaseínaJailson SilvaNoch keine Bewertungen
- Moléculas, Íons e Seus CompostosDokument24 SeitenMoléculas, Íons e Seus CompostosÍcaro MychelNoch keine Bewertungen
- Exercicios Geometria Molecular e Polaridade PDFDokument3 SeitenExercicios Geometria Molecular e Polaridade PDFUilsonNoch keine Bewertungen
- Dispositivos 1-Semicondutores - Exercicios-V2.2Dokument2 SeitenDispositivos 1-Semicondutores - Exercicios-V2.2José Dos SantosNoch keine Bewertungen
- Preparação metalográfica, medição de dureza e tratamentos de açoDokument9 SeitenPreparação metalográfica, medição de dureza e tratamentos de açoMarcelo LiraNoch keine Bewertungen
- 2 Lista de ExercíciosDokument2 Seiten2 Lista de Exercíciosmari santosNoch keine Bewertungen
- Exercícios - Química - Físico QuímicaDokument51 SeitenExercícios - Química - Físico QuímicamariafbellincantaNoch keine Bewertungen
- Espectroscopia de Infravermelho - EXERCICIOS1Dokument6 SeitenEspectroscopia de Infravermelho - EXERCICIOS1Renato ZanNoch keine Bewertungen
- Exercícios de eletroquímica para o 3o ano do ensino médioDokument3 SeitenExercícios de eletroquímica para o 3o ano do ensino médioRamonquimicoNoch keine Bewertungen
- Apostila Forno de Fusão e CopelaçãoDokument76 SeitenApostila Forno de Fusão e CopelaçãoOtavio DuarteNoch keine Bewertungen
- 9º Ano EF Química Vanessa Oliveira PDFDokument35 Seiten9º Ano EF Química Vanessa Oliveira PDFDaniela FortunatoNoch keine Bewertungen
- Dilatação térmica exercíciosDokument3 SeitenDilatação térmica exercíciosJasminNoch keine Bewertungen
- PKa Do Ácido AcéticoDokument7 SeitenPKa Do Ácido AcéticoFABIANA DOS SANTOS SABINONoch keine Bewertungen
- N 1541 PDFDokument14 SeitenN 1541 PDFEzequiel CastilhoniNoch keine Bewertungen
- Atividade Ligações Químicas - CovalentesDokument2 SeitenAtividade Ligações Químicas - CovalentesALAINE NASCIMENTO FERREIRANoch keine Bewertungen
- Bandas de Energia nos CristaisDokument8 SeitenBandas de Energia nos CristaisJoel Augusto Moura PortoNoch keine Bewertungen
- Quimica Manual 2007Dokument218 SeitenQuimica Manual 2007Vagner Fafetine100% (5)
- Equilíbrio de complexos exercíciosDokument1 SeiteEquilíbrio de complexos exercíciosedniltongamaNoch keine Bewertungen
- Exercícios Propriedades ColigativasDokument3 SeitenExercícios Propriedades ColigativasLareska Rocha100% (1)
- Diagrama de blocos da planta de celuloseDokument5 SeitenDiagrama de blocos da planta de celuloseCaio R. FrancisquetteNoch keine Bewertungen
- Funções Inorgânicas-1Dokument186 SeitenFunções Inorgânicas-1DavidNoch keine Bewertungen
- Estrutura atômica e propriedades dos elementosDokument19 SeitenEstrutura atômica e propriedades dos elementosManuel Jose lemosNoch keine Bewertungen
- Prova Fisica Neja 2 Luiza H PradoDokument1 SeiteProva Fisica Neja 2 Luiza H PradoCarla Rodrigues SouzaNoch keine Bewertungen