Beruflich Dokumente
Kultur Dokumente
Ejercicio de Ciclo Ericsson
Hochgeladen von
David Ospina Moreno0%(1)0% fanden dieses Dokument nützlich (1 Abstimmung)
195 Ansichten19 SeitenEste documento describe un ciclo termodinámico de Ericsson que consta de 4 pasos: 1) Compresión isoterma del gas, 2) Expansión a presión constante calentando el gas, 3) Expansión isoterma reduciendo la presión, 4) Enfriamiento a presión constante. Se calcula el trabajo, calor y cambios de energía en cada paso usando las ecuaciones de la termodinámica para procesos cuasiestáticos de un gas ideal.
Originalbeschreibung:
Originaltitel
Ejercicio de ciclo Ericsson
Copyright
© © All Rights Reserved
Verfügbare Formate
PPTX, PDF, TXT oder online auf Scribd lesen
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenEste documento describe un ciclo termodinámico de Ericsson que consta de 4 pasos: 1) Compresión isoterma del gas, 2) Expansión a presión constante calentando el gas, 3) Expansión isoterma reduciendo la presión, 4) Enfriamiento a presión constante. Se calcula el trabajo, calor y cambios de energía en cada paso usando las ecuaciones de la termodinámica para procesos cuasiestáticos de un gas ideal.
Copyright:
© All Rights Reserved
Verfügbare Formate
Als PPTX, PDF, TXT herunterladen oder online auf Scribd lesen
0%(1)0% fanden dieses Dokument nützlich (1 Abstimmung)
195 Ansichten19 SeitenEjercicio de Ciclo Ericsson
Hochgeladen von
David Ospina MorenoEste documento describe un ciclo termodinámico de Ericsson que consta de 4 pasos: 1) Compresión isoterma del gas, 2) Expansión a presión constante calentando el gas, 3) Expansión isoterma reduciendo la presión, 4) Enfriamiento a presión constante. Se calcula el trabajo, calor y cambios de energía en cada paso usando las ecuaciones de la termodinámica para procesos cuasiestáticos de un gas ideal.
Copyright:
© All Rights Reserved
Verfügbare Formate
Als PPTX, PDF, TXT herunterladen oder online auf Scribd lesen
Sie sind auf Seite 1von 19
Ejercicio de ciclo Ericsson
Andrés Felipe Pinto Arias 41142081
Enunciado
• Se tiene un cilindro vertical de paredes no aislantes, en cuyo interior
se encuentra aire (considerado como un gas ideal diatómico). El
cilindro tiene sección cuadrada de lado 4 cm y está cerrado por un
pistón horizontal que puede deslizarse sin rozamiento.
• Inicialmente el pistón se encuentra a una altura de 10 cm y el aire
está en equilibrio térmico y mecánico con el exterior a una
temperatura de 300 K y una presión 100 kPa.
Se procede entonces a efectuar el siguiente ciclo
• A→B El gas se comprime lentamente, colocando sobre la tapa el
equivalente a 4 kg de arena, sin que se modifique la temperatura
exterior.
• B→C Sin retirar la arena, se calienta lentamente el gas, hasta que el
volumen vuelve a ser el inicial.
• C→D Manteniendo constante la nueva temperatura, se van retirando
los granos de arena hasta que no queda ni uno.
• D→A Se enfría gradualmente el gas, hasta que su volumen vuelve a
ser el inicial.
A→B
En el primer paso tenemos que se va aumentando lentamente la
presión sobre el gas, manteniéndose constante la temperatura. El
proceso es una compresión isoterma, que podemos suponer
cuasiestática. En todo momento se cumple la ley de Boyle
B→C
En el segundo proceso se aumenta la temperatura, pero el pistón
puede moverse. Esto quiere decir que se trata de una expansión a
presión constante. Gráficamente corresponde a un segmento
horizontal en un diagrama pV.
C→D
En el tercer paso la presión disminuye lentamente, hasta volver a ser la
presión inicial, sin que cambie la temperatura. Al tratarse de una
expansión isoterma cuasiestática, volvemos a tener un arco de
hipérbola entre los estados C y D. Para el estado C tenemos
D→A
En el último paso se reduce la temperatura, con el pistón libre. La
presión permanece constante, lo que implica un nuevo segmento
inicial. El estado final A' tiene la misma presión que A y el mismo
volumen que A, por lo que A' = A y el ciclo se cierra.
Trabajo, calor y energía
A partir de los valores anteriores es fácil hallar cada una de las
magnitudes energéticas, ya que al ser todos los procesos
cuasiestáticos, poseen expresiones en función de la presión y volumen
inicial y final de cada paso.
A→B
El primer paso es una compresión isoterma cuasiestática de un gas
ideal. Puesto que no varía la temperatura, tampoco lo hace la energía
interna
ni la entalpía
El trabajo no es nulo, ya que se comprime el gas. Su valor es,
como corresponde a un proceso isotermo,
Sustituyendo los valores numéricos
El calor lo calculamos aplicando el primer principio de la termodinámica
B→C
En el segundo paso se realiza trabajo a presión constante siendo su
expresión
D→A
En el último paso se realiza trabajo a presión constante de nuevo
Das könnte Ihnen auch gefallen
- Tarea Ciclos Stirling, Ericsson y DieselDokument30 SeitenTarea Ciclos Stirling, Ericsson y DieselMario O. M. Ordaz83% (6)
- Ciclo de Ericsson 1Dokument5 SeitenCiclo de Ericsson 1María MartínezNoch keine Bewertungen
- Ciclo EricssonDokument3 SeitenCiclo EricssonPilar AymachoqueNoch keine Bewertungen
- Ciclo Stirling - Ciclo EricssonDokument77 SeitenCiclo Stirling - Ciclo EricssonJose Gomez0% (2)
- Ciclo EricssonDokument7 SeitenCiclo EricssonIsaac DiazNoch keine Bewertungen
- Problemas de EngranesDokument13 SeitenProblemas de Engranesたましろ あきらNoch keine Bewertungen
- Tarea Termodinamica Capitulo 2Dokument6 SeitenTarea Termodinamica Capitulo 2P Javier Riveras50% (2)
- Enunciados Ejercicios Entregados en Clase Examen 1Dokument6 SeitenEnunciados Ejercicios Entregados en Clase Examen 1Jennifer YataNoch keine Bewertungen
- Ejercicio Ciclo Brayton IdealDokument4 SeitenEjercicio Ciclo Brayton IdealChristopher GarzaNoch keine Bewertungen
- TF1121 Problemario1 AJ07aDokument4 SeitenTF1121 Problemario1 AJ07aHenry Ojeda100% (1)
- Laboratorio N°8 TermoGraf V5.7 Termodinámica IDokument16 SeitenLaboratorio N°8 TermoGraf V5.7 Termodinámica ILunaNoch keine Bewertungen
- Ciclo EricssonDokument3 SeitenCiclo EricssonJamirDiazMechanNoch keine Bewertungen
- Cambios en La Entalpía de Gases RealesDokument1 SeiteCambios en La Entalpía de Gases RealesAlexander OrtizNoch keine Bewertungen
- Deber Termodinamica Final-BDokument14 SeitenDeber Termodinamica Final-BFabricio Andrés Segarra ReyesNoch keine Bewertungen
- Ejercicios Entropia PDFDokument12 SeitenEjercicios Entropia PDFAlonso SanchezNoch keine Bewertungen
- Termodinamica Cengel 8 Ed 531 A 534Dokument4 SeitenTermodinamica Cengel 8 Ed 531 A 534phoenix eastwoodNoch keine Bewertungen
- Banco Preguntas 08Dokument8 SeitenBanco Preguntas 08Fernando VíctorNoch keine Bewertungen
- Aplicaciones Del Ciclo EricssonDokument4 SeitenAplicaciones Del Ciclo EricssonE-s VidaNoch keine Bewertungen
- Practica 2º ParcialDokument2 SeitenPractica 2º ParcialFabiola Jose jorgeNoch keine Bewertungen
- Problemas de TermodinámicaDokument29 SeitenProblemas de TermodinámicaRobertsGonzalesSalinas80% (5)
- Se Ejecuta Un Ciclo de Aire Estándar Dentro de Un Sistema Cerrado de CilindroDokument1 SeiteSe Ejecuta Un Ciclo de Aire Estándar Dentro de Un Sistema Cerrado de CilindroAngel M. LizanoNoch keine Bewertungen
- Tarea 1 GM - Davis SisalemaDokument9 SeitenTarea 1 GM - Davis SisalemaDavis SisalemaNoch keine Bewertungen
- Tarea 2 B-2-1Dokument1 SeiteTarea 2 B-2-1Cristhofer Javier TomaláNoch keine Bewertungen
- Discusión 4 Cii-19Dokument5 SeitenDiscusión 4 Cii-19Rodrigo PalaciosNoch keine Bewertungen
- 5 Taller - 1ra Ley SCDokument2 Seiten5 Taller - 1ra Ley SCNelson RamirezNoch keine Bewertungen
- Gu A Ejercicios Resueltos para Examen PDFDokument10 SeitenGu A Ejercicios Resueltos para Examen PDFIvan Torobeo PariguanaNoch keine Bewertungen
- Problemas : La Entropía y El Principio Del Incremento de EntropíaDokument22 SeitenProblemas : La Entropía y El Principio Del Incremento de EntropíaAlejandro Luna Hernández0% (2)
- Templabilidad y Curvas JominyDokument18 SeitenTemplabilidad y Curvas JominymattkidoNoch keine Bewertungen
- Cuestionario MCIDokument2 SeitenCuestionario MCIFred Albert100% (1)
- LT3 P4 RefrigeracionMPDokument6 SeitenLT3 P4 RefrigeracionMPDaysi SanchezNoch keine Bewertungen
- Laboratorio N°5 - TermodinamicaDokument7 SeitenLaboratorio N°5 - TermodinamicaEnrique LauNoch keine Bewertungen
- Beattie-Bridgeman InvestigacionDokument6 SeitenBeattie-Bridgeman InvestigacionJorge Di AntonioNoch keine Bewertungen
- Problema # 1 Ciclo de Carnot..Dokument6 SeitenProblema # 1 Ciclo de Carnot..AbiMirandaNoch keine Bewertungen
- Ejemplo 10Dokument2 SeitenEjemplo 10Jenny GuangasiNoch keine Bewertungen
- Ejercicios - Cap (1,2,3,4,5,6) (Faires)Dokument9 SeitenEjercicios - Cap (1,2,3,4,5,6) (Faires)Bryan ChuquimarcaNoch keine Bewertungen
- Hoja de Ejercicios 1 02-2020Dokument1 SeiteHoja de Ejercicios 1 02-2020Alexander FloresNoch keine Bewertungen
- Ciclo EricssonDokument6 SeitenCiclo EricssonPaul R. BankzNoch keine Bewertungen
- Ejercicio 6-80EDokument1 SeiteEjercicio 6-80ETeodoro CarpioNoch keine Bewertungen
- Ciclo Ericsson Terminado 1Dokument11 SeitenCiclo Ericsson Terminado 1Jar RSNoch keine Bewertungen
- Trabajo TermodinamicaDokument8 SeitenTrabajo TermodinamicawilsonNoch keine Bewertungen
- Capitulo #13 Parte B Relaciones Principales Del Factor de VisionDokument3 SeitenCapitulo #13 Parte B Relaciones Principales Del Factor de VisionMAYCON MARCOS TICONA TARQUINoch keine Bewertungen
- Preguntas Ciclo DieselDokument1 SeitePreguntas Ciclo DieselTonyAndrade0% (1)
- Ejercicios Máquinas ElectricasDokument2 SeitenEjercicios Máquinas ElectricasfranNoch keine Bewertungen
- Investigación Termodinámica II Ciclo Stirling y EricsonDokument7 SeitenInvestigación Termodinámica II Ciclo Stirling y EricsonDanny GuzmánNoch keine Bewertungen
- Boletín 3 15-16Dokument2 SeitenBoletín 3 15-16Li0% (1)
- Cap 10Dokument6 SeitenCap 10Jonnathanthan JmAlNoch keine Bewertungen
- Guia de Tutoria 2 Temas 2.1 A 2.4Dokument6 SeitenGuia de Tutoria 2 Temas 2.1 A 2.4Jose Daniel RuizNoch keine Bewertungen
- UNIDAD 2 - Segunda ParteDokument35 SeitenUNIDAD 2 - Segunda ParteUlises MaldonadoNoch keine Bewertungen
- Clase 6.3Dokument19 SeitenClase 6.3Jean LuqueNoch keine Bewertungen
- Diseño de Elementos - Problema 2Dokument2 SeitenDiseño de Elementos - Problema 2Mario J. Díaz ZegarraNoch keine Bewertungen
- Deber1 Termo2Dokument2 SeitenDeber1 Termo2victor_mero_179570% (1)
- Ejemplo Resuelto de Un Proceso Isobarico PDFDokument1 SeiteEjemplo Resuelto de Un Proceso Isobarico PDFRub E GuaNoch keine Bewertungen
- GTP6Dokument4 SeitenGTP6Santi BerntzNoch keine Bewertungen
- Diagrama Presion VolumenDokument12 SeitenDiagrama Presion VolumenMiguel LincangoNoch keine Bewertungen
- 4 Tarea de Primera Ley de La TermodinámicaDokument5 Seiten4 Tarea de Primera Ley de La TermodinámicaAtomAppleNoch keine Bewertungen
- Ciclo Teórico de Motor Otto PDFDokument7 SeitenCiclo Teórico de Motor Otto PDFErick GarzónNoch keine Bewertungen
- Investigación Del Ciclo de Otto, Ciclo de Carnot, Tubo Venturi y Aplicación de La Ecuación de Bernoulli.Dokument14 SeitenInvestigación Del Ciclo de Otto, Ciclo de Carnot, Tubo Venturi y Aplicación de La Ecuación de Bernoulli.Jonathan StevenNoch keine Bewertungen
- Ciclo Otto y Ciclo DieselDokument12 SeitenCiclo Otto y Ciclo DieselJunior Hinojosa SuaresNoch keine Bewertungen
- Manual de Refrigeracion BasicaDokument86 SeitenManual de Refrigeracion Basicapesoli39100% (5)
- Ciclo Otto y DieselDokument5 SeitenCiclo Otto y DieselBrigitteNoch keine Bewertungen
- Elites GlobalesDokument350 SeitenElites GlobalesAquiles PintoNoch keine Bewertungen
- Plan de Evaluacion Proyecto Ii Comunicacion SocialDokument3 SeitenPlan de Evaluacion Proyecto Ii Comunicacion SocialManama DarwisNoch keine Bewertungen
- Tablas 1Dokument78 SeitenTablas 1BrunoSouza1991Noch keine Bewertungen
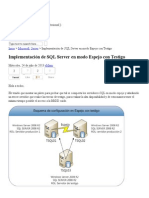
- Implementación de SQL Server en Modo Espejo Con Testigo PDFDokument20 SeitenImplementación de SQL Server en Modo Espejo Con Testigo PDFplumbeus01Noch keine Bewertungen
- Civilizaciones FluvialesDokument17 SeitenCivilizaciones FluvialesNATASHA ALCIVARNoch keine Bewertungen
- Tesis Nacional Actividad FisicaaDokument224 SeitenTesis Nacional Actividad FisicaaMg Mario Ramos Torres67% (3)
- Venta y CierreDokument3 SeitenVenta y CierrePatrick Cardenas GutierrezNoch keine Bewertungen
- Curso de Iniciacion de MatematicaDokument6 SeitenCurso de Iniciacion de MatematicaAnabel OrtizNoch keine Bewertungen
- Practica 5 Herencia IIDokument11 SeitenPractica 5 Herencia IIjulissa guevaraNoch keine Bewertungen
- Tarea No 2 Contabilidad GubernamentalDokument6 SeitenTarea No 2 Contabilidad GubernamentalBrigada SantiagoNoch keine Bewertungen
- Contaminación - SeparataDokument4 SeitenContaminación - SeparataAzter MagolloNoch keine Bewertungen
- 17 Fragmentacion de TuberiaDokument13 Seiten17 Fragmentacion de Tuberiafred1827Noch keine Bewertungen
- El Factor de Dios en ColombiaDokument2 SeitenEl Factor de Dios en ColombiaGabriela GamboaNoch keine Bewertungen
- Examen Dibujar FuerzasDokument6 SeitenExamen Dibujar Fuerzasjose ObandoNoch keine Bewertungen
- Arado Cincel y Arado SubsoladorDokument10 SeitenArado Cincel y Arado SubsoladorKathe AguilarNoch keine Bewertungen
- Manual PSIMDokument21 SeitenManual PSIMEsbany Lanchipa SanchezNoch keine Bewertungen
- Tall Metro Port Til 213 SecaDokument2 SeitenTall Metro Port Til 213 SecaTeam HeritageNoch keine Bewertungen
- Presentacion de GNLDokument26 SeitenPresentacion de GNLCarrillo RomerNoch keine Bewertungen
- Ejercicios de Costos de AlmacenajeDokument1 SeiteEjercicios de Costos de AlmacenajeGianmarco Waldy Ccahuana SarmientoNoch keine Bewertungen
- Primer Parcial - Tema 2Dokument3 SeitenPrimer Parcial - Tema 2Maldonado NadinNoch keine Bewertungen
- FilosofiaDokument2 SeitenFilosofiaPaula Vila NoyaNoch keine Bewertungen
- RD 487 Manipulación Manual de CargasDokument3 SeitenRD 487 Manipulación Manual de CargasAntonio JiménezNoch keine Bewertungen
- Elaboracion Del Vino de ManzanaDokument23 SeitenElaboracion Del Vino de ManzanaYess Flores Delgado50% (2)
- HDSM - 0929 - Divosan Forte - 08.03.2018Dokument11 SeitenHDSM - 0929 - Divosan Forte - 08.03.2018Camila BuenoNoch keine Bewertungen
- Sesion 2 Desapego EmocionalDokument18 SeitenSesion 2 Desapego EmocionalRonald Roy Rivera RamosNoch keine Bewertungen
- Herramientas ManualesDokument17 SeitenHerramientas ManualesSantos martinezNoch keine Bewertungen
- Guia Sistema MuscularDokument11 SeitenGuia Sistema Muscularyamid acostaNoch keine Bewertungen
- Maqueta GEALDokument52 SeitenMaqueta GEALcbfodrtfNoch keine Bewertungen
- PROYECTO 2 SEM 3 2do - BGUDokument22 SeitenPROYECTO 2 SEM 3 2do - BGUroariolka PonceNoch keine Bewertungen
- Máxima Tensión de Contacto Admisible Por El Cuerpo Humano Según Normas IEC e IEEEDokument7 SeitenMáxima Tensión de Contacto Admisible Por El Cuerpo Humano Según Normas IEC e IEEELuisa Fernanda RamirezNoch keine Bewertungen