Beruflich Dokumente
Kultur Dokumente
Thermodynamik 2 Diplomklausur SS 04
Hochgeladen von
sdgoadamCopyright
Verfügbare Formate
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
Verfügbare Formate
Thermodynamik 2 Diplomklausur SS 04
Hochgeladen von
sdgoadamCopyright:
Verfügbare Formate
Klausur zur Vorlesung Thermodynamik 2 Prof. Dr. B.
Atakan, Abteilung Maschinenbau;Universitt Duisburg-Essen
03.09.2004
Thermodynamik Klausur SS 2004
Bitte lesen Sie erst alle Aufgaben durch, bevor Sie beginnen. Nur Lsungsbltter auf denen Ihr Name steht, knnen anerkannt werden. Wenn Sie mehrere Anstze zur Lsung machen, kennzeichnen Sie bitte deutlich, welche Ihre endgltige Lsung ist. Bitte unterstreichen Sie die jeweiligen Endergebnisse jeder Teilaufgabe. Geben Sie bitte bei Ihren Berechnungen in wenigen Stichworten jeweils an, um welche Art von Prozess (z.B.: isochor, adiabat etc.) oder Zustnde bzw. Stoffmodelle (siedende Flssigkeit, ideales Gas etc.) es sich handelt Streichen Sie bitte jede bearbeitete Teilaufgabe in der folgenden (Punkte-) Tabelle durch. Die Dauer betrgt 90 Minuten Erlaubte Hilfsmittel sind: i. Taschenrechner (nicht-programmierbar) ii. Dampftafeln iii. Formelsammlung iv. Blatt (DIN A4) beliebig beidseitig handschriftlich beschrieben
Die vorlufige Punkteverteilung betrgt: Aufgabe 1
5 5 5 15 10 8 15 0 0 3 3 0 0 8 4 0 0 0 4 0 0 29 36 20 15
Summe
2
5
3
5
4
5
Zusammen
100
1/5
Klausur zur Vorlesung Thermodynamik 2 Prof. Dr. B. Atakan, Abteilung Maschinenbau;Universitt Duisburg-Essen
03.09.2004
1)
Einige kleinere Fragen und Zusammenhnge: a. Wie ndert sich das chemische Potential einer Komponente in einer Mischung idealer Gase, wenn 1) nur der Gesamtdruck steigt, wenn 2) nur die Temperatur steigt bzw. wenn 3) nur der Partialdruck der Komponente steigt? (Alle anderen Variablen, T, p oder ni seien whrend der jeweiligen nderung unverndert.) b. Wie wird sich die maximal gewinnbare Arbeit einer bei der Temperatur T1 exergonischen und exothermen Reaktion ndern, wenn Sie bei hherer Temperatur T2 (T2>T1) ausgefhrt wird? c. In einem Auto ist das Geblse an und innen herrscht eine Lufttemperatur von 22C, die Auentemperatur betrgt -5C. Die Fensterscheibe (50 cm x 130 cm) aus Glas habe eine Dicke von 10 mm (=1.4 W/(m K)), auen sei der Wrmebergangskoeffizient 14 W/(m2 K), innen betrgt er 5 W/(m2 K). Geben Sie die Auentemperatur der Scheibe an, wird die Scheibe vereisen? d. Geben Sie an, wieviel Arbeit man mindestens aufwenden muss, um 1 kmol Luft (O2:N2=1:3.76) isotherm, isobar in Sauerstoff und Stickstoff zu zerlegen (Randbedingung und Daten: T=298 K, p=1 bar, M(O2)=32 g/mol, M(N2)=28 g/mol, R=8.314 J/(K mol)). e. Ursprnglich reines festes Phosphorpentachlorid (PCl5) wird aufgeheizt und steht bei einem Druck von 2 bar und einer Temperatur von 250C im Gleichgewicht mit Phosphortrichlorid (PCl3) und Chlor (Cl2). Unter diesen Bedingungen sind alle drei Komponenten gasfrmig. Im Gleichgewicht wurde ein Chlor-Molenbruch von x(Cl2)=0.4 gemessen. Geben Sie die weiteren Molenbrche, die Gleichgewichtskonstante Kp und die freie Standard-Reaktionsenthalpie an.
2)
An einem heien Sommertag herrscht ein Luftdruck von 1 bar, bei 35C und einer relativen Feuchte von 90% [0]. Eine Klimaanlage soll 30 m3/min (Gesamtvolumenstrom) Auenluft ansaugen und Luft bei 20C und 55% relativer Feuchte bereitstellen [4], indem die Luft entsprechend abgekhlt wird [2], Kondensat entfernt und daraufhin wieder aufgeheizt wird [3]. All dies erfolgt isobar. Zum Ansaugen der Luft befindet sich ein Ventilator mit einer Leistungsaufnahme von 1.1 kW im Ansaugstutzen der Klimaanlage [1]. Sie knnen das beiliegende Mollier-Diagramm zur Lsung benutzen und drfen
2/5
Klausur zur Vorlesung Thermodynamik 2 Prof. Dr. B. Atakan, Abteilung Maschinenbau;Universitt Duisburg-Essen
03.09.2004
kinetische Energien vernachlssigen. {RLuft=0.287 kJ/(kg K)} (Hinweis: Sie mssen bei einem Punkt ber das Diagramm hinaus extrapolieren) a. Tragen Sie alle Zustnde, mit Ausnahme von Zustand [2], in das Mollier Diagramm ein. b. Auf welche Temperatur muss abgekhlt werden? c. Wie hoch ist der Massenstrom an Kondensat?
d. Geben Sie die zu- und abgefhrten Wrmeleistungen an. e. Wie hoch wre die minimal zuzufhrende elektrische Leistung der Klimaanlage? Machen Sie einen Vorschlag, wie durch eine vernderte Anordnung der Komponenten der Stromverbrauch reduziert werden kann. f. Die Luft strmt vollstndig in einen Raum, in dem das Fenster offen steht und 15 m3/min Auenluft einstrmt. In welchem Zustand (T, Wasserbeladung) strmt die Luft aus, wenn wir den Raum sonst als adiabat ansehen drfen. 3) Ein Generator, der mit Propan betrieben wird, soll bei Stromausfllen, die bis zu 3 Tage dauern knnen, die Versorgung mit Strom gewhrleisten. Das Propan (C3H8, Daten s. Tabelle) wird mit Luft (O2:N2=1:3.76) bei =2 verbrannt. Der thermische Wirkungsgrad des Generators betrgt 27%, die elektrische Leistung betrgt 10 kW. Brennstoff und Luft strmen bei 25C ein, das Abgas wird bei 50K ber dem Taupunkt ausgestoen. Der Druck bei dem die Edukte eintreten und das Abgas austritt betrgt 1.05 bar. a. Welche Temperatur hat das Abgas? b. Wieviel Propan muss vorrtig sein, um den Generator drei Tage betreiben zu knnen?
4)
In einem Betrieb fllt ein Massenstrom von 5 kg/s trockengesttigter Wasserdampf bei 100C an [1]. An einer anderen Stelle wird eine geringere Menge Wasserdampf bei 2 bar und 200C bentigt [2], hierzu wird ein Kompressor eingesetzt, der durch eine Turbine angetrieben wird. Der Massenstrom im Zustand [1] wird geteilt, so dass ein Teil durch die Turbine und der andere durch den Kompressor geleitet wird, die gesamte Leistung der Turbine wird zum Betrieb des Kompressors eingesetzt, so dass keine externe Leistung bentigt wird. Der Nassdampf, der die Turbine bei 0.075 bar verlsst hat einen
3/5
Klausur zur Vorlesung Thermodynamik 2 Prof. Dr. B. Atakan, Abteilung Maschinenbau;Universitt Duisburg-Essen
03.09.2004
Dampfgehalt von x=0.95 vor[3]. Turbine und Kompressor knnen als adiabat angesehen werden. a. Welcher Massenstrom im Zustand [2] steht zur Verfgung? b. Wie hoch ist der Exergieverlust in Turbine und Kompressor? (Umgebungsbedingung: 290K, 1.013 bar)
4/5
Klausur zur Vorlesung Thermodynamik 2 Prof. Dr. B. Atakan, Abteilung Maschinenbau;Universitt Duisburg-Essen
03.09.2004
Wrmekapazitt cp0, molare Bildungsenthalpie hf,0 und absolute molare Entropie s0 ausgewhlter Verbindungen bei 25 C und 100 kPa Substanz Argon Graphit Schwefel Wasserstoff Sauerstoff Stickstoff Wasser Wasser Kohlenmonoxid Kohlendioxid Schwefeldioxid Ammoniak Methan Acetylen Ethen Ethan Propan Butan Oktan Oktan Ethanol Methanol Formel Ar C S H2 O2 N2 H2O H2O CO CO2 SO2 NH3 CH4 C2H2 C2H4 C2H6 C3H8 C4H10 C8H18 C8H18 C2H6O CH3OH Zustand g s s g g g g l g g g g g g g g g g g l l l
0 M c p0 s0m fh m g/mol J/mol K kJ/mol J/mol K 39.948 20.786 0.00 154.843 12.011 8.527 0.00 5.795 32.064 22.640 0.00 31.8 2.016 28.824 0.00 130.684 31.999 29.355 0.00 205.142 28.013 29.125 0.00 191.611 18.015 33.577 -241.83 188.833 18.015 75.290 -285.84 69.94 28.011 29.142 -110.53 197.653 44.011 37.110 -393.52 213.795 64.063 39.870 -296.83 248.22 17.031 35.060 -46.11 192.45 16.043 35.309 -74.87 186.256 26.038 43.930 226.73 200.958 28.054 43.560 52.28 219.548 30.07 52.630 -84.67 229.602 44.097 73.513 -103.85 270.019 58.124 96.748 -126.15 310.227 114.23 188.866 -208.45 466.835 114.23 249.707 -249.95 360.896 46.069 111.460 -276.72 160.7 32.042 81.579 -239.45 126.61
5/5
Das könnte Ihnen auch gefallen
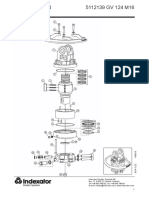
- Ersatzteilliste GV124 M16Dokument3 SeitenErsatzteilliste GV124 M16Luka JelovčanNoch keine Bewertungen
- Elektronika PincontrolDokument15 SeitenElektronika Pincontrolakomocar0% (1)
- Container REDA WebDokument19 SeitenContainer REDA WebIonela GaciaNoch keine Bewertungen
- Ensoniq FDDDokument2 SeitenEnsoniq FDDbobi123Noch keine Bewertungen
- Pcnews 14Dokument64 SeitenPcnews 14Franz FialaNoch keine Bewertungen
- Logilink Wlan Repeater Wl0148 ManualDokument16 SeitenLogilink Wlan Repeater Wl0148 ManualTobNoch keine Bewertungen
- Zenza Bronica SCA386 - HowtoDokument4 SeitenZenza Bronica SCA386 - Howtoreisch70Noch keine Bewertungen