Beruflich Dokumente
Kultur Dokumente
Abiturprüfung 2023: Chemie, Leistungskurs
Hochgeladen von
Super NerdOriginaltitel
Copyright
Verfügbare Formate
Dieses Dokument teilen
Dokument teilen oder einbetten
Stufen Sie dieses Dokument als nützlich ein?
Sind diese Inhalte unangemessen?
Dieses Dokument meldenCopyright:
Verfügbare Formate
Abiturprüfung 2023: Chemie, Leistungskurs
Hochgeladen von
Super NerdCopyright:
Verfügbare Formate
CH LK HT 1 (GG)
Seite 1 von 4
Name: _______________________
Abiturprüfung 2023
Chemie, Leistungskurs
Aufgabenstellung:
Anlaufen und Reinigen von Silber
1. Erläutern Sie die im Experiment a) gemachten Beobachtungen ohne Anlegen einer
Spannung mithilfe zugehöriger Reaktionsgleichungen. Berechnen Sie die Masse an
Silber, die sich in Experiment b) abscheidet. Erläutern Sie den Vorteil der Verwendung
von Silber (Experiment b)) als Anodenmaterial gegenüber Graphit (Experiment c)) unter
Einbeziehung der Reaktionsgleichungen für beide Elektrodenvorgänge.
(18 Punkte)
2. Berechnen Sie die Spannung, die mindestens aufgebracht werden muss, um einen Gegen-
stand nach Experiment c) zu versilbern. Erläutern Sie mithilfe der NERNST-Gleichung,
welchen Einfluss die Hydroxid-Ionen-Konzentration auf die aufzubringende Spannung
hat. Beurteilen Sie, ob es sinnvoller ist, Gegenstände galvanisch zu versilbern als sie
lediglich in eine Silbersalz-Lösung zu legen. (16 Punkte)
3. Erklären Sie die Beobachtungen bei der Behandlung von angelaufenem Silber im Labor.
Beurteilen Sie die Aussagen der Zitate zum Anlaufen von Silber unter der Annahme,
dass die aufgelisteten Reaktionen für diesen Vorgang verantwortlich sind.
(14 Punkte)
4. Erläutern Sie auch unter Angabe von Reaktionsgleichungen die elektrochemischen
Vorgänge beim Reinigen von Silber nach der Aluminium-Salz-Methode. Beurteilen
Sie die beiden Verfahren zur Silberreinigung, indem Sie Vor- und Nachteile beider
Verfahren gegenüberstellen. (18 Punkte)
Zugelassene Hilfsmittel:
• Taschenrechner (grafikfähiger Taschenrechner / CAS-Taschenrechner)
• Periodensystem
• Wörterbuch zur deutschen Rechtschreibung
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
CH LK HT 1 (GG)
Seite 2 von 4
Name: _______________________
Fachspezifische Vorgaben:
Silber besitzt viele Eigenschaften, die es für Gebrauchsgegenstände nützlich machen. Es hat
unter allen Metallen den höchsten Glanz und wirkt bakterientötend. Somit sind Silbergegen-
stände nicht nur optisch schön, sondern auch hygienisch. Daher findet Silber auch Verwen-
dung bei der Herstellung von Besteck.
Silberbesteck besteht meistens nicht aus reinem Silber, da Silber nicht hart genug ist und
das Besteck sich leicht verformen würde. Bei Silberbesteck aus „Hartsilber“ wird ein aus
einem Stahlkern bestehendes Besteck galvanisch mit einer dünnen Silberschicht überzogen.
Experimente zum Versilbern einer Gabel
Eine elektrochemische Silberabscheidung ist häufig schwierig, da sich Silber oftmals nicht
als gleichmäßige Schicht, sondern in Form von unregelmäßigen Verästelungen abscheidet.
a) In einem Laborexperiment konnte das Versilbern einer Gabel aus Eisen nachvollzogen
werden. Hierzu legte man eine Eisengabel in eine Silbernitrat-Lösung. Innerhalb weniger
Minuten bildeten sich kleine schwarze Verästelungen an der Eisengabel.
b) In einem weiteren Experiment verwendete man ein Becherglas, welches mit einer alkali-
schen Silbernitrat-Lösung der Konzentration c = 1 mol·L–1 und pH = 14 gefüllt wurde.
Die Gabel und ein Silberblech wurden in die Lösung gebracht und mit den Polen einer
Gleichspannungsquelle verbunden. Im Anschluss wurde mit einer Stromstärke von
5 Ampere für 10 Minuten galvanisiert.
c) In Experiment b) wurde das Silberblech durch eine Graphitelektrode ausgetauscht. Die
Gabel überzog sich mit einer Silberschicht. Im Gegensatz zur Verwendung einer Anode
aus Silber beobachtete man hier eine Gasentwicklung an der Graphitelektrode.
Anlaufen von Silber
Obwohl es sich bei Silber um ein Edelmetall handelt, läuft es mit der Zeit an. In einem
Buch zu Korrosion und Korrosionsschutz kann man folgende Zitate finden:
„In trockenen und feuchten Atmosphären ist Silber immun gegen korrosiven Angriff. Eine
Oxidation zu Ag2O unterhalb 180 °C ist zwar nachzuweisen, eine sichtbare Oxidschicht
tritt nicht auf.“
„Die Ursache für dieses Anlaufen sind dünne Schichten aus dem schwarzen Ag2S, die sich
an der Oberfläche bilden, selbst wenn nur Spuren von H2S in der Atmosphäre zugegen
sind. Über den Reaktionsmechanismus ist man sich nicht im Klaren, und auch die stöchio-
metrischen Verhältnisse sind nicht geklärt. Im Einzelnen ist die Frage offen, ob der Anlauf-
vorgang […] unter der Beteiligung von Luftsauerstoff abläuft.“
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
CH LK HT 1 (GG)
Seite 3 von 4
Name: _______________________
Die hier zu vermutenden Teilreaktionen mit den entsprechenden Standardpotentialen E°
lauten:
2 Ag + H2S ⇄ Ag2S + 2 H+ + 2 e– –0,036 V
4 OH– ⇄ O2 + 2 H2O + 4e– 0,4 V
Ag ⇄ Ag+ + e– 0,8 V
Behandlung von angelaufenem Silber im Labor
Auch Silberbleche im Labor laufen mit der Zeit an. Hält man ein angelaufenes Reinsilber-
blech in die nichtleuchtende Brennerflamme, so wird dieses wieder blank.
Reinigen von angelaufenem Silberbesteck im Haushalt
In Haushaltsratgebern werden unterschiedliche Maßnahmen zum Reinigen des angelaufe-
nen Silberbestecks vorgeschlagen:
• Zahnpasta-Methode:
Mit einer weichen Bürste wird das Besteck vorsichtig mit Zahnpasta eingerieben. Die
Silbersulfid-Schicht wird hierbei mechanisch abgetragen. Anschließend wird die Paste
mit Wasser abgewaschen.
• Aluminium-Salz-Methode:
In einer Schüssel werden mehrere Teelöffel Kochsalz mit warmem Wasser vermischt,
bis sich das Salz gelöst hat. Dann gibt man ein wenig Essig hinzu. Das Silberbesteck
wird locker in Aluminiumfolie eingewickelt, sodass es Kontakt mit der Folie hat und für
10 Minuten in dieser Lösung belassen. Bei diesem Verfahren werden die Silber-Ionen
wieder in Silber-Atome umgewandelt. Die freiwerdenden Sulfid-Ionen reagieren in der
essigsauren Lösung zunächst zu Hydrogensulfid-Ionen (HS–) und weiter zu Schwefel-
wasserstoff-Molekülen (H2S).
Nach dem Auspacken des Silberbestecks aus der Aluminiumfolie ist das Besteck wieder
blank. Die Aluminiumfolie weist eine raue Oberfläche und kleine Löcher auf. Der Geruch
von Schwefelwasserstoff ist wahrzunehmen.
Schwefelwasserstoff ist ein sehr giftiges Gas. Der Mensch kann es bereits in äußerst ge-
ringen Konzentrationen riechen, die bei kurzzeitiger Wahrnehmung unproblematisch sind.
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
CH LK HT 1 (GG)
Seite 4 von 4
Name: _______________________
Zusatzinformationen:
Faraday-Konstante
F = 96485 A ⋅ s·mol–1
Faraday-Gesetz
I·t=n·z·F
M(Ag) = 107,9 g·mol–1
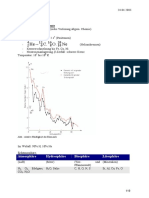
Sonderform der NERNST-Gleichung für Sauerstoff-Halbzellen:
0,059 V 1
𝐸𝐸(OH − /O2 , H2 O) = 𝐸𝐸 0 (OH − /O2 , H2 O) + ∙ lg 4
4 𝑐𝑐 (OH − )
Standardpotentiale
bei T = 298,15 K, p = 101,325 kPa und c = 1 mol·L–1
reduzierte Form ⇄ oxidierte Form + z · e– Standardpotential E° in V
Al ⇄ Al3+ + 3 e– –1,66
Fe ⇄ Fe2+ + 2 e– –0,41
4 OH- ⇄ O2 + 2 H2O + 4 e– +0,40 (pH = 14)
Ag ⇄ Ag+ + e– +0,80
Anmerkung zum Zitat:
Quelle:
Kunze, Egon (Hrsg.): Korrosion und Korrosionsschutz. Band 1: Einführung und wissen-
schaftliche Grundlagen. Weinheim: Wiley-VCH Verlag 2001, S. 1589 – 1590
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 1 (GG)
Seite 1 von 9
Unterlagen für die Lehrkraft
Abiturprüfung 2023
Chemie, Leistungskurs
1. Aufgabenart
Bearbeitung einer Aufgabe, die auf fachspezifischen Vorgaben basiert
2. Aufgabenstellung1
Anlaufen und Reinigen von Silber
1. Erläutern Sie die im Experiment a) gemachten Beobachtungen ohne Anlegen einer
Spannung mithilfe zugehöriger Reaktionsgleichungen. Berechnen Sie die Masse an
Silber, die sich in Experiment b) abscheidet. Erläutern Sie den Vorteil der Verwendung
von Silber (Experiment b)) als Anodenmaterial gegenüber Graphit (Experiment c)) unter
Einbeziehung der Reaktionsgleichungen für beide Elektrodenvorgänge.
(18 Punkte)
2. Berechnen Sie die Spannung, die mindestens aufgebracht werden muss, um einen Gegen-
stand nach Experiment c) zu versilbern. Erläutern Sie mithilfe der NERNST-Gleichung,
welchen Einfluss die Hydroxid-Ionen-Konzentration auf die aufzubringende Spannung
hat. Beurteilen Sie, ob es sinnvoller ist, Gegenstände galvanisch zu versilbern, als sie
lediglich in eine Silbersalz-Lösung zu legen. (16 Punkte)
3. Erklären Sie die Beobachtungen bei der Behandlung von angelaufenem Silber im Labor.
Beurteilen Sie die Aussagen der Zitate zum Anlaufen von Silber unter der Annahme,
dass die aufgelisteten Reaktionen für diesen Vorgang verantwortlich sind.
(14 Punkte)
4. Erläutern Sie auch unter Angabe von Reaktionsgleichungen die elektrochemischen
Vorgänge beim Reinigen von Silber nach der Aluminium-Salz-Methode. Beurteilen
Sie die beiden Verfahren zur Silberreinigung, indem Sie Vor- und Nachteile beider
Verfahren gegenüberstellen. (18 Punkte)
1 Die Aufgabenstellung deckt inhaltlich alle drei Anforderungsbereiche ab.
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 1 (GG)
Seite 2 von 9
3. Materialgrundlage
• https://silber.info/ (Zugriff 31.01.2023)
• https://www.chemie.de/lexikon/Silber.html (Zugriff 31.01.2023)
• https://www.chemieunterricht.de/dc2/tip/07_05.htm (Zugriff 31.01.2023)
• https://www.schmuck.de/wie-reinige-ich-silber-die-zahnpasta-methode/
(Zugriff 31.01.2023)
• https://www.schmuck.de/wie-reinige-ich-silber-die-aluminium-salz-methode/
(Zugriff 31.01.2023)
• https://www.tifoo.de/silberelektrolyt (Zugriff 31.01.2023)
• Kunze, Egon (Hrsg.): Korrosion und Korrosionsschutz. Band 1: Einführung und wissen-
schaftliche Grundlagen. Weinheim: Wiley-VCH Verlag 2001, S. 1589 – 1590
4. Bezüge zum Kernlehrplan und zu den Vorgaben 2023
Die Aufgaben weisen vielfältige Bezüge zu den Kompetenzerwartungen und Inhaltsfeldern
des Kernlehrplans bzw. zu den in den Vorgaben ausgewiesenen Fokussierungen auf.
Im Folgenden wird auf Bezüge von zentraler Bedeutung hingewiesen.
1. Inhaltsfelder und inhaltliche Schwerpunkte
Elektrochemie
• Elektrochemische Gewinnung von Stoffen
• Mobile Energiequellen
• Quantitative Aspekte elektrochemischer Prozesse
• Korrosion und Korrosionsschutz
2. Medien/Materialien
• entfällt
5. Zugelassene Hilfsmittel
• Taschenrechner (grafikfähiger Taschenrechner / CAS-Taschenrechner)
• Periodensystem
• Wörterbuch zur deutschen Rechtschreibung
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 1 (GG)
Seite 3 von 9
6. Vorgaben für die Bewertung der Schülerleistungen
Teilleistungen – Kriterien
a) inhaltliche Leistung
Teilaufgabe 1
Anforderungen maximal
erreichbare
Punktzahl
Der Prüfling
1 erläutert die im Experiment a) gemachten Beobachtungen ohne Anlegen einer Span- 8
nung mithilfe zugehöriger Reaktionsgleichungen, z. B.:
• Silber liegt als einwertiges Ion beziehungsweise in seiner oxidierten Form vor.
Da Eisen unedler ist als Silber, findet eine Elektronenübertragung statt:
Fe + 2 Ag+→ Fe2+ + 2 Ag.
• Es bildet sich elementares Silber, welches man als Verästelungen sieht:
Ag+ + e– → Ag.
• Eisen geht in Lösung: Fe → Fe2+ + 2e–.
2 berechnet die Masse an Silber, die sich im Experiment b) abscheidet: 4
• I·t=n·z·F
5 A · 600 s = (Ag) · 1 · 96485 A · s·mol–1
n(Ag) = 0,031 mol,
• m(Ag) = n(Ag) · M(Ag)= 3,35 g
Es werden 3,35 g Silber abgeschieden.
3a erläutert den Vorteil der Verwendung von Silber (Experiment a)) als Anodenmaterial 4
an Stelle von Graphit (Experiment b)) unter Einbeziehung der Reaktionsgleichun-
gen für beide Elektrodenvorgänge, z. B.:
• Silberanode:
Anode: Ag → Ag+ + e–
Kathode: Ag+ + e– → Ag,
• Graphitanode:
Anode: 4 OH–→ O2 + 4 e– + 2 H2O
Kathode: Ag+ + e– → Ag.
3b erläutert den Vorteil der Verwendung von Silber (Experiment b)) als Anodenmaterial 2
an Stelle von Graphit (Experiment c)) unter Einbeziehung der Reaktionsgleichungen
für beide Elektrodenvorgänge, z. B.:
• Die Silber-Ionen-Konzentration bleibt in der Lösung konstant, während sie bei
der Verwendung einer Graphitanode kontinuierlich abnehmen würde.
Hinweis: Alternativ kann auch darauf eingegangen werden, dass die Konzentration
an Hydroxid-Ionen abnimmt, was sich auf die Leitfähigkeit der Lösung auswirkt.
4 erfüllt ein weiteres aufgabenbezogenes Kriterium. (2)
Teilaufgabe 2
Anforderungen maximal
erreichbare
Punktzahl
Der Prüfling
1 berechnet die Spannung, die mindestens aufgebracht werden muss, um einen Gegen- 4
stand nach Experiment c) zu versilbern, z. B.:
• Die Silber-Ionen liegen mit einer Konzentration von 1 mol·L–1 vor. Ebenso liegen
die Hydroxid-Ionen mit einer Konzentration von 1 mol·L–1 vor, da ein pH-Wert
von 14 herrscht. Somit können die Standardpotentiale direkt verrechnet werden.
• U = E(A) – E(D) = 0,8 V – 0,4 V = 0,4 V
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 1 (GG)
Seite 4 von 9
2 erläutert mithilfe der NERNST-Gleichung, welchen Einfluss die Hydroxid-Ionen- 6
Konzentration auf die aufzubringende Spannung hat, z. B.:
• Bei Hydroxid-Ionen-Konzentrationen größer 1 wird der Logarithmus der
NERNST-Gleichung negativ.
• Je höher die Konzentration der Hydroxid-Ionen, desto geringer das Halbzellen-
potential.
• Hierdurch wird der Abstand des Potentials von dem der Silberhalbzelle größer,
und die zur Elektrolyse notwendige Spannung erhöht sich.
Hinweis: Auch die Argumentation niedrigerer Hydroxid-Ionen-Konzentrationen ist
als richtig zu werten.
3 beurteilt, ob es sinnvoller ist, Gegenstände galvanisch zu versilbern, als sie lediglich 6
in eine Silbersalz-Lösung zu legen, z. B.:
• Silber scheidet sich beim Galvanisieren ab, ohne dass das darunterliegende un-
edlere Metall in Lösung geht. Die aufgebrachte Silberschicht hält besser, und es
wird ein gleichmäßiges Abscheiden erreicht.
• Man kann die Menge an abgeschiedenem Metall berechnen und beeinflussen.
• Ein galvanisches Versilbern ist dem bloßen Einlegen in eine Silberlösung vorzu-
ziehen.
Hinweis: Auch andere sinnvolle Lösungen sind als richtig zu werten.
4 erfüllt ein weiteres aufgabenbezogenes Kriterium. (2)
Teilaufgabe 3
Anforderungen maximal
erreichbare
Punktzahl
Der Prüfling
1 erklärt die Beobachtungen bei der Behandlung von angelaufenem Silber im Labor, 2
z. B.:
• Beim Erhitzen von Silbersulfid in der Brennerflamme entsteht wieder elementares
Silber.
2a beurteilt die Aussagen der Zitate zum Anlaufen von Silber unter der Annahme, dass 4
die aufgelisteten Reaktionen für diesen Vorgang verantwortlich sind, z. B.:
• Silber wird nicht durch Sauerstoff oxidiert. Dies zeigen die entsprechenden Po-
tentiale. Die Reaktion von Silber mit Sauerstoff dürfte nicht stattfinden, da das
Potential von Silber zu hoch ist.
• Dass das Auftreten zur Bildung von Ag2O unter 180 °C nachweisbar ist, kann
mithilfe der Potentiale nicht erklärt werden.
2b beurteilt die Aussagen der Zitate zum Anlaufen von Silber unter der Annahme, dass 8
die aufgelisteten Reaktionen für diesen Vorgang verantwortlich sind, z. B.:
• Die Teilgleichungen
2 Ag + H2S ⇄ Ag2S + 2 H+ + 2 e– und
–
4 OH ⇄ O2 + 2 H2O + 4e–
können durch ihre Potentiale gleichzeitig ablaufen.
• Silber kann hier zu Silber-Ionen oxidiert werden, da die Reaktion mit Schwefel-
wasserstoff ein verhältnismäßig niedrigeres Standardpotential besitzt.
• Sauerstoff dient hier als Elektronen-Akzeptor.
• Unter diesen Voraussetzungen müssten sowohl Schwefelwasserstoff als auch
Sauerstoff vorhanden sein, damit das Silber anläuft.
3 erfüllt ein weiteres aufgabenbezogenes Kriterium. (2)
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 1 (GG)
Seite 5 von 9
Teilaufgabe 4
Anforderungen maximal
erreichbare
Punktzahl
Der Prüfling
1 erläutert auch unter Angabe von Reaktionsgleichungen die elektrochemischen Vor- 8
gänge beim Reinigen von Silber nach der Aluminium-Salz-Methode, z. B.:
• Beim Kontakt zwischen der Alufolie und dem Besteck entsteht ein kurzge-
schlossenes galvanisches Element, ein Lokalelement.
• Aluminium ist unedler als Silber und wird oxidiert. Die Silber-Ionen werden zu
Silber-Atomen reduziert, die sich als elementares Silber abscheiden.
• Das Kochsalz dient als Elektrolyt, erhöht die Leitfähigkeit der Lösung und
beschleunigt die Elektronenübergänge.
• Reaktionsgleichungen:
Reduktion: Ag2S + 2 e–→ 2 Ag + S2-,
Oxidation: Al → Al3+ + 3 e–,
Gesamtreaktion: 3 Ag2S + 2 Al → 6 Ag + 2 Al3+ + 3 S2–.
Hinweis: Eine erweiterte Reaktionsgleichung, die die Bildung von H2S vorsieht, ist
ebenfalls als richtig zu bewerten.
2a beurteilt die beiden Verfahren zur Silberreinigung, indem er Vor- und Nachteile 8
beider Verfahren gegenüberstellt, z. B.:
• Vorteile der Aluminium-Salz-Methode:
– einfache Durchführung, preiswert verfügbare Materialien,
– Erhaltung des Silbers durch Reduktion der Silber-Ionen,
• Nachteile der Aluminium-Salz-Methode:
– Geruchsbelästigung und mögliche Gefährdung durch Schwefelwasserstoff,
• Vorteile der Zahnpasta-Methode:
– einfache Durchführung, preiswerte Materialien,
• Nachteile Zahnpasta-Methode:
– Abtragung der Silber-Atome, bei häufiger Anwendung drohende Abtragung
der Silberschicht,
– Kratzer am Silber auf Grund der mechanischen Belastung.
2b beurteilt die beiden Verfahren zur Silberreinigung, indem er Vor- und Nachteile 2
beider Verfahren gegenüberstellt, z. B.:
• Unter Abwägung der Vor- und Nachteile ist die Aluminium-Salz-Methode
überlegen, da bei dieser Methode die Silberschicht erhalten bleibt, keine Kratzer
entstehen und gegen die Geruchsbelästigung gelüftet werden kann bzw. die Rei-
nigung im Freien durchgeführt werden kann.
Hinweis: Auch andere sinnvolle Argumentationen sind als richtig zu werten. Pro
Methode sind mindestens ein Vorteil und ein Nachteil zu nennen.
3 erfüllt ein weiteres aufgabenbezogenes Kriterium. (2)
b) Darstellungsleistung
Anforderungen maximal
erreichbare
Punktzahl
Der Prüfling
1 führt seine Gedanken schlüssig, stringent und klar aus. 5
2 • strukturiert seine Darstellung sachgerecht und übersichtlich, 4
• verwendet eine differenzierte und präzise Sprache,
• veranschaulicht seine Ausführungen durch geeignete Skizzen, Schemata etc.,
• gestaltet seine Arbeit formal ansprechend.
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 1 (GG)
Seite 6 von 9
7. Bewertungsbogen zur Prüfungsarbeit
Name des Prüflings: ____________________________________ Kursbezeichnung: ____________
Schule: _____________________________________________
Teilaufgabe 1
Anforderungen Lösungsqualität
Der Prüfling maximal
erreichbare
EK2 ZK DK
Punktzahl
1 erläutert die im … 8
2 berechnet die Masse … 4
3a erläutert den Vorteil … 4
3b erläutert den Vorteil … 2
4 erfüllt ein weiteres aufgabenbezogenes Kriterium: (2)
……………………………………………………………..
……………………………………………………………..
Summe 1. Teilaufgabe 18
Teilaufgabe 2
Anforderungen Lösungsqualität
Der Prüfling maximal
erreichbare
EK ZK DK
Punktzahl
1 berechnet die Spannung … 4
2 erläutert mithilfe der … 6
3 beurteilt, ob es … 6
4 erfüllt ein weiteres aufgabenbezogenes Kriterium: (2)
……………………………………………………………..
……………………………………………………………..
Summe 2. Teilaufgabe 16
2 EK = Erstkorrektur; ZK = Zweitkorrektur; DK = Drittkorrektur
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 1 (GG)
Seite 7 von 9
Teilaufgabe 3
Anforderungen Lösungsqualität
Der Prüfling maximal
erreichbare EK ZK DK
Punktzahl
1 erklärt die Beobachtungen … 2
2a beurteilt die Aussagen … 4
2b beurteilt die Aussagen … 8
3 erfüllt ein weiteres aufgabenbezogenes Kriterium: (2)
……………………………………………………………..
……………………………………………………………..
Summe 3. Teilaufgabe 14
Teilaufgabe 4
Anforderungen Lösungsqualität
Der Prüfling maximal
erreichbare EK ZK DK
Punktzahl
1 erläutert auch unter … 8
2a beurteilt die beiden … 8
2b beurteilt die beiden … 2
3 erfüllt ein weiteres aufgabenbezogenes Kriterium: (2)
……………………………………………………………..
……………………………………………………………..
Summe 4. Teilaufgabe 18
Summe der 1., 2., 3. und 4. Teilaufgabe 66
Darstellungsleistung
Anforderungen Lösungsqualität
Der Prüfling maximal
erreichbare
EK ZK DK
Punktzahl
1 führt seine Gedanken … 5
2 strukturiert seine Darstellung … 4
Summe Darstellungsleistung 9
Summe insgesamt (inhaltliche und Darstellungsleistung) 75
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 1 (GG)
Seite 8 von 9
Festlegung der Gesamtnote (Bitte nur bei der letzten bearbeiteten Aufgabe ausfüllen.)
Lösungsqualität
maximal
erreichbare EK ZK DK
Punktzahl
Übertrag der Punktsumme aus der ersten bearbeiteten Aufgabe 75
Übertrag der Punktsumme aus der zweiten bearbeiteten Aufgabe 75
Punktzahl der gesamten Prüfungsleistung 150
aus der Punktsumme resultierende Note gemäß nachfolgender
Tabelle
Note ggf. unter Absenkung um bis zu zwei Notenpunkte
gemäß § 13 Abs. 2 APO-GOSt
Paraphe
Berechnung der Endnote nach Anlage 4 der Abiturverfügung auf der Grundlage von § 34 APO-GOSt
Die Klausur wird abschließend mit der Note ________________________ (____ Punkte) bewertet.
Unterschrift, Datum:
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 1 (GG)
Seite 9 von 9
Grundsätze für die Bewertung (Notenfindung)
Für die Zuordnung der Notenstufen zu den Punktzahlen ist folgende Tabelle zu verwenden:
Note Punkte Erreichte Punktzahl
sehr gut plus 15 150 – 143
sehr gut 14 142 – 135
sehr gut minus 13 134 – 128
gut plus 12 127 – 120
gut 11 119 – 113
gut minus 10 112 – 105
befriedigend plus 9 104 – 98
befriedigend 8 97 – 90
befriedigend minus 7 89 – 83
ausreichend plus 6 82 – 75
ausreichend 5 74 – 68
ausreichend minus 4 67 – 60
mangelhaft plus 3 59 – 50
mangelhaft 2 49 – 41
mangelhaft minus 1 40 – 30
ungenügend 0 29 – 0
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
CH LK HT 2 (GG)
Seite 1 von 4
Name: _______________________
Abiturprüfung 2023
Chemie, Leistungskurs
Aufgabenstellung:
Ballistische Schutzwesten
1. Geben Sie die Monomere sowie den Reaktionstyp der Synthese des Polyester-Präpoly-
mers an. Erläutern Sie unter Angabe einer Reaktionsgleichung mit Strukturformeln die
Bildungsreaktion des Polyester-Präpolymers und erklären Sie, wie sich diese zugunsten
einer besseren Produktausbeute steuern lässt. (16 Punkte)
2. Erläutern Sie unter Angabe des Reaktionstyps den Ablauf der Reaktion für die Herstel-
lung von Cumol aus Benzol und Propen in Einzelschritten. Geben Sie begründet ein
mögliches Nebenprodukt an. (16 Punkte)
3. Erklären Sie die einzelnen Reaktionsschritte der Bildung von Poly-α-methylstyrol aus
α-Methylstyrol unter Zugabe eines organischen Peroxids. Geben Sie für diese Teilschritte
Reaktionsschemata an. Begründen Sie den Einsatz des Copolymers aus α-Methylstyrol
und dem Polyester-Präpolymer in Schutzwesten anstelle von Poly-α-methylstyrol.
(16 Punkte)
4. Vergleichen Sie die zwischenmolekularen Wechselwirkungen im Polyaramid und im
Hochleistungspolyethen mithilfe von geeigneten Strukturformelausschnitten. Erklären
Sie, wie Verzweigungen in Polyethenketten die zwischenmolekularen Wechselwir-
kungen beeinflussen. Erläutern Sie, dass die Art der zwischenmolekularen Wechsel-
wirkungen allein nicht ausreichend ist, um die Zugfestigkeit der Fasern einzuordnen.
(18 Punkte)
Zugelassene Hilfsmittel:
• Taschenrechner (grafikfähiger Taschenrechner / CAS-Taschenrechner)
• Periodensystem
• Wörterbuch zur deutschen Rechtschreibung
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
CH LK HT 2 (GG)
Seite 2 von 4
Name: _______________________
Fachspezifische Vorgaben:
Ballistische Schutzwesten – auch „kugelsichere Westen“ genannt – dienen dazu, die Trägerin
oder den Träger vor der tödlichen Wirkung von Geschossen aus Schusswaffen zu schützen.
Sie werden von Polizistinnen und Polizisten auf der ganzen Welt während ihres Dienstes
verwendet.
Das Geschoss bleibt nach einem Beschuss in der Weste und die Energie des Einschlags
wird auf eine möglichst große Fläche verteilt. Damit dies sicher gelingt, bestehen die
Kleidungsstücke aus einem Faser-Kunststoff-Verbund (FKV), einem Werkstoff, bei dem
Verstärkungsfasern in einen Kunststoff (Matrix) eingebettet werden. Der FKV muss sehr
reißfest sein und darf auch bei hohen Temperaturen nicht schmelzen.
Abbildung 1:
Faser-Kunststoff-Verbund (FKV) – Verstärkungsfasern werden von einer Kunststoffmatrix umgeben.
(Quelle: Lechler, Katharina; Menner, Marietta: Lehrerhandbuch – Faserverbundwerkstoffe.
Universität Augsburg 2016, S. 8)
Herstellung der Matrix
Die Matrix besteht aus einem Copolymer, das aus α-Methylstyrol und einem kurzkettigen
Polyester-Präpolymer gebildet wird.
Das benötigte α-Methylstyrol wird in einem zweischrittigen Verfahren gewonnen. Zuerst
reagieren in einer säurekatalysierten Reaktion Propen und Benzol zu Cumol. Anschließend
erfolgt eine Dehydrierung, die das Monomer bildet.
H3C CH2
O O O
HO O H
n
α-Methylstyrol Polyester-Präpolymer
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
CH LK HT 2 (GG)
Seite 3 von 4
Name: _______________________
Herstellung der Verstärkungsfasern
Es gibt unterschiedliche Verstärkungsfasern, die sich für den Einsatz in einer solchen Art
von Schutzweste eignen. Am häufigsten werden Fasern aus Polyaramid oder Hochleistungs-
polyethen verwendet. Hochleistungspolyethen besteht aus völlig unverzweigten, d. h. nur
linearen Ketten, während die Polymerketten in normalem Polyethen auch Verzweigungen
haben. Beide Kunststoffe, Polyaramid und Hochleistungspolyethen, werden nach der Her-
stellung zuerst gesponnen und danach verstreckt, so dass große Bereiche mit parallelen Mole-
külketten entstehen (kristalline Bereiche). Die fertigen Fasern bettet man bei der Matrix-
bildung ein, es entsteht eine Platte aus einem Faser-Kunststoff-Verbund.
Zusatzinformationen:
Kristallisationsgrad
Die Kristallisation ist der Übergang eines Kunststoffs in einen hochgeordneten Zustand.
Der Kristallisationsgrad gibt an, welcher Anteil des Werkstoffs diesen Zustand erreicht hat.
Zugfestigkeit
Ein Probekörper mit definierten Abmessungen wird mittels einer Prüfmaschine auseinander-
gezogen. Die maximale Kraft pro mm² bis zum Zerreißen ist die Zugfestigkeit.
Tabelle 1: Kristallisationsgrad und Zugfestigkeit von Polyaramid und verschiedenen
Polyethen-Sorten
Kristallisationsgrad Zugfestigkeit
Polyaramid 52 % 2800 – 2900 N/mm²
Hochleistungspolyethen 85 % 3000 – 4000 N/mm²
Polyethen (LD)1 35 – 50 % 20 N/mm²
Polyethen (HD)2 55 – 75 % 27 N/mm²
1
Polyethen (LD): Polyethen mit einer geringen Dichte (0,915 g/cm³ bis 0,935 g/cm³)
2
Polyethen (HD): Polyethen mit einer hohen Dichte (0,94 g/cm³ bis 0,97 g/cm³)
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
CH LK HT 2 (GG)
Seite 4 von 4
Name: _______________________
O O
H CH2 R
N N R CH2
OH
H H n
n
Polyaramid Polyethen
H3C CH3
R
H3C CH2 O O
Benzol Propen Cumol allgemeine Form eines
organischen Peroxids
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 2 (GG)
Seite 1 von 9
Unterlagen für die Lehrkraft
Abiturprüfung 2023
Chemie, Leistungskurs
1. Aufgabenart
Bearbeitung einer Aufgabe, die auf fachspezifischen Vorgaben basiert
2. Aufgabenstellung1
Ballistische Schutzwesten
1. Geben Sie die Monomere sowie den Reaktionstyp der Synthese des Polyester-Präpoly-
mers an. Erläutern Sie unter Angabe einer Reaktionsgleichung mit Strukturformeln die
Bildungsreaktion des Polyester-Präpolymers und erklären Sie, wie sich diese zugunsten
einer besseren Produktausbeute steuern lässt. (16 Punkte)
2. Erläutern Sie unter Angabe des Reaktionstyps den Ablauf der Reaktion für die Herstel-
lung von Cumol aus Benzol und Propen in Einzelschritten. Geben Sie begründet ein
mögliches Nebenprodukt an. (16 Punkte)
3. Erklären Sie die einzelnen Reaktionsschritte der Bildung von Poly-α-methylstyrol aus
α-Methylstyrol unter Zugabe eines organischen Peroxids. Geben Sie für diese Teilschritte
Reaktionsschemata an. Begründen Sie den Einsatz des Copolymers aus α-Methylstyrol
und dem Polyester-Präpolymer in Schutzwesten anstelle von Poly-α-methylstyrol.
(16 Punkte)
4. Vergleichen Sie die zwischenmolekularen Wechselwirkungen im Polyaramid und im
Hochleistungspolyethen mithilfe von geeigneten Strukturformelausschnitten. Erklären
Sie, wie Verzweigungen in Polyethenketten die zwischenmolekularen Wechselwir-
kungen beeinflussen. Erläutern Sie, dass die Art der zwischenmolekularen Wechsel-
wirkungen allein nicht ausreichend ist, um die Zugfestigkeit der Fasern einzuordnen.
(18 Punkte)
1 Die Aufgabenstellung deckt inhaltlich alle drei Anforderungsbereiche ab.
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 2 (GG)
Seite 2 von 9
3. Materialgrundlage
• AVK Industrievereinigung Verstärkte Kunststoffe e. V. (Hrsg.):
Handbuch Faserverbundkunststoffe. Vieweg + Teubner, Wiesbaden 2010
• Zhu, Guoqi et al.: Penetration of laminated Kevlar by Projectiles.
In: International Journal of Solids and Structures, Volume 29, Issue 4, Page 399 to 420.
Amsterdam: Elsevier 1992
4. Bezüge zum Kernlehrplan und zu den Vorgaben 2023
Die Aufgaben weisen vielfältige Bezüge zu den Kompetenzerwartungen und Inhaltsfeldern
des Kernlehrplans bzw. zu den in den Vorgaben ausgewiesenen Fokussierungen auf.
Im Folgenden wird auf Bezüge von zentraler Bedeutung hingewiesen.
1. Inhaltsfelder und inhaltliche Schwerpunkte
Organische Produkte – Werkstoffe und Farbstoffe
• Organische Verbindungen und Reaktionswege
• Organische Werkstoffe
• Farbstoffe und Farbigkeit
• Konzentrationsbestimmung durch Lichtabsorption
2. Medien/Materialien
• entfällt
5. Zugelassene Hilfsmittel
• Taschenrechner (grafikfähiger Taschenrechner / CAS-Taschenrechner)
• Periodensystem
• Wörterbuch zur deutschen Rechtschreibung
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 2 (GG)
Seite 3 von 9
6. Vorgaben für die Bewertung der Schülerleistungen
Teilleistungen – Kriterien
a) inhaltliche Leistung
Teilaufgabe 1
Anforderungen maximal
erreichbare
Punktzahl
Der Prüfling
1 gibt die Monomere sowie den Reaktionstyp der Synthese des Polyester-Präpolymers 4
an.
● O O
HO OH
OH
HO und
• Es handelt sich um eine Veresterung, um eine Substitutions- oder um eine
Additions-Eliminierungsreaktion.
Hinweis: Es genügt, wenn der Prüfling eine Bezeichnung angibt.
2a erläutert unter Angabe einer Reaktionsgleichung mit Strukturformeln die Bildungs- 4
reaktion des Polyester-Präpolymers, z. B.:
O O
+ OH
n HO OH n HO
O O O
HO O H + (2n-1) H2O
n
2b erläutert unter Angabe einer Reaktionsgleichung mit Strukturformeln die Bildungs- 2
reaktion des Polyester-Präpolymers, z. B.:
• Eine Carboxygruppe des Maleinsäure-Moleküls reagiert mit einer Hydroxy-
gruppe des Buten-1,4-diol-Moleküls unter Abspaltung eines Wasser-Moleküls
und Bildung einer Estergruppe.
3 erklärt, wie sich diese zugunsten einer besseren Produktausbeute steuern lässt, z. B.: 6
• Da eine Veresterung umkehrbar ist, liegen Produkte und Edukte im chemischen
Gleichgewicht vor.
• Dieses Gleichgewicht kann durch die Veränderung der Stoffmengen von Produk-
ten und Edukten im Reaktionsgemisch beeinflusst werden.
• Dies kann zum Beispiel durch den Entzug des entstehenden Wassers geschehen.
4 erfüllt ein weiteres aufgabenbezogenes Kriterium. (2)
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 2 (GG)
Seite 4 von 9
Teilaufgabe 2
Anforderungen maximal
erreichbare
Punktzahl
Der Prüfling
1a erläutert unter Angabe der Reaktionsschritte die Herstellung von Cumol aus Benzol 6
und Propen, z. B.:
CH2 CH3
+
+ +
HC H C H
CH3 CH3
CH3 CH3
CH3 CH CH
CH3 CH3
+H
+ +
C H
+ H
CH3
1b erläutert unter Angabe der Reaktionsschritte die Herstellung von Cumol aus Benzol 6
und Propen, z. B.:
• Das Wasserstoff-Ion reagiert mit dem Propen-Molekül unter Auflösung der
Doppelbindung und der Bildung eines Carbenium-Ions.
• Das Carbenium-Ion tritt als elektrophiles Teilchen mit den π-Elektronen des
Benzol-Moleküls in Wechselwirkung (π-Komplex).
• Es wird ein mesomeriestabilisierter σ-Komplex gebildet, und abschließend er-
folgt die Rearomatisierung durch Protonenabspaltung.
2 gibt begründet ein mögliches Nebenprodukt an. 4
Hinweis: Es gibt zwei mögliche Betrachtungsweisen dieser Aufgabe, von der ledig-
lich eine erwartet wird.
• Möglichkeit 1: Es bildet sich ein primäres Carbenium-Ion und damit entsteht
Propylbenzol.
H + H
CH2 C
HC + H
+
H2C
CH3 CH3
CH2 CH3
CH2
• Möglichkeit 2: Es ergibt sich eine Zweitsubstitution, z. B.:
H3C CH3
CH
CH3
CH
CH3
3 erfüllt ein weiteres aufgabenbezogenes Kriterium. (2)
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 2 (GG)
Seite 5 von 9
Teilaufgabe 3
Anforderungen maximal
erreichbare
Punktzahl
Der Prüfling
1 erklärt die einzelnen Reaktionsschritte der Bildung von Poly-α-methylstyrol aus 6
α-Methylstyrol unter Zugabe eines organischen Peroxids, z. B.:
• Erzeugung von Startradikalen: Bildung von zwei Startradikalen durch homoly-
tische Spaltung, z. B. eines organischen Peroxids (entweder durch Licht oder
einen Katalysator),
• Kettenstart: Reaktion des Startradikals, z. B. mit einem α-Methylstyrol-Molekül,
• Kettenwachstum: wiederholte Reaktion des gebildeten Radikals mit einem
α-Methylstyrol-Molekül,
• Kettenabbruch: Reaktion zweier Radikale zu einem Molekül, das kein Radikal ist.
2 gibt für diese Teilschritte Reaktionsschemata an. 4
Hinweis: Es wird erwartet, dass der Prüfling Reaktionsschemata in
Strukturformelschreibweise für die unter 1 genannten Schritte angibt.
3 begründet den Einsatz des Copolymers aus α-Methylstyrol und dem Polyester- 6
Präpolymer in Schutzwesten anstelle von Poly-α-methylstyrol, z. B.:
• Poly-α-methylstyrol ist als Polymer für die Matrix nicht geeignet, da es als
Thermoplast schmelzen kann.
• Die zugesetzten Polyester-Präpolymer-Moleküle enthalten mehrere reaktive
Doppelbindungen, sind also für die Polymerisation multifunktionale Moleküle.
Über diese Moleküle erfolgt eine Vernetzung des entstehenden Polymers.
• Es bildet sich ein Duroplast, der auch bei hohen Temperaturen nicht weich wird
und die Verstärkungsfaser fest einbindet.
4 erfüllt ein weiteres aufgabenbezogenes Kriterium. (2)
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 2 (GG)
Seite 6 von 9
Teilaufgabe 4
Anforderungen maximal
erreichbare
Punktzahl
Der Prüfling
1a vergleicht die zwischenmolekularen Wechselwirkungen im Polyaramid und im 4
Hochleistungspolyethen mithilfe von geeigneten Strukturformelausschnitten, z. B.:
• Strukturformelausschnitt Polyaramid
• Strukturformelausschnitt Polyethen
... ...
... ...
... ...
1b vergleicht die zwischenmolekularen Wechselwirkungen im Polyaramid und im 4
Hochleistungspolyethen mithilfe von geeigneten Strukturformelausschnitten, z. B.:
• Im Polyaramid gibt es Wasserstoffbrücken zwischen den Amidgruppen und
Van-der-Waals-Wechselwirkungen zwischen den aromatischen Ringen.
• Beim Polyethen können sich die unverzweigten Polymerketten geordnet aneinan-
derlagern und aufgrund der regelmäßigen Anordnungen leicht Van-der-Waals-
Wechselwirkungen ausbilden.
2 erklärt, wie Verzweigungen in Polyethenketten die zwischenmolekularen Wechsel- 4
wirkungen beeinflussen.
• Die Verzweigungen verhindern, dass sich die Polyethenketten parallel zueinan-
der anordnen.
• Dadurch bilden sich keine hochgeordneten Zustände aus, in denen die Van-der-
Waals-Kräfte besonders ausgeprägt sind.
3 erläutert, dass die Art der zwischenmolekularen Wechselwirkungen allein nicht 6
ausreichend ist, um die Zugfestigkeit der Fasern einzuordnen, z. B.:
• Wasserstoffbrücken (Dipol-Dipol-Wechselwirkungen) bei polaren Strukturen
wie im Polyaramid sind deutlich stärker als Van-der-Waals-Kräfte bei unpolaren
Ketten wie im Polyethen.
• Bei gleichem Kristallisationsgrad hat deshalb das Polyaramid die höhere Zug-
festigkeit.
• Hat das Polyethen im Vergleich zum Polyaramid einen deutlich höheren Kristalli-
sationsgrad, so kann seine Zugfestigkeit die des Polyaramid übertreffen.
4 erfüllt ein weiteres aufgabenbezogenes Kriterium. (2)
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 2 (GG)
Seite 7 von 9
b) Darstellungsleistung
Anforderungen maximal
erreichbare
Punktzahl
Der Prüfling
1 führt seine Gedanken schlüssig, stringent und klar aus. 5
2 • strukturiert seine Darstellung sachgerecht und übersichtlich, 4
• verwendet eine differenzierte und präzise Sprache,
• veranschaulicht seine Ausführungen durch geeignete Skizzen, Schemata etc.,
• gestaltet seine Arbeit formal ansprechend.
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 2 (GG)
Seite 8 von 9
7. Bewertungsbogen zur Prüfungsarbeit
Name des Prüflings: ____________________________________ Kursbezeichnung: ____________
Schule: _____________________________________________
Teilaufgabe 1
Anforderungen Lösungsqualität
Der Prüfling maximal
erreichbare
EK2 ZK DK
Punktzahl
1 gibt die Monomere … 4
2a erläutert unter Angabe … 4
2b erläutert unter Angabe … 2
3 erklärt, wie sich … 6
4 erfüllt ein weiteres aufgabenbezogenes Kriterium: (2)
……………………………………………………………..
……………………………………………………………..
Summe 1. Teilaufgabe 16
Teilaufgabe 2
Anforderungen Lösungsqualität
Der Prüfling maximal
erreichbare EK ZK DK
Punktzahl
1a erläutert unter Angabe … 6
1b erläutert unter Angabe … 6
2 gibt begründet ein … 4
3 erfüllt ein weiteres aufgabenbezogenes Kriterium: (2)
……………………………………………………………..
……………………………………………………………..
Summe 2. Teilaufgabe 16
2 EK = Erstkorrektur; ZK = Zweitkorrektur; DK = Drittkorrektur
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 2 (GG)
Seite 9 von 9
Teilaufgabe 3
Anforderungen Lösungsqualität
Der Prüfling maximal
erreichbare EK ZK DK
Punktzahl
1 erklärt die einzelnen … 6
2 gibt für diese … 4
3 begründet den Einsatz … 6
4 erfüllt ein weiteres aufgabenbezogenes Kriterium: (2)
……………………………………………………………..
……………………………………………………………..
Summe 3. Teilaufgabe 16
Teilaufgabe 4
Anforderungen Lösungsqualität
Der Prüfling maximal
erreichbare EK ZK DK
Punktzahl
1a vergleicht die zwischenmolekularen … 4
1b vergleicht die zwischenmolekularen … 4
2 erklärt, wie Verzweigungen … 4
3 erläutert, dass die … 6
4 erfüllt ein weiteres aufgabenbezogenes Kriterium: (2)
……………………………………………………………..
……………………………………………………………..
Summe 4. Teilaufgabe 18
Summe der 1., 2., 3. und 4. Teilaufgabe 66
Darstellungsleistung
Anforderungen Lösungsqualität
Der Prüfling maximal
erreichbare
EK ZK DK
Punktzahl
1 führt seine Gedanken … 5
2 strukturiert seine Darstellung … 4
Summe Darstellungsleistung 9
Summe insgesamt (inhaltliche und Darstellungsleistung) 75
Die Festlegung der Gesamtnote erfolgt auf dem Auswertungsbogen in LK HT 1.
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
CH LK HT 3 (GG)
Seite 1 von 4
Name: _______________________
Abiturprüfung 2023
Chemie, Leistungskurs
Aufgabenstellung:
Carmoisin – Synthese und Einsatz als Lebensmittelfarbstoff
1. Geben Sie die Kennzeichen aromatischer Systeme an. Erläutern Sie anhand der
Molekülstrukturen das unterschiedliche Verhalten von Stoff A (Naphthalin) und
Stoff B (1,2,3,4,5,8-Hexahydronaphthalin) gegenüber Brom. Erläutern Sie den Ablauf
der Reaktion von Stoff B und Brom in Einzelschritten. (16 Punkte)
2. Geben Sie den Reaktionstyp für die der Sulfonierung von 1-Naphthol zugrundeliegen-
den Reaktion an. Erläutern Sie den Ablauf dieser Reaktion in Einzelschritten. Begrün-
den Sie die Position, an der die Sulfonierung von 1-Naphthol erfolgt. (12 Punkte)
3. Entwickeln Sie unter Angabe des Reaktionstyps und der beteiligten Stoffe eine Reaktions-
gleichung für die in Schritt II der Carmoisin-Synthese ablaufende Reaktion. Geben Sie
begründend die bei diesem Schritt einzuhaltenden Reaktionsbedingungen an. Entwickeln
Sie unter Angabe des Reaktionstyps eine Reaktionsgleichung für die in Schritt III der
Carmoisin-Synthese ablaufende Reaktion. (18 Punkte)
4. Erklären Sie am Beispiel von Carmoisin unter Bezug auf Tabelle 1 und das angegebene
Extinktionsmaximum den Zusammenhang zwischen Lichtabsorption und Farbigkeit.
Begründen Sie anhand der Molekülstruktur die Farbigkeit von Carmoisin. Erläutern Sie
am Beispiel der Konzentrationsbestimmung von Carmoisin in Limonade die Grundlagen
und Durchführung des fotometrischen Messverfahrens. (20 Punkte)
Zugelassene Hilfsmittel:
• Taschenrechner (grafikfähiger Taschenrechner / CAS-Taschenrechner)
• Periodensystem
• Wörterbuch zur deutschen Rechtschreibung
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
CH LK HT 3 (GG)
Seite 2 von 4
Name: _______________________
Fachspezifische Vorgaben:
Carmoisin (E 122) ist ein synthetischer, in Europa zugelassener Lebensmittelfarbstoff. Das
feste Natriumsalz ist gut wasserlöslich und beständig gegen Licht und Hitze. Das Extinktions-
maximum von Carmoisin liegt bei 516 nm. Carmoisin wird aufgrund seiner intensiven
Farbe u. a. für Getränke, Süß- und Zuckerwaren, Marzipan, Puddingpulver, Kunstspeiseeis,
Fruchtkonserven, Fertigsuppen und Paniermehl verwendet.
- +
SO 3 Na
N
N
OH - +
SO 3 Na
Carmoisin (Natriumsalz)
Carmoisin kann aus bicyclischen Kohlenwasserstoffverbindungen hergestellt werden, die
ein Naphthalin-Grundgerüst tragen. Naphthalin (Stoff A) ist ein weißer Feststoff, der in
unpolaren Lösemitteln gut löslich ist. Gibt man elementares Brom (Br2) zu einer Naphthalin-
lösung, entfärbt sich die Lösung nicht. Im Vergleich dazu entfärbt sich eine Lösung aus
1,2,3,4,5,8-Hexahydronaphthalin (Stoff B) und elementarem Brom schnell.
8 1
7 2
6 3
5 4
Naphthalin 1,2,3,4,5,8-Hexahydronaphthalin
(Stoff A) (Stoff B)
Für die Carmoisin-Synthese können die beiden Naphthalin-Derivate 1-Hydroxynaphthalin
(1-Naphthol) und 1-Aminonaphthalin eingesetzt werden (Abbildung 1). Beide Verbindungen
werden zunächst sulfoniert, indem sie mit konzentrierter Schwefelsäure (H2SO4) versetzt
werden. Dabei dienen Schwefeltrioxid-Moleküle (SO3) als Reaktionspartner, die in der
konzentrierten Schwefelsäure gelöst vorliegen. Bei der Sulfonierung (Schritte Ia und Ib)
entstehen 4-Hydroxynaphthalin-1-sulfonsäure und 4-Aminonaphthalin-1-sulfonsäure.
Beide Verbindungen lassen sich in verdünnter Natronlauge lösen und reagieren unter
bestimmten Bedingungen zum gewünschten Farbstoff Carmoisin. Dabei wird 4-Amino-
naphthalin-1-sulfonsäure zunächst in ein Zwischenprodukt überführt (Schritt II) und der
Reaktionsansatz anschließend mit 4-Hydroxynaphthalin-1-sulfonsäure versetzt (Schritt III).
Konzentrationsbestimmung
Seit 2010 müssen Lebensmittel, die Lebensmittelfarbstoffe der Farbstoffklasse enthalten,
zu der auch Carmoisin gehört, mit dem Warnhinweis „Kann Aktivität und Aufmerksamkeit
bei Kindern beeinträchtigen“ versehen sein. Zur Überprüfung der Einhaltung der für die
einzelnen Lebensmittel festgelegten Höchstmengen an Farbstoffen werden Konzentrations-
bestimmungen durchgeführt. In Limonade, die als einzigen zugesetzten Farbstoff Carmoisin
enthält, lässt sich die Konzentration des Farbstoffs gut fotometrisch ermitteln.
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
CH LK HT 3 (GG)
Seite 3 von 4
Name: _______________________
OH NH2
1-Hydroxynaphthalin 1-Aminonaphthalin
(1-Naphthol)
Ia Ib
SO 3H SO 3H
OH NH2
4-Hydroxynaphthalin-1- 4-Aminonaphthalin-1-
sulfonsäure sulfonsäure
II
Zwischenprodukt
III
- +
SO 3 Na
N
N
OH - +
SO 3 Na
Carmoisin (Natriumsalz)
Abbildung 1: Synthese von Carmoisin aus Naphthalin-Derivaten
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
CH LK HT 3 (GG)
Seite 4 von 4
Name: _______________________
Zusatzinformationen:
Als ein Derivat (von lateinisch derivare ‚ableiten‘) wird in der Chemie ein Stoff ähnlicher
Struktur bezeichnet. Derivate sind z. B. Stoffe, die an Stelle eines Wasserstoff-Atoms ein
anderes Atom oder eine ganze Atomgruppe besitzen bzw. bei denen ein oder mehrere
Atome/Atomgruppen entfernt wurden.
Schwefeltrioxid-Moleküle sind planar gebaut und enthalten drei gleichlange Bindungen
zwischen dem Schwefel-Atom und den Sauerstoff-Atomen.
δd–- δd–-
O δd++ O
S
O
–-
δd
Tabelle 1: Zusammenhang von absorbierter Strahlung, zugehöriger Spektralfarbe und
beobachteter Komplementärfarbe.
Wellenlänge λ in nm Spektralfarbe Komplementärfarbe
< 400 ultraviolett farblos
400 – 435 violett gelbgrün
435 – 480 blau gelb
480 – 490 grünblau orange
490 – 500 blaugrün rot
500 – 560 grün purpur
560 – 580 gelbgrün violett
580 – 595 gelb blau
595 – 605 orange grünblau
605 – 770 rot blaugrün
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 3 (GG)
Seite 1 von 7
Unterlagen für die Lehrkraft
Abiturprüfung 2023
Chemie, Leistungskurs
1. Aufgabenart
Bearbeitung einer Aufgabe, die auf fachspezifischen Vorgaben basiert
2. Aufgabenstellung1
Carmoisin – Synthese und Einsatz als Lebensmittelfarbstoff
1. Geben Sie die Kennzeichen aromatischer Systeme an. Erläutern Sie anhand der
Molekülstrukturen das unterschiedliche Verhalten von Stoff A (Naphthalin) und
Stoff B (1,2,3,4,5,8-Hexahydronaphthalin) gegenüber Brom. Erläutern Sie den Ablauf
der Reaktion von Stoff B und Brom in Einzelschritten. (16 Punkte)
2. Geben Sie den Reaktionstyp für die der Sulfonierung von 1-Naphthol zugrundeliegen-
den Reaktion an. Erläutern Sie den Ablauf dieser Reaktion in Einzelschritten. Begrün-
den Sie die Position, an der die Sulfonierung von 1-Naphthol erfolgt. (12 Punkte)
3. Entwickeln Sie unter Angabe des Reaktionstyps und der beteiligten Stoffe eine Reaktions-
gleichung für die in Schritt II der Carmoisin-Synthese ablaufende Reaktion. Geben Sie
begründend die bei diesem Schritt einzuhaltenden Reaktionsbedingungen an. Entwickeln
Sie unter Angabe des Reaktionstyps eine Reaktionsgleichung für die in Schritt III der
Carmoisin-Synthese ablaufende Reaktion. (18 Punkte)
4. Erklären Sie am Beispiel von Carmoisin unter Bezug auf Tabelle 1 und das angegebene
Extinktionsmaximum den Zusammenhang zwischen Lichtabsorption und Farbigkeit.
Begründen Sie anhand der Molekülstruktur die Farbigkeit von Carmoisin. Erläutern Sie
am Beispiel der Konzentrationsbestimmung von Carmoisin in Limonade die Grundlagen
und Durchführung des fotometrischen Messverfahrens. (20 Punkte)
1 Die Aufgabenstellung deckt inhaltlich alle drei Anforderungsbereiche ab.
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 3 (GG)
Seite 2 von 7
3. Materialgrundlage
• Fieser, Louis Frederick; Fieser, Mary: Organische Chemie. Weinheim: Verlag Chemie 1972,
2. verbesserte Auflage
• https://www.lebensmittellexikon.de/a0002270.php (Zugriff 05.01.2022)
• https://roempp.thieme.de/lexicon/RD-01-04166?searchterm=carmoisin&context=search
(Zugriff 05.01.2022)
• https://universal_lexikon.de-academic.com/276601/Naphtholsulfons%C3%A4uren
(Zugriff 05.02.2022)
4. Bezüge zum Kernlehrplan und zu den Vorgaben 2023
Die Aufgaben weisen vielfältige Bezüge zu den Kompetenzerwartungen und Inhaltsfeldern
des Kernlehrplans bzw. zu den in den Vorgaben ausgewiesenen Fokussierungen auf.
Im Folgenden wird auf Bezüge von zentraler Bedeutung hingewiesen.
1. Inhaltsfelder und inhaltliche Schwerpunkte
Organische Produkte – Werkstoffe und Farbstoffe
• Organische Verbindungen und Reaktionswege
• Reaktionsabläufe
• Organische Werkstoffe
• Farbstoffe und Farbigkeit
• Konzentrationsbestimmung durch Lichtabsorption
2. Medien/Materialien
• entfällt
5. Zugelassene Hilfsmittel
• Taschenrechner (grafikfähiger Taschenrechner / CAS-Taschenrechner)
• Periodensystem
• Wörterbuch zur deutschen Rechtschreibung
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 3 (GG)
Seite 3 von 7
6. Vorgaben für die Bewertung der Schülerleistungen
Teilleistungen – Kriterien
a) inhaltliche Leistung
Teilaufgabe 1
Anforderungen maximal
erreichbare
Punktzahl
Der Prüfling
1 gibt die Kennzeichen aromatischer Systeme an, z. B.: 4
• planares Ringsystem,
• delokalisiertes π-Elektronensystem,
• Mesomeriestabilisierung,
• Hückel-Regel (alternativ: [4n + 2] π-Elektronen).
2 erläutert anhand der Molekülstrukturen das unterschiedliche Verhalten von Stoff A 6
(Naphthalin) und Stoff B (1,2,3,4,5,8-Hexahydronaphthalin) gegenüber Brom, z. B.:
• Bei Stoff A (Naphthalin) handelt es sich um eine aromatische Verbindung mit
delokalisiertem π-Elektronensystemen, die aufgrund des Energiegewinns durch
Mesomerie energieärmer und stabiler ist.
• Eine elektrophile Addition von Brom an den Aromaten kann aufgrund der Meso-
meriestabilisierung nicht erfolgen.
• Bei Stoff B liegen isolierte Doppelbindungen vor, die leichter elektrophil angreif-
bar sind; hier erfolgt bei Raumtemperatur eine elektrophile Addition der Brom-
Moleküle an die Doppelbindungen.
3 erläutert den Ablauf der Reaktion von Stoff B und Brom in Einzelschritten. 6
Hinweis: Es wird erwartet, dass der Prüfling auf die typischen Schritte einer elektro-
philen Addition eingeht.
Schritt 1: Annäherung eines Brom-Moleküls an die C=C-Doppelbindung mit tempo-
rärer Polarisierung der Elektronenpaarbindung, Wechselwirkung des positiv teil-
geladenen Brom-Atoms und der Doppelbindung (Tradukt), heterolytische Trennung
der Bindung des Brom-Moleküls und Bildung eines Bromonium-Ions (Interdukt)
sowie eines Bromid-Ions.
Schritt 2: Anlagerung eines Bromid-Ions am Bromonium-Ion (Bildung einer
1,2-Dibromverbindung).
4 erfüllt ein weiteres aufgabenbezogenes Kriterium. (2)
Teilaufgabe 2
Anforderungen maximal
erreichbare
Punktzahl
Der Prüfling
1 gibt den Reaktionstyp für die der Sulfonierung von 1-Naphthol zugrundeliegenden 2
Reaktion an, z. B.:
• Reaktionstyp: elektrophile Substitution.
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 3 (GG)
Seite 4 von 7
2 erläutert den Ablauf dieser Reaktion in Einzelschritten. 6
Hinweis: Es wird erwartet, dass der Prüfling ausgehend von dem elektrophilen
Angriff der Schwefeltrioxid-Moleküle (stark positiv teilgeladene Schwefel-Atome) die
Bildung eines π-Komplexes und die Bildung des mesomeriestabilisierten σ-Komplexes
erläutert sowie auf die Rearomatisierung eingeht und dies anhand geeigneter
Molekülausschnitte darstellt.
3 begründet die Position, an der die Sulfonierung von 1-Naphthol erfolgt. 4
Hinweis: Es wird erwartet, dass der Prüfling auf die aktivierende (+M-Effekt) und
in o- und p-Position dirigierende Wirkung der Hydroxygruppe sowie die Bevorzu-
gung der p-Position aus sterischen Gründen eingeht.
4 erfüllt ein weiteres aufgabenbezogenes Kriterium. (2)
Teilaufgabe 3
Anforderungen maximal
erreichbare
Punktzahl
Der Prüfling
1 entwickelt unter Angabe des Reaktionstyps und der beteiligten Stoffe eine Reaktions- 8
gleichung für die in Schritt II der Carmoisin-Synthese ablaufende Reaktion, z. B.:
• Reaktionstyp: Diazotierung,
• beteiligte Stoffe: 4-Aminonaphthalin-1-sulfonsäure, Natriumnitrit und Salzsäure
(alternativ: salpetrige Säure oder Nitrosyl-Kationen),
• Reaktionsgleichung:
SO 3H SO 3H
+ NO2- + 2 H+ + 2 H2O
NH2 N
.
+
N
2 gibt begründend die bei diesem Reaktionsschritt einzuhaltenden Reaktionsbedin- 4
gungen an.
Hinweis: Es wird erwartet, dass der Prüfling darauf eingeht, dass die bei der Reak-
tion entstehenden Diazonium-Ionen bei höheren Temperaturen zerfallen können und
aus diesem Grund alle entsprechenden Lösungen der Schritte, in denen Diazonium-
Ionen entstehen oder reagieren sollen, auf unter 5 °C gekühlt werden.
3 entwickelt unter Angabe des Reaktionstyps eine Reaktionsgleichung für die in 6
Schritt III der Carmoisin-Synthese ablaufende Reaktion, z. B.:
• Reaktionstyp: Azokupplung (alternativ: elektrophile Substitution),
• Reaktionsgleichung:
SO 3H SO 3H SO 3H
+
+ N + H
N
OH
OH N SO 3H
.
+
N
4 erfüllt ein weiteres aufgabenbezogenes Kriterium. (2)
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 3 (GG)
Seite 5 von 7
Teilaufgabe 4
Anforderungen maximal
erreichbare
Punktzahl
Der Prüfling
1 erklärt am Beispiel von Carmoisin unter Bezug auf Tabelle 1 und das angegebene 6
Extinktionsmaximum den Zusammenhang zwischen Lichtabsorption und Farbigkeit.
Hinweis: Es wird erwartet, dass der Prüfling Aussagen macht zu den Spektralfarben
des weißen Lichts, der Anregung von Elektronen und dem Energiestufenmodell der
Lichtabsorption, dem Extinktionsmaximum des angegebenen Farbstoffs sowie zum
Zusammenhang zwischen absorbierter Spektralfarbe und Eigenfarbe des Farbstoffs
(z. B.: Extinktionsmaximum von 516 nm beim Carmoisin, absorbierte Spektralfarbe
Grün, Eigenfarbe Purpur).
2 begründet anhand der Molekülstruktur die Farbigkeit von Carmoisin. 6
Hinweis: Es wird erwartet, dass der Prüfling am Beispiel von Carmoisin Aussagen
zum vorliegenden ausgedehnten System konjugierter Doppelbindungen (Chromophor)
und zum Mesomeriemodell macht: mesomere Grenzstrukturen, Delokalisation von
konjugierten π-Elektronen, Einfluss von Donator-/Akzeptorgruppen, hier z. B. der
Hydroxygruppe als Donatorgruppe.
3 erläutert am Beispiel der Konzentrationsbestimmung von Carmoisin in Limonade 8
die Grundlagen und Durchführung des fotometrischen Messverfahrens.
Hinweis: Es wird erwartet, dass der Prüfling auf das Lambert-Beer-Gesetz als
Grundlage des fotometrischen Messverfahrens, nach dem die Extinktion eines Farb-
stoffes proportional zur Konzentration des Farbstoffes ist, sowie auf folgende
Durchführungsschritte eingeht: Erstellung einer Kalibriergeraden (Extinktions-
messung verschiedener Carmoisinlösungen bekannter Konzentrationen, Auftragen
der Extinktionswerte gegen die Konzentrationen), alternativ: Ermittlung des mola-
ren Extinktionskoeffizienten; anschließend Messung einer Limonadenprobe unter
gleichen Bedingungen (alle Messungen werden in Küvetten gleicher Schichtdicke
bei der Wellenlänge des Extinktionsmaximums, hier 516 nm, durchgeführt); Ablesen
der Konzentration des Farbstoffes in der Limonadenprobe direkt an der Kalibrier-
geraden, alternativ: Berechnung mithilfe des molaren Extinktionskoeffizienten.
4 erfüllt ein weiteres aufgabenbezogenes Kriterium. (2)
b) Darstellungsleistung
Anforderungen maximal
erreichbare
Punktzahl
Der Prüfling
1 führt seine Gedanken schlüssig, stringent und klar aus. 5
2 • strukturiert seine Darstellung sachgerecht und übersichtlich, 4
• verwendet eine differenzierte und präzise Sprache,
• veranschaulicht seine Ausführungen durch geeignete Skizzen, Schemata etc.,
• gestaltet seine Arbeit formal ansprechend.
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 3 (GG)
Seite 6 von 7
7. Bewertungsbogen zur Prüfungsarbeit
Name des Prüflings: ____________________________________ Kursbezeichnung: ____________
Schule: _____________________________________________
Teilaufgabe 1
Anforderungen Lösungsqualität
Der Prüfling maximal
erreichbare
EK2 ZK DK
Punktzahl
1 gibt die Kennzeichen … 4
2 erläutert anhand der … 6
3 erläutert den Ablauf … 6
4 erfüllt ein weiteres aufgabenbezogenes Kriterium: (2)
……………………………………………………………..
……………………………………………………………..
Summe 1. Teilaufgabe 16
Teilaufgabe 2
Anforderungen Lösungsqualität
Der Prüfling maximal
erreichbare
EK ZK DK
Punktzahl
1 gibt den Reaktionstyp … 2
2 erläutert den Ablauf … 6
3 begründet die Position … 4
4 erfüllt ein weiteres aufgabenbezogenes Kriterium: (2)
……………………………………………………………..
……………………………………………………………..
Summe 2. Teilaufgabe 12
2 EK = Erstkorrektur; ZK = Zweitkorrektur; DK = Drittkorrektur
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Ministerium für Schule und Bildung NRW CH LK HT 3 (GG)
Seite 7 von 7
Teilaufgabe 3
Anforderungen Lösungsqualität
Der Prüfling maximal
erreichbare EK ZK DK
Punktzahl
1 entwickelt unter Angabe … 8
2 gibt begründend die … 4
3 entwickelt unter Angabe … 6
4 erfüllt ein weiteres aufgabenbezogenes Kriterium: (2)
……………………………………………………………..
……………………………………………………………..
Summe 3. Teilaufgabe 18
Teilaufgabe 4
Anforderungen Lösungsqualität
Der Prüfling maximal
erreichbare EK ZK DK
Punktzahl
1 erklärt am Beispiel … 6
2 begründet anhand der … 6
3 erläutert am Beispiel … 8
4 erfüllt ein weiteres aufgabenbezogenes Kriterium: (2)
……………………………………………………………..
……………………………………………………………..
Summe 4. Teilaufgabe 20
Summe der 1., 2., 3. und 4. Teilaufgabe 66
Darstellungsleistung
Anforderungen Lösungsqualität
Der Prüfling maximal
erreichbare
EK ZK DK
Punktzahl
1 führt seine Gedanken … 5
2 strukturiert seine Darstellung … 4
Summe Darstellungsleistung 9
Summe insgesamt (inhaltliche und Darstellungsleistung) 75
Die Festlegung der Gesamtnote erfolgt auf dem Auswertungsbogen in LK HT 1.
Abiturprüfung 2023 – Nur für den Dienstgebrauch!
Das könnte Ihnen auch gefallen
- Loesungen Zum BuchDokument20 SeitenLoesungen Zum BuchAlbertus HolbeinNoch keine Bewertungen
- Galvanotechnik - ReferatDokument10 SeitenGalvanotechnik - Referatsolvalou_Noch keine Bewertungen
- WT2 MB Klausurvorbereitung WS2013Dokument4 SeitenWT2 MB Klausurvorbereitung WS2013Mathias Waßer100% (1)
- Alte Chemie Klausuren Uni HamburgDokument20 SeitenAlte Chemie Klausuren Uni HamburgpanakosNoch keine Bewertungen
- Satzglieder - Dativobjekt U - AkkusativobjektDokument2 SeitenSatzglieder - Dativobjekt U - AkkusativobjektKaren Maged RizkNoch keine Bewertungen
- Änderungsanzeige Und Anträge Im Renten Service Der Deutschen PostDokument2 SeitenÄnderungsanzeige Und Anträge Im Renten Service Der Deutschen PostLatoya ScottNoch keine Bewertungen
- 01 - LK2016 - HT - Redox-Gold FälschenDokument3 Seiten01 - LK2016 - HT - Redox-Gold Fälschenc0181511Noch keine Bewertungen
- Abiturprüfung 2021: Chemie, LeistungskursDokument38 SeitenAbiturprüfung 2021: Chemie, LeistungskursSuper NerdNoch keine Bewertungen
- SäurekorrosiokDokument7 SeitenSäurekorrosioknuredin elhosinyNoch keine Bewertungen
- ElektrometallurgieDokument19 SeitenElektrometallurgieMatias Garcia LabrañaNoch keine Bewertungen
- Korrosion: SchulversuchspraktikumDokument15 SeitenKorrosion: SchulversuchspraktikumasdfasddfNoch keine Bewertungen
- Elektrochemie III - Die Nernstgleichung Und Ihre AnwendungDokument25 SeitenElektrochemie III - Die Nernstgleichung Und Ihre AnwendungAndres QuenguanNoch keine Bewertungen
- AC Klausur GÖK 16. Dezember 2009Dokument10 SeitenAC Klausur GÖK 16. Dezember 2009xlj0331Noch keine Bewertungen
- 01 - LK2016 - HT - Redox-Gold Fälschen - LösungDokument9 Seiten01 - LK2016 - HT - Redox-Gold Fälschen - Lösungc0181511Noch keine Bewertungen
- 11 - KA2 - Übungen Zur Klassenarbeit - VerbDokument3 Seiten11 - KA2 - Übungen Zur Klassenarbeit - Verbbendix.pfeiferNoch keine Bewertungen
- Protokoll V09Dokument7 SeitenProtokoll V09Marvin StruveNoch keine Bewertungen
- SLA Chemistry Term 2Dokument6 SeitenSLA Chemistry Term 2meera.khalifa130Noch keine Bewertungen
- Thermodynamics of Antimony, Arsenic and Tin in SteelDokument7 SeitenThermodynamics of Antimony, Arsenic and Tin in SteelNishan GajurelNoch keine Bewertungen
- 04 GutmannDokument35 Seiten04 Gutmannmekki1Noch keine Bewertungen
- RedoxreaktionenDokument15 SeitenRedoxreaktionenOdranoel RellekNoch keine Bewertungen
- Nernst GleichungDokument7 SeitenNernst GleichungRichterNoch keine Bewertungen
- Baustoffkunde Zusammenfassung Klausuren 2.0Dokument17 SeitenBaustoffkunde Zusammenfassung Klausuren 2.0m.elmoursi02Noch keine Bewertungen
- Ionenbindung, - Strukturtypen, - Metalle - SkriptDokument45 SeitenIonenbindung, - Strukturtypen, - Metalle - SkriptRafael R.Noch keine Bewertungen
- FSP Pruefungsbeispiel Chemie T-KursDokument2 SeitenFSP Pruefungsbeispiel Chemie T-KursCheick DIASSONoch keine Bewertungen
- 1 Chemie Ist Wie Wirtschaft: Chemie - Die Stimmt!" 2017/2018 Aufgabenblatt 2. Runde - Klasse 9Dokument5 Seiten1 Chemie Ist Wie Wirtschaft: Chemie - Die Stimmt!" 2017/2018 Aufgabenblatt 2. Runde - Klasse 9Quốc NguyễnNoch keine Bewertungen
- 10.1.1 Lösung - Wiederholungs-Übung BindungstypenDokument2 Seiten10.1.1 Lösung - Wiederholungs-Übung BindungstypenFinn- FinnNoch keine Bewertungen
- AC II - 1. Klausur WS 1516 - MascottoDokument2 SeitenAC II - 1. Klausur WS 1516 - MascottoflorcimusaNoch keine Bewertungen
- Uebungsblatt 2-2020 - Loesungen-FreigeschaltetDokument9 SeitenUebungsblatt 2-2020 - Loesungen-FreigeschaltetFerryNoch keine Bewertungen
- Fachsemester 2, Anorganische Chemie 1Dokument102 SeitenFachsemester 2, Anorganische Chemie 1fur den kriegNoch keine Bewertungen
- Chemie Heft Raj 2022-2023 9BDokument7 SeitenChemie Heft Raj 2022-2023 9BArdra RajNoch keine Bewertungen
- TUT - Molare Massen, Stoffmengen Und Chemische GleichungenDokument3 SeitenTUT - Molare Massen, Stoffmengen Und Chemische Gleichungenteipel21Noch keine Bewertungen
- Lösungen ÜbungsaufgabenDokument1 SeiteLösungen ÜbungsaufgabenNgọc NghĩaNoch keine Bewertungen
- 2-8 Gr25 SL 2022Dokument10 Seiten2-8 Gr25 SL 2022Sakon UkonNoch keine Bewertungen
- 1 6 A IonenbindungDokument2 Seiten1 6 A IonenbindungkekekNoch keine Bewertungen
- Subiecte Chimie Anorganică Bac 2022Dokument2 SeitenSubiecte Chimie Anorganică Bac 2022Otilia Serescu0% (1)
- 4713 Chapter 08exDokument22 Seiten4713 Chapter 08exchinensisNoch keine Bewertungen
- Korrosion: Experimentalvortrag Vom 18.01.2007Dokument23 SeitenKorrosion: Experimentalvortrag Vom 18.01.2007Luca AndraeNoch keine Bewertungen
- ChemiefragenzweiDokument4 SeitenChemiefragenzweiAleks SohanNoch keine Bewertungen
- Übungsaufgaben Dichteste Packung WS 23 - 24Dokument8 SeitenÜbungsaufgaben Dichteste Packung WS 23 - 24florcimusaNoch keine Bewertungen
- Potentiometrie I Potentiometrische Simultantitration Zweier Basen"Dokument10 SeitenPotentiometrie I Potentiometrische Simultantitration Zweier Basen"IvaNoch keine Bewertungen
- Ek26 AnleitungDokument71 SeitenEk26 Anleitungxbains1507Noch keine Bewertungen
- Materialwissenschaft Eine KlausurDokument6 SeitenMaterialwissenschaft Eine Klausurzimba79Noch keine Bewertungen
- Seminar 0209Dokument201 SeitenSeminar 0209dominiktreo680Noch keine Bewertungen
- Organische Chemie - 1Dokument74 SeitenOrganische Chemie - 1Tibor KeményNoch keine Bewertungen
- 1930 Abel, E. Schmid, H. WeissKinetik Der SalpetersäureDokument18 Seiten1930 Abel, E. Schmid, H. WeissKinetik Der SalpetersäurefalconeyerNoch keine Bewertungen
- Gesetz B5 HEAT-GI S2021 LaborberichtDokument7 SeitenGesetz B5 HEAT-GI S2021 LaborberichtScribdTranslationsNoch keine Bewertungen
- Chemical Properties of MetalsDokument7 SeitenChemical Properties of MetalsDAKSH GREAD DPSN-STDNoch keine Bewertungen
- 1858-1871 GT 0912 PDFDokument14 Seiten1858-1871 GT 0912 PDFCicero Gomes de SouzaNoch keine Bewertungen
- 2 - Redoxreaktionen Zwischen Metall Und MetallsalzlösungenDokument3 Seiten2 - Redoxreaktionen Zwischen Metall Und Metallsalzlösungenthomas schuhmannNoch keine Bewertungen
- E D Chimie Anorganica 2024 Var Simulare LGEDokument2 SeitenE D Chimie Anorganica 2024 Var Simulare LGEMarin FlorinaNoch keine Bewertungen
- KA1 ChemieDokument18 SeitenKA1 ChemieJoan FergusomNoch keine Bewertungen
- Stöch Thermo GrundlagenDokument2 SeitenStöch Thermo GrundlagenРенат ФайзрахмановNoch keine Bewertungen
- Elektrochemische WasserenthrtunggwfDokument8 SeitenElektrochemische WasserenthrtunggwfArturo Avellaneda TauchertNoch keine Bewertungen
- 12.2 - 4 - Technische VerfahrenDokument2 Seiten12.2 - 4 - Technische VerfahrensmintermanNoch keine Bewertungen
- AC - II Mascotto WS19 20 - ErstterminDokument2 SeitenAC - II Mascotto WS19 20 - ErstterminflorcimusaNoch keine Bewertungen
- Interkristalline KorrosionDokument13 SeitenInterkristalline KorrosionHagen_of_TronjeNoch keine Bewertungen
- So Geht S 1Dokument10 SeitenSo Geht S 1Anežka ChrtkovaNoch keine Bewertungen
- 3.2 Schüler Schreiben OCR PAG AufDokument3 Seiten3.2 Schüler Schreiben OCR PAG AufScribdTranslationsNoch keine Bewertungen
- Chemie Zusammenfassung Pharma KfuDokument40 SeitenChemie Zusammenfassung Pharma KfuDora RadmanovićNoch keine Bewertungen
- Chemie 2022Dokument16 SeitenChemie 2022Jessica KuhnholdNoch keine Bewertungen
- EnergetikDokument2 SeitenEnergetikshahedzyadah3Noch keine Bewertungen
- Brünieren: Ein Überblick zu historischen und neueren Verfahren Mit über 90 Rezepturen und zahlreichen Anleitungen 48 FarbfotosVon EverandBrünieren: Ein Überblick zu historischen und neueren Verfahren Mit über 90 Rezepturen und zahlreichen Anleitungen 48 FarbfotosNoch keine Bewertungen
- German Language KitDokument6 SeitenGerman Language KitmilisaNoch keine Bewertungen
- BMW Motorrad Communicationsystem User Manual PDFDokument486 SeitenBMW Motorrad Communicationsystem User Manual PDFMiguel Angel BrovelliNoch keine Bewertungen
- Vergleich Verfassung 1848 Und 1871Dokument2 SeitenVergleich Verfassung 1848 Und 1871Simona HochmuthNoch keine Bewertungen
- Alex Collier Über Die GeschichteDokument17 SeitenAlex Collier Über Die Geschichtewolf gangNoch keine Bewertungen
- Empathie MaterialDokument5 SeitenEmpathie MaterialMirza MesicNoch keine Bewertungen
- Vdi 2447 2011-04Dokument36 SeitenVdi 2447 2011-04Ibrahim Rebhi AlzoubiNoch keine Bewertungen
- 800 Classic Ornaments and DesignsDokument157 Seiten800 Classic Ornaments and Designs3d maxNoch keine Bewertungen
- Bewerbung DSH MasterDokument10 SeitenBewerbung DSH MasterYoussef AboualiNoch keine Bewertungen